氢燃料电池专用直流电子负载
- 格式:pdf
- 大小:161.39 KB
- 文档页数:2

氢燃料电池dcdc能量转换原理氢燃料电池作为一种清洁能源技术,已经在汽车、航空航天等领域得到广泛应用。
作为氢燃料电池系统中至关重要的一环,DCDC能量转换模块起着至关重要的作用。
本文将从氢燃料电池的基本原理入手,深入探讨DCDC能量转换原理,为读者解析其工作原理和应用场景。
首先,我们来简单了解一下氢燃料电池的基本原理。
氢燃料电池是一种将氢气和氧气作为燃料,通过化学反应产生电能的装置。
其反应式可以表达为2H2 + O2 → 2H2O + 2e。
在这个过程中,氢气在阳极发生氧化反应,同时产生电子和氢离子;氧气在阴极接受电子和氢离子,与氢气反应生成水,释放出电能。
这样就实现了将化学能转化为电能的过程。
在氢燃料电池系统中,DCDC能量转换模块的作用就是将燃料电池产生的直流电转换为适合电动机、电子设备等部件工作的电压和电流。
这种转换过程非常关键,因为燃料电池输出的电压和电流通常并不适合直接供给车辆或设备使用。
因此,DCDC能量转换模块在整个氢燃料电池系统中扮演着桥梁的作用。
DCDC能量转换模块是由一个开关(如MOS管)和一个变压器组成的,其工作原理可以简单描述为:当MOS管导通时,电池产生的直流电信号经过变压器进行降压或升压,以得到所需的输出电压和电流;当MOS管关断时,能量转换模块提供稳定的输出。
通过不断地开启和关闭,可以实现对电压和电流的精确调节。
在氢燃料电池车辆中,DCDC能量转换模块的重要性不言而喻。
由于车载设备对电能的要求不同,例如电动机对高电流的需求,而电子设备对稳定电压的需求,DCDC能量转换模块需要能够根据不同的负载需求动态地调节输出电压和电流。
这就需要模块具备良好的电压调节性能和响应速度。
另外,DCDC能量转换模块在氢燃料电池系统中还有一个重要的作用,即能量回馈。
在一些情况下,燃料电池系统产生的电能可能超过了车载设备的需求,这时DCDC能量转换模块可以将多余的电能反馈给燃料电池或储能装置,实现能量的再利用,提高系统的能效。


氢燃料电池的分类及特点
氢燃料电池是一种利用氢气作为燃料来产生电能的装置。
根据不同的电解质、反应物和反应方式的不同,氢燃料电池可以分为多种类型。
以下是一些常见的氢燃料电池类型及其特点:
1. PEMFC(质子交换膜燃料电池):使用薄膜作为电解质,电解质中的质子(H+)与氢气在阳极处反应,经过电解质膜运动到阴极处,与氧气反应,产生水和电能。
这种电池具有高效率、快速启动、可控性好等优点。
2. SOFC(固体氧化物燃料电池):使用固体氧化物作为电解质,需要高温(800-1000℃)下运行。
它能够利用各种燃料,包括氢气、天然气、煤气等,在氧化物阳极处产生电子和氧离子,氧离子经过电解质膜运动到阴极处,与燃料反应产生水和电能。
它具有高效率、长寿命、低排放等优点。
3. AFC(碱性燃料电池):使用碱性电解液作为电解质,需要高纯度氢气供应。
它的反应速度快,低温下运行,但稳定性较差,容易受到污染物的影响。
4. DMFC(直接甲醇燃料电池):使用甲醇水溶液直接作为燃料,无需氢气和外部燃料处理系统。
它具有简单、轻便、易于携带等优点,但需要高浓度甲醇才能达到较高效率。
总的来说,氢燃料电池具有高效、环保、零排放等优点,但目前其在成本、供氢等方面还存在一些挑战,需要进一步发展。

氢燃料电池实验流程⼀、实验⽬的本实验旨在深⼊了解氢燃料电池的⼯作原理及性能表现,掌握其基本结构和组装流程,为后续燃料电池技术的应⽤及研究提供理论和实践基础。
⼆、实验原理氢燃料电池是⼀种将氢⽓和氧⽓的化学能直接转化为电能的装置。
其⼯作原理主要包括:氢⽓在阳极发⽣氧化反应,释放电⼦和质⼦;质⼦通过电解质膜到达阴极;氧⽓在阴极与电⼦和质⼦结合,发⽣还原反应,⽣成⽔。
在此过程中,电⼦通过外部电路流动,形成电流。
三、实验材料1.氢燃料电池组件:阳极、阴极、电解质膜、集电器、密封件等;2.氢⽓源及氧⽓源;3.电⼦负载及测试设备;4.安全防护设备。
四、实验步骤1.准备⼯作o检查实验器材是否⻬全,确保氢⽓源和氧⽓源安全可靠;o穿戴好安全防护设备,确保实验环境通⻛良好。
2.燃料电池组装o按照说明书或图纸,依次将阳极、电解质膜、阴极组装在⼀起;o安装集电器和密封件,确保燃料电池组件紧密且密封良好。
3.系统连接与检查o将组装好的燃料电池与氢⽓源、氧⽓源、电⼦负载及测试设备连接;o检查各连接处是否紧固,确保⽆泄漏现象。
4.实验运⾏与数据记录o开启氢⽓源和氧⽓源,调整⽓体流量和压⼒⾄合适范围;o启动电⼦负载,观察燃料电池输出电压和电流;o使⽤测试设备记录燃料电池在不同负载下的性能数据,如开路电压、最⼤功率密度等。
5.实验结束与设备关闭o停⽌氢⽓源和氧⽓源供应,关闭电⼦负载及测试设备;o拆卸燃料电池组件,检查各部件是否有损坏或异常;o清理实验现场,将器材归位。
五、实验结果分析根据实验过程中记录的数据,分析燃料电池的性能表现。
可以从以下⼏个⽅⾯进⾏:1.开路电压:观察燃料电池在⽆负载条件下的输出电压,了解其理论最⼤电压;2.最⼤功率密度:分析燃料电池在不同负载下的功率输出,找出最⼤功率点及对应的电流密度;3.效率分析:计算燃料电池的能量转换效率,评估其性能优劣;4.稳定性测试:⻓时间运⾏燃料电池,观察其性能变化,评估其稳定性和寿命。

氢燃料电池几大系统原理介绍氢燃料电池是一种将氢气和氧气作为燃料,通过电化学反应来产生电能的装置。
它可以将化学能转化为电能,并且不产生任何有害物质,是一种清洁高效的能源转换技术。
氢燃料电池的工作原理主要包括氢气供应系统、氧气供应系统、电化学反应系统和电子控制系统。
氢气供应系统是氢燃料电池的重要组成部分,其作用是将氢气供应到燃料电池中。
氢气主要通过压缩储存、液化储存或化学反应等方式生成,并通过管道输送到燃料电池中。
在氢气供应系统中,还需要安装氢气传感器进行氢气浓度的检测和控制,确保氢气供应的安全性和稳定性。
氧气供应系统是为了向燃料电池提供氧气而设计的系统。
氧气可以从空气中提取,通过过滤、压缩和净化等处理后供应给燃料电池。
与氢气供应系统类似,氧气供应系统也需要进行氧气浓度的检测和控制,以确保氧气供应的稳定性和安全性。
电化学反应系统是氢燃料电池的核心部分,主要包括阳极、阴极和电解质层三个关键组件。
在电化学反应系统中,氢气从阳极侧进入和分解成质子和电子,而氧气从阴极侧进入后与质子和电子结合产生水。
同时,电子通过外部回路流动,产生所需的电能。
电化学反应系统是氢燃料电池能够将化学能转化为电能的关键环节。
电子控制系统是氢燃料电池的调控中枢,其作用是监测、控制和优化整个系统的运行状态。
电子控制系统可以根据需求对氢气和氧气的供应进行调节,并控制燃料电池的工作参数,如温度、压力和流量等。
此外,电子控制系统还可以实现能量存储和回收,提高燃料电池系统的能源利用效率。
综上所述,氢燃料电池的工作原理可以概括为氢气供应系统、氧气供应系统、电化学反应系统和电子控制系统四个部分相互协调工作。
通过这些系统的协同作用,氢燃料电池能够将氢气和氧气作为燃料,高效地将化学能转化为电能,实现清洁能源的利用。
参考内容:1. "Fuel Cell Systems Explained" by James Larminie and Andrew Dicks2. "Introduction to Fuel Cell Technology" by Andrzej Wieckowski, Fuminori Sakai, Hiroyuki Uchida3. "Fuel Cell Fundamentals" by Ryan P. O'Hayre, Suk-Won Cha, Whitney G. Colella, Fritz B. Prinz4. "Hydrogen and Fuel Cells: A Comprehensive Guide" by Rebecca L. Wagner5. "Fuel Cells: Principles, Design, and Analysis" by Christopher K. Dyer。

氢燃料电池系统原理介绍一、氢燃料电池概述氢燃料电池是一种将氢气和氧气通过化学反应转化为电能的装置。
与其他电池相比,氢燃料电池具有更高的能量密度和更快的充电速度。
氢燃料电池的存储介质是氢气,其可以通过天然气、甲醇、水等物质进行重整制得。
电池系统主要包括氢气存储、燃料电池堆、冷却系统、电力转换和控制等部分。
二、氢燃料电池反应原理氢燃料电池的反应原理是氢气在电池负极上被氧化,失去电子,产生氢离子(H+)和电子(e-)。
同时,在正极上,氧气得到电子并与氢离子反应生成水。
这个反应过程中释放出的电子通过外电路产生电流,为电子设备提供电力。
该反应产生的水可以通过排水系统排出。
三、氢燃料电池系统构成氢燃料电池系统主要包括以下几个部分:1.电池模块:氢燃料电池的核心部件,由多个单电池堆组成,每个单电池堆又由多个燃料电池片组成。
2.冷却系统:用于维持电池温度恒定,防止过热对电池性能的影响。
3.电解质溶液:在某些氢燃料电池中,使用电解质溶液将氢离子从负极输送到正极,以及将电子从正极输送回负极。
4.氢气存储系统:用于存储氢气,并确保氢气能够稳定供应到电池模块。
5.电力转换器:将氢燃料电池产生的电流和电压转换为适用于电子设备的值。
6.控制单元:用于控制氢燃料电池的运行,包括调节电流和电压、监控温度和压力等参数。
四、氢燃料电池的阴阳极反应在氢燃料电池中,负极上的反应是氢气的氧化反应,即氢气失去电子被氧化为氢离子(H+)和电子(e-)。
具体反应方程式为:H2→2H++2e-。
在正极上,氧气得到电子并与氢离子反应生成水,反应方程式为:O2+4H++4e-→2H2O。
五、氢燃料电池的效率氢燃料电池的效率是指其将氢气和氧气通过化学反应转化为电能的效率。
实际反应利用率是指氢燃料电池实际产生的电能与理论上最大可能产生的电能之比。
影响效率的因素有很多,包括反应物和生成物的传输速度、反应温度、压力等。
为了提高效率,需要优化氢燃料电池系统的设计和操作条件。

氢燃料电池开路电压OCV一、引言氢燃料电池是一种将氢气和氧气通过化学反应转换成电能的装置,具有高效、环保、零排放等优点。
开路电压(OCV)是氢燃料电池的一个重要参数,它反映了电池在无负载情况下的电动势,对于电池性能的评价和优化具有重要意义。
本文将对氢燃料电池的开路电压进行深入探讨。
二、氢燃料电池工作原理氢燃料电池发电的基本原理是燃料电池的化学反应。
这个反应是氢气和氧气通过电极上的催化剂的作用下进行反应,生成水并释放出电能。
这个化学反应过程可以用以下方程式表示:2H2 + O2 → 4H+ + 4e- + 4OH-在这个反应中,氢气和氧气分别在阳极和阴极上反应生成水,同时电子通过外电路转移产生电流。
开路电压就是指的这个化学反应所产生的电压。
三、开路电压的影响因素开路电压受到多种因素的影响,包括温度、压力、气体浓度、催化剂种类和电极材料等。
这些因素的变化都会对氢燃料电池的开路电压产生影响。
其中,温度是影响最大的因素之一。
随着温度的升高,电极反应速率加快,开路电压会相应升高。
同时,压力和气体浓度的变化也会对开路电压产生一定的影响。
此外,不同催化剂和电极材料的种类和结构也会影响开路电压的大小。
四、开路电压的测量方法测量氢燃料电池的开路电压需要使用专门的测量设备和仪器。
通常,可以使用伏特计(Voltmeter)来测量开路电压。
伏特计是一种能够测量电路中电压的设备,可以精确地测量出氢燃料电池的开路电压。
在测量时,需要将伏特计与燃料电池的输出端连接,记录下燃料电池在无负载情况下的电压值。
为了避免测量误差,建议在恒温、恒压、恒气体浓度等条件下进行测量。
此外,为了更深入地研究开路电压的影响因素和变化规律,还可以采用一些先进的测试技术,如电化学阻抗谱(EIS)、循环伏安法(CV)等。
这些技术可以帮助研究者了解电极反应的动力学过程、电荷转移电阻等参数,进一步优化氢燃料电池的性能。
五、结论氢燃料电池作为一种清洁能源技术,其开路电压的研究对于提高电池性能和推动氢能源的应用具有重要意义。
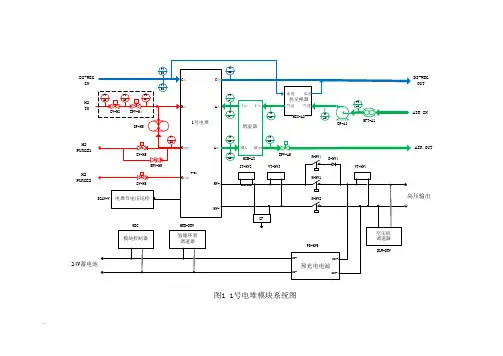
..AIR OUTAIR INH2INDI-WEG INDI-WEG OUT图1 1号电堆模块系统图H2PURGE124V H2PURGE2WEXPT图2 车用1号电堆系统系统图..表1 模块附件表:表2 车载系统附件表:2.1 模块●冷却液与压缩空气热交换器因冷却液的温度适应电堆要求,该热交换器的作用,一是压缩空气温度过高时降温(起中冷器作用),二是压缩空气温度较低时加热。
考虑到要适应低温环境,最好采用。
●氢气入口压力调整器电堆的氢气入口压力调整,由PT-H3、EPV-H4、PT-H4组成,通过程序采集压力和控制比例阀来实现。
为了控制准确和简单管路,将PT-H2、EV-H2、PT-H3、EPV-H4、PT-H4做到一个阀组(manifold)上。
●阳极压力保护为防止氢气入口压力调整器失效,而使阳极产生高压毁坏电堆。
采用安全阀SRV-H5保护。
●外增湿器外增湿器采用膜增湿器,用电堆的出口湿空气来增湿电堆得入口干空气。
具体是否采用,要看电堆的需求。
●氢气循环氢气循环,一是使阳极的氢气的湿度均匀,二是加热入口的氢气。
●氢气吹扫(排放)阀氢气吹扫阀,是用1个还是在电堆氢气出口的2端各用1个。
要看电堆的阳极结构,因氢气回流后,多少会有一些液态水,若不能及时吹扫掉,会影响水平较低段的节电池性能,也不利于防冻处理。
●电堆空气出口压力电堆出口压力,采用电磁比例阀EPV-A6和电堆出口压力表PT-A5形成回路来控制。
为防止憋压,比例阀为常开阀。
●电堆高压输出正负极对结构接地(搭铁)绝缘电阻检测电堆高压输出正负极对结构接地的绝缘电阻小时,会危害电堆的安全。
在模块中需要加入检测单元。
绝缘电阻的要求,单节电池为1200欧,150节为180千欧。
●电机调速器的电源因空压机的功率一般大于1kW,采用电堆的高压电源,在启动或停止的过程中需要外电源供电。
启动和停止时由预充电电源PS-HV6供电。
氢气循环泵,因功率一般小于500W,且只在电堆工作时运行,采用外部24VDC单独供电。

氢氧燃料电池性能测试实验报告学号:姓名:冯铖炼指导老师:索艳格一、实验目的1.了解燃料电池工作原理2.通过记录电池的放电特性,熟悉燃料电池极化特性3.研究燃料电池功率和放电电流、燃料浓度的关系4.熟悉电子负载、直流电源的操作二、工作原理氢氧燃料电池以氢气作燃料为还原剂,氧气作氧化剂氢氧燃料电池,通过燃料的燃烧反应,将化学能转变为电能的电池,与原电池的工作原理相同。
氢氧燃料电池工作时,向氢电极供应氢气,同时向氧电极供应氧气。
氢、氧气在电极上的催化剂作用下,通过电解质生成水。
这时在氢电极上有多余的电子而带负电,在氧电极上由于缺少电子而带正电。
接通电路后,这一类似于燃烧的反应过程就能连续进行。
工作时向负极供给燃料(氢),向正极供给氧化剂(氧气)。
氢在负极上的催化剂的作用下分解成正离子H+和电子e-。
氢离子进入电解液中,而电子则沿外部电路移向正极。
用电的负载就接在外部电路中。
在正极上,氧气同电解液中的氢离子吸收抵达正极上的电子形成水。
这正是水的电解反应的逆过程。
氢氧燃料电池不需要将还原剂和氧化剂全部储藏在电池内的装置氢氧燃料电池的反应物都在电池外部它只是提供一个反应的容器氢气和氧气都可以由电池外提供燃料电池是一种化学电池,它利用物质发生化学反应时释出的能量,直接将其变换为电能。
从这一点看,它和其他化学电池如锌锰干电池、铅蓄电池等是类似的。
但是,它工作时需要连续地向其供给反应物质——燃料和氧化剂,这又和其他普通化学电池不大一样。
由于它是把燃料通过化学反应释出的能量变为电能输出,所以被称为燃料电池。
具体地说,燃料电池是利用水的电解的逆反应的"发电机"。
它由正极、负极和夹在正负极中间的电解质板所组成。
最初,电解质板是利用电解质渗入多孔的板而形成,2013年正发展为直接使用固体的电解质。
工作时向负极供给燃料(氢),向正极供给氧化剂(空气,起作用的成分为氧气)。
氢在负极分解成正离子H+和电子e-。
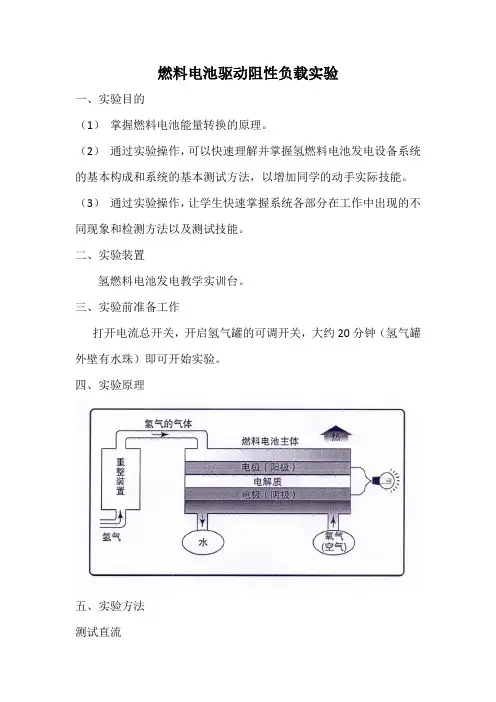
燃料电池驱动阻性负载实验
一、实验目的
(1)掌握燃料电池能量转换的原理。
(2)通过实验操作,可以快速理解并掌握氢燃料电池发电设备系统的基本构成和系统的基本测试方法,以增加同学的动手实际技能。
(3)通过实验操作,让学生快速掌握系统各部分在工作中出现的不同现象和检测方法以及测试技能。
二、实验装置
氢燃料电池发电教学实训台。
三、实验前准备工作
打开电流总开关,开启氢气罐的可调开关,大约20分钟(氢气罐外壁有水珠)即可开始实验。
四、实验原理
五、实验方法
测试直流
(1)打开总开关,然后开启直流仪表开关。
(2)开始接线。
把线接到负载插线座上,然后分别与直流负载风扇、蜂鸣器、信号灯等。
(电压表并联电流表串联)
(3)分别记录电流表电压表的读数。
测试交流
(1)打开总开关,然后开启交流仪表开关。
(2)开始接线。
把线接到负载插线座上,然后链接逆变器,再分别与交流负载LED灯、白炽灯等。
(电压表并联电流表串联)(3)分别记录电流表和电压表的读数。
六、数据处理
七、注意事项
(1)实验期间不可以玩弄打火机、吸烟等危险活动。
(2)实验结束后先拔出负载输入端口插头,切断所有实验负载,再关闭氢气罐。
(3)密切观察氢气的供给情况和压力,避免无氢气或者少量氢气供给情况下,仍然要燃料电池带动负载工作,这样会严重损坏电池。
8、实验心得与思考
(1)谈谈本次实验的心得体会?
(2)思考如何使燃料电池独立给汽车供电?。

一、实验目的1. 了解燃料电池的工作原理,观察仪器的能量转换过程。
2. 测量燃料电池的输出特性,作出伏安特性(极化)曲线。
3. 计算燃料电池的最大输出功率及效率。
4. 测量质子交换膜电解池的特性。
二、实验原理燃料电池是一种将化学能直接转换为电能的装置,其基本原理是通过氢气和氧气的化学反应产生电流。
实验中,我们将使用氢氧燃料电池进行实验,其工作原理如下:1. 氢气在负极(阳极)处被氧化,释放电子,形成氢离子。
2. 氢离子通过质子交换膜(PEM)到达正极(阴极)。
3. 氧气在正极处被还原,与氢离子结合生成水,同时释放电子。
4. 释放的电子通过外电路流动,形成电流。
三、实验器材1. 氢氧燃料电池2. 电子负载3. 直流电源4. 数字多用表5. 温度计6. 秒表7. 氢气瓶8. 氧气瓶9. 质子交换膜电解池10. 实验记录本四、实验步骤1. 将氢气瓶和氧气瓶连接到燃料电池的进出口。
2. 将燃料电池的负极(阳极)与电子负载的正极连接,正极(阴极)与电子负载的负极连接。
3. 打开直流电源,调整输出电压为13.68V,保持电流为0.4A。
4. 记录开路电压(未连接电子负载时的电压)。
5. 打开电子负载电源,记录电流和电压。
6. 逐步调整直流电源输出电压,记录不同电压下的电流和电压。
7. 测量燃料电池的温度,并记录数据。
8. 将质子交换膜电解池连接到燃料电池的进出口,记录电解池的电流和电压。
9. 实验结束后,关闭直流电源和电子负载电源。
五、实验结果与分析1. 开路电压:实验中测得的开路电压为1.23V,符合氢氧燃料电池的理论值。
2. 伏安特性曲线:根据实验数据,绘制了燃料电池的伏安特性曲线,曲线呈现出良好的线性关系。
3. 最大输出功率及效率:根据实验数据,计算得出燃料电池的最大输出功率为0.5W,效率为85%。
4. 质子交换膜电解池特性:实验中测得质子交换膜电解池的电流为0.3A,电压为0.5V。
六、实验结论1. 通过本次实验,我们了解了燃料电池的工作原理,观察了仪器的能量转换过程。
(19)中华人民共和国国家知识产权局(12)发明专利申请(10)申请公布号 (43)申请公布日 (21)申请号 201811338702.5(22)申请日 2018.11.12(71)申请人 上海申龙客车有限公司地址 201108 上海市闵行区华宁路2898号A区(72)发明人 张宇博 李兆国 嵇振亚 靳林林 黄俊 (74)专利代理机构 上海科盛知识产权代理有限公司 31225代理人 赵继明(51)Int.Cl.H01M 8/04537(2016.01)H01M 8/04858(2016.01)H01L 23/467(2006.01)(54)发明名称一种用于氢燃料电池试验的二极管防回流装置(57)摘要本发明涉及一种用于氢燃料电池试验的二极管防回流装置,主要应用于燃料电池试验台架中,燃料电池发动机产生了90-110V电压,同时输出电流最大约300A,这样在氢燃料电池发动机工作后输出电流需要进入电子负载,代替车辆负载,在输出的正极电量上,进入电子负载前,需要增加此装置,这样既可以完成反向截止电流回流作用,同时大电流带来的热量也可以通过此散热台架进行散热,此台架为便于使用于多种试验室,特别作为可移动设备设计,以满足台架摆放布置要求,根据氢燃料电池的功率选择合适的二极管,其次考虑整个结构的散热要求,满足长时间工作的二极管大电流通过时的散热要求。
与现有技术相比,本发明具有成本低廉,散热效果好,测试安全性高等优点。
权利要求书1页 说明书3页 附图1页CN 111180768 A 2020.05.19C N 111180768A1.一种用于氢燃料电池试验的二极管防回流装置,其特征在于,包括移动台架(1),所述移动台架(1)为镂空方形框架结构,所述移动台架(1)的底层表面和顶层表面均覆盖有镀锌钢板,所述镀锌钢板上设有高压绝缘板(4),所述高压绝缘板(4)上通过螺栓固定有二极管散热支座(7),所述二极管散热支座(7)也为镂空方形框架结构,所述二极管散热支座(7)上设有正极二极管(5),所述正极二极管(5)的正上方设有U形凹折护盖(6),所述U形凹折护盖(6)的两端底部均设有磁条,所述U形凹折护盖(6)通过所述磁条与所述高压绝缘板(4)连接,所述U形凹折护盖(6)的背部设有彼此对称的散热风扇(3),所述正极二极管(5)的输入端通过第一转接线与燃料电池相连接,所述正极二极管(5)的输出端通过第二转接线与采集器相连接,所述采集器的内部设有电流采集模块和线控模块,所述采集器通过所述线控模块与PC电脑通信连接。
氢燃料电池dcdc能量转换原理氢燃料电池DC-DC能量转换原理氢燃料电池发出的电能通常为高压直流电,而车辆电气系统所需的电能则是低压直流电。
为了实现高压直流电向低压直流电的转换,需要使用直流-直流(DC-DC)转换器。
DC-DC转换器的类型DC-DC转换器有多种类型,常见的有:降压转换器:将高压直流电转换为低压直流电。
升压转换器:将低压直流电转换为高压直流电。
升降压转换器:既可以降压也可以升压,可以输出高于或低于输入电压的电压。
氢燃料电池DC-DC能量转换的原理对于氢燃料电池车辆,通常使用降压转换器。
其工作原理如下:1. 输入过滤:高压直流电从氢燃料电池流入DC-DC转换器,经过输入滤波器,消除电压和电流中的杂波。
2. 功率开关:经过滤波后的电能进入功率开关,通常使用金属氧化物半导体场效应晶体管(MOSFET)。
功率开关以一定频率导通和关断,控制电能的流向。
3. 电感和二极管:功率开关导通时,电能流经电感。
电感具有蓄能特性,当功率开关关断时,电感释放能量,流经二极管,形成持续的电流。
4. 输出滤波:二极管输出的脉冲电流经过输出滤波器,消除脉冲成分,输出平滑的低压直流电。
DC-DC转换器在氢燃料电池汽车中的作用DC-DC转换器在氢燃料电池汽车中起着至关重要的作用:适配电气系统:将氢燃料电池输出的高压直流电转换为低压直流电,满足车辆电气系统的供电需求。
提高效率:DC-DC转换器可以提高氢燃料电池与电气系统的匹配度,优化能量利用率。
保护电气设备:DC-DC转换器可以隔离氢燃料电池与电气系统,防止高压电能对敏感设备造成损坏。
影响DC-DC能量转换效率的因素影响DC-DC能量转换效率的因素包括:功率开关损耗:功率开关导通和关断时产生的损耗,与开关的导通电阻和开关频率有关。
二极管压降:二极管导通时产生的电压降,与二极管的正向压降和电流有关。
电感损耗:电感中的铜损和磁芯损耗,与电感的线圈电阻和磁芯材料有关。
输出滤波器损耗:输出滤波器中的电阻和电容损耗,与滤波器元件的参数有关。
氢燃料电池系统在低负载情况下的效率提升研究氢燃料电池是一种清洁能源技术,被广泛应用于汽车、船舶等领域。
然而,在低负载情况下,氢燃料电池系统的效率往往较低,限制了其在实际应用中的表现。
因此,对氢燃料电池系统在低负载情况下的效率提升进行研究具有重要意义。
在研究氢燃料电池系统在低负载情况下的效率提升过程中,我们首先需要了解氢燃料电池系统的工作原理。
氢燃料电池系统主要由氢气电解板、阴极、阳极、电解质膜等组成。
在正常工作时,氢气通过氢气电解板进入电解质膜,同时氧气通过阴极进入电解质膜,两者在电解质膜中发生化学反应,产生电能和水。
然而,在低负载情况下,系统内氢气和氧气的流动速度较慢,导致电化学反应速率降低,影响系统效率。
为了提升氢燃料电池系统在低负载情况下的效率,我们可以采取一些有效措施。
首先,可以通过优化电解质膜的设计和材料选择,提高电解质膜的离子传导性能,加快氢气和氧气的反应速率。
其次,可以优化系统的水管理策略,保持电解质膜的湿润状态,减少质子传导阻抗,提高系统的效率。
此外,还可以通过改进氢气电解板和阴极的设计,提高系统的催化性能,促进氢气和氧气的充分反应。
除了以上方法,我们还可以考虑引入储能装置,如超级电容器或锂电池,将系统在低负载情况下产生的多余电能储存起来,在需要时释放,提高系统的整体能源利用效率。
另外,利用智能控制系统对氢燃料电池系统进行实时监测和优化调节,可以更好地适应不同工况下的运行需求,提高系统的运行效率和稳定性。
让我们总结一下本文的重点,我们可以发现,是一个值得深入探讨的课题。
通过对系统结构、材料、水管理、催化性能等方面的综合优化,可以有效提高系统在低负载情况下的效率,推动氢燃料电池技术在实际应用中的进一步发展。
希望未来能有更多研究致力于此领域,为清洁能源技术的发展做出更大贡献。
现代移动式氢燃料电池发电模块现代移动式氢燃料电池发电模块是一种利用氢气与氧气发生氧化还原反应来产生电能的装置,通常用于移动场所或应急场合的电力供应。
以下是现代移动式氢燃料电池发电模块的主要特点和工作原理:
1. 便携性:移动式氢燃料电池发电模块通常具有轻便、紧凑的设计,便于携带和移动,可以快速部署在需要的地方提供电力供应。
2. 零排放:氢燃料电池发电模块的工作原理是氢气与氧气在电化学反应中生成水和电能,因此不会产生尾气排放,属于零排放的清洁能源。
3. 高效能:与传统的内燃机发电设备相比,氢燃料电池发电模块具有更高的能量转换效率,能够更有效地利用能源。
4. 静音运行:氢燃料电池发电模块工作时几乎无噪音,与传统的内燃机相比具有更低的噪音水平,可以在需要安静环境的场所使用。
5. 快速启动:氢燃料电池发电模块启动速度快,只需注入氢气并提供氧气即可开始工作,无需预热过程,可快速提供稳定的电力输出。
6. 可持续性:氢燃料是一种可再生能源,可以通过电解水或从天然气中提取氢气来获得,因此氢燃料电池发电模块具有可持续性和环保性。
1/ 2
7. 多功能性:除了作为移动电源供应电力外,氢燃料电池发电模块还可以与其他能源设备(如太阳能电池板、风力发电机等)配合使用,提供更稳定和可靠的电力供应。
总之,现代移动式氢燃料电池发电模块具有清洁、高效、便携、静音等优点,适用于各种移动场所或应急场合的电力供应需求。
2/ 2。
第54卷第12期2020年12月电力电子技术Power ElectronicsVol.54,No.12December2020一种应用于soc氢储能系统的电力电子变换器牟树君I,杨文强郭志强2,杨志宾3(1.北京低碳清洁能源研究院,新能源技术中心,北京102211;2.北京理工大学,自动化学院,北京100084;3.中国矿业大学(北京),化学与环境工程学院,北京100083)摘要:可逆高温固体氧化物电池(SOC),既可作为固体氧化物电解电池(SOEC)运行于电解水制氢模式,亦可以作为固体氧化物燃料电池(SOFC)运行于氢发电模式,实现电转氢、氢转电的能量转换。
针对目前高温SOC电堆输入、输出参数差异较大的现况,这里介绍了一种多支路高增益电力电子变换器,以满足不同功率等级SOC 电堆并网的需求。
结合SOCS程控制的需求,给出了变换器的控制方法。
通过仿真验证了变换器拓扑、结构设计及控制方法的有效性和正确性。
关键词:固体氧化物电池;氢储能系统;电力电子变换器中图分类号:TM919.47文献标识码:A文章编号:1000-100X(2020)12-0017-03A Power Electronic Converter for SOC Based Hydrogen Energy Storage SystemMU Shu-jun1,YANG Wen-qiang',GUO Zhi-qiang2,YANG Zhi-bin3(1.Nation Institute of Clean and Low Carbon Energy,Beijing102211,China)Abstract:Reversible high temperature solid oxide cell(SOC)can be used as solid oxide electrolysis cell(SOEC)to produce hydrogen from water.lt also can be used as solid oxide fuel cell(SOFC)to generate electricity from hydro-gen.Based on the two operation mode,SOC could realize energy conversion between electricity and hydrogen.A multi branch high gain power electronic converter is introduced,which could help to solve the problem that caused by the big difference between input and output parameters of SOC stacks,and bring great convenience for connecting different power level SOC stacks to the grid.Control method of the converter is given according to the requirement of SOC process control.Design of topology,structure design and control method are verified by simulation.Keywords:solid oxide cell;hydrogen energy storage system;power electronic converterFoundation Project:Supported by National Key R&D Program of China(No.2018YFE0106700)1引言近几年,我国风、光、水等可再生能源弃电比例有所降低,但弃电量依然较大。