预包装高硅铸铁辅助阳极-详细图例说明
- 格式:pdf
- 大小:383.84 KB
- 文档页数:3

辅助阳极油气储运工程07级本科二班姓名:黄伟学号:200711011230辅助阳极辅助阳极用做阴极保护系统中的辅助电极,称为辅助阳极,通过其本身的溶解,与介质(如土壤、水)、电源、管道形成电回路。
辅助阳极在不同的环境中使用不同的材料,有高硅铸铁阳极,铂钛阳极,铂铌阳极,钛基金属氧化物阳极,石墨阳极,埋地金属氧化物阳极等。
辅助阳极的基本要求在外加电流阴极保护系统中与直流电源正极相连接的电极称为辅助阳极。
它的作用是使外加阴极电流得以从阳极经过介质流到被保护体, 构成电流的回路。
辅助阳极的电化学性能、机械性能、工艺性能以及阳极的形状, 布置方法等均对阴极保护的效果有重要的影响, 因此, 必须合理地选用阳极材料。
辅助阳极应满足以下要求:(1) 具有良好的导电性和较小的表面输出电阻;(2) 在高电流密度下阳极极化小, 而排流量大。
即在一定的电压下, 阳极单位面积上能通过较大的电流;(3)具有较低的溶解速度, 耐蚀性好, 使用寿命长;(4) 具有一定的机械强度、耐磨、耐冲击振动;(5) 材料带源方便, 价格便宜, 容易制作。
辅助阳极是外加电流阴极保护系统的重要组成部分。
阴极保护是基于电化学腐蚀原理的一种防腐蚀手段。
阴极保护是基于电化学腐蚀原理的一种防腐蚀手段。
阴极保护分为牺牲阳极保护和强制电流保护两种方法。
在这里我们只研究辅助阳极法。
牺牲阳极法将被保护金属和一种可以提供阴极保护电流的金属和合金(即牺牲阳极)相连,使被保护体极化以降低速率的方法。
在被保护金属与牺牲阳极所形成的大地电池中,被保护金属体为阴极,牺牲阳极的电位往往负于被保护金属体的电位,在保护电池中是阳极,被腐蚀消耗,故此称之为“牺牲”阳极。
通常用作牺牲阳极的材料有镁和镁合金、锌合金、铝合金等。
镁阳极适用于淡水和土壤电阻率较高的土壤中,锌阳极大多用于土壤电阻率较低的土壤和海水中,铝阳极主要应用在海水、海泥以及原油储罐污水介质中。
牺牲阳极保护法的主要特点是: (1) 适用范围广,尤其是中短距离和复杂的管网 (2) 阳极输出电流小,发生阴极剥离的可能性小 (3) 随管道安装一起施工时,工程量较小 (4) 运行期间,维护工作简单。


金属的电化学腐蚀与防护1.将金属M 连接在钢铁设施表面,可减缓水体中钢铁设施的腐蚀。
在题图所示的情境中,下列有关说法正确的是A .阴极的电极反应式为2Fe 2e Fe -+-=B .金属M 的活动性比Fe 的活动性弱C .钢铁设施表面因积累大量电子而被保护D .钢铁设施在河水中的腐蚀速率比在海水中的快【答案】C【分析】该装置为原电池原理的金属防护措施,为牺牲阳极的阴极保护法,金属M 作负极,钢铁设备作正极,据此分析解答。
【详解】A.阴极的钢铁设施实际作原电池的正极,正极金属被保护不失电子,故A 错误;B.阳极金属M 实际为原电池装置的负极,电子流出,原电池中负极金属比正极活泼,因此M 活动性比Fe 的活动性强,故B 错误;C.金属M 失电子,电子经导线流入钢铁设备,从而使钢铁设施表面积累大量电子,自身金属不再失电子从而被保护,故C 正确;D.海水中的离子浓度大于河水中的离子浓度,离子浓度越大,溶液的导电性越强,因此钢铁设施在海水中的腐蚀速率比在河水中快,故D 错误;故选:C。
2.在生产生活中,金属腐蚀所带来的损失非常严重,所以防止金属腐蚀已经成为科学研究和技术领域的重大问题。
某化学兴趣小组的同学在实验室对金属腐蚀进行了探究。
(1)分别在三个洁净干燥的试管中各加入一个洁净无锈的铁钉,再向Ⅰ、Ⅱ号两个试管中分别加入经煮沸迅速冷却的蒸馏水,然后向Ⅱ号试管中加入少量植物油,将Ⅲ号试管塞上木塞。
请判断:________号试管中的铁钉最容易生锈。
由此可见,铁制品生锈需要的条件是________________。
(2)如图2所示,处于A、B、C三种不同环境中的铁片,被腐蚀的速率由大到小的顺序是________(用字母表示)。
(3)据报道,全世界每年因为金属腐蚀造成的直接经济损失约达7 000亿美元,我国因金属腐蚀造成的损失约占国民生产总值的4%。
①钢铁在发生电化学腐蚀时,负极反应为__________________。
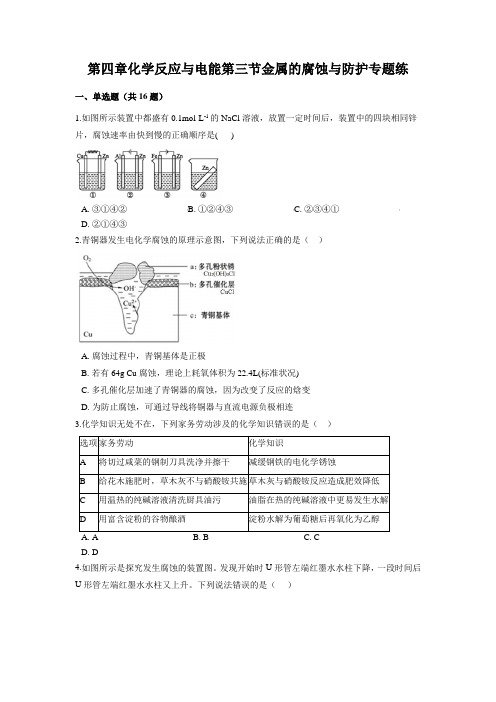
第四章化学反应与电能第三节金属的腐蚀与防护专题练一、单选题(共16题)1.如图所示装置中都盛有0.1mol·L-1的NaCl溶液,放置一定时间后,装置中的四块相同锌片,腐蚀速率由快到慢的正确顺序是( )A. ③①④②B. ①②④③C. ②③④①D. ②①④③2.青铜器发生电化学腐蚀的原理示意图,下列说法正确的是()A. 腐蚀过程中,青铜基体是正极B. 若有64g Cu腐蚀,理论上耗氧体积为22.4L(标准状况)C. 多孔催化层加速了青铜器的腐蚀,因为改变了反应的焓变D. 为防止腐蚀,可通过导线将铜器与直流电源负极相连3.化学知识无处不在,下列家务劳动涉及的化学知识错误的是()A. AB. BC. CD. D4.如图所示是探究发生腐蚀的装置图。
发现开始时U形管左端红墨水水柱下降,一段时间后U形管左端红墨水水柱又上升。
下列说法错误的是()A. 两种腐蚀负极的电极反应式均为Fe-2e -=Fe 2+B. 开始时发生的是析氢腐蚀C. 一段时间后发生的是吸氧腐蚀D. 析氢反应的总反应式为2Fe+O 2+2H 2O=2Fe(OH)25.海港、码头的钢制管桩会受到海水的长期侵蚀,常用外加电流法对其进行保护,如图所示,其中高硅铸铁为惰性辅助阳极。
下列说法错误的...是( )A. 钢制管桩应与电源的负极相连B. 通电后外电路的电子被强制流向钢制管桩C. 高硅铸铁及钢制管桩周边没有电极反应发生D. 保护电流应该根据环境条件变化进行调整6.根据下列实验操作和现象所得结论正确的是( )A. AB. BC. CD. D7.下列说法不正确的是( )A. 保护天然气管道时,将铁制管道与电源的正极相连B. 等物质的量的铁完全腐蚀生成Fe 2O 3后,发生析氢腐蚀和吸氧腐蚀过程中消耗O 2的物质的量之比为1∶3C. 电解精炼铜,用粗铜作阳极,纯铜作阴极,CuSO4溶液作电解质D. 在海轮外壳上镶入锌块,可减缓船体的腐蚀速率8.化学与生产生活息息相关,下列有关叙述错误的是A. 镀锡铁的抗腐蚀性比镀锌铁更强B. 给手机充电时,电能转化为化学能C. 泡沫灭火器的化学反应原理涉及水解反应D. 电热水器用镁棒防止内胆腐蚀,原理是牺牲阳极的阴极保护法9.在古代,中国长期以丝绸、瓷器、茶叶等为国家名片,新中国成立以来,“中国名片”有中国航天、军事、天文等,这些领域的发展受到全世界瞩目,而这些领域与化学更有着密切的联系。

河南汇龙合金材料有限公司刘珍外加电流阴极保护辅助阳极的选择及计算河南汇龙刘珍为大家讲解辅助阳极又称阳极接地装置,阳极地床。
它是外加电流阴极保护中不可缺少的重要组成部分,辅助阳极的好坏决定了阴极保护系统的使用寿命和保护距离,也决定了外加电流阴极保护系统的保护效果,如果处置不当,则阴极保护系统无法正常运行,甚至还坏对其他进出产生杂散电流干饶。
恒电位仪通过辅助阳极把保护电流送入土壤,经土壤流入被保护的管道,使管道表面进行阴极极化(防止电化学腐蚀)电流再由管道流入恒电位仪负极形成一个回路,这一回路形成了一个电解池,管道为负极处于还原环境中,防止腐蚀;而辅助阳极进行氧化反应,遭受腐蚀,也可能是周围电解质被氧化。
阴保站的电能60%消耗在阳极接地电阻上,故阳极材料的选择和埋设方式、场所的选择,对减小电阻节约电能是至关重要的。
阳极材料必须有良好的导电性能,在与土壤或地下水接触时有稳定的接地电阻,即使在高电流密度下,其表面的极化较小;化学稳定性好,在恶劣环境中腐蚀率小;有一定的机械强度并便于加工和安装;价格低来源方便。
河南汇龙合金材料有限公司刘珍一般来说,阳极埋设地区的土壤越潮湿,土壤电阻率越低,阳极埋设越深,阳极床的接地电阻越小。
有时,当土壤和阳极床的地质结构不能满足阳极接地电阻的要求时,会采用在阳极地床的回填区域添加一些极化剂,以增加土壤导电性能,减少地床接地电阻。
1、辅助阳极埋设位置的选择辅助阳极与管道距离愈远电流分布愈均匀,但过远会增加引线上的电压降和投资。
从实测数据来看辅助阳极距汇流点200米以内时,对电流分布影响较大,远于300米后影响就不大了。
故在长输管道的干线上阳极一般设在距管道300~500米之间为宜。
管道较短或油气管道较密集的地区,采用50~300米之间是合适的。
花格线设计是450m,对于土壤电阻率很大的地区是否过远,是值得研究的问题。
因此对处于特殊地形、环境的管道,辅助阳极的距离和埋设方式应根据现场情况慎重选定。

2021届高三化学二轮复习检测训练 化学电源(B )1.科学家近年发明了一种新型2Zn CO -水介质电池。
电池示意图如图,电极为金属锌和选择性催化材料,放电时,温室气体2CO 被转化为储氢物质甲酸等,为解决环境和能源问题提供了一种新途径。
下列说法错误的是( )A.放电时,负极反应为24Zn 2e 4OH Zn(OH)----+=B.放电时,1 mol 2CO 转化为HCOOH ,转移的电子数为2 molC.充电时,电池总反应为24222Zn OH) 2Zn O 4OH O (2H --=+↑++D.充电时,正极溶液中OH -浓度升高2.二氧化碳的过量排放可对海洋生物的生存环境造成很大影响,其原理如下图所示。
下列叙述错误的是( )A .海水酸化能引起3HCO -浓度增大、23CO -浓度减小B .海水酸化能促进3CaCO 的溶解,导致珊瑚礁减少C .2CO 能引起海水酸化,其原理为3HCO -23+CO H -+D .使用太阳能、氢能等新能源可改善珊瑚的生存环境3.一种高性能的碱性硼化钒(2VB )—空气电池如下图所示,其中在2VB 电极发生反应:32442VB 16OH 11e VO 2B(OH)4H O ----+-=++该电池工作时,下列说法错误的是( )A.负载通过0.04 mol 电子时,有0.224 L (标准状况)2O 参与反应B.正极区溶液的pH 降低、负极区溶液的pH 升高C.电池总反应为3222444VB 11O 20OH 6H O 8B(OH)4VO ---+++=+D.电流由复合碳电极经负载、2VB 电极、KOH 溶液回到复合碳电极4.微生物脱盐电池是一种高效、经济的能源装置,利用微生物处理有机废水获得电能,同时可实现海水淡化。
现以NaCl 溶液模拟海水,采用情性电极,用下图装置处理有机废水(以含3CH COO -的溶液为例)。
下列说法错误的是( )A.负极反应为322CH COO 2H O 8e 2CO 7H --++-=↑+B.隔膜1为阳离子交换膜,隔膜2为阴离子交换膜C.当电路中转移1mol 电子时,模拟海水理论上除盐58.5gD.电池工作一段时间后,正、负极产生气体的物质的量之比为2:15.采用惰性电极,以去离子水和氧气为原料通过电解法制备双氧水的装置如下图所示。
题型10 电解与电化学腐蚀1.[2019江苏]将铁粉和活性炭的混合物用NaCl溶液湿润后,置于如图所示装置中,进行铁的电化学腐蚀实验。
下列有关该实验的说法正确的是A.铁被氧化的电极反应式为Fe−3e−Fe3+B.铁腐蚀过程中化学能全部转化为电能C.活性炭的存在会加速铁的腐蚀D.以水代替NaCl溶液,铁不能发生吸氧腐蚀【答案】C【解析】根据实验所给条件可知,本题铁发生的是吸氧腐蚀,负极反应为:Fe−2e−=Fe2+;正极反应为:O2+2H2O +4e−=4OH−;据此解题;A.在铁的电化学腐蚀中,铁单质失去电子转化为二价铁离子,即负极反应为:Fe−2e−=Fe2+,错误;B.铁的腐蚀过程中化学能除了转化为电能,还有一部分转化为热能,错误;C.活性炭与铁混合,在氯化钠溶液中构成了许多微小的原电池,加速了铁的腐蚀,正确;D.以水代替氯化钠溶液,水也呈中性,铁在中性或碱性条件下易发生吸氧腐蚀,错误。
2.【2018新课标1卷】最近我国科学家设计了一种CO2+H2S协同转化装置,实现对天然气中CO2和H2S 的高效去除。
示意图如图所示,其中电极分别为ZnO@石墨烯(石墨烯包裹的ZnO)和石墨烯,石墨烯电极区发生反应为:①EDTA-Fe2+-e-=EDTA-Fe3+②2EDTA-Fe3++H2S=2H++S+2EDTA-Fe2+该装置工作时,下列叙述错误的是A.阴极的电极反应:CO2+2H++2e-=CO+H2OB.协同转化总反应:CO2+H2S=CO+H2O+SC.石墨烯上的电势比ZnO@石墨烯上的低D.若采用Fe3+/Fe2+取代EDTA-Fe3+/EDTA-Fe2+,溶液需为酸性【答案】C【解析】该装置属于电解池,CO2在ZnO@石墨烯电极上转化为CO,发生得到电子的还原反应,为阴极,石墨烯电极为阳极,发生失去电子的氧化反应,则详解:A、CO2在ZnO@石墨烯电极上转化为CO,发生得到电子的还原反应,为阴极,电极反应式为CO2+H++2e-=CO+H2O,正确;B、根据石墨烯电极上发生的电极反应可知①+②即得到H2S-2e-=2H++S,因此总反应式为CO2+H2S=CO+H2O+S,正确;C、石墨烯电极为阳极,与电源的正极相连,因此石墨烯上的电势比ZnO@石墨烯电极上的高,错误;D、由于铁离子、亚铁离子均易水解,所以如果采用Fe3+/Fe2+取代EDTA-Fe3+/EDTA-Fe2+,溶液需要酸性,正确。