出具医疗器械产品出口销售证明登记表
- 格式:doc
- 大小:21.00 KB
- 文档页数:1

山东省食品药品监督管理局关于出具医疗器械产品出口销售证明有关事宜的通知文章属性•【制定机关】山东省食品药品监督管理局•【公布日期】2017.05.03•【字号】•【施行日期】2017.05.03•【效力等级】地方规范性文件•【时效性】现行有效•【主题分类】医疗管理正文山东省食品药品监督管理局关于出具医疗器械产品出口销售证明有关事宜的通知为加强医疗器械产品出口销售证明管理工作,便利我省医疗器械产品出口,现就我省出具医疗器械产品出口销售证明工作的有关事宜通知如下:一、按照省局《关于实施医疗器械产品出口销售证明管理规定的通知》(鲁食药监械〔2015〕186号)要求,由设区的市级食品药品监督管理局(以下简称“市局”)负责办理辖区内医疗器械出口生产企业的《医疗器械产品出口销售证明》。
经国家总局分类界定,在中华人民共和国境内不按医疗器械管理的产品,不得出具医疗器械产品出口销售证明。
二、为在我国已取得医疗器械产品注册证书及生产许可证书,或已办理医疗器械产品备案及生产备案的相关生产企业出具的《医疗器械产品出口销售证明》,参照《国家食品药品监督管理总局关于发布医疗器械产品出口销售证明管理规定通告》(2015年第18号)执行。
三、为了鼓励医疗器械产品出口,对省内尚未进入中国市场销售仅供出口的医疗器械生产企业,若符合《医疗器械监督管理条例》第四十四条以及《医疗器械生产监督管理办法》第七十条规定,取得有效《医疗器械出口备案凭证》,且出口备案凭证载明的医疗器械包括拟办理出口销售证明的产品,市局可按规定程序和要求办理出口销售证明。
出口销售证明书的主要内容为:兹证明上述产品在中国生产,尚未进入中国市场。
该产品出口不受限制(样式见附件)。
国家总局对仅供出口医疗器械另有规定的,从其规定。
四、各市局应按规定及时公开《医疗器械产品出口销售证明》相关信息,并严格按《医疗器械产品出口销售证明管理规定》要求对相关企业实施监管。
附件:《医疗器械出口销售证明》格式山东省食品药品监督管理局2017年5月3日。

医疗器械出口证明书医疗器械出口证明书1. 引言本证明书旨在为某医疗器械进行出口提供必要的证明和文件。
该医疗器械符合国际标准和要求,符合出口国家/地区的相关法规和规定。
以下是关于该医疗器械的详细信息和出口证明。
2. 基本信息- 产品名称:- 产品型号:- 产品描述:- 创造商名称:- 创造商地址:- 出口商名称:- 出口商地址:3. 产品规格和性能在此章节中,详细描述该医疗器械的规格和性能。
包括但不限于以下方面:- 产品尺寸和外观描述- 技术指标和性能参数- 主要材料和组成部件- 使用方法和操作要求- 安全性能和应急措施- 产品配件和附件说明4. 产品质量认证和符合性在此章节中,说明该医疗器械的质量认证和符合性。
包括但不限于以下方面:- 相关标准和法规要求- Quality Management System (QMS) 认证- 产品的质量控制和检测方法- 产品符合性测试报告- 产品质量保证和售后服务5. 法规合规性在此章节中,说明该医疗器械的法规合规性。
包括但不限于以下方面:- 产品注册和许可证情况- 出口国家/地区的相关法规和规定- 产品符合性评估和认证- 标签和标识要求6. 包装和运输在此章节中,说明该医疗器械的包装和运输要求。
包括但不限于以下方面:- 包装方式和材料要求- 运输方式和条件- 防护措施和包装标识7. 文件清单在此章节中,列出了与本证明书相关的所有文件和附件。
- 附件1:产品说明书- 附件2:质量认证证书- 附件3:符合性测试报告- 附件4:注册和许可证明文件8. 法律名词及注释在此章节中,解释与本证明书相关的法律名词和注释。
- 法律名词1:解释- 法律名词2:解释。

办理医疗器械产品出口销售证明书为进一步简化办事流程,提高办事效率和服务水平,省局决定组织市局办理医疗器械产品出口销售证明书。
现将有关事项通知如下:一、市局办理医疗器械产品出口销售证明书的内涵本着便民高效、方便相对人的原则,各市局作为医疗器械产品出口销售证明书的办理点,以省局名义按规定的程序、时限、标准和要求,办理医疗器械产品出口销售证明书有关事项。
自2008年7月1日起,申请人按照属地管理原则到所在地省辖市食品药品监管局递交申请材料,办理医疗器械产品出口销售证明书。
二、办理医疗器械产品出口销售证明书程序(一)接收本辖区内医疗器械产品出口销售证明书的申请材料:在《江苏省食品药品监督管理局行政审批内部流转单》(附件1)上登记申请人有关信息后,出具《申请材料接收单》(附件2)。
(二)受理:在5个工作日内,按照办理医疗器械产品出口销售证明书形式审查指南(附件3)对材料进行形式审查。
对申请材料不齐全或不符合法定形式的,出具《补正材料通知书》(附件4),并一次性告知申请人需要补正的全部内容;对申报资料齐全或已经按照要求提交全部补正申请材料的,出具《受理通知书》(附件5),作出受理决定;不予受理的,要及时出具《不予受理通知书》(附件6),做出不予受理决定,并告知申请人享有依法申请行政复议和行政诉讼的权利。
(三)审查:按照办理条件,对申请人提交的申请材料进行合法性和真实性审查。
对符合办理条件的,在《江苏省食品药品监督管理局行政审批内部流转单》上提出书面审核意见;需要补充完善的,在10日内制作《行政审批实质审查补正材料告知书》(附件7),由受理人员一次性告知申请人。
(四)复审:各市局医疗器械处负责人对照审查标准进行复审,并在《江苏省食品药品监督管理局行政审批事项内部流转单》上作出准予证明或不予证明的建议。
(五)审定:各市局分管领导签署意见。
(六)确认:对准予证明的,在医疗器械产品出口销售证明书和申请表上盖章,确认并制作准予确认决定书(附件8);不予证明的,在申请表上写明意见并阐明理由,制作不予确认(附件9)决定书。
医疗器械销售企业记录表格以下是医疗器械销售企业的记录表格,用于记录企业的销售活动和销售信息。
该表格旨在帮助企业管理并跟踪销售情况,确保销售活动的合规性和有效性。
销售记录表格记录说明- 日期:记录销售活动的日期,使用"yyyy-mm-dd"格式。
日期:记录销售活动的日期,使用"yyyy-mm-dd"格式。
- 销售人员:记录参与销售活动的销售人员姓名。
销售人员:记录参与销售活动的销售人员姓名。
- 销售产品:记录销售的产品名称。
销售产品:记录销售的产品名称。
- 客户姓名:记录购买产品的客户姓名。
客户姓名:记录购买产品的客户姓名。
- 联系方式:记录客户的联系方式,例如手机号码或电子邮箱。
联系方式:记录客户的联系方式,例如手机号码或电子邮箱。
- 销售金额:记录销售金额(以元为单位)。
销售金额:记录销售金额(以元为单位)。
使用指南1. 在每次进行销售活动后,填写记录表格,确保填写准确和完整。
2. 每次销售活动的记录应按日期顺序排列。
3. 销售人员应在对应的列中填写个人姓名。
4. 记录表格可用于追踪销售金额和客户购买情况。
注意事项:- 管理人员应定期审核销售记录表格,以确保销售活动的合规性。
- 销售记录表格中的信息应保密并妥善保存。
- 对于涉及敏感或机密信息的销售活动,建议进一步采取必要的安全措施,以防止信息泄露。
以上是医疗器械销售企业记录表格的相关内容,请按照要求使用该表格进行记录和管理销售活动。
如有需要可根据实际情况进行调整和补充。



四川省食品药品监督管理局关于印发《四川省关于出具医疗器械产品出口销售证明书的管理规定》的通知文章属性•【制定机关】四川省食品药品监督管理局•【公布日期】2010.11.10•【字号】川食药监械[2010]20号•【施行日期】2010.11.08•【效力等级】地方规范性文件•【时效性】现行有效•【主题分类】进出口贸易正文四川省食品药品监督管理局关于印发《四川省关于出具医疗器械产品出口销售证明书的管理规定》的通知(川食药监械〔2010〕20号)各市(州)食品药品监督管理局:为有效证明我省医疗器械生产企业及其出口医疗器械产品的合法性,方便于我省医疗器械产品的出口,依据《医疗器械监督管理条例》和国家食品药品监督管理局《关于出具医疗器械产品出口销售证明书的管理规定》(国食药监械[2004]34号),我局制订了《四川省关于出具医疗器械产品出口销售证明书的管理规定》,现印发给你们,自发布之日起施行。
附件:四川省关于出具医疗器械产品出口销售证明书的管理规定二〇一〇年十一月十日附件:四川省关于出具医疗器械产品出口销售证明书的管理规定根据国际贸易惯例,为有效证明四川省医疗器械生产企业及其出口医疗器械产品的合法性,依据《医疗器械监督管理条例》和国家食品药品监督管理局《医疗器械注册管理办法》、《医疗器械生产监督管理办法》以及《关于出具医疗器械产品出口销售证明书的管理规定》,特制定本规定。
一、本规定中所称医疗器械产品,是指经我国食品药品监督管理部门批准,在四川省境内合法生产的医疗器械产品。
二、四川省医疗器械产品的生产企业或出口企业可直接向四川省食品药品监督管理局申请出具医疗器械产品出口销售证明书,申请时应填写医疗器械产品出口销售证明书申请表(见附件1),同时提交下列材料(复印件加盖证书所属企业公章):(一)出口产品生产者的《医疗器械生产企业许可证》复印件;(二)出口企业和/或生产企业《营业执照》复印件;(三)拟出口产品的《医疗器械注册证》复印件(国内未注册仅供出口的产品除外);(四)申请者填写完整的《医疗器械产品出口销售证明书》三份;(五)申请者提交材料真实、合法的责任声明原件。

医疗器械出口证明书尊敬的贵公司:首先,我谨代表XX公司,向贵公司表示诚挚的问候和慎重的感谢!我公司是一家专业从事医疗器械研发、生产和销售的企业。
自成立以来,本公司一直以为人们的健康服务为己任,致力于开发和生产高品质、安全可靠的医疗器械产品,以满足世界各地患者和医疗机构的需求。
此次,我公司计划向贵公司出口以下医疗器械产品:1. XXXX型X线透视机(100台)2. XXXX型高频电刀(200台)3. XXXX型心电监护仪(300台)4. XXXX型手术台(50台)5. XXXX型麻醉机(100台)我们自信地宣称,以上产品已按照ISO XXXX国际标准进行了设计、生产和质量控制,并通过了相关的质量认证机构的审核和认证。
这些产品在国内市场上已经获得了广泛的认可和好评,被众多医疗机构广泛采用。
同时,这些产品也符合贵国相关的医疗器械注册和使用的要求。
我公司本着以质量求生存、以信誉求发展的原则,始终把产品质量和用户体验放在第一位。
我们的生产工艺严格,采用了先进的设备和技术,确保产品的质量和性能稳定可靠。
我们拥有一支经验丰富的研发团队,不断创新和改进产品,以满足医疗行业的不断发展和需求变化。
关于产品的质量控制,我公司制定了严格的质量管理体系,从原材料采购开始,到成品检测和包装物流管理,我们严格按照ISO XXXX标准进行操作。
检验鉴定部门对每批产品进行检测合格后,才能出厂。
在运输和仓储过程中,我们保证产品的完整性和安全性。
我们配备了专业的售后服务团队,随时随地为用户提供技术支持和解决问题。
针对贵公司可能对于我公司的生产能力和交货能力有所关注,我们愿意在签订合同后提供详细的生产计划,并承诺按时交货。
我们拥有现代化的生产线和强大的供应链管理,能够满足大批量订单的需求。
我们会提前与贵公司协商好交货时间和运输方式,以确保产品按时到达贵公司。
同时,我们还能提供安装调试和售后服务,以解除贵公司的后顾之忧。
我们希望能够与贵公司达成长期稳定的合作关系,在共同追求医疗事业发展的同时互利共赢。

医疗器械出口销售资格证明办理事项办理对象:境内医疗器械受理条件:在我国已取得医疗器械产品注册证书及生产许可证书,或已办理医疗器械产品备案及生产备案的,食品药品监督管理部门可为相关生产企业出具《医疗器械产品出口销售证明》。
办理方式:网上办理、线下办理实施主体:市场监督管理局(广东政务服务可直接搜寻办理事项)(市局负责一类、省局负责二、三类医疗器出口证明)办理时限:受理后10个工作日左右法规依据:国家食品药品监督管理总局关于发布医疗器械产品出口销售证明管理规定的通告(2015年第18号)、《关于出具医疗器械产品出口销售证明有关事宜的通知》(食药监办械安〔2015〕433号)办理流程:申请资料准备→网上填报信息(广东政务服务)→提交申请资料申请资料准备:1.营业执照2.医疗器械产品出口销售证明登记表(注:登记表可分为单一产品或多产品的登记表填写)3.医疗器械生产许可证/备案凭证4.医疗器械注册证/备案凭证5.生产企业质量信用等级证明6.企业不在生产整改及涉案期间的自我保证声明7.材料真实性自我保证声明注意事项:1.申报资料的准备:1)出口销售证明登记表可分为单一产品和多产品的登记表填写2)填写多产品时,应提供相应产品的注册证3)填写的产品名称与注册证上的名称一样,如产品名称后有括号备注,也需要填写并翻译4)信用等级证明、不在整改及涉案期间,若未涉及,可直接出一份声明2.网上信息填报1)下表中,证明类型有三种模式:A.单产品+无规格型号附件(该类型需要在产品信息中填写产品注册证信息)B.单产品+多规格型号附件(该类型只需上传登记表即可,不用在产品信息中填写)C.多产品+多规格型号附件(该类型需要在产品信息中填写所申报产品的注册信息)附件:国家食品药品监督管理总局关于发布医疗器械产品出口销售证明管理规定的通告(2015年第18号)医疗器械产品出口销售证明管理规定第一条为进一步规范食品药品监督管理部门出具医疗器械出口销售证明的服务性事项的办理,便利医疗器械生产企业产品出口,特制定本规定。
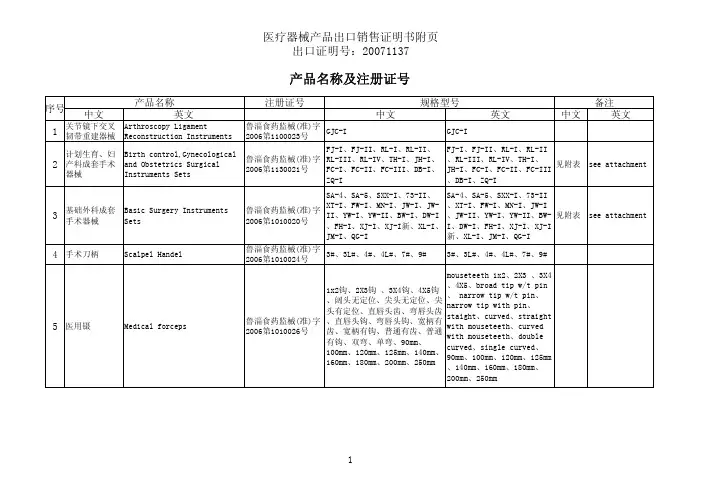
注册证号中文英文中文英文中文英文1关节镜下交叉韧带重建器械Arthroscopy LigamentReconstruction Instruments鲁淄食药监械(准)字2006第1100023号GJC-I GJC-I2计划生育、妇产科成套手术器械Birth control,Gynecologicaland Obstetrics SurgicalInstruments Sets鲁淄食药监械(准)字2006第1130021号FJ-I、FJ-II、RL-I、RL-II、RL-III、RL-IV、TH-I、JH-I、FC-I、FC-II、FC-III、DB-I、ZQ-IFJ-I、FJ-II、RL-I、RL-II、RL-III、RL-IV、TH-I、JH-I、FC-I、FC-II、FC-III、DB-I、ZQ-I见附表see attachment3基础外科成套手术器械Basic Surgery InstrumentsSets鲁淄食药监械(准)字2006第1010020号SA-4、SA-5、SXX-I、73-II、XT-I、FW-I、MN-I、JW-I、JW-II、YW-I、YW-II、BW-I、DW-I、FH-I、XJ-I、XJ-I新、XL-I、JM-I、QG-ISA-4、SA-5、SXX-I、73-II、XT-I、FW-I、MN-I、JW-I、JW-II、YW-I、YW-II、BW-I、DW-I、FH-I、XJ-I、XJ-I新、XL-I、JM-I、QG-I见附表see attachment4手术刀柄Scalpel Handel鲁淄食药监械(准)字2006第1010024号3#、3L#、4#、4L#、7#、9#3#、3L#、4#、4L#、7#、9#5医用镊Medical forceps鲁淄食药监械(准)字2006第1010026号1x2钩、2X3钩 、3X4钩、4X5钩、阔头无定位、尖头无定位、尖头有定位、直唇头齿、弯唇头齿、直唇头钩、弯唇头钩、宽柄有齿、宽柄有钩、普通有齿、普通有钩、双弯、单弯、90mm、100mm、120mm、125mm、140mm、160mm、180mm、200mm、250mmmouseteeth 1x2、2X3 、3X4、4X5、broad tip w/t pin、 narrow tip w/t pin、narrow tip with pin、staight、curved、straightwith mouseteeth、curvedwith mouseteeth、doublecurved、single curved、90mm、100mm、120mm、125mm、140mm、160mm、180mm、200mm、250mm规格型号产品名称产品名称及注册证号序号备注注册证号中文英文中文英文中文英文规格型号产品名称产品名称及注册证号序号备注6止血钳Haemostatic Forceps鲁淄食药监械(准)字2006第1010030号无直钩、弯无钩、直有钩、弯有钩、小弯、中弯、大弯、直蚊式、弯蚊式、124.5mm、125mm、139mm、140mm、158mm、159mm、160mm、178mm、179mm、180mm、197mm、200mm、213mm、217mm、217.5mm、218m、219.5mm、220mm、238mm、240mm、243mm、247.5mmstriaght w/t mouseteeth、curved w/t mouseteeth、striaght with mouseteeth 、curved w/t mouseteeth、slight curved、medium curved、storng curved、straight mosquito、curved mosquito、124.5mm、125mm 、139mm、140mm、158mm、159mm、160mm、178mm、179mm、180mm、197mm、200mm、213mm、217mm、217.5mm、218m、219.5mm、220mm、238mm、240mm、243mm、247.5mm 7帕巾钳Towel Forceps鲁淄食药监械(准)字2006第1100027号90mm、110mm、140mm、90mm、110mm、140mm、8医用剪Surgical Scissors鲁淄食药监械(准)字2006第1100025号直头、弯头、直圆头、弯圆头、直尖头、弯尖头、直尖圆头、弯尖圆头、138mm、140mm、158mm、160mm、178mm、180mm、200mm 、220mm、250mmstraight、curved、straight blunt/blunt、curved blunt/blunt、straight sharp/sharp、cruved sharp/sharp、straight sharp/blunt、cruved sharp/blunt、138mm 、140mm、158mm、160mm、178mm、180mm、200mm、220mm、250mm注册证号中文英文中文英文中文英文规格型号产品名称产品名称及注册证号序号备注9持针钳Needle Holders鲁淄食药监械(准)字2006第1010028号直型细针、弯型细针、双弯型细针、左角型细针、右角型细针、端式细针、直型粗针、弯型粗针、双弯型粗针、左角型粗针、右角型粗针、端式粗针、直型无损伤针、弯型无损伤针128-250mmstraight withoutgroov,curved without groov,double curvedwithout groov,end without groov,straight with groov,curved withgroov,double curved with groov,left-angled with groov,right-angled with groov,end withgroov,stright atraumatic needles,cruved atraumatic needles,full length 128mm-250mm 10口腔科类成套手术器械Oral Surgery Instruments Sets鲁淄食药监械(准)字2006第1060022号BY-I、CK-IBY-I、CK-I见附表see attachment11组织钳Tissue Forceps鲁淄食药监械(准)字2006第1010029号140mm、155mm、160mm、180mm、190mm、210mm、240mm140mm、155mm、160mm、180mm、190mm、210mm、240mm12海绵钳Sponge forceps鲁淄食药监械(准)字2006第1010031号直无齿、弯无齿、直有齿、弯有齿、12X180、8X180、10X180、12X180、8X220、8X250、10X220、10X250、12X220、12X250srtaight with teeth、straigh w/t teeth、curvedwith teeth、curved w/tteeth、12X180、8X180、10X180、12X180、8X220、8X250、10X220、10X250、12X220、12X25013颅脑手术头架Head Resting System鲁食药监械(准)字2005第2030009号(更)TJ-II、TJ-III TJ-II、TJ-III注册证号中文英文中文英文中文英文规格型号产品名称产品名称及注册证号序号备注14颅脑神经外科成套手术器械Neuro Surgery Instruments Set鲁食药监械(准)字2005第2030008号(更)SS-2、SS-3、SSL-I、SSL-II、SSX-I、BC-I SS-2、SS-3、SSL-I、SSL-II、SSX-I、BC-I 见附表see attachment15颈椎腰椎外科成套手术器械CervicalVertebra,Intervertebra Disc Surgiacal Instruments Sets 鲁食药监械(准)字2005第2100007号(更)ZX-I、JZ-IIZX-I、JZ-II见附表see attachment16胸腔心血管外科手术器械Thoracic and Cardiovascular Surgical Instruments 鲁食药监械(准)字2005第2070006号(更)XW-I,XZ,XZ-I,XZ-II XW-I,XZ,XZ-I,XZ-II 见附表see attachment17血管吻合轮Vessel Suturing Rings 国食药监械(准)字2007第3461165号 1.5、2、2.5、3、3.5、4、5、6、7、8、9.5、11(mm) 1.5、2、2.5、3、3.5、4、5、6、7、8、9.5、11(mm)18综合电动器械Orthopedic Electro-Surgical Motors 鲁食药监械(准)字2005第2100054号(更)XKL-II,XKL-III,XGD-I,XGD-II,XGD-III XKL-II,XKL-III,XGD-I,XGD-II,XGD-III 见附表see attachment19五官科成套手术器械Eye,Ear,Nose and Throat Surgical Instrumets Sets鲁淄食药监械(准)字2006第1010019号WG-IWG-I见附表see attachment。
医疗器械产品出口销售证明书申请表注:此表可复印,产品名称、型号规格填写不下可另附页。
医疗器械产品出口销售证明书FREE SALE CERTIFICATE FOR EXPORTATION OF MEDICAL DEVICES PRODUCTS证书编号:2005-001Certificate No.:XXXX-XXX产品名称:Product(s):型号规格:Model:生产企业:Manufacturer:生产企业地址:Address of manufacturer:兹证明上述产品符合中华人民共和国有关标准,已在中国注册,准许在中国市场销售。
该产品出口不受限制。
This is to certify that the above product(s) comply with the relevant standards of the People,s Republic of China, have been registered and are allowed to be sold in China. The exportation of product(s) is not restricted.中华人民共和国安徽省食品药品监督管理局Anhui Food and Drug Administration, People,s Republic of China年月日(此证明书自发证之日起有效期2年)(This certificate is valid for two years from the date of issuance)医疗器械产品出口销售证明书FREE SALE CERTIFICATE FOR EXPORTATION OF MEDICAL DEVICES PRODUCTS证书编号:XXXX-XXXCertificate No.:XXXX-XXX产品名称:Product(s):型号规格:Model:生产企业:Manufacturer:生产企业地址:Address of manufacturer:兹证明上述产品未在中国注册,尚未进入中国市场。
注册证号中文英文中文英文中文英文1关节镜下交叉韧带重建器械Arthroscopy LigamentReconstruction Instruments鲁淄食药监械(准)字2006第1100023号GJC-I GJC-I2计划生育、妇产科成套手术器械Birth control,Gynecologicaland Obstetrics SurgicalInstruments Sets鲁淄食药监械(准)字2006第1130021号FJ-I、FJ-II、RL-I、RL-II、RL-III、RL-IV、TH-I、JH-I、FC-I、FC-II、FC-III、DB-I、ZQ-IFJ-I、FJ-II、RL-I、RL-II、RL-III、RL-IV、TH-I、JH-I、FC-I、FC-II、FC-III、DB-I、ZQ-I见附表see attachment3基础外科成套手术器械Basic Surgery InstrumentsSets鲁淄食药监械(准)字2006第1010020号SA-4、SA-5、SXX-I、73-II、XT-I、FW-I、MN-I、JW-I、JW-II、YW-I、YW-II、BW-I、DW-I、FH-I、XJ-I、XJ-I新、XL-I、JM-I、QG-ISA-4、SA-5、SXX-I、73-II、XT-I、FW-I、MN-I、JW-I、JW-II、YW-I、YW-II、BW-I、DW-I、FH-I、XJ-I、XJ-I新、XL-I、JM-I、QG-I见附表see attachment4手术刀柄Scalpel Handel鲁淄食药监械(准)字2006第1010024号3#、3L#、4#、4L#、7#、9#3#、3L#、4#、4L#、7#、9#5医用镊Medical forceps鲁淄食药监械(准)字2006第1010026号1x2钩、2X3钩 、3X4钩、4X5钩、阔头无定位、尖头无定位、尖头有定位、直唇头齿、弯唇头齿、直唇头钩、弯唇头钩、宽柄有齿、宽柄有钩、普通有齿、普通有钩、双弯、单弯、90mm、100mm、120mm、125mm、140mm、160mm、180mm、200mm、250mmmouseteeth 1x2、2X3 、3X4、4X5、broad tip w/t pin、 narrow tip w/t pin、narrow tip with pin、staight、curved、straightwith mouseteeth、curvedwith mouseteeth、doublecurved、single curved、90mm、100mm、120mm、125mm、140mm、160mm、180mm、200mm、250mm规格型号产品名称产品名称及注册证号序号备注注册证号中文英文中文英文中文英文规格型号产品名称产品名称及注册证号序号备注6止血钳Haemostatic Forceps鲁淄食药监械(准)字2006第1010030号无直钩、弯无钩、直有钩、弯有钩、小弯、中弯、大弯、直蚊式、弯蚊式、124.5mm、125mm、139mm、140mm、158mm、159mm、160mm、178mm、179mm、180mm、197mm、200mm、213mm、217mm、217.5mm、218m、219.5mm、220mm、238mm、240mm、243mm、247.5mmstriaght w/t mouseteeth、curved w/t mouseteeth、striaght with mouseteeth 、curved w/t mouseteeth、slight curved、medium curved、storng curved、straight mosquito、curved mosquito、124.5mm、125mm 、139mm、140mm、158mm、159mm、160mm、178mm、179mm、180mm、197mm、200mm、213mm、217mm、217.5mm、218m、219.5mm、220mm、238mm、240mm、243mm、247.5mm 7帕巾钳Towel Forceps鲁淄食药监械(准)字2006第1100027号90mm、110mm、140mm、90mm、110mm、140mm、8医用剪Surgical Scissors鲁淄食药监械(准)字2006第1100025号直头、弯头、直圆头、弯圆头、直尖头、弯尖头、直尖圆头、弯尖圆头、138mm、140mm、158mm、160mm、178mm、180mm、200mm 、220mm、250mmstraight、curved、straight blunt/blunt、curved blunt/blunt、straight sharp/sharp、cruved sharp/sharp、straight sharp/blunt、cruved sharp/blunt、138mm 、140mm、158mm、160mm、178mm、180mm、200mm、220mm、250mm注册证号中文英文中文英文中文英文规格型号产品名称产品名称及注册证号序号备注9持针钳Needle Holders鲁淄食药监械(准)字2006第1010028号直型细针、弯型细针、双弯型细针、左角型细针、右角型细针、端式细针、直型粗针、弯型粗针、双弯型粗针、左角型粗针、右角型粗针、端式粗针、直型无损伤针、弯型无损伤针128-250mmstraight withoutgroov,curved without groov,double curvedwithout groov,end without groov,straight with groov,curved withgroov,double curved with groov,left-angled with groov,right-angled with groov,end withgroov,stright atraumatic needles,cruved atraumatic needles,full length 128mm-250mm 10口腔科类成套手术器械Oral Surgery Instruments Sets鲁淄食药监械(准)字2006第1060022号BY-I、CK-IBY-I、CK-I见附表see attachment11组织钳Tissue Forceps鲁淄食药监械(准)字2006第1010029号140mm、155mm、160mm、180mm、190mm、210mm、240mm140mm、155mm、160mm、180mm、190mm、210mm、240mm12海绵钳Sponge forceps鲁淄食药监械(准)字2006第1010031号直无齿、弯无齿、直有齿、弯有齿、12X180、8X180、10X180、12X180、8X220、8X250、10X220、10X250、12X220、12X250srtaight with teeth、straigh w/t teeth、curvedwith teeth、curved w/tteeth、12X180、8X180、10X180、12X180、8X220、8X250、10X220、10X250、12X220、12X25013颅脑手术头架Head Resting System鲁食药监械(准)字2005第2030009号(更)TJ-II、TJ-III TJ-II、TJ-III注册证号中文英文中文英文中文英文规格型号产品名称产品名称及注册证号序号备注14颅脑神经外科成套手术器械Neuro Surgery Instruments Set鲁食药监械(准)字2005第2030008号(更)SS-2、SS-3、SSL-I、SSL-II、SSX-I、BC-I SS-2、SS-3、SSL-I、SSL-II、SSX-I、BC-I 见附表see attachment15颈椎腰椎外科成套手术器械CervicalVertebra,Intervertebra Disc Surgiacal Instruments Sets 鲁食药监械(准)字2005第2100007号(更)ZX-I、JZ-IIZX-I、JZ-II见附表see attachment16胸腔心血管外科手术器械Thoracic and Cardiovascular Surgical Instruments 鲁食药监械(准)字2005第2070006号(更)XW-I,XZ,XZ-I,XZ-II XW-I,XZ,XZ-I,XZ-II 见附表see attachment17血管吻合轮Vessel Suturing Rings 国食药监械(准)字2007第3461165号 1.5、2、2.5、3、3.5、4、5、6、7、8、9.5、11(mm) 1.5、2、2.5、3、3.5、4、5、6、7、8、9.5、11(mm)18综合电动器械Orthopedic Electro-Surgical Motors 鲁食药监械(准)字2005第2100054号(更)XKL-II,XKL-III,XGD-I,XGD-II,XGD-III XKL-II,XKL-III,XGD-I,XGD-II,XGD-III 见附表see attachment19五官科成套手术器械Eye,Ear,Nose and Throat Surgical Instrumets Sets鲁淄食药监械(准)字2006第1010019号WG-IWG-I见附表see attachment。
医疗器械出口证明书医疗器械出口证明书文档编号:[编号]日期:[日期]本证明书由以下部分组成:1. 申请信息2. 申请人信息3. 医疗器械信息4. 进口国家/地区要求5. 质量控制体系6. 目的国/地区标准符合性7. 验证和检验报告8. 产品标识和说明9. 其他附件1. 申请信息本次出口申请的医疗器械信息如下:- 医疗器械名称:- 医疗器械型号:- 医疗器械用途及描述:- 出口数量:- 出口国家/地区:- 出口日期:2. 申请人信息申请人的详细信息如下:- 公司名称:- 公司地址:- 联系人姓名:- 联系人方式:- 联系人电子邮件:- 公司注册证明文件附在附件中。
3. 医疗器械信息医疗器械的详细信息如下:- 医疗器械名称:- 型号:- 用途:- 技术参数:- 主要材料:- 生产厂商:- 生产国家/地区:- 其他相关信息:4. 进口国家/地区要求根据进口国/地区的要求,我们确认以下信息已经满足要求:- 进口许可证- 注册要求- 标识和包装要求- 设备清单和说明书- 防护措施要求- 验收测试和认可要求- 其他要求(如有):5. 质量控制体系我们的质量控制体系按照以下标准执行:- ISO 13485质量管理体系- 相关法规和标准要求- 生产过程控制和追溯性- 检验和测试要求- 不符合和投诉处理程序- 内部审核和改进计划6. 目的国/地区标准符合性我们的产品满足以下目的国/地区的相关标准:- 国家/地区标准编号:[编号]- 标准名称:[名称]- 标准内容概述:[内容概述]7. 验证和检验报告以下是我们的产品的验证和检验报告:- 验证报告:- [报告1]- [报告2]- 检验报告:- [报告1]- [报告2]8. 产品标识和说明我们的产品包含以下标识和说明:- 产品标识:- 产品名称和型号- 公司商标- CE标志- 使用说明书:- 产品描述和用途说明- 安装和操作指南- 维护和保养说明- 安全注意事项9. 其他附件本文档附件包括以下文件:- 公司注册证明文件- 验证和检验报告- 包装和标签样品- 相关法规和标准文件附:本文所涉及的法律名词及注释- 进口许可证:进口国/地区颁发的许可证,允许产品进入其市场的文件。