医用口罩说明书审查要点
- 格式:ppt
- 大小:54.50 KB
- 文档页数:1

医用口罩产品注册技术审查指导原则医用口罩是一种用于防止病原体传播的重要防护设备,近年来,随着全球疾病传播的增加,医用口罩的需求也大幅上升。
为了确保医用口罩的质量和安全性,各国都制定了相关的产品注册技术审查指导原则。
下面,我将从四个方面对医用口罩产品注册技术审查指导原则进行详细介绍。
一、产品材料要求:医用口罩的质量和安全性与其材料的选择和使用密切相关。
医用口罩的主要材料包括无纺布、熔喷布、鼻梁条、弹性带等。
在产品注册技术审查过程中,需要对这些材料的质量和性能进行评估。
具体要求包括材料的对人体的刺激性、致敏性、生物相容性等,确保材料在使用过程中不会对人体造成伤害。
二、产品结构设计要求:医用口罩的结构设计直接关系到其过滤效果和透气性。
在产品注册技术审查中,需要对口罩的结构设计进行评估和验证。
具体要求包括口罩的结构是否合理、是否满足阻隔微粒的要求、是否透气等。
此外,还需要对口罩的接口部分进行评估,确保口罩在佩戴时能够与人脸接触紧密,避免空气和微粒的渗透。
三、产品性能测试要求:医用口罩的性能测试是确保其质量和安全性的重要手段。
在产品注册技术审查中,需要对医用口罩进行一系列的性能测试。
具体要求包括:过滤效率测试、呼吸阻力测试、细菌过滤效率测试等。
通过这些测试可以评估医用口罩的过滤效果和透气性能,确保其能够有效阻隔病原体的传播。
四、生产质量控制要求:医用口罩的生产质量控制是确保产品质量和安全性的关键环节。
在产品注册技术审查中,需要对生产过程进行评估和验证。
具体要求包括:生产设备的验证、生产工艺的控制、人员操作的规范等。
通过建立科学的生产质量控制流程,可以保证医用口罩的质量和安全性。
以上就是医用口罩产品注册技术审查指导原则的详细介绍。
通过这些原则的指导,可以确保医用口罩的质量和安全性,提高其在疾病防控中的有效性。
在未来,我们需要进一步加强对医用口罩产品注册技术审查的研究和完善,以应对全球疾病传播的挑战。

医用防护口罩技术要求及检验方法GB 19083-2010 对医用防护口罩的技术要求和检验方法做了详细的规定。
该标准属于强制性标准,凡是医用防护口罩产品都应符合标准规定的所有要求,对于医用防护口罩的检验也要严格按照标准执行。
医用防护口罩技术要求及检验方法01基本要求基本要求:口罩应覆盖佩戴者的口鼻部,应有良好的面部密合性,表面不得有破洞、污渍,不应有呼气阀。
检验方法:取3个口罩,在300 lx ~700 lx的照度下目力检查,应符合以上要求。
02鼻夹鼻夹要求:口罩上应配有鼻夹。
鼻夹应具有可调节性。
检验方法:按照说明书规定的使用方法调节,应符合以上要求。
03口罩带口罩带要求:口罩带应调节方便。
应有足够强度固定口罩位置。
每根口罩带与口罩体连接点的断裂强力应不小于10N。
检验方法:•样品数量:取4个口罩,打开包装,其中2个进行温度预处理,2个不进行预处理。
•温度预处理条件。
预处理条件为:a、70℃±3℃ 环境试验箱中放置24 h。
b、-30℃±3℃环境试验箱中放置24 h。
注:经温度预处理后应在室温条件下恢复至少4h。
•通过目力检查和拉力试验装置测量,结果均应符合调节方便、有足够强度固定口罩的位置,以及每根口罩带与口罩体连接点的断裂强力应不小于10N。
04过滤效率与气流阻力过滤效率要求:在气体流量为85 L/min 情况下,口罩对非油性颗粒过滤效率应符合表1的要求。
过滤效率等级等级过滤效率%1级≥ 952级≥ 993级≥ 99.97▲ 表1气流阻力:在气体流量为85 L/min 情况下,口罩的吸气阻力不得超过343.2 Pa (35 mm H2O)。
检验方法:•样品数量:应该使用6个口罩样品进行试验。
3个经过温度预处理,3个不经过预处理。
•温度预处理条件:a、70℃±3℃ 环境试验箱中放置24 h。
b、-30℃±3℃环境试验箱中放置24 h。
注:经温度预处理后应在室温条件下恢复至少4h。

医用口罩出厂检验报告医用口罩是一种重要的防护用品,用于预防呼吸道传染病的传播。
为了确保医用口罩的质量和效果,出厂前需要进行严格的检验,以下是一份医用口罩出厂检验报告。
一、产品基本信息1.产品名称:医用口罩2.生产厂商:XXX医疗器械有限公司3.生产日期:XXXX年XX月XX日二、检验内容本次检验主要包括以下内容:1.外观检验2.材料成分分析3.抗菌性能检验4.过滤效率检验5.使用寿命检验6.包装标示检验三、外观检验1.包装:产品在包装过程中,是否完好无损,无明显破损或变形。
2.外观:产品整体外观无明显变色、污渍或异味,无褶皱、裂纹、毛刺等。
3.面罩:面罩表面光滑,无明显凹凸、破损、裂纹等。
四、材料成分分析1.面罩材料:通过化学分析,确认面罩材料为医用级别的非织造布。
2.带子材料:通过化学分析,确认带子材料为聚合物材料,无刺激性物质。
五、抗菌性能检验1.抗菌能力:通过实验室检测,确认产品具有一定的抗菌能力,能够有效抑制细菌的生长。
2.抗真菌性能:通过实验室检测,确认产品具有抗真菌性能,能够有效抑制真菌的生长。
六、过滤效率检验1.颗粒物过滤效率:通过实验室检测,确认产品的颗粒物过滤效率达到医用标准要求。
在不同粒径的颗粒物中,能够过滤掉一定比例的颗粒物。
2.细菌过滤效率:通过实验室检测,确认产品的细菌过滤效率达到医用标准要求。
能够过滤掉一定比例的细菌。
七、使用寿命检验1.使用年限:通过实验室模拟实际使用条件,评估产品的使用寿命。
确认产品能够在正常使用条件下保持一定的过滤效率和防护性能。
八、包装标示检验2.说明书:检查产品是否附带使用说明书,内容是否准确清晰。
上述检验项目均符合医用口罩质量监管要求,产品合格。
总结:本次医用口罩出厂检验结果显示,该产品的外观良好,材料成分符合医用标准,具有一定的抗菌性能和过滤效率,使用寿命符合要求。
同时,产品的包装标示也齐全清晰。
因此,该医用口罩通过了出厂检验,可以放心使用。

不合格1、口罩片四边对称整齐,超声波压边平整。
2、布面不能有褶皱、污渍、破损 3、两条耳带长度相同且符合要求耳带焊接位置左右对称齐平,无明显错位。
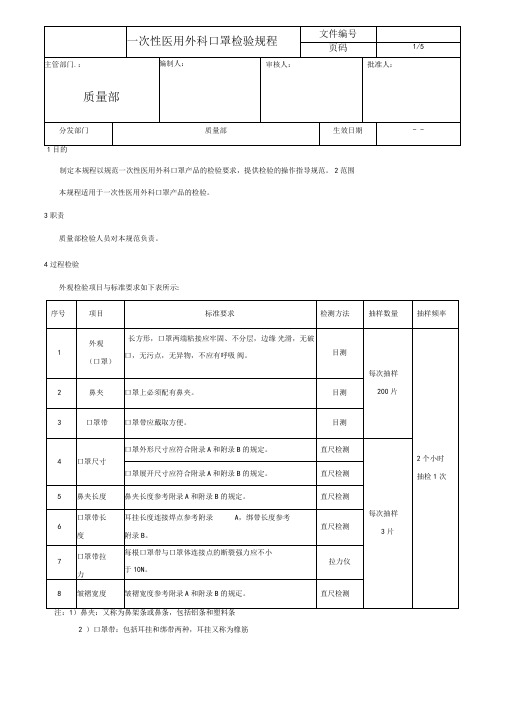
耳带焊点过大外观要求1、 外观:整洁、形状完好,表面不得有破损、污渍;2、 成品尺寸:17.5×9.5±0.5cm;3、 鼻梁条长度:大于 8.0cm;4、 耳带线尺寸:18±1cm;5、 片体与耳带线焊接点断裂强力:大于10N;
5、耳带无焊点毛刺、焊穿。
以下常见不合格状态图示
一次性使用医用口罩外观检验要求
技术要求:
4、耳带焊点不能过大
示例
合格耳带焊点正常的两面
耳带焊穿耳带焊点不完全鼻梁条刺穿、外露7、耳带不能焊偏、 鼻梁条不能刺穿外露耳带焊偏6、耳带焊点不能过小,耳带焊点应压合完全。
耳带焊点毛刺焊点过小。

医用口罩检验作业指导书1、目的本指导书规定了医用口罩检验的技术要求、测试方法及检验规则。
2、适用范围本指导书适用于所有一次性医用口罩、防尘口罩等。
3、引用标准3.1 GB19083-2010 医用防护口罩技术要求3.2 YY0469-2004 医用外科口罩技术要求3.3 YY/T0969-2013 一次性使用医用口罩技术要求4、检验依据如有客户要求或产品标志中规定的要求,按客户要求或产品标志中规定的要求,若没有规定按本作业指导书进行检验。
如涉及到安全项目检验的按进口国标准检验。
5、检验设备略6、作业内容:6.1 检验前准备在产品检验前,需获取产品的相关详细资料或由客户提供的确认样品。
同时根据客户的要求确定检验流程和重点检验的项目。
当检验人员到达现场、发现存在与实际提供资料不符合时,需及时通知客户,以确定检验流程是否正常进行。
6.2抽样检验6.2.1 根据相关资料,对已经完完包装的产品进行清点,以确定产品已经完成包装或产品包装已达到客户认可的完成比例。
6.2.2 在已完成包装的产品中,按照常规检验抽样水平AQL,如客户有特殊要求则按客户要求,随机抽取检验样品,按《产品抽样作业指导书》实施。
6.3 产品包装及产品信息收集6.3.1 产品包装信息收集收集产品的包装信息,(包括:外箱箱唛、彩盒、条码、合格标签、说明书等),对产品包装进行测量或称重(根据客户要求),并将产品包装信息(包括包装尺寸、包装重量、包装方法等)记录在检验报告中。
6.4 产品资料检验根据收取的资料、对产品的包装资料(包括:外箱箱唛、彩盒、条码、合格标签、说明书等),产品描述(产品形状、结构、尺寸等)进行核查,确定是否符合要求,不符点记录在检验报告中。
6.5 产品的检验6.5.1 包装的检验6.5.2 产品外观检验:依据客户的要求外观检查光照度,产品距光源1~1.2m 40W日光灯下,用目视检查,检查视距:300~450mm。
6.5.3 生物指标6.5.3.1 包装上标识有“灭菌”或“无菌”字样或图示的口罩应为无菌。
医用外科口罩说明书【产品名称】医用外科口罩【型号规格】型号:非无菌型;规格:175mm×95mm。
尺寸偏差范围不超过±5%。
【结构组成】产品由口罩体、鼻夹和口罩带组成。
【预期用途】用于覆盖住使用者的口、鼻及下颌,为防止病原体微生物、体液、颗粒物等的直接透过提供物理屏障。
【产品性能】1.口罩外观应整洁,形状完好,表面不得有破损、污渍。
2.口罩佩戴好后,应能罩住佩戴者的鼻、口至下颌。
应符合标志的设计尺寸及允差。
3.口罩上应配有鼻夹,鼻夹由可塑性材料制成,鼻夹长度应不小于8.0cm。
4.口罩带应戴取方便。
每根口罩带与口罩体连接点处的断裂强力应不小于10N。
5.2mL合成血液以16.0kPa(120mmHg)压力喷向口罩外侧面后,口罩内侧面不应出现渗透。
6.细菌过滤效率(BFE),口罩的细菌过滤效率应不小于95%。
7.颗粒过滤效率(PFE),口罩对非油性颗粒的过滤效率应不小于30%。
8.压力差(△P),口罩两侧面进行气体交换的压力差△p应不大于49Pa。
9.口罩材料应釆用不易燃材料;口罩离开火焰后燃烧不大于5s。
10.口罩微生物指标应符合【禁忌症】无。
【注意事项】(1)产品为一次性使用,禁止重复使用。
(2)使用前应检查包装完整性,如发现包装破损,严禁使用。
(3)产品非无菌提供。
使用前需要灭菌的应当说明灭菌的方法(包括参数等)。
(4)产品开封后应尽快使用。
(5)口罩潮湿后、受到患者血液、体液污染后,应及时更换。
(6)产品使用后按照《医疗废物管理条例》的要求处理。
(7)没有经过灭菌处理的不能在有无菌要求的环境下使用。
【使用方法】1.把褶皱打开,让口罩完全伸展。
2.贴着脸,让鼻夹挨着鼻梁。
3.一边包住脸,一边戴上耳挂。
4.将口罩下端拉至下颚,以保证大面积防护效果。
5.每次佩戴后,必须进行佩戴气密性检查,双手捂住口鼻,呼气,若感觉有气体从鼻夹处漏出,重新调整鼻夹,若感觉气体从口罩两侧漏出,进一步向脑后方调整头带位置。
一次性医用口罩技术要求及检验方法(参考)注:本标准不适用于医用防护口罩,医用外科口罩。
专业术语定义:01 细菌过滤效率英文:bacterial filtration efficiency;BFE在规定流量下,口罩材料对含菌悬浮粒子滤除的百分数。
02 通气阻力英文:flame retardation properties口罩在规定面积和规定流量下的阻力,用压差表示。
单位为Pa。
一次性使用医用口罩技术要求及检验方法:01 外观技术要求:口罩外观应整洁、形状完好,表面不得有破损、污渍。
检验方法:用3个样品进行检验,目视检查,应符合以上要求。
02 结构与尺寸技术要求:口罩佩戴好后,应能罩住佩戴者的口、鼻至下颌。
应符合设计的尺寸,最大偏差应不超过±5%。
检验方法:随机抽取3个样品进行检验,实际佩戴,并以通用或专用量具测量,应符合以上要求。
03 鼻夹技术要求:1)口罩上应配有鼻夹,鼻夹由可塑性材料制成。
2)鼻夹长度应不小于8.0cm。
检验方法:1)随机抽取3个样品进行检验。
检查鼻夹材质并手试弯折,应符合以上技术要求。
2)随机抽取3个样品进行检验。
取出鼻夹,以通用或专用量具测量,鼻夹长度应不小于8.0cm。
04 口罩带技术要求:1)口罩应戴取方便。
2)每根口罩带与口罩体连接处的断裂强力应不小于10N。
检验方法:1)随机抽取3个样品进行检验,通过佩戴检查其调节情况,应符合以上技术要求。
2)随机抽取3个样品进行检验,以10N的静拉力进行测量,持续5s,结果应符合以上技术要求。
05 细菌过滤效率(BFE)技术要求:口罩的细菌过滤效率应不小于95%。
检验方法:随机抽取3个样品进行检验,按照YY 0469中细菌过滤效率测试方法进行检验,结果均应符合过滤效率不小于95%。
06 通气阻力技术要求:口罩两侧面进行气体交换的通气阻力应不大于49 Pa/cm²。
检验方法:1)随机抽取3个样品进行检验;2)检验部位:取口罩中心部位进行检验;检验过程:检验用气体流量需调整至(8±0.2)L/min,样品检验区内直径为25mm,测试样品检验面积为A。
一次性医用口罩检验规范距离/mm2±12±12±15.2.2结构检验标准口罩应由三层材料复合而成,中间层为过滤层。
5.2.3口罩应能够覆盖使用者的口、鼻及下颌,并与使用者的脸部紧密贴合,无明显漏气现象。
5.3性能检验标准5.3.1细菌过滤效率(BFE)检验标准5.3.1.1试验原理将含有细菌的气溶胶经口罩过滤后,采集过滤前后气溶胶中细菌的数量,计算细菌过滤效率。
5.3.1.2试验方法按照XXX》标准进行试验。
5.3.1.3检验结果细菌过滤效率应不低于95%。
5.3.2通气阻力检验标准5.3.2.1试验原理在规定流量下,测量口罩的通气阻力。
5.3.2.2试验方法按照XXX》标准进行试验。
5.3.2.3检验结果通气阻力应不大于49Pa/cm²。
本文件属XXX财产,未经文控中心许可,任何人不得复印XXXXXX口XXX文件编号文件名称版本一次性医用口罩检验规范A0页次5 / 7生效日期6.标志、包装、运输和贮存6.1标志6.1.1口罩包装盒应标明以下内容:a)生产企业名称;b)产品名称;c)生产日期或批号;d)使用期限;e)执行标准;f)产品型号。
6.1.2口罩本身应标明以下内容:a)生产企业名称;b)产品名称;c)执行标准;d)产品型号;e)过期日期。
6.2包装6.2.1口罩应采用单独包装,包装材料应具有防潮、防尘、防污染等性能。
6.2.2包装箱应具有防潮、防尘、防污染等性能,并应标明生产企业名称、产品名称、批号、数量、生产日期、执行标准等信息。
6.3运输6.3.1口罩在运输过程中应避免强烈震动、阳光直射、雨淋、污染等情况。
6.3.2口罩应存放在干燥、通风、无腐蚀性气体、无有害气体的环境中。
6.4贮存6.4.1口罩应存放在干燥、通风、无腐蚀性气体、无有害气体的环境中。
6.4.2口罩的贮存期限为2年。
本文件属XXX财产,未经文控中心许可,任何人不得复印XXXXXX口XXX文件编号文件名称版本一次性医用口罩检验规范A0页次6 / 7生效日期7.附录7.1口罩抽样检验方案7.1.1每批次应随机抽取不少于32个样品进行检验。
更改历史
1目的
为加强质量控制,规范指导检验过程,制定本规程。
2适用范围
适用于一次性医用口罩说明书的质量检验,评价其质量水平。
3职责
质量部
4要求
4.1外观
无肉眼可见污渍,破损。
4.2尺寸
长为(XX-XX)cm,宽为(XX-XX)cm。
4.3文本
应与附录A保持一致。
5检验方法
5.1外观
目视观察,应符合要求。
5.2尺寸
取通用量具测量,应符合要求。
5.3文本
取标准件进行比对检验,应符合要求。
6检验类型和抽样水平
6.1检验分为型式检验和入厂检验。
6.2型式检验所有项目均应检验。
6.3入厂检验项目为4.1、4.2。
6.4抽样水平
6.4.1型式检验选择一次性抽样,判别水平为I,4.1/4.2RQL为20 ,4.3必须全部合格。
6.4.2入厂检验选择一次性抽样,抽样水平为I,4.1、4.2AQL为6.5。
7包装、储存要求
7.1XX个/包,包装为XX包装。
7.2储存在阴凉位置。
8有效期
有效期为3年。
附录A
产品说明书
【产品标签和包装标识的解释】
切勿再次使用包装破损时切勿使用怕晒防潮
批次代码制造日期查阅使用说明
【说明书编制日期】。