质量管理体系内部审核全部内部审核实施计划
- 格式:doc
- 大小:25.00 KB
- 文档页数:2
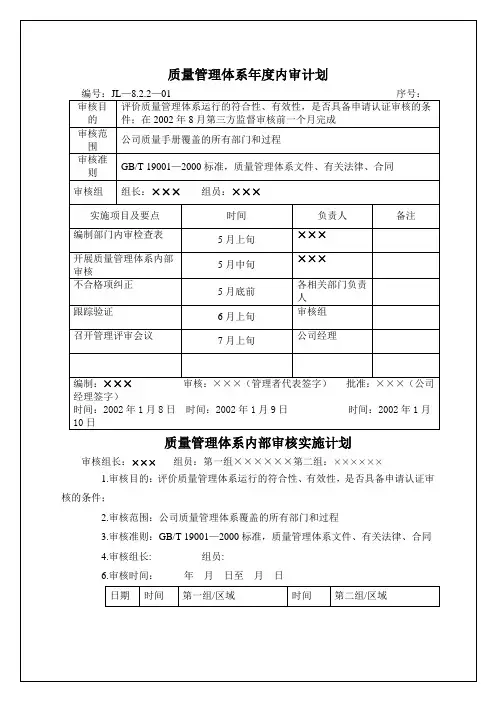
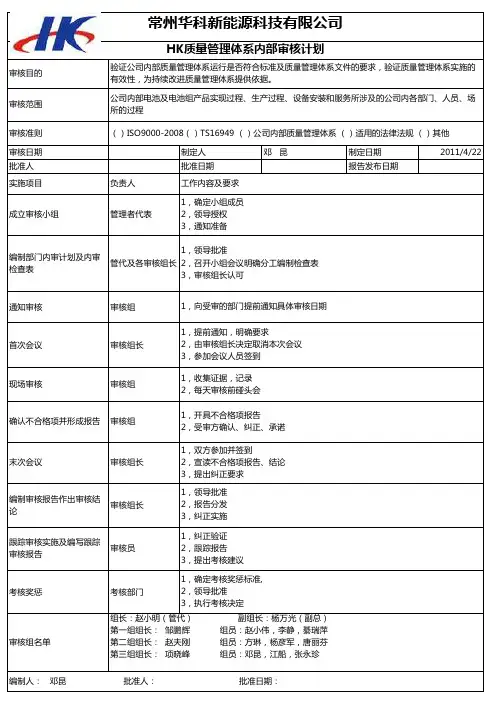
审核目的审核范围审核准则审核日期制定人邓 昆制定日期2011-4-22批准人批准日期报告发布日期实施项目负责人成立审核小组管理者代表编制部门内审计划及内审检查表管代及各审核组长通知审核审核组首次会议审核组长现场审核审核组确认不合格项并形成报告审核组末次会议审核组长编制审核报告作出审核结论审核组长跟踪审核实施及编写跟踪审核报告审核员考核奖惩考核部门审核组名单1,纠正验证2,跟踪报告3,提出考核建议1,确定考核奖惩标准,2,领导批准3,执行考核决定编制人: 邓昆 批准人: 批准日期:组长:赵小明(管代) 副组长:杨万光(副总)第一组组长: 邹鹏辉 组员:赵小伟,李静,綦瑞萍第二组组长: 赵夫刚 组员:方琳,杨彦军,唐丽芬第三组组长: 项晓峰 组员:邓昆,江船,张永珍工作内容及要求1,确定小组成员2,领导授权3,通知准备1,领导批准2,召开小组会议明确分工编制检查表3,审核组长认可1,向受审的部门提前通知具体审核日期1,提前通知,明确要求2,由审核组长决定取消本次会议3,参加会议人员签到1,收集证据,记录2,每天审核前碰头会1,开具不合格项报告2,受审方确认、纠正、承诺1,双方参加并签到2,宣读不合格项报告、结论3,提出纠正要求1,领导批准2,报告分发3,纠正实施常州华科新能源科技有限公司HK质量管理体系内部审核计划验证公司内部质量管理体系运行是否符合标准及质量管理体系文件的要求,验证质量管理体系实施的有效性,为持续改进质量管理体系提供依据。
公司内部电池及电池组产品实现过程、生产过程、设备安装和服务所涉及的公司内各部门、人员、场所的过程()ISO9000-2008()TS16949 ()公司内部质量管理体系 ()适用的法律法规 ()其他。

内部质量审核计划1. 背景介绍内部质量审核是指在企业内部对质量管理体系的有效性、合理性、可持续性等方面进行的定期评估和监督活动。
通过内部质量审核,可以发现和纠正存在的问题,改进质量管理体系,提高产品和服务的质量,增强企业的竞争力。
2. 本次质量审核的目的和范围本次质量审核的目的是检查公司质量管理体系是否已经完善并且符合相关的要求。
审核范围涵盖了公司全面的质量控制和管理活动,包括:•产品质量控制•文档控制•培训和人员素质•设备和维护管理•第三方服务商管理•消息响应能力•风险管理3. 审核人员审核人员包括公司的内部审核员和外部独立审核员。
内部审核员负责审核公司各部门的质量管理情况,并对有关问题汇总并进行分析。
外部独立审核员负责评估公司的质量管理体系是否满足相关标准和法规的要求,并提供独立的意见和建议。
4. 审核计划4.1 准备阶段在审核准备阶段,审核组与公司管理代表会进行初步沟通,以确定内部质量审核的范围、审核计划和审核程序。
还需要对公司的质量手册、程序文件、标准规章等进行审核准备。
审核组在准备阶段需要完成下列工作:•对审核计划进行修订和完善•审核组成员培训•审核组成员能力评估•审核组成员指派4.2 实施阶段在实施阶段,审核组会执行审核计划,对有关部门的质量控制和管理活动进行审查。
审核组负责对每个审核项目进行记录,并提供与结果相关的证据。
实施阶段需要完成下列工作:•审核准备工作,执行内部审核计划•进行会议,再次审查准备工作•实施现场审核4.3 报告和跟踪阶段在报告和跟踪阶段,审核组需要向公司管理代表提交审核意见和报告。
公司管理代表需要分析审核报告和意见,以确定有关工作的改进计划和时间表。
报告和跟踪阶段需要完成下列工作:•审核报告撰写和提交•会议,对审核报告进行讨论•跟踪工作推进情况5. 审核发现和处理在内部质量审核过程中发现的问题,应当在第一时间得到妥善处理。
对于审核发现的问题,需要遵循公司相关的流程和要求进行记录、整改、验证和关闭。

质量管理体系内部评审操作规程1、目的:通过定期对公司质量管理体系的运行情况进行全面的检查和评价,加强纠正或预防措施的实施管理,以证实质量管理体系运行的适宜性、充分性和有效性。
2、依据:根据新版GSP的规定制定本规程。
3、范围:适用于本公司质量管理体系的内部评审。
主要包括质量方针目标、质量管理文件、组织机构的配置、人力资源的配置、设施设备、质量风险活动控制等。
4、责任者:4.1 企业质量负责人主持质量管理体系的评审活动。
4.2质管部经理负责质量体系年度审核工作的组织实施。
4.3 GSP内审小组人员负责评价项目的考察和推进。
4.4 各相关部门负责准备、提供与本部门工作有关的评审所需资料,并负责实施管理评审中提出的相关纠正与预防措施。
5、操作规程:5.1质量管理体系的内部审核质量管理体系的内部审核包括质量体系审核、药品质量审核和服务质量审核。
5.1.1质量体系审核的对象主要是在实施GSP 的过程中,影响药品质量和服务质量的质量职能和相关场所。
5.1.2应保证每年对质量管理体系所涉及的所有部门和场所至少审核一次。
5.1.3因药品质量原因而发生重大质量事故,并造成严重后果的,应组织专项内部质量审核。
5.1.4服务质量出现重大问题或客户投诉、新闻曝光,造成不良影响时,应进行专项内部质量审核。
5.1.5国家有关法律、法规和规章有较大的更改时,企业方针、目标、组织机构人员设置、经营结构、设施设备、质量管理体系文件及相应计算机系统发生较大变化时,应进行专项内部质量审核。
5.2内部质量审核的准备5.2.1审核计划内容;审核的目的和依据;审核的范围、要点及方式;审核人员及分工;日程安排。
5.2.2审核应以公司的质量管理体系文件为依据。
5.3审核规程5.3.1内部质量审核每年进行一次,由企业主管质量负责人主持。
5.3.2由企业主管质量负责人组织编制年度审核计划,经企业领导批准后正式行文。
并将“审核计划”提前发至被审核部门。


质量管理体系的内部审核和管理评审一、引言质量管理体系的内部审核和管理评审是确保组织持续改进和客户满意度的关键步骤。
本文将探讨内部审核和管理评审在质量管理体系中的作用、流程及其重要性。
二、内部审核1. 定义内部审核是指组织内部对质量管理体系实施情况进行独立、系统性评估的过程。
它旨在发现和纠正质量体系中的问题,并确保其符合相关标准和要求。
2. 流程(1)确定审核目标:明确审核的范围和目标,制定审核计划。
(2)准备审核:收集和分析相关文件和记录,了解质量管理体系的运作情况。
(3)进行审核:进行现场审核,检查制度文件、记录和过程,与相关人员进行访谈。
(4)编写审核报告:编写审核发现的问题和建议,以及改进措施。
(5)审核跟踪:跟踪和验证组织是否及时纠正了发现的问题,并确保改进的有效实施。
(1)发现问题:通过内部审核,可以发现质量管理体系中的问题和不足之处,及时采取纠正措施,避免问题扩大化。
(2)改进体系:通过审核结果和建议,组织可以对质量管理体系进行持续改进,提升产品和服务质量,增强竞争力。
(3)保持合规性:内部审核有助于确保组织符合相关标准和法规要求,避免风险和违规行为。
三、管理评审1. 定义管理评审是指组织高层对质量管理体系的运作进行全面评估和审查的过程。
它旨在确保质量目标的实现、持续改进和资源的合理分配。
2. 流程(1)确定评审议题:讨论质量管理体系的各个方面,明确评审的议题和目的。
(2)召开评审会议:组织相关人员参加评审会议,共同讨论质量管理体系的运作情况。
(3)审查结果和数据:审查并分析质量管理体系的绩效数据、客户反馈等信息,了解体系运行情况。
(4)制定改进计划:根据评审结果,制定并跟踪改进计划,确保问题得到解决并持续改进。
(1)领导参与:管理评审使组织高层能够全面了解质量管理体系的运作情况,积极参与决策和资源的分配。
(2)持续改进:通过管理评审,组织可以识别质量管理体系中的机会和问题,制定改进计划,并确保其有效实施。

2012年上半年质量体系内部审核工作计划
一、审核目的:
通过本次内审及时对质量管理体系文件的符合性和体系运行的有效性进行检查,发现不符合项并采取纠正措施,以持续改进和确保试验检测工作科学、公正,推动体系文件的实施运行。
二、审核依据:
1、《实验室资质认定评审准则》(国认实函)〔2006〕141号
2、《质量手册》、《程序文件》、作业指导书、结果质量控制计划等管理体系文件
3、适用的国家法律、法规及标准、规范、规程
4、与质量有关的上级文件
三、审核范围:
1、最高管理者、技术负责人、质量负责人
2、综合业务室、质量管理室、试验检测室、办公室、财务室
四、内审组成员:
组长:赵慧
组员:李峰、李月玲、王锦
五、审核方式及要求:
1、由内审组长编写《内审检查计划表》,质量负责人审核,内审员遵守审核的客观性、独立性、系统性原则如实填写《内审检查记录表》。
2、内审组组织召开会议,对审核情况进行小结,经内审组集体讨论,
组长决定提出不合格项报告。
3、受审核方对内审组开展的不合格项事实进行确认后,认真分析原因,制定纠正措施,并积极整改。
4、在内审结束后,内审组对受审核方制定的纠正措施和实施情况进行验证。
六、审核时间安排:
从2012年6月25日至6月28日结束。
七、附表:
《2012年上半年质量体系内部审核计划表》
审批:编制:
日期: 2012年6月18日。

质量管理体系的内部审核一、引言质量管理体系是组织为追求和保证产品或服务质量而采取的一系列管理系统和措施。
其中,内部审核是质量管理体系的关键组成部分,旨在确保体系的有效性和合规性。
本文将分析质量管理体系的内部审核及其重要性,以及如何进行有效的内部审核。
二、质量管理体系的内部审核概述内部审核是由组织内部人员进行的一项活动,通过对质量管理体系相关文件和过程的评审,检查其是否符合质量管理体系的要求和标准。
内部审核的目标是确保质量管理体系的有效性、合规性和持续改进。
三、内部审核的重要性1. 保证符合法规和标准内部审核是组织监控和评估自身质量管理体系是否符合法规和标准的重要手段。
通过内部审核,可以及时发现和纠正与法规和标准不符的问题,确保组织的合规性。
2. 发现潜在问题和风险内部审核不仅关注质量管理体系的合规性,同时也关注潜在问题和风险。
通过内部审核,可以发现可能存在的问题和风险,并采取相应的措施进行预防和改进,降低质量风险。
3. 提升质量管理体系效能内部审核是质量管理体系持续改进的重要工具。
通过内部审核,可以识别出质量管理体系中的不足之处,提出改进意见和建议,推动质量管理体系不断完善和提升。
四、内部审核的实施步骤1. 确定审核计划在进行内部审核前,组织需制定详细的审核计划,包括审核的范围、时间安排和内部审核人员的选择等。
审核计划要综合考虑组织的资源和需求,确保审核的有效性和实施顺利。
2. 进行文件和记录的审核内部审核的第一步是对质量管理体系相关文件和记录进行审核。
审核人员应仔细评估这些文件和记录是否符合质量管理体系的要求和标准,有无潜在问题和风险。
3. 进行现场审核与采访内部审核的核心环节是对现场过程和相关人员的审核与采访。
审核人员应按照审核计划进行现场访问,观察和记录质量管理体系的实施情况,与相关人员进行交流和采访,了解他们对质量管理体系的理解和应用情况。
4. 汇总和分析审核结果审核人员需将审核结果进行汇总和分析。
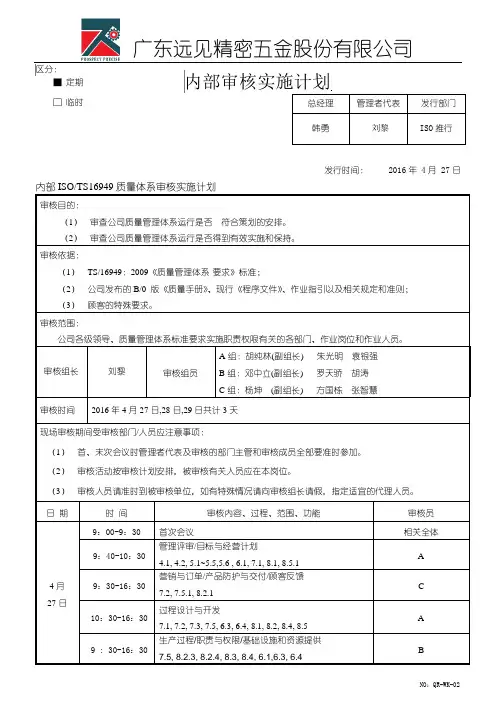
区分:■定期□临时发行时间: 2016年 4月 27日审核目的:(1)审查公司质量管理体系运行是否符合策划的安排。
(2)审查公司质量管理体系运行是否得到有效实施和保持。
审核依据:(1)TS/16949:2009《质量管理体系-要求》标准;(2)公司发布的B/0 版《质量手册》、现行《程序文件》、作业指引以及相关规定和准则;(3)顾客的特殊要求。
审核范围:公司各级领导、质量管理体系标准要求实施职责权限有关的各部门、作业岗位和作业人员。
审核组长刘黎审核组员A组:胡纯林(副组长) 朱光明袁银强B组:邓中立(副组长) 罗天骄胡涛C组:杨坤(副组长) 方国栋张智慧审核时间2016年4月27日,28日,29日共计3天现场审核期间受审核部门/人员应注意事项:(1)首、末次会议时管理者代表及审核的部门主管和审核成员全部要准时参加。
(2)审核活动按审核计划安排,被审核有关人员应在本岗位。
(3)审核人员请准时到被审核单位,如有特殊情况请向审核组长请假,指定适宜的代理人员。
日期时间审核内容、过程、范围、功能审核员4月27日9:00-9:30 首次会议相关全体9:40-10:30管理评审/目标与经营计划4.1, 4.2,5.1~5.5,5.6 ,6.1,7.1,8.1, 8.5.1A9:30-16:30营销与订单/产品防护与交付/顾客反馈7.2, 7.5.1, 8.2.1C10:30-16:30过程设计与开发7.1, 7.2, 7.3, 7.5, 6.3, 6.4, 8.1, 8.2, 8.4, 8.5A9 : 30-16:30生产过程/职责与权限/基础设施和资源提供7.5, 8.2.3, 8.2.4, 8.3, 8.4, 6.1,6.3, 6.4B总经理管理者代表发行部门韩勇刘黎ISO推行内部审核实施计划4月28日9:00-12:00采购过程7.4, 8.4 C 9:00-12:00产品防护与交付7.4.3, 7.5.3, 7.5.4, 7.5.5 B 13:30-16:30人力资源管理6.2 C实际生产生产过程/过程产品的监视和测量(shift 2)7.5, 8.2.3, 8.2.4, 8.3, 8.4, 6.3, 6.4B 9:00-12:00监视和测量装置管理/不合格品控制/设备工装管理8.2, 8.3,7.5.1.5A 13:30-16:30数据分析/纠正预防措施/文件记录控制8.3, 8.4, 8.5 ,4.2.3A4月29日8:30-9:30内部审核8.2.2C 10:30-11:30 审核报告准备/其它审核组13:30-14:30 末次会议相关全体14:30 结束/ 14:30-17:00 不符合项改善报告发放至责任部门审核组附件:审核过程与各职能部门对应参考表(如下图表)序号过程主要涉及部门审核组1 管理评审/目标与经营计划管理者代表/总经理 A2 营销与订单营业部 C3 过程设计与开发工程部 A4 生产过程生产部 B5 产品防护与交付PMC部 C6 顾客反馈营业部 C7 文件记录控制体系推行 A8 人力资源管理人力资源部 B9 基础设施和资源提供生产部 B10 设备工装管理生产部 A11 监视和测量装置管理品质部 A12 采购过程控制采购部 C13 过程产品的监视和测量品质部 B14 不合格品控制生产部 A15 数据分析品质部 A16 标识和可追溯性生产部 A17 目标与经营计划营业部 C18 职责与权限人力资源部 B19 内部审核体系推行 C20 管理评审体系推行 C21 纠正预防措施品质部 A。

内部审核实施计划
NO:
1 审核目的:
检查本公司质量管理体系是否符合ISO9001:2008 & ISO 13485:2003(YY/T 0287—2003)《医疗器械质量管理体系用于法规的要求》标准要求,质量体系是否有效运行。
2 审核依据:
ISO9001:2008 & ISO13485:2003(YY/T 0287—2003)标准、公司质量手册及质量管理体系文件。
3 审核覆盖产品:
轮椅、助行器、拐杖、洗澡椅。
4 审核时间:
2010 年 9月 10 日
5 现场审核期间请被审核方有关人员参加下列活动:
首、末次会议:总经理、副总经理、管理者代表及与审核有关的部门负责人、管理人员参加。
审核活动:按审核时间安排,被审核方有关人员应在本岗位上。
6 审核员分组:
审核组长:
A组 B组:
7 审核安排:
按审核时间表。
1
审核时间表
备注:
1 本次审核中,按照ISO9001:2008 & YY/T 0287标准要求进行。
2本次审核中,每组在审核各部门时,均要审核:
文件控制(4.2.3)、质量方针(5.3)、质量目标(5.4.1)、记录控制(4.2.4)、培训(6.2)、纠正和预防措施(8.5)。
编制:批准: 日期:。
质量管理体系内部审核制度1.目的通过内审及时发现和纠正质量体系存在的问题,并持续保持改进,保证质量管理体系有效运行。
2。
依据2.1《中国人民共和国药品管理法》、《中华人民共和国药品管理法实施条例》及药品管理法律、法规和有关规定。
2。
2《药品经营质量管理规范》3.适用范围适用于公司质量管理体系各环节的审核。
4。
职责4。
1质量负责人负责组织对质量管理体系进行内部评审。
4.2质量部门具体负责实施质量管理体系内审工作。
4。
3各部门协助开展内审工作。
5.制度内容5.1概念5.1质量管理体系内审的概念质量管理体系内审是指公司在规定的时间段内,对照《药品经营质量管理规范》及相关法律法规、公司自身管理要求,对公司质量管理状况进行全面的检查与评审,以核实公司质量体系运行的充分性、适宜性和有效性,从而不断改进。
5。
2质量管理体系内审的时间:5.2。
1年度内审:每年第十一月下旬进行。
5。
2。
2专项内审:当公司质量管理体系发生重大变化时应适时进行专项评审:a)组织结构、药品经营范围、库房发生重大变化时;b)当国家有关法律、法规和规章有较大的更改时。
5。
3质量管理体系评审的内容:5。
3.1组织机构及人员资质情况;5。
3.2岗位职责履行情况;5.3.3质量体系文件;5。
3。
4业务流程;5.3。
5设施设备配备管理情况。
5.4质量管理体系评审的程序5。
4.1质量部门负责编制内审计划,并经质量负责人批准,内审计划包括:a)内审时间、内审方案和内审范围等;b)内审标准;c)内审小组成员。
5。
4。
2内审小组按照标准实施检查,如实、准确记录发现的问题或存在的缺陷。
5.4.3检查工作结束后,内审小组确定不符合项目,提出相应的整改要求及整改时限,交责任部门进行整改。
5.4。
4质量部门根据确定的整改时限要求,监督整改措施的落实、完成情况。
5。
4。
5内审小组对质量管理体系进行评审,形成评审报告.5。
4.6根据内审结果提出下一年度的质量管理工作计划.。
16949质量管理体系年度审核计划一、审核目的为了确保公司的质量管理体系符合 ISO/TS 16949 标准的要求,持续有效地运行,不断提高产品质量和管理水平,特制定本年度的审核计划。
通过审核,发现质量管理体系中存在的问题和不足之处,采取相应的纠正措施和预防措施,以实现质量管理体系的持续改进。
二、审核范围本次审核涵盖公司与质量管理体系相关的所有部门和过程,包括但不限于设计开发、采购、生产制造、检验检测、销售服务等。
三、审核依据1、 ISO/TS 16949 质量管理体系标准。
2、公司的质量管理体系文件,包括质量手册、程序文件、作业指导书等。
3、相关的法律法规和客户要求。
四、审核频次和时间安排1、内部审核计划进行两次内部审核,分别在上半年和下半年进行。
第一次内部审核定于具体时间 1,为期X天。
第二次内部审核定于具体时间 2,为期X天。
2、管理评审管理评审每年进行一次,定于具体时间 3,为期X天。
3、外部审核第三方认证机构的监督审核预计在具体时间 4进行,具体时间以认证机构的通知为准。
五、审核组成员审核组组长:组长姓名审核组成员:成员姓名 1、成员姓名 2、成员姓名3……六、审核内容和要点1、质量管理体系文件的符合性和有效性检查质量手册、程序文件、作业指导书等文件是否符合 ISO/TS 16949 标准的要求。
审核文件的更新和修订情况,确保文件的及时性和有效性。
2、管理职责评估高层管理者对质量管理体系的重视程度和支持力度。
审查质量方针和质量目标的制定、分解、实施和监控情况。
3、资源管理检查人力资源的配备、培训和考核情况。
审核设备设施的维护保养和管理情况。
4、产品实现过程设计开发过程的策划、输入、输出、评审、验证和确认。
采购过程的供应商管理、采购控制和进货检验。
生产制造过程的工艺控制、生产计划、过程检验和标识追溯。
检验检测过程的检验标准、检验设备、检验记录和不合格品控制。
5、测量、分析和改进内部审核和管理评审的实施情况。
质量管理体系内部审核计划一、审核目的1、评价审计局质量管理体系的符合性和有效性;2、提供进一步改进的信息。
二、审核范围审计局审计过程(包括财政审计、经济责任审计、固定资产投资审计、财务收支审计、专项审计、审计调查)及相关活动。
三、审核性质例行审核四、审核依据1、GB/T19001—2000idtISO9001:2000;2、审计局质量管理体系文件;3、适用的法律法规和其他要求。
五、审核组成员审核组长:XXX组员:XX、XX、XX、XX、XX、XX、XX、XX六、审核时间计划在2009年5月下旬及10月中旬进行二次内部审核,具体时间另行通知。
XX区审计局二〇〇九年一月四日附:审核日程审核日程具体安排如下:日期时间A组涉及主要过程B组涉及主要过程日8:30-9:00首次会议9:00-11:30局长、管代 4.1,5.1-5.6,6.1,8.1,8.2.3,8.5法规科4.2.3,4.2.4,6.2.26.3,7.1,7.2,7.5.1-7.5.5,8.2.4,8.3,8.4 11:30-12:30午餐、休息12:30-14:30纪检组8.2.1基本建设审计科7.1,7.2,7.5.1,7.5.3,7.5.4,7.5.514:30-16:30经济责任审计科7.1,7.2,7.5.1,7.5.37.5.4,7.5.5内审经贸审计科7.1,7.2,7.5.1,7.5.3,7.5.4,7.5.528日8:30-10:30财政金融审计科7.1,7.2,7.5.1,7.5.37.5.4,7.5.5办公室4.2,6.2,7.4,7.5.3,7.5.4,7.5.5,8.2.2,8.510:30-11:30行政事业审计科7.1,7.2,7.5.1,7.5.37.5.4,7.5.5 11:30-12:30午餐、休息12:30-15:00审核组内部汇总15:00-16:00末次会议注:1首、末次会议请审计局高层领导、部门负责人及相关人员参加。
生产线质量管理体系内部审核方案下载提示:该文档是本店铺精心编制而成的,希望大家下载后,能够帮助大家解决实际问题。
文档下载后可定制修改,请根据实际需要进行调整和使用,谢谢!本店铺为大家提供各种类型的实用资料,如教育随笔、日记赏析、句子摘抄、古诗大全、经典美文、话题作文、工作总结、词语解析、文案摘录、其他资料等等,想了解不同资料格式和写法,敬请关注!Download tips: This document is carefully compiled by this editor. I hope that after you download it, it can help you solve practical problems. The document can be customized and modified after downloading, please adjust and use it according to actual needs, thank you! In addition, this shop provides you with various types of practical materials, such as educational essays, diary appreciation, sentence excerpts, ancient poems, classic articles, topic composition, work summary, word parsing, copy excerpts, other materials and so on, want to know different data formats and writing methods, please pay attention!一、引言随着市场竞争的日益激烈,企业对产品质量的要求越来越高,因此建立一个完善的质量管理体系已经成为企业的当务之急。
质量管理体系2016年内部审核报告一、内部审核的时间:2016年10月18~19日。
二、受审核部门:总经理、管理者代表、行政人事部、质量部、市场营销部、技术部、开发部、设备工程部、采购部、生产部、仓库。
三、内部审核组成员名单:组长:XX第一组:XXX、XXX、XXX、XXX第二组:XXX、XXX、XXX、XXX第三组:XXX、XXX、XXX、XXX四、内部审核目的1.检查和评价公司的质量管理体系是否符合策划的要求,是否符合ISO 9001:2008标准的要求和适用法律法规的要求,验证对体系实施、保持和持续改进的有效性和充分性;2.检查质量方针和质量目标的贯彻落实情况,是否在各部门有效展开并得到实施;3.通过审核进一步验证质量管理体系文件的可操作性;4.检查如何以顾客为关注焦点,顾客满意和与顾客沟通过程,增强满足顾客要求意识。
五、审核范围XX公司XXX的生产和服务全过程涉及到的有关的部门和相关岗位。
六、审核依据1.ISO 9001:2008《质量管理体系要求》标准;2.公司所策划和制定的质量手册,程序文件、作业文件、技术规范以及相关规定和准则;3.公司提供产品所适用的法律法规;4.必要时的相关产品销售合同和质量计划。
七、审核方式1、与最高管理层人员座谈贯彻实施标准的“领导作用”情况2、听取各职能部门负责人对自己职责权限情况以及本部门职责范围内的体系运行状况;3、根据“质量管理体系内部审核计划”的安排,由审核小组分别到应所审的职能部门对其应实施标准的章节条款。
对实施状态收集审核发现,审核应用抽样方法进行;4、对各部门工作现场和生产岗位作业现场的环境适宜性,设备设施管理等状况进行检查。
八、内审首、末次会议参加人员参加人员有包括总经理、管理者代表、各分管副总、各部门的主管/负责人及审核组成员。
九、内部审核综述根据公司2016年年度内审计划,经总经理和管理者代表批准成立了以杨厚胤为组长的13人内审小组。
公司内审组依据ISO9001:2008标准和《管理体系内部审核程序》规定要求,于2016年10月18~19日对生产的镍氢电池和锂离子电池的设计开发、生产和销售、检验和售后服务过程以及所涉及的部门和高层管理者进行质量管理体系内部审核,抽查了公司办公及生产场所。
内部质量审核控制工作程序内部质量审核控制工作程序一、编制目的内部质量审核是指为了评估和改进组织的质量管理体系的运行情况而进行的一项活动。
其目的是通过审核来发现、纠正和预防质量管理体系中存在的问题,确保组织达到质量管理体系的目标。
二、审核范围内部质量审核范围涵盖了整个组织的质量管理体系,包括各个部门、环节及关键过程。
三、审核标准内部质量审核按照国际标准ISO 9001:2015进行执行,并结合组织自身的实际情况进行审核。
四、审核组成1. 审核组长:负责审核的组织、协调审核的进行,编制审核计划和审核报告。
2. 审核员:根据审核计划,参与实施审核,收集、整理和评价审核所得证据,提交审核报告。
五、审核计划1. 审核组长和相关部门负责人协商制定审核计划,确定审核的时间、地点、审核标准等。
2. 审核计划应提前通知被审核部门,包括审核目的、内容、要求等。
六、审核准备1. 审核组成员应对被审核部门的相关文件、记录进行充分了解和准备。
2. 审核组成员应带齐必要的工作用具,如:笔、纸、相机等。
七、审核实施1. 审核组按照审核计划进行入场会议,概述审核目的、方式、程序和要求。
2. 审核组根据审核计划,对被审核部门进行分组或分工,开始实施审核。
3. 审核组根据审核依据,进行现场核查、记录采集等工作。
4. 审核期间,审核组应与被审核部门的工作人员进行有效沟通,了解工作情况。
5. 审核过程中,如发现问题,应及时与被审核部门进行沟通和交流,共同寻求问题的解决办法。
八、审核报告1. 审核组应在审核结束后,及时填写审核报告,包括审核目的、范围、方法、依据、结论等内容。
2. 审核报告应包括对组织质量管理体系的评价,指出存在的问题及改进措施。
3. 审核报告应及时提交给被审核部门,要求被审核部门在规定时间内提出整改措施和改进方案。
九、整改和改进1. 被审核部门应根据审核报告中指出的问题,及时制定整改计划和改进方案。
2. 被审核部门应在规定时间内完成整改,并将整改情况报告审核组。
一个完整的ISO9001质量管理体系内部审核(内审)应包括哪些步骤目前,很多企业对ISO 9001质量管理体系的了解比过去更深入,管理也越来越规范。
内部审核是检验质量管理体系运行绩效的有效方法,是推动持续改进的动力,因此,内审员的审核质量就显得尤其重要。
如何进行内部审核也是很多管理者关心的问题,一个完整的ISO9001质量管理体系内部审核(内审)应包括哪些步骤呢?本文将就内部审核的方法与技巧与各位质量人分享,内容仅供参考。
◆◆◆◆01 .内部审核的策划与准备1.编制年度审核计划每年年初,质量负责人组织编制年度审核计划,审核方式分为管理体系全过程审核及管理体系要素审核,管理体系全过程审核每年至少安排一次,制定的年度计划应覆盖管理体系涉及全要素和所有部门。
当出现以下特殊情况时应增加审核频次:a. 管理体系有重大变更或机构和职能发生重大变更时;b.内部监督员发现某质量要素存在严重不符合项;c.出现质量事故,或客户对某一环节连续申诉、投诉;d.认证认可机构安排现场评审或监督评审前;年度审核计划经审批后,组织实施。
2.审核前准备①成立内审组:质量负责人依据管理体系审核年度计划的审核内容和审核对象组建内审组,内审组成员应经培训考核合格,取得内审员资格证书,且内审员与被审核部门无直接责任关系。
质量负责人召开内审组组员会议,任命内审组组长和宣读内审员守则,并依据内审年度计划提出本次评审目的、范围内容和要求。
②内审实施计划的制定:内审组长制定内审实施计划,要依据本机构的职能分配表编制各受审核部门的审查内容,由质量负责人审批后实施。
实施计划应在正式审核前一周由内审组长发至各有关部门和人员。
③审核组预备会:内审实施计划经质量负责人批准后,审核组长召开审核组预备会议,研究有关体系文件并应决定是否需要补充文件,明确分工和要求,确保每位内审员都清楚了解审核任务,全部完成审核前的准备工作。
④编制检查表:审核前,内审员应根据分工编制检查表,内审检查表编制的好坏直接影响内审实施的质量,因此在整个内审中至关重要。
内部审核实施计划
QR/QP-09-02 版本/修改次数:01/00
№:001
审核组长: 刘国洪 2004年3月25日 第1
页 共1页
1.审核目的:
⑴检查本公司质量管理体系是否符合ISO 9001:2000标准及公司《质量手册》
和《程序文件》的要求。
⑵检查本公司质量管理体系是否得到有效实施和保持。
2.审核依据:⑴ISO 9001:2000标准;⑵本公司的《质量手册》和《程序文件》;
⑶适用的法律法规。
3.审核覆盖产品:密封圈、减震件。
4.审核时间:2004年03月25日~26日
5.审核组构成:A组:刘国洪 B组:包建斌
6.现场审核期间被审核方有关人员参加下列活动:
首、末次会议:最高管理者及管理者代表和审核有关的管理人员参加。
审核活动:按审核日程安排,被审核方有关人员在本岗位。
7.审核安排:
日期 时 间 审核组别 部门 审核涉及质量管理体系标准要求
3.25
7:30-8:00 A、B 全体部门 首次会议
8:00-12:00 A、B 总经理及 管理者代表 4.1、4.2.1、4.2.2、5.1、5.2、5.3、5.4.1、5.4.2、5.5.1、5.5.2、5.5.3、6.1、6.3、8.1、
8.2.3
13:00-16:30 A、B
生技部(车间) 6.3、6.4、7.1、7.5.1、7.5.2、7.5.3、7.5.5、
8.3
3.26
7:30-12:00 A 质检部
7.4.3、7.5.3、7.6、8.2.4、8.3、8.4、8.5.1、
8.5.2、8.5.3
13:00-14:30 A、B 供销部
7.2、7.5.4、7.5.1e)、7.5.5、8.2.1
7.4.1、7.4.2、7.4.3
14:30-16:00 A、B 办公室 4.2.3、4.2.4、6.2
16:00-16:30 A、B 编写不合格报告
16:30-17:00 A、B 全体部门 末次会议
审核每个部门均可能审核的要素 5.3、5.4.1、5.5.1、5.5.3
4.07 8:00-10:00 B 总经理及管理者代表 5.6、8.2.2
编制/日期: 审批/日期: