人源化抗体
- 格式:doc
- 大小:18.00 KB
- 文档页数:3
什么是抗体人源化目前,用细胞工程制备人单抗在技术上和伦理上都存在一些难题,治疗性抗体的开发就集中在具有治疗前景的鼠源单抗上。
但是鼠源单抗对人体具有异源性反应,可诱发人抗鼠抗体效应(Human anti-mouse antibodies, HAMA反应),使得单抗的治疗效果明显滞后。
随着基因重组技术的发展和人们对抗体结构认识的深入,研究者们尝试对鼠源性抗体进行改造,致力于在保留与抗原结合的高亲和力的基础上,减少异源性抗体的免疫原性,推动抗体人源化研发的进程。
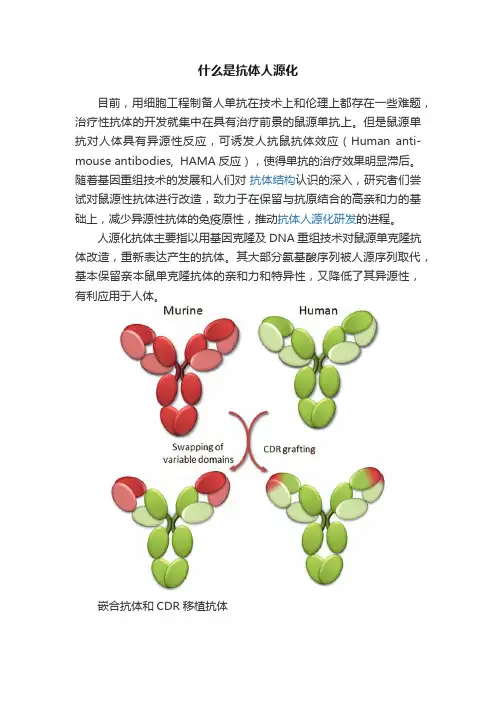
人源化抗体主要指以用基因克隆及DNA重组技术对鼠源单克隆抗体改造,重新表达产生的抗体。
其大部分氨基酸序列被人源序列取代,基本保留亲本鼠单克隆抗体的亲和力和特异性,又降低了其异源性,有利应用于人体。
嵌合抗体和CDR移植抗体根据人源化程度不同,单抗又可分为嵌合抗体(60%-70%人源化氨基酸序列)和CDR(complementarity-determining region)移植抗体(90%-95%人源化氨基酸序列)。
1、人-鼠嵌合抗体人-鼠嵌合抗体(chimeric antibody):第一代人源化抗体。
其是在基因水平上将鼠源单克隆抗体的V区和人抗体的C区(variable region, 可变区)连接,在合适的宿主细胞内表达可得到人-鼠嵌合抗体。
嵌合抗体用于人体所产生的HAMA反应比鼠源单抗明显减弱;另外,人源C区(constant region,恒定区)可更有效地介导人体一些免疫反应,如CDC(complement-dependent cytotoxicity, CDC, 依赖补体的细胞毒性作用),ADCC(antibody dependent cell mediated cytotoxicity, 抗体依赖的细胞介导的细胞毒性作用)。
2、CDR移植抗体嵌合抗体虽然可以部分解决异种蛋白的排斥问题,但由于其还含有鼠源V区,依然有可能会诱发HAMA反应,干扰抗体疗效,诱发超敏反应,在临床上其应用会受到一定限制。


人源化单克隆抗体研究进展人源化单克隆抗体是一种具有高度特异性和亲和力的生物药物,通过杂交瘤技术将鼠源单克隆抗体的可变区与人类抗体的恒定区进行交换,以减少免疫原性,提高治疗效果。
近年来,随着科技的不断进步,人源化单克隆抗体研究取得了显著的进展,为肿瘤、自身免疫性疾病、神经系统疾病等治疗领域提供了新的思路和方法。
研究现状:人源化单克隆抗体方法、成果与不足人源化单克隆抗体研究主要包括抗体库的建立、抗体筛选和优化、以及抗体生产等多个环节。
目前,研究人员已成功建立了多种人源化单克隆抗体,并应用于临床试验,取得了一定的疗效。
例如,针对肿瘤治疗的人源化单克隆抗体药物能够特异性地识别肿瘤细胞,并通过激活免疫反应来杀死肿瘤细胞。
然而,人源化单克隆抗体研究仍存在一定的不足之处,如抗体药物的免疫原性、毒副作用等问题需要进一步解决。
研究方法:人源化单克隆抗体研究实验设计与数据分析人源化单克隆抗体研究的实验设计主要包括建立人源化抗体库、筛选和优化抗体,以及进行药效和毒理试验等。
在实验过程中,需要采集和处理大量的实验数据,并进行深入的统计分析和比对,以获得抗体的最佳配对组合和最佳治疗剂量等参数。
成果和不足:人源化单克隆抗体研究的成果与不足人源化单克隆抗体研究在肿瘤、自身免疫性疾病、神经系统疾病等多个治疗领域取得了显著的成果。
例如,针对肿瘤治疗的人源化单克隆抗体药物已经成功应用于临床试验,并显示出较好的疗效和安全性。
在自身免疫性疾病和神经系统疾病治疗领域的人源化单克隆抗体药物也在研发和试验阶段。
然而,人源化单克隆抗体研究仍存在一定的不足之处,如抗体药物的免疫原性、毒副作用等问题需要进一步解决。
同时,抗体药物的生产成本较高,限制了其在临床上的广泛应用。
尽管人源化单克隆抗体研究取得了一定的成果,但仍存在许多问题需要进一步解决。
未来,研究人员需要进一步探索人源化单克隆抗体的作用机制和优化方法,以获得更高效、安全、低成本的药物。
同时,需要加强抗体药物的工艺研究,提高生产效率和降低生产成本。

抗体人源化是什么?
抗体人源化,是重组抗体(单克隆抗体)生产制备实验研究的重要组成部分。
所谓抗体人源化,为从鼠源性抗体往人源性抗体发展的过程。
百余年前,抗体与抗原特异性结合、抗体被动免疫特性等原理的揭示,开辟了疾病诊断的新途径。
而1975年单克隆抗体技术的问世,加快了这一方法的广泛应用。
初期,临床上使用的单抗多数为鼠源性单抗,由于人和小鼠的种属特异性,鼠源性抗体的使用存在种种限制。
鼠抗体虽然对靶抗原是特异的,可以与靶抗原特异性结合,但它不能激活相应的人体效应系统,如抗体依赖的细胞介导的细胞毒作用(ADCC)、补体依赖的细胞毒作用(CDC)等,从而无法正常的发生抗原-抗体反应;此外,鼠抗体作为外源蛋白进入人体,会使人体免疫系统产生应答,产生以鼠抗体作为抗原的特异性抗体,即产生人抗鼠抗体(human anti.mouse antibody,HAMA),通常异源蛋白在人体内会很快得到清除,半衰期很短。
由于鼠源性抗体在临床应用上存在种种限制,人们利用重组DNA技术对鼠源抗体进行人源化改造,使抗体人源化。


全人源化单抗(Fully Human Monoclonal Antibody)人源化 mAb 基本上解决了鼠抗体的最重要问题——免疫原性,但是人源化过程仍很繁复且费用昂贵,它需要广泛的计算机模型设计,即使如此,大量反复试验仍不可避免,因为要试验各种氨基酸置换以测定对目标选择性和结合亲和力的有害作用。
而全人源化单克隆抗体是指将人类抗体基因通过转基因或转染色体技术,将人类编码抗体的基因全部转移至基因工程改造的抗体基因缺失动物中,使动物表达人类抗体,达到抗体完全人源化的目的。
目前生产完全人源化抗体的方法主要包括抗体库技术和人源性抗体转基因小鼠技术两种。
抗体库技术抗体库技术包括噬菌体抗体库技术和核糖体展示技术。
噬菌体抗体库技术:是利用噬菌体表达外源基因的一项新技术,是将抗体重链可变区(VH)和轻链可变区(VL)基因与噬菌体的外壳蛋白Ⅲ(PⅢ)或外壳蛋白Ⅷ(PⅧ)基因随机重组,继而感染大肠杆菌,后经增殖并在噬菌体表面以抗体片段 Fab 或单链抗体可变区(ScFv)一外壳蛋白的融合蛋白形式表达。
这种噬菌体颗粒可以特异识别抗原,又能感染宿主菌进行再扩增,经过“吸附一洗脱一扩增”过程,就能筛选并富集特异性抗体。
所构建的抗体库称为全套抗体库,从中筛选到的抗体称为噬菌体抗体。
其最大特点是实现了直接将基因型和表型联系在一起,可以快速而高效地从大量克隆中筛选出表达特异性的抗体核糖体展示技术:将基因型和表型联系在一起,编码蛋白的 DNA 在体外进行转录与翻译,由于对 DNA 进行了特殊的加工与修饰,如去掉3′ 末端终止密码子,核糖体翻译到 mRNA 末端时,由于缺乏终止密码子,停留在 mRNA 的3′末端不脱离,从而形成蛋白质-核糖-2mRNA 三聚体,将目标蛋白特异性的配基固相化,如:固定在 ELISA 微孔或磁珠表面,含有目标蛋白的核糖体三聚体就可在ELISA 板孔中或磁珠上被筛选出,对筛选分离得到的复合物进行分解,释放出的 mRNA 进行逆转录酶链聚合反应(RT-PCR),PCR 产物进入下一轮循环,经过多次循环,最终可使目标蛋白和其编码的基因序列得到富集和分离。

人源化单克隆抗体的制备方法人源化单克隆抗体的制备方法1. 引言人源化单克隆抗体作为一种重要的生物药物,在医学诊断和治疗上发挥着重要的作用。
它们能够通过特异性结合目标物质,如病毒、癌细胞等,以识别、中和或破坏它们,具有广泛的应用前景。
人源化单克隆抗体通过将小鼠源的初始抗体进行改造和人源化,弥补了小鼠抗体在人体内产生反应的缺陷,进而提高了其临床应用的安全性和有效性。
2. 人源化单克隆抗体的制备方法2.1 选择目标抗原在制备人源化单克隆抗体之前,首先需要明确目标抗原。
这是指研究人员要制备对特定疾病或病原体具有高度特异性的抗体。
目标抗原的选择对于后续的实验设计和结果分析至关重要。
2.2 制备小鼠源的初始抗体为了制备人源化单克隆抗体,通常需要使用小鼠或其他动物作为初步制备抗体的源头。
研究人员通过免疫注射小鼠来激发其免疫系统产生特定抗原的抗体。
之后,从小鼠体内提取抗体进行初步鉴定和筛选。
2.3 克隆筛选通过克隆和筛选的过程,选择那些对目标抗原具有高度特异性的抗体克隆。
这一步骤的目的是从小鼠源的初始抗体中挑选出性能最佳的抗体克隆,为后续的人源化操作打下基础。
2.4 人源化改造人源化改造是将小鼠源的初始抗体转化为具有人源特性的抗体。
在这一步骤中,研究人员会通过基因工程技术将小鼠源抗体的大部分小鼠特异性区域替换为人源的同源区域,以减少人体对外源蛋白的免疫反应。
这可以通过重组DNA技术,将人源抗体的DNA序列嵌入到小鼠源抗体的DNA序列中,使其具有人源性。
2.5 生产和纯化经过人源化改造的抗体需要进行大规模的生产和纯化。
这通常通过基因工程的方法,在合适的细胞系中表达和生产抗体。
随后,使用各种纯化技术,如亲和层析、离子交换层析等,将抗体从混合物中纯化出来,以获得高纯度的人源化单克隆抗体。
3. 个人观点和理解人源化单克隆抗体的制备方法是一项复杂的过程,其中涉及到多个关键步骤和技术。
通过人源化改造,可以将小鼠源的初始抗体转化为具有人源特性的抗体,从而提高其在人体内的安全性和有效性。


人源化抗体:构建的核心原则与策略第一代人源化抗体是通过将鼠源McAb的可变区与人抗体的恒定区相结合,形成了一种嵌合抗体。
尽管这两部分在空间结构上相对独立,使得其独特的抗原亲和力得以保持,但由于嵌合抗体中仍然包含鼠源McAb的可变区,因此在应用时仍可能引发强烈的HAMA反应。
为了克服这一问题,科学家们进一步进行了改进,将鼠源McAb可变区中的相对保守的骨架区(Framework region,FR)替换为人的FR,而仅保留抗原结合部位的互补决定区(Complementarity-Determining region,CDR)。
这种改进使得抗体真正实现了人源化。
然而,FR作为抗体的脚手架,不仅为CDR提供了空间构象环境,有时还参与抗体结合位点正确构象的形成,甚至与抗原的结合。
因此,简单的CDR移植往往会导致原抗体亲和力的丧失或降低。
为了解决这一问题,目前科学家们已经探索出了四种策略,旨在优化FR和CDR之间的相互作用,以恢复或提高人源化抗体的亲和力。
这些策略的实施将有助于进一步提升抗体人源化的效果,为医学研究和治疗提供更多的可能性。
人源化抗体构建原则与策略1.模板替换在使用与鼠对应部分有较大同源性的人抗体FR替换鼠FR时,通常有两种途径可供选择。
第一种途径是采用同一个(或少数几个)具有已知晶体结构数据的人源抗体可变区框架(如VH中的NEW、KOL,VL中的REI等)作为基本模板,通过序列比较与分子模建,确定人、鼠间存在种源差异的氨基酸残基,特别是与鼠CDR密切作用的氨基酸残基,在替换过程中予以保留。
为了确保CDR的空间构象得以维持,需要特别关注原来抗体CDR下方的堆积残基以及周围的残基。
这种方法的优势在于,已知的人源FR晶体结构为残基替换提供了明确的信息。
然而,其不足之处在于可能难以保持鼠CDR的天然构象,从而可能导致抗体亲和力的降低或丧失。
第二条途径是在已有的抗体序列库中搜索与鼠McAb FR具有最大同源性的人源FR进行替换。


人源化抗体
人源化抗体主要指鼠源单克隆抗体通过基因克隆及DNA重组技术等进行改造,重新表达的抗体,其大部分氨基酸序列为人源序列取代,基本保留亲本鼠单克隆抗体的亲和力和特异性,同时又降低了其异源性,有利应用于人体。
然而,即使通过嵌合抗体技术把C区替换,人源化抗体V区的互补决定区(CDR)和框架区(FR)也仍有可能诱导相当强的抗体反应。
因此,研究者开始着手将部分CDR和FR区也改造为人抗体序列,以便能进一步提高抗体的人源化程度,降低药物抗体反应发生的可能。
经过数年的研究和改进,人们已经创建并完善了以重构抗体、表面重塑抗体、去免疫化抗体和链替换抗体等为代表的多种人源化抗体技术。
人源化抗体技术
重构抗体
重构抗体是由异源抗体中和抗原结合相关的残基与人抗体重新剪接构建的抗体,包括互补决定区移植、部分互补决定区移植和特定决定区转移。
构建重构抗体的流程:①克隆分析亲本鼠单抗的V区基因,确定CDR和FR区;②通过数据库检索比对及辅助计算机分子模拟等,找出有最大同源性的人FR 区模板;③确定需要保留和改变的关键残基,经基因合成、真核表达、检测实际结合效果后,对需要保留和改变的关键残基进行相应的修正;④最终获得高亲和力的、具有与亲本鼠单抗相同抗原结合表位的人源化抗体。
表面重塑抗体
表面重塑抗体是通过对异源抗体表面氨基酸残基进行人源化改造而获得的人源化抗体。
表面重塑抗体的库构建流程:①首先在结构数据库中寻找鼠源的最大同源性蛋白,利用相应的软件并采用分子三维结构分析的方式确定表面残基的位置;②在公用数据库中寻找最大同源性的人抗体序列,在相应的表面残基位置上尝试替换为相应的人抗体残基(替换中要兼顾考虑被替换残基的侧链匹配情况和与CDR是否在空间上紧邻);③确定替换后的残基种类,即可采用定点突变或基因合成等方法获得
人源化后的表面重塑抗体V区基因;④克隆入相应的表达载体进行表达,并分析改造后的抗原结合情况。
去免疫化抗体
去免疫化抗体的构建与前面介绍的其他人源化抗体技术类似,其技术流程主要分为以下5个步骤:①建立亲本鼠单抗的三位结构分子模型,通常需要在最大同源性已知三维结构抗体的三维结构模型的引导下,由相应的计算机软件完成;②利用相关的公用数据库,来寻找鼠单抗序列可能的人T细胞识别表位,也允许同时通过体外试验来确定可能的人T细胞识别表位;③通过以人胚系VH和VL基因为模板并与之比对,结合已有的不破坏原抗体结构和抗原结合位点的人源化抗体改造规律,确定需要被替换的残基;④通过分子模拟检验这些被替换的残基;⑤表达改造后的抗体,并检验改造的效果。
链替换抗体
链替换抗体严格意义上属于一种全人源抗体,但由于该技术仍然需要鼠单抗为源头进行构建,因此这里将其作为一类特殊的人源化抗体进行介绍。
前面介绍的重构抗体技术和表面重塑抗体技术本质上都是在异源单抗的序列中引入不同程度的人抗体序列,以期减少改造后抗体免疫原性。
而链替换抗体是在定向选择技术的指导下,逐步将异源抗体的轻、重链完全替换为人抗体序列,最终获得与亲本鼠单抗识别结合同一抗原的全人抗体。
经典的链替换抗体库技术:①原始的亲本鼠单抗V区基因将被克隆并用于构建嵌合的Fab或scFv等可应用于抗体库技术的抗体;②构建含人抗体轻链的杂合型轻链抗体库;③经过筛选获得含亲本鼠单抗重链和人抗体轻链的杂合型抗体;④重链进一步被替换,构建成含人抗体重链和被选定的目标人抗体轻链的全人抗体库;⑤再经筛选过程,将得到与原亲本鼠单抗结合识别同一抗原的全人抗体基因。
人源化抗体的临床应用
1.在自身免疫性疾病方面的应用
在对自身免疫疾病的治疗中,人源化的单抗药物通过清除激活的细胞,阻滞其功能,或将升高的促炎细胞因子水平降至正常水平而抑制过度的免疫病理学反应。
现有的
研究表明,抗体对系统性红斑狼疮、多发性硬化、风湿性关节炎和溃疡性结肠炎都有良好的治疗效果,并且随着技术发展将会应用于更多疾病的治疗。
2.在肿瘤治疗方面的应用
一些人源化的单克隆抗体的研制,主要是针对那些与肿瘤发生、发展相关的靶分子,如治疗非霍奇金淋巴瘤的抗CD20的嵌合抗体Ritu以及针对肿瘤靶位VEGF、CD33等研发的人员化抗体。
这些靶分子在正常细胞有表达,但在部分肿瘤细胞中高/低表达,因此可作为肿瘤特异的标志物。
3.在器官移植中的应用
将一些研制的人源化单抗应用于器官移植,可减轻移植后发生的排斥反应,以保护移植器官的功能,如治疗性抗体类药物抗CD3单抗即被用于心脏、肾脏和肝脏移植排斥的逆转。