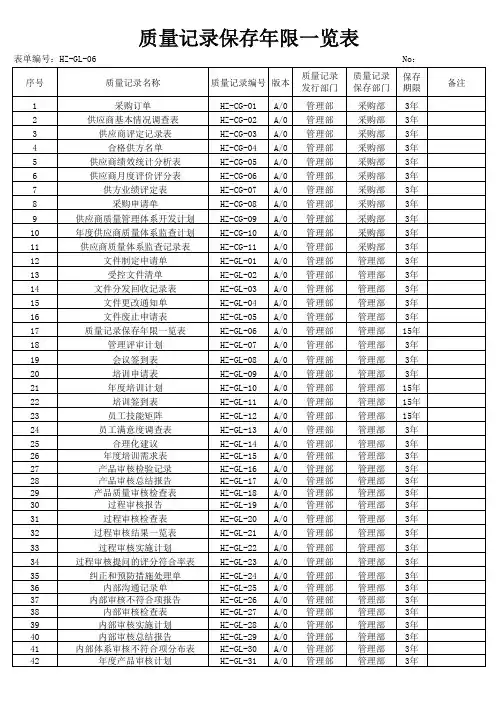
质量记录保存年限表
- 格式:doc
- 大小:49.50 KB
- 文档页数:2

1.目的
加强质量、环境记录的控制,保证记录的有效性。
2.适用范围
本标准适用于程序文件所涉及的各类质量、环境记录。
3.权限
各有关部门按本规定对质量、环境记录进行分类、装订、造册并保存。
4.管理重点
4.1 记录的分类
4.1.1 质量记录按性质分为证明体系有效运行和产品符合规定要求两大类质量记录。
4.1.2 环境记录是证明环境符合规定要求的记录。
4.1.3 按保存期限分为A级、B级、C级三类。
a) A级(长期):涉及关键质量、环境特性且对质量、环境跟踪有重要证实作用或对公司的生产、经营、管理有长远意义的。
保存期15年以上(必要时,或顾客提出要求时,可永久保存);
b) B级(中期):涉及重要质量、环境特性且有跟踪必要或对公司的生产、经营、管理有一定指导意义的。
保存期10年以上;
c) C级(短期):一般性记录。
一般保存期5年以上。
4.2 记录的保存部门
4.2.1 附表中列出的保存部门是管理手册中规定的主要职责部门。
4.2.2 同一种记录除了主要指责部门外,相关部门也应该加以保存。
4.3 记录保存期限
附表中所列部门应按表中规定期限对记录进行保存。
5 检查与考核
由ISO室每年检查考核一次。
6.本程序更改记录表。


质量记录保存期限规定质量记录保存期限规定为了确保产品质量的可追溯性和监督管理的有效性,许多国家和地区都制定了质量记录保存期限规定。
这种规定旨在要求企业在一定期限内保留相关质量记录,以备查证和监督使用。
下面将介绍一种常见的质量记录保存期限规定。
根据相关法律法规和相关行业标准,质量记录保存期限一般分为两个方面,即一般质量记录和特殊质量记录。
对于一般质量记录,即指产品质量检测、检验、检疫等日常工作中产生的一般质量记录,保存期限一般为两年。
这些记录主要涉及产品的样品编号、检测方法、检测结果、评定标准等重要信息,是产品质量可追溯性的重要依据。
根据规定,企业需要将这些记录按照一定的分类和编号方式保存,并至少保存两年。
这样一来,无论是供货商对原料和成品进行质量追溯,还是监督部门对企业质量管理的抽查,都能够通过这些记录进行查证。
对于特殊质量记录,即指一些重要的质量事件所产生的记录,保存期限一般为五年。
这些记录主要包括产品质量事故的调查报告、产品召回记录、质量投诉处理记录等重要信息。
这些记录的保存期限较长,是为了确保相关质量事件能够长期监督和追溯。
在保存这些记录时,企业需要特别注明相关事件的起止日期、责任人和处理结果,并将这些记录归档保存,以备后续参考和查证。
除了一般质量记录和特殊质量记录,对于一些特殊情况下产生的质量记录,保存期限也有相应规定。
比如,对于产品的质量问题导致的法律案件,相关质量记录的保存期限延长至案件结案之后。
这种规定是为了确保相关质量记录可以供司法机关和相关当事人查证和依据法律进行相应的处理。
质量记录保存期限的规定不仅对于企业的质量管理和监督有重要意义,也对于消费者的权益保护起到了积极作用。
消费者通过查询质量记录可以了解产品质量的历史信息,从而判断产品是否符合标准和要求。
同时,监督部门和司法机关也可以通过质量记录查证企业的质量管理和法律遵从程度,以便采取相应的监管措施和制裁。
总之,质量记录保存期限规定是一个重要的质量管理和监督工具。
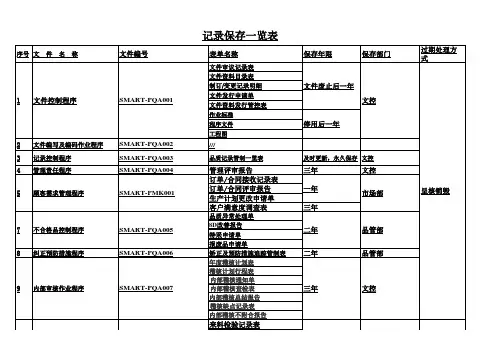
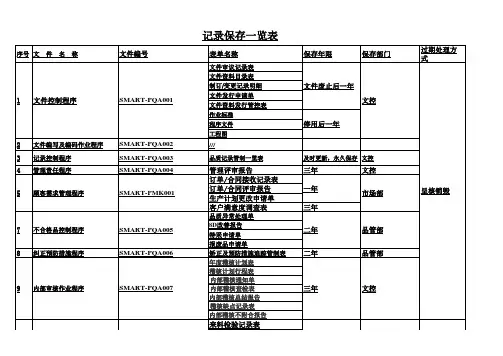
记录保存一览表
目检
3
目检不良分析表4SMT ( )时段日报表1测试不良记录表2测试点检报表1维修日报表2烙铁温度&漏电点检表1加班申请表2月加班统计表3
请购单6内部联络单7流转单1车间温度记录表2超声波夹具清洗记录表3静电皮点检记录表4静电环测试记录表1每日工作汇报记录4生产效率达成日报表5生产日报表6SMT 生产时段日报表手摆
1手摆机种追踪明细1设备保养点检记录表—JUKI 贴片机2机器设备一级保养卡--OmniExcel 3机器设备一级保养卡—LF-30884机器设备一级保养卡—MPM UP2000呈核销毁
文员报表环境生产汇总保养目检测试修理。


药品各种记录、文件保存时限1.保存至超过药品有效期一年,但不得少于三年(1)药品生产、经营企业采购药品时按规定留存的资料和销售凭证。
(药品流通监督管理办法,P184,12条)(2)医疗机构药品购进记录。
(药品流通监督管理办法,P185,25条)(3)医疗机构药品验收记录必须保存至超过药品有效期1年,但不得少于3年.(医疗机构药品监督管理办法(试行),P198,10条)2.超过有效期两年(1)疾病预防控制机构、接种单位购进疫苗时的证明文件:超过疫苗有效期两年。
(疫苗流通和预防接种管理条例,P103,17条)(2)疫苗生产企业、疫苗批发企业的购销记录:超过疫苗有效期两年.(18条)(3)疾病预防控制机构的购进、分发、供应记录:超过疫苗有效期两年。
(18条)3.一年事项(1)托运或自行运输麻醉、一类精神药申领的运输证明有效期1年。
(麻醉药品和精神药品管理条例,P83,52条)(2)医疗机构制剂使用过程中发现不良反应,保留的病历和有关检验、检查报告单等原始记录至少一年备查。
(医疗机构制剂配制质量管理规范(试行),P210,65条)(3)《基本医疗保险药品目录》新药增补工作每年进行一次。
(城镇职工基本医疗保险用药范围管理暂行办法,P238,11条)(4)《中国药典》增补本,原则上每年一版。
(药品标准,P22)(5)社会保险经办机构与定点零售药店签订的协议有效期一般为1年。
(城镇职工基本医疗保险定点零售药店管理暂行办法,P236,8条)4。
两年事项(1)医疗机构有关配制制剂的记录和质量检验记录应完整归档,至少保存2年备查。
(医疗机构制剂配制质量管理规范,P209,52条)(2)《基本医疗保险药品目录》每两年调整一次.(城镇职工基本医疗保险用药范围管理暂行办法,P238,11条)(3)定点批发企业的条件:单位及工作人员2年内没有违反有关禁毒的法律、行政法规的行为。
(麻醉药品和精神药品管理条例,P80,23条)(4)《药品广告审查表》原件保存2年.(药品广告审查办法,P248,17条)(5)医疗机构调整抗菌药物供应目录的周期原则上为2年,最短不得少于1年。

质量记录分类及保存期限规定
1 目的
加强质量记录的控制,保证记录的有效性。
2 适用范围
本标准适用于程序文件所涉及的各类质量记录。
3 管理职责
各有关部门按本规定对质量记录进行分类、装订、造册并保存。
4 工作程序
4.1 质量记录的分类
4.1.1 质量记录按性质分为证明质量体系有效运行和产品符合规定要求两大类质量记录。
4.1.2 按保存期限分为永久、十年、五年、三年四类。
4.2 质量记录的保存部门
4.2.1 附表中列出的保存部门是质量手册中规定的主要职责部门。
4.2.2 同一种质量记录除了主要职责部门外,相关的部门也应该加以保存。
4. 3 质量记录保存期限
4.3.1 附表中所列部门应按表中规定期限对质量记录进行保存。
4.3.2 同一种质量记录除了主要职责部门按规定保存外,相关部门也应按附表规定进行保存。
见附录A:《质量记录保存期限表》
5 检查与考核
由体系中心每年检查考核一次。
《质量记录分类及保存期限规定》。

药品各种记录、文件保存时限1.保存至超过药品有效期一年,但不得少于三年(1)药品生产、经营企业采购药品时按规定留存的资料和销售凭证。
(药品流通监督管理办法,P184,12条)(2)医疗机构药品购进记录。
(药品流通监督管理办法,P185,25条)(3)医疗机构药品验收记录必须保存至超过药品有效期1年,但不得少于3年。
(医疗机构药品监督管理办法(试行),P198,10条)2.超过有效期两年(1)疾病预防控制机构、接种单位购进疫苗时的证明文件:超过疫苗有效期两年。
(疫苗流通和预防接种管理条例,P103,17条)(2)疫苗生产企业、疫苗批发企业的购销记录:超过疫苗有效期两年。
(18条)(3)疾病预防控制机构的购进、分发、供应记录:超过疫苗有效期两年。
(18条)3.一年事项(1)托运或自行运输麻醉、一类精神药申领的运输证明有效期1年。
(麻醉药品和精神药品管理条例,P83,52条)(2)医疗机构制剂使用过程中发现不良反应,保留的病历和有关检验、检查报告单等原始记录至少一年备查。
(医疗机构制剂配制质量管理规范(试行),P210,65条)(3)《基本医疗保险药品目录》新药增补工作每年进行一次。
(城镇职工基本医疗保险用药范围管理暂行办法,P238,11条)(4)《中国药典》增补本,原则上每年一版。
(药品标准,P22)(5)社会保险经办机构与定点零售药店签订的协议有效期一般为1年。
(城镇职工基本医疗保险定点零售药店管理暂行办法,P236,8条)4.两年事项(1)医疗机构有关配制制剂的记录和质量检验记录应完整归档,至少保存2年备查。
(医疗机构制剂配制质量管理规范,P209,52条)(2)《基本医疗保险药品目录》每两年调整一次。
(城镇职工基本医疗保险用药范围管理暂行办法,P238,11条)(3)定点批发企业的条件:单位及工作人员2年内没有违反有关禁毒的法律、行政法规的行为。
(麻醉药品和精神药品管理条例,P80,23条)(4)《药品广告审查表》原件保存2年。

药品各种记录文件保存时限药品各种记录、文件保存时限1.保存至超过药品有效期一年,但不得少于三年(1)药品生产、经营企业采购药品时按规定留存的资料和销售凭证。
(药品流通监督管理办法,P184,12条)(2)医疗机构药品购进记录。
(药品流通监督管理办法,P185,25条)(3)医疗机构药品验收记录必须保存至超过药品有效期1年,但不得少于3年。
(医疗机构药品监督管理办法(试行),P198,10条)2.超过有效期两年(1)疾病预防控制机构、接种单位购进疫苗时的证明文件:超过疫苗有效期两年。
(疫苗流通和预防接种管理条例,P103,17条)(2)疫苗生产企业、疫苗批发企业的购销记录:超过疫苗有效期两年。
(18条)(3)疾病预防控制机构的购进、分发、供应记录:超过疫苗有效期两年。
(18条)3.一年事项(1)托运或自行运输麻醉、一类精神药申领的运输证明有效期1年。
(麻醉药品和精神药品管理条例,P83,52条)(2)医疗机构制剂使用过程中发现不良反应,保留的病历和有关检验、检查报告单等原始记录至少一年备查。
(医疗机构制剂配制质量管理规范(试行),P210,65条)(3)《基本医疗保险药品目录》新药增补工作每年进行一次。
(城镇职工基本医疗保险用药范围管理暂行办法,P238,11条)(4)《中国药典》增补本,原则上每年一版。
(药品标准,P22)(5)社会保险经办机构与定点零售药店签订的协议有效期一般为1年。
(城镇职工基本医疗保险定点零售药店管理暂行办法,P236,8条)4.两年事项(1)医疗机构有关配制制剂的记录和质量检验记录应完整归档,至少保存2年备查。
(医疗机构制剂配制质量管理规范,P209,52条)(2)《基本医疗保险药品目录》每两年调整一次。
(城镇职工基本医疗保险用药范围管理暂行办法,P238,11条)(3)定点批发企业的条件:单位及工作人员2年内没有违反有关禁毒的法律、行政法规的行为。
(麻醉药品和精神药品管理条例,P80,23条)(4)《药品广告审查表》原件保存2年。
药品各种记录、文件保存时限1.保存至超过药品有效期一年,但不得少于三年(1)药品生产、经营企业采购药品时按规定留存的资料和销售凭证。
(药品流通监督管理办法,P184,12条)(2)医疗机构药品购进记录。
(药品流通监督管理办法,P185,25条)(3)医疗机构药品验收记录必须保存至超过药品有效期1年,但不得少于3年。
(医疗机构药品监督管理办法(试行),P198,10条)2.超过有效期两年(1)疾病预防控制机构、接种单位购进疫苗时的证明文件:超过疫苗有效期两年。
(疫苗流通和预防接种管理条例,P103,17条)(2)疫苗生产企业、疫苗批发企业的购销记录:超过疫苗有效期两年。
(18条)(3)疾病预防控制机构的购进、分发、供应记录:超过疫苗有效期两年。
(18条)3.一年事项(1)托运或自行运输麻醉、一类精神药申领的运输证明有效期1年。
(麻醉药品和精神药品管理条例,P83,52条)(2)医疗机构制剂使用过程中发现不良反应,保留的病历和有关检验、检查报告单等原始记录至少一年备查。
(医疗机构制剂配制质量管理规范(试行),P210,65条)(3)《基本医疗保险药品目录》新药增补工作每年进行一次。
(城镇职工基本医疗保险用药范围管理暂行办法,P238,11条)(4)《中国药典》增补本,原则上每年一版。
(药品标准,P22)(5)社会保险经办机构与定点零售药店签订的协议有效期一般为1年。
(城镇职工基本医疗保险定点零售药店管理暂行办法,P236,8条)4.两年事项(1)医疗机构有关配制制剂的记录和质量检验记录应完整归档,至少保存2年备查。
(医疗机构制剂配制质量管理规范,P209,52条)(2)《基本医疗保险药品目录》每两年调整一次。
(城镇职工基本医疗保险用药范围管理暂行办法,P238,11条)(3)定点批发企业的条件:单位及工作人员2年内没有违反有关禁毒的法律、行政法规的行为。
(麻醉药品和精神药品管理条例,P80,23条)(4)《药品广告审查表》原件保存2年。