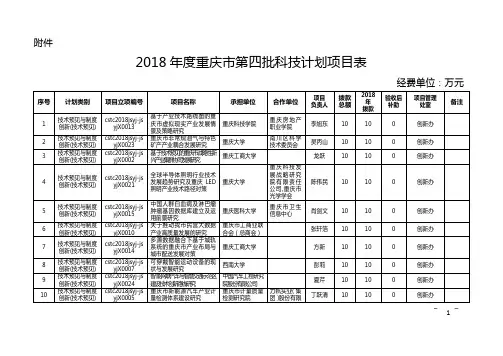
2018年重庆技术预见与制度创新专项项目拟立项清单
- 格式:doc
- 大小:194.00 KB
- 文档页数:5

重庆市科学技术局关于印发重庆市科研项目管理办法的通知正文:---------------------------------------------------------------------------------------------------------------------------------------------------- 重庆市科学技术局关于印发重庆市科研项目管理办法的通知渝科局发〔2019〕11号各区县科技行政主管部门,在渝高等学校、科研院所,有关单位:《重庆市科研项目管理办法》已经重庆市科学技术局2018年第5次局长办公会审议通过,现予印发。
重庆市科学技术局2019年2月15日重庆市科研项目管理办法第一章总则第一条为贯彻落实《国务院关于优化科研管理提升科研绩效若干措施的通知》(国发〔2018〕25号)文件精神,进一步规范科研项目管理,根据中共中央办公厅、国务院办公厅《关于进一步完善中央财政科研项目资金管理等政策的若干意见》和《关于深化项目评审、人才评价、机构评估改革的意见》,以及市委办公厅、市政府办公厅《关于进一步完善我市财政科研项目资金管理等政策的实施意见》有关要求,制定本办法。
第二条本办法所称重庆市科研项目(以下简称项目)是指市科学技术局(以下简称市科技局)根据全市经济社会发展和科技创新需要,利用市级财政科技发展资金资助的科学技术研究开发活动。
第三条本办法坚持“权责清晰、配置科学、管理透明、程序规范、监督有力”的原则,适用于项目申报、立项、实施、结题等组织与管理工作。
第二章项目管理与实施主体第四条项目的组织实施与管理由市科技局、项目承担单位、项目组成员、科技咨询专家、第三方机构共同完成。
项目承担单位、项目组成员和科技咨询专家应当在“重庆市科技管理信息系统”(以下简称科技管理系统)中注册备案,且达到社会信用等级和科研信用等级的相关要求。
申报项目的企业原则上应符合重庆市科技型企业标准,并在“重庆市科技型企业管理信息系统”中完成入库注册。

重庆市科学技术局关于印发《重庆市科研项目管理办法》的通知(渝科局发〔2019〕11号)各区县科技行政主管部门,在渝高等学校、科研院所,有关单位:《重庆市科研项目管理办法》已经重庆市科学技术局2018年第5次局长办公会审议通过,现予印发。
重庆市科学技术局2019年2月15日重庆市科研项目管理办法第一章总则第一条为贯彻落实《国务院关于优化科研管理提升科研绩效若干措施的通知》(国发〔2018〕25号)文件精神,进一步规范科研项目管理,根据中共中央办公厅、国务院办公厅《关于进一步完善中央财政科研项目资金管理等政策的若干意见》和《关于深化项目评审、人才评价、机构评估改革的意见》,以及市委办公厅、市政府办公厅《关于进一步完善我市财政科研项目资金管理等政策的实施意见》有关要求,制定本办法。
第二条本办法所称重庆市科研项目(以下简称项目)是指市科学技术局(以下简称市科技局)根据全市经济社会发展和科技创新需要,利用市级财政科技发展资金资助的科学技术研究开发活动。
第三条本办法坚持“权责清晰、配置科学、管理透明、程序规范、监督有力”的原则,适用于项目申报、立项、实施、结题等组织与管理工作。
第二章项目管理与实施主体第四条项目的组织实施与管理由市科技局、项目承担单位、项目组成员、科技咨询专家、第三方机构共同完成。
项目承担单位、项目组成员和科技咨询专家应当在“重庆市科技管理信息系统”(以下简称科技管理系统)中注册备案,且达到社会信用等级和科研信用等级的相关要求。
申报项目的企业原则上应符合重庆市科技型企业标准,并在“重庆市科技型企业管理信息系统”中完成入库注册。
第五条市科技局负责统筹制定项目管理制度规范,统筹发布项目指南、配置项目经费和下达立项计划,统筹组织第三方机构的遴选、管理、监督,统筹实施项目经费的使用监督、绩效评价等项目管理重大事项,统筹推进科研诚信、科技报告、科学数据等项目综合监管体系建设。
第六条项目承担单位应当是具有独立法人资格的企业、高等学校、科研院所等单位或其他具有科研和科技服务能力的机构,分为项目牵头单位(含独立申报与实施项目的单位)和项目参与单位。

药物临床试验中生物样本管理常见问题及措施建议Δ谢江川*,谢林利,马攀,潘辛梅,曹丽亚,张馨,陈勇川 #(陆军军医大学第一附属医院药学部,重庆 400038)中图分类号 R 951 文献标志码 A 文章编号 1001-0408(2024)05-0524-05DOI 10.6039/j.issn.1001-0408.2024.05.03摘要 目的 为完善药物临床试验生物样本管理相关标准操作规程(SOP )及生物样本的管理提供参考。
方法 以《药物临床试验质量管理规范》《药物临床试验数据现场核查要点》《人类遗传资源管理条例实施细则》《药物临床试验机构资格认定检查细则》为参照,根据笔者临床试验项目的管理经验,通过统计质控表、申办方上报的方案偏离(PD ),对2016年7月-2023年5月笔者负责管理的药物临床试验项目在生物样本管理方面出现的不规范操作进行分析,并提出生物样本规范化管理的建议。
结果与结论 纳入了60项药物临床试验项目,共发现生物样本管理相关不规范项101条。
生物样本采集、保存、处理为生物样本管理不规范操作发生率最高的环节,不规范项条数分别占总条数的37.62%、25.74%、21.78%。
规范生物样本的管理需多方努力,比如机构办及伦理委员会在项目立项时对试验方案、知情同意书、遗传办申请书中涉及生物样本采集及处理的一致性等进行仔细审核,项目启动时机构办质控员应关注授权的人员是否出席并参加培训,项目开展阶段主要研究者、研究护士、采集人员、处理人员、运送人员、中心实验室相关人员、机构办质控员是否各司其职。
在此基础上,生物样本管理各参与方应做好有效沟通,发现问题及时上报,并针对关键环节进行专项学习。
关键词 药物临床试验;生物样本;生物样本管理Common problems and suggestions of biological sample management in drug clinical trials XIE Jiangchuan ,XIE Linli ,MA Pan ,PAN Xinmei ,CAO Liya ,ZHANG Xin ,CHEN Yongchuan (Dept. of Pharmacy , the First Affiliated Hospital of Army Medical University ,Chongqing 400038,China )ABSTRACTOBJECTIVE To provide a reference for improving the relevant standard operating procedures (SOP ) and biologicalsample management in drug clinical trials. METHODS According to Good Clinical Practice , Data On-site Verification Points of Drugs Clinical Trials , Human Genetic Resources Management Regulations Implementation Rules , Qualification Examination Rules of Drug Clinical Trials Institution , based on the experience of managing clinical trials programs , the irregularities in biological samples management were analyzed by using statistical quality control tables and protocol deviation (PD ) reported by sponsors , in the context of the quality control of drug clinical trials projects managed by the author from July 2016 to May 2023. The precautions in various aspects of sample management were put forward. RESULTS & CONCLUSIONS A total of 101 biospecimen-related irregularities were found in the 60 drug clinical trials projects. Biological sample collection , preservation , and handling were the aspects with the highest incidence of irregular operations in biological sample management , accounting for 37.62%, 25.74%, and 21.78%, respectively. Regulating the management of biospecimens requires multiple efforts. The institutional office and the ethics committee carefully reviewed the consistency of the protocols , informed consent , and genetic office application involving biospecimen collection and handling when the project was initiated. Institutional office quality controllers should pay attention to the attendance and training of authorized personnel at project initiation. The principal investigator , research nurse , collector , handler , transporter , relevant personnel of the central laboratory , and institutional office quality controller have their roles during the project implementation phase. On this basis , all parties involved in the management of biological samples should do a good job of effective communication , find problems and report them in time , and conduct special studies on key aspects.KEYWORDSdrug clinical trials ; biological sample ; biological sample management生物样本(如血浆、血清、尿液、粪便、组织和细胞等)的管理是药物临床试验中非常重要的环节,涵盖生物样本采集、保存、运输、检测以及检测后的处理等,其不仅影响试验的最终结果,而且生物样本及其信息的安全还关系着种族基因信息保密、公众健康、国家安全和社会公共利益[1]。

加快建设西部陆海新通道,是以习近平同志为核心的党中央作出的重大战略部署,是《中华人民共和国国民经济和社会发展第十四个五年规划和2035年远景目标纲要》确定的重大工程,是党的二十大提出的重要战略任务。
建设西部陆海新通道,为重庆向南出海、加快建设内陆开放高地打开了新大门,为西部地区加快融入全球经济开拓了新空间,是新时代新征程新重庆建设的重大任务[1]。
重庆市与通道沿线尤其是同属《区域全面经济伙伴关系协定》(Regional Comprehensive Economic Partnership ,RCEP )框架下的东盟国家,农产品贸易互补性强、农业跨国投资与合作潜力大、“三农”发展经验交流互鉴的意义深远,因此,重庆市“三农”在通道建设中承担重要角色。
建设西部陆海新通道,为重庆市“三农”发展带来重大机遇,也提出更高要求。
如何在加快建设西部陆海新通道中展现“三农”担当,是重庆市共建共享西部陆海新通道迫切需要研究的现实问题。
1文献梳理与问题提出西部陆海新通道,是在共建“一带一路”的框架下,以重庆市为运营和组织中心,中国西部12个省(区、市)与海南省、广东省湛江市、湖南省怀化市等共同打造的连接“一带”和“一路”的陆海联动大通道、国际物流大通道、国际贸易大通道和开放大通道。
通道海铁联运主干线以重庆市为陆路运营中心、以钦州港为陆海运营节点、以新加坡港为海运终点,连通西部昆明市、成都市、兰州市、西安市、西宁市、乌鲁木齐市等地及中西亚、中东欧各国,是强化中国与通道共建国家经贸合作,维护全球供应链稳定的综合性国际大通道[2]。
在复杂严峻的国内外形势下,党的二十大报告提出“加快建设西部陆海新通道”,收稿日期:2023-07-12基金项目:重庆市科学技术局技术预见与制度创新专项“重庆市促进预制菜产业高质量发展的政策研究”(CSTB2022TFII-DIX0074);西南大学社科中央高校基本科研业务费一般项目“新型农业经营主体的经营风险与市场化风险管理工具运用研究”(SWU1909418);重庆市财政局“‘一带一路’关键技术合作交流专项”(KYLX20231000217)。

重庆市发展和改革委员会关于组织申报2018年高技术产业技术开发专项的通知文章属性•【制定机关】重庆市发展和改革委员会•【公布日期】2018.10.22•【字号】渝发改技〔2018〕1243号•【施行日期】2018.10.22•【效力等级】地方规范性文件•【时效性】现行有效•【主题分类】科学技术综合规定正文重庆市发展和改革委员会关于组织申报2018年高技术产业技术开发专项的通知有关区县发展改革委,开发区投资主管部门:为促进大数据智能化产业发展,培育经济发展新动力,推动大数据智能化技术研发与实体经济深度融合,经研究,拟组织实施2018年大数据智能化产业技术开发专项。
请组织2018年大数据智能化领域认定的市级工程研究中心承担单位进行申报。
现将专项有关工作通知如下:一、专项支持重点专项重点支持2018年大数据智能化领域认定的市级工程研究中心,在大数据、人工智能、物联网等关键核心技术和应用技术领域开展的共性技术研发、新产品开发等产业技术研发项目。
二、专项实施要求(一)申请专项项目应具备以下基本条件:1﹒健全的财务核算与管理体系,建立统计报表制度;2﹒具有高水平的研发团队和经营团队;3﹒落实场地、资金等项目建设条件;4﹒拥有较高水平的科研成果、知识产权明晰;5﹒研发项目内容符合《重庆市以大数据智能化为引领的创新驱动发展战略行动计划(2018—2020)》中明确的智能化产业、智能化应用和技术研发的主要方向,能为我市大数据智能化产业发展提供技术支撑,并有显著的经济和社会效益;6﹒纳税信用良好,无违纪、违规、违法行为;7﹒项目未获取过国家和市级财政资金支持;8﹒项目应为已经开展研究或明确今年内启动研究,且在近3年完成研究任务并推动成果转化。
(二)符合支持重点和有关条件的项目单位,按照《重庆市高技术产业发展项目管理暂行办法》(渝财教〔2009〕227号)和《重庆市高技术产业技术研究与开发资金管理办法》要求,编制产业技术开发项目资金申请报告(提纲见附件2),报送至所在区县发展改革部门、开发区投资主管部门。
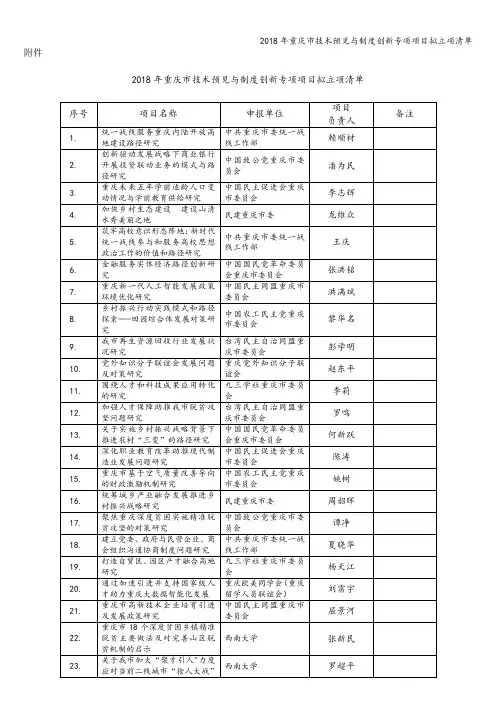
关于申报2020年技术预见与制度创新专项项目的通知(2020)为做好2020年度技术预见与制度创新专项项目申报工作,结合年度工作安排,现将有关事项通知:一、内涵定位重庆市技术预见与制度创新专项分为技术预见、制度创新两类项目。
技术预见类项目旨在通过对科学、技术、经济和社会在未来一段时间内进行整体化预测,系统地选择那些具有战略意义的研究领域、关键技术和通用技术,发挥市场对资源配置的决定性作用,实现经济与社会利益最大化。
制度创新类项目旨在针对决策和管理实践中提出的复杂性、系统性课题,综合运用自然科学、社会科学和工程技术的多门类、多学科知识,运用定性和定量相结合的系统分析和论证手段,进行跨学科、多层次的综合性研究,提供决策咨询服务。
二、项目类别2020年技术预见与制度创新专项项目类别为:技术预见类项目和制度创新类项目。
组织方式:公开申报和定向委托(择优)。
其中,公开申报按照申报指南方向自主选题申报,定向委托(择优)由市科技局根据科技创新决策需要直接明确委托(择优)单位。
三、重点支持方向及说明(一)公开申报1. 技术预见类项目支持方向:主要围绕新能源汽车、智能网联汽车、智能制造、云计算大数据、集成电路、机器人、区块链、高端装备、通用航空、仪器仪表、新材料、工业互联网、物联网、传感器、智能终端、虚拟现实、大健康、环保装备、应急装备、智慧城市、畜禽种业、主要农经作物种业等领域,开展“十四五”时期技术创新重点方向研究。
研究要求:调查摸清相关领域技术创新基本情况,梳理总结技术创新现状及问题,研究技术创新方向、重点和路径,提出技术创新的对策建议,为决策部门制定技术创新规划、技术创新方案提供决策参考。
支持对象:主要支持市级产业技术创新战略联盟牵头单位组织联盟成员单位开展技术预见研究。
成果形式:技术预见报告、产业技术发展规划、产业技术路线图等,以及2000字左右的技术创新重点方向或对策建议。
实施周期及资助强度:该类项目原则上按面上项目申报,实施周期为半年,资助强度为10万元/项。
项目类别:□技术预见□制度创新申报类别:□公开申报□定向委托重庆市技术预见与制度创新专项项目申报书(下载版仅用于预填报)重庆市科学技术局二0二0年一月制填报须知1、单位和个人信息注册。
项目申报单位、项目负责人和项目组成员应当事先在“重庆市科技管理信息系统”中注册备案,且达到社会信用等级和科研信用等级的相关要求。
2、科技型企业入库注册。
申报项目的企业原则上应符合重庆市科技型企业标准,无严重违法失信和不良科研诚信记录,并在“重庆市科技型企业管理信息系统”完成入库注册。
3、科研诚信承诺。
项目负责人和项目牵头单位须出具“科研诚信承诺书”,盖章后作为附件上传,承诺事项纳入科研信用管理。
4、合作协议。
有合作单位的项目,必须签订“科研项目合作协议”,签章后作为附件上传。
5、提交确认。
项目提交前请项目负责人和项目承担单位务必检查确认,一旦提交至“重庆市科技管理信息系统”,将不予修改、退回。
6、纸质申报书报送。
项目提交审核后应通过“重庆市科技管理信息系统”在线打印具有数字指纹的申报书正式版,完善相关签字、签章,并按申报通知要求报送,才视为有效申报。
二、项目指标(一)约束性考核指标(技术预见类所有项目必填)1.(□技术预见综合报告;或□产业技术研究报告;或□产业技术路线图;或□产业技术规划)。
其主要内容包括等方面。
(划横线部分表述在300字以内) 2.产业政策建议或研究报告摘要__份。
---------------------------------------------------------------- (一)约束性考核指标(制度创新类所有项目必填)1.研究报告份,其主要内容包括等方面。
(划横线部分表述在300字以内)2.决策咨询建议或研究报告摘要__份。
(二)选择性考核指标(技术预见类项目,至少勾选一项)---------------------------------------------------------------------------(二)选择性考核指标(制度创新类项目,至少勾选一项)(三)其他指标(不纳入结题验收考核)注:项目负责人申请和主持在研的技术预见与制度创新项目不超过1项,项目组成员参与申请和在研的技术预见与制度创新项目不超过2项。
总投资27300亿!涉及化工、医药、能源行业近百项,重庆2018年重点建设项目公布!今日摘要重庆政府网消息,重庆市人民政府办公厅日前发布《关于做好2018年市级重点项目实施有关工作的通知》,首度公布2018年市级重点项目清单。
2018年市级重点项目包括年度建设项目和前期准备项目。
其中,年度建设项目697个,总投资2万亿元,年度计划投资4000亿元;前期准备项目168项,估算总投资7300亿元。
其中涉及:天然气、化工、医药、食品行业近百项。
小编已为大家整理好本行业项目表,恭迎各位看官查看。
2018年市级重点年度建设项目名单项目名称项目法人建设起止年限建设性质潼南骐福天然气液化工厂重庆骐福能源有限公司2016—2020 续建麻柳沿江开发区天然气分布式能源项目重庆同晟祺新能源技术有限公司2018—2020 新开工川气东送二线(重庆段)中石化川气东送管道有限公司2018—2020 新开工涪陵白涛—南川水江输气管道中石化重庆管道公司2018—2020 新开工南川水江—武隆仙女山天然气管道重庆祥龙天然气有限公司2018—2020 新开工长寿晏家—北碚水土输气管道重庆聚祥天然气有限公司2018—2020 新开工重庆关西涂料有限公司迁址及扩建项目重庆关西涂料有限公司2017—2018 完工华峰年产20万吨/年环己酮项目重庆华峰化工有限公司2018—2019 新开工华邦制药生产基地重庆华邦制药有限公司两江分公司2016—2018 完工重庆医科大学生物科重庆医科大学2017—2018 完工技产业园西南药业新研发生产基地西南药业股份有限公司2015—2018 完工中药口服固体制剂数字化车间项目天圣制药集团股份有限公司2016—2018 完工华森医药GSP配送中心及药品、保健类制品GMP生产基地重庆华森制药股份有限公司2017—2018 完工重庆参天科瑞制药有限公司眼用制剂项目重庆参天科瑞制药有限公司2017—2018 完工★艾斯勒克斯项目原料药工厂重庆惠源医药有限公司2017—2018 完工太极医药城A区太极科技创新中心及院士工作站重庆太极实业(集团)股份有限公司2016—2018 完工智能装备园(一期)萨摩(重庆)医疗器材有限公司2017—2018 完工智翔金泰项目重庆智翔金泰生物制药有限公司2017—2025 续建上海博唯生物预防性重组蛋白疫苗产业化项目重庆博唯佰泰生物制药有限公司2017—2020 续建忠县医药产业基地重庆天地药业有限责任公司2016—2020 续建太极医药城B区前处理、提取、制剂车间及附属工程太极集团重庆涪陵制药厂有限公司2017—2019 续建制药工业项目天圣制约集团股份有限公司2017—2020 续建秀山县医药产业园重庆海王生物工程有限公司2017—2020 续建天圣制药集团重庆中药加工基地天圣制药集团股份有限公司2017—2019 续建智睿生物产业园研发及孵化中心重庆智睿投资有限公司2017—2019 续建艾斯勒克斯项目制剂工厂(惠源制药项目)重庆惠源医药有限公司、重庆泰润制药有限公司2018—2020 新开工原料药与制剂项目福安药业集团重庆博圣制药有限公司2018—2019 新开工中药材在线分离纯化天圣制药集团股份有限公2018—2019 新开工车间项目司医疗耗材、医药等生产经营项目天圣集团重庆仙明医疗器械有限公司2018—2019 新开工新型凝血分析系统设计制造项目重庆鼎润医疗器械有限责任公司2018—2019 新开工医药中间体GMP平台更新升级项目重庆英斯凯化工有限公司2018—2020 新开工万利来化工搬迁项目重庆市万利来化工股份有限公司2016—2018 完工年产60万吨双氧水项目重庆宏大化工科技有限公司2017—2018 完工天然气制合成气项目巴斯夫聚氨酯(重庆)有限公司2017—2018 完工新华化工厂搬迁项目重庆新华化工厂2016—2018 完工电子灌封材料生产项目重庆江川化工(集团)有限公司2017—2019 续建甲基丙烯酸甲酯、甲基丙烯酸和甲基丙烯酸特种酯项目重庆奕翔化学有限公司2018—2019 新开工己二腈项目重庆中平紫光科技发展有限公司2018—2020 新开工有机溶液NMP生产和回收利用项目重庆市中润化工有限公司2018—2019 新开工东方希望万盛煤化6万吨/年碳酸二甲酯项目东方希望集团有限公司2018—2018 新开工50万吨车用醇醚燃油项目重庆峰圣石化有限公司2018—2019 新开工油橄榄深加工项目重庆德纳油橄榄开发有限公司2017—2020 续建阿兴记三峡库区肉兔产业融合发展园区重庆阿兴记实业有限公司2016—2019 续建金健米业重庆粮油食品基地一期金健米业(重庆)有限公司2017—2019 续建重庆红九九食品深加工项目重庆红九九食品有限公司2018—2019 新开工好姑爷辣椒酱食品生产项目重庆好姑爷食品有限公司2018—2019 新开工面粉加工项目益海(重庆)食品有限公司2018—2019 新开工粮油食品深加工项目(大豆压榨)益海(重庆)食品有限公司2018—2019 新开工2018年市级重点项目准备名单项目名称建设规模及主要建设内容责任单位磨溪—铜梁输气管道新建天然气输气管线65千米,设计年输送气量40亿立方米。
重庆市人民政府、重庆市人民政府办公厅2018年5月文件
目录
佚名
【期刊名称】《重庆市人民政府公报》
【年(卷),期】2018(000)010
【摘要】重庆市人民政府关于印发重庆市开展市场准人负面清单制度改革试点总体方案的通知(渝府发[2018]11号)重庆市人民政府关于表彰第十一届重庆市青少年科技创新市长奖的决定(渝府发[2018]12号)重庆市人民政府关于完善进出口商品质量安全风险预警和快速反应监管体系切实保护消费者权益的通知(渝府发[2018]14号).
【总页数】2页(P37-38)
【正文语种】中文
【中图分类】D630.1
【相关文献】
1.重庆市人民政府、重庆市人民政府办公厅2017年5月文件目录 [J], ;
2.重庆市人民政府、重庆市人民政府办公厅2016年5月份文件目录 [J], ;
3.重庆市人民政府、重庆市人民政府办公厅2018年1月文件目录 [J], 无;
4.重庆市人民政府、重庆市人民政府办公厅2018年2月文件目录 [J], 无;
5.重庆市人民政府、重庆市人民政府办公厅2018年3月文件目录 [J], 无;
因版权原因,仅展示原文概要,查看原文内容请购买。
2018年重大科技专项拟立项项目1. 项目背景2018年,中国政府拟定了一份重大科技专项计划,旨在加强国家在关键领域的科技创新。
该计划的重点是推动中国经济结构转型升级,促进技术进步和实现经济可持续发展。
本文将介绍其中一些拟立项的项目。
2. 项目一:5G网络建设5G网络是指第五代移动通信技术,将大大提升传输速度、减小时延和提升网络容量。
在今后的智能化时代,5G将成为物联网、自动驾驶车辆、工业互联网、智慧医疗等领域的核心技术。
因此,建设5G网络是本次科技专项计划的一个重要部分。
项目目标:建设覆盖全国的5G网络,支撑物联网、自动驾驶、智能交通等应用。
项目预计完成时间:2020年底。
3. 项目二:新能源汽车研发生产新能源汽车作为环保型车辆已经得到了越来越多的关注,是国家推动绿色出行的重要力量。
本项目旨在推动新能源汽车研发和生产,提高轻量化技术、电池技术以及电机控制等方面的技术水平。
项目目标:生产出一批性能更加优异的新能源汽车,降低车辆的负面影响,实现减排和环保。
项目预计完成时间:2022年底。
4. 项目三:大数据应用与创新大数据是指数据量大、数据种类多、数据处理速度快的数据集合。
大数据技术将在未来的很长时间内,成为各行各业智能化转型和升级的关键技术领域之一。
本项目旨在推动大数据技术在制造业生产、社会公共服务以及医疗健康等领域的应用和创新。
项目目标:推进大数据在制造业生产过程中的应用,发布实用性强的大数据产品,改善社会公共服务和医疗健康服务质量。
项目预计完成时间:2021年底。
5. 项目四:人工智能探索和应用人工智能是指计算机程序以人类智慧为样本或指引,独立完成智能决策和任务的能力。
本项目旨在推动人工智能技术的创新发展,为各行各业的科技智能化提供支持。
项目目标:提高人工智能技术的水平和可靠性,大规模推广应用人工智能技术。
项目预计完成时间:2023年底。
6. 项目五:信息安全保障随着社会的数字化、网络化发展,数据安全成为了世界各国共同面临的挑战。