醇 和 醚(3)a
- 格式:ppt
- 大小:659.50 KB
- 文档页数:16

醇和醇反应生成醚的反应类型-回复醇和醇反应生成醚是一种醚化反应,也称为醚化反应。
在这种反应中,醇分子中的羟基(-OH)与其他醇分子中的氢原子(-H)发生酸碱中和反应,生成水分子和醚化合物。
醚是一类含有碳-氧-碳(C-O-C)键的有机化合物,它可以分为对称醚和不对称醚两种类型。
对称醚是指两侧连接醚氧原子的碳原子都相同的醚,而不对称醚则是指两侧连接醚氧原子的碳原子不相同的醚。
醚化反应通常是在酸性条件下进行。
酸性条件可以提供酸性质子(H+),使得醇分子中的羟基成为带正电荷的羟基离子(-OH2+)。
在这种情况下,醇分子中的羟基离子会成为亲核试剂,与其他醇分子中的氢原子发生亲核取代反应。
亲核取代反应是一种化学反应,其中亲核试剂攻击一个含有部分正电荷的电子富集区域,从而替换其中的一个原子或团。
在醇和醇的反应中,亲核试剂是带正电荷的羟基离子,而电子富集区域是含有氢原子的醇分子。
亲核试剂的攻击将导致一个氢原子被醇分子中的氧原子替换掉,形成一个氧原子连接两个碳原子的醚链。
同时,被替换的氢原子与亲核试剂的氢原子结合形成水分子。
这是醚化反应的关键步骤。
在醚化反应中,反应物的选择也很重要。
通常,一方面参与反应的醇分子需要具有较强的酸性,以便产生足够的亲核试剂。
另一方面,参与反应的醇分子需要具有较强的碱性,以便接受亲核试剂的攻击。
这样,反应才能更好地进行。
此外,反应的速度也取决于反应物中的各种因素,如浓度、温度、溶剂等。
较高的浓度和温度通常会加速反应速度,因为它们增加了反应物碰撞的频率和能量。
而合适的溶剂则可以提供反应物的离散性和活性。
总而言之,醇和醇反应生成醚是一种醚化反应,酸性条件下的亲核取代反应是这一过程的关键步骤。
通过酸性质子的提供和亲核试剂的攻击,醇分子中的羟基离子替换了其他醇分子中的氢原子,形成了醚化合物和水分子。
反应物的选择、浓度、温度和溶剂等因素都会影响反应速度和产物的选择。
这种反应在有机化学中具有广泛的应用,用于合成不同类型的醚化合物。

醇和醇反应生成醚的反应类型在有机化学中,醇和醇反应是一种常见的反应类型,指的是两个醇分子通过脱水缩合形成一个醚分子的过程。
这种反应在实验室和工业领域都有广泛的应用,尤其在药物、香料、涂料等行业中具有重要价值。
醇和醇反应生成醚的反应类型主要有以下几种:1.威廉姆逊合成:这是最早发现的醇与醇生成醚的反应,由英国化学家威廉姆逊于1859年首次报道。
该反应通常在酸性条件下进行,如氢氧化铝、磷酸等催化剂。
反应过程中,两个醇分子脱去一个水分子,形成一个醚分子。
例如,甲醇与乙醇反应生成甲乙醚:CH3OH + C2H5OH → CH3C2H5O2.醚化反应:这是一种在碱性条件下进行的醇与醇生成醚的反应。
通常使用金属钠、氢氧化钠等强碱作为催化剂。
反应过程中,醇分子脱去一个氢离子,形成一个醚分子。
例如,甲醇与乙醇反应生成甲乙醚:CH3OH + C2H5O H → CH3C2H5O3.斯托克豪森反应:这是一种在酸性条件下,醇与醇生成环醚的反应。
通常使用磷酸、硫酸等催化剂。
反应过程中,两个醇分子脱去一个水分子,形成一个环醚分子。
例如,甲醇与乙醇反应生成环甲乙醚:CH3OH + C2H5OH → (CH3)2C(OH)2反应条件的选择对醇和醇反应生成醚的反应类型和产率具有重要影响。
在实际应用中,需要根据目标醚的结构和用途,选择合适的反应条件。
醇和醇反应在药物、香料、涂料等行业具有重要应用价值。
例如,通过醇和醇反应,可以合成许多具有重要生物活性的化合物,如抗病毒药物、抗癌药物等。
此外,醇和醇反应还可以用于制备高分子材料,如聚醚、聚酯等,这些材料在工程、医疗等领域具有广泛应用。
总之,醇和醇反应作为一种重要的有机化学反应,在科学研究和实际应用中具有重要意义。
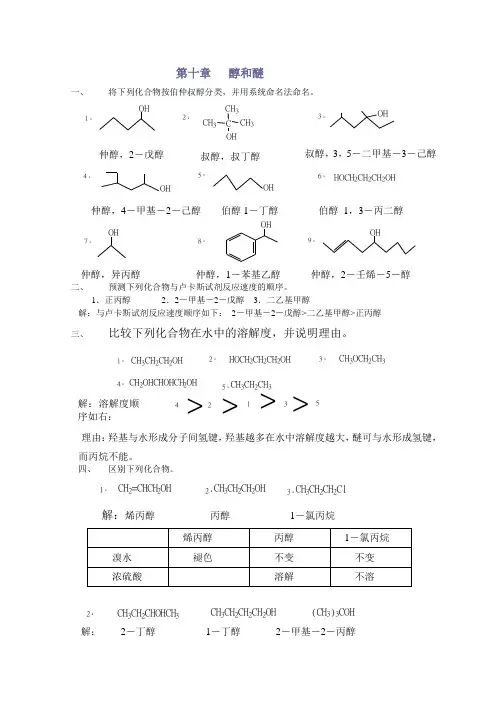
第十章 醇和醚一、将下列化合物按伯仲叔醇分类,并用系统命名法命名。
1.2.CH 3CH 3CH 3C OH3.OH4.OH 5.OH6HOCH 2CH 2CH 2OH7.OHOH8.9.OHOH仲醇,异丙醇 仲醇,1-苯基乙醇 仲醇,2-壬烯-5-醇二、 预测下列化合物与卢卡斯试剂反应速度的顺序。
1.正丙醇 2.2-甲基-2-戊醇 3.二乙基甲醇解:与卢卡斯试剂反应速度顺序如下: 2-甲基-2-戊醇>二乙基甲醇>正丙醇 三、比较下列化合物在水中的溶解度,并说明理由。
1.CH 3CH 2CH 2OH2.HOCH 2CH 2CH 2OH3.CH 3OCH 2CH 34.CH 2OHCHOHCH 2OH5.CH 3CH 2CH 342135>>>>理由:羟基与水形成分子间氢键,羟基越多在水中溶解度越大,醚可与水形成氢键,而丙烷不能。
四、区别下列化合物。
1.CH 2=CHCH 2OH 2.CH 3CH 2CH 2OH3.CH 3CH 2CH 2Cl解:烯丙醇 丙醇 1-氯丙烷2.CH 3CH 2CHOHCH 3CH 3CH 2CH 2CH 2OH (CH 3)3COH解: 2-丁醇 1-丁醇 2-甲基-2-丙醇3.α-苯乙醇 β-苯乙醇解:与卢卡斯试剂反应,α-苯乙醇立即变浑, β-苯乙醇加热才变浑。
六、 写出下列化合物的脱水产物。
1.CH 3CH 2C(CH 3)2OHCH 3CH=C(CH 3)22.(CH 3)2CCH 2CH 2OHH 2SO 41moleH 2O(CH 3)2C=CHCH 2OH3.CH 2CHCH3H +CH=CHCH 34.CH 2CHCH(CH 3)2+CH=CHCH(CH 3)25.CH 3CH=CCH 3CH 2C(CH 3)C(CH 3)CH 2CH 3CH 3C CH 3=CHCH 3OHOH七、 比较下列各组醇和溴化氢反应的相对速度。


鉴别醇和醚的化学方法
鉴别醇和醚的常用化学方法有以下几种:
1. 酸碱反应法:将待鉴别化合物加入一定量的酸性或碱性溶液中,若产生气泡,则表明化合物中含有醇;若无反应,则可能为醚。
2. Lucas试剂法:向待鉴别化合物中加入Lucas试剂(浓盐酸和氯化亚铁的混合物),加热后若形成浑浊的混合物,则表明化合物中含有1、2或3度醇;若产生无色液体,则表明化合物为醚。
3. 碘液试验法:向待鉴别化合物中加入碘液(碘化钠溶液),若产生黄色颜色,则表明化合物中可能含有醇;若无反应,则可能为醚。
4. 嗅觉法:由于醇具有刺鼻的气味,而醚则无气味或轻微芳香味,因此可以通过嗅觉进行初步区分。
需要注意的是,使用化学方法进行鉴别时应注意条件的选择和控制,方法操作的正确性和准确性。
同时,这些方法虽然可以用来进行初步的区分,但不能确定化合物的具体结构和成分等信息,需要结合其他分析方法进行综合分析。

醇和醇反应生成醚的反应类型醇和醇反应生成醚是一种醚化反应,也被称为醚化缩合反应。
在这个反应中,两个醇分子经过酸催化或酸碱双催化作用,发生醚化反应生成醚。
这是一种重要的有机合成反应,常用于制备醚的方法之一。
醚化反应的机理可以分为两个步骤:首先是质子转移,然后是质子歧化。
质子转移是指一个醇分子将氢原子离去,生成一个质子,并转移给另一个醇分子中的氧原子。
质子歧化是指在质子转移的基础上,生成一个氧离子和一个亲电性中心,然后这两个中心再次结合形成醚。
醚化反应的步骤可以表示为以下化学方程式:R-OH + R'-OH → R-O-R' + H2O其中,R和R'代表醇分子中的有机基团。
醚化反应的催化剂通常是酸。
在酸催化下,醇分子中的氧原子上的质子容易被剥夺,形成含正离子的中间物质。
然后,醇分子中的另一个氧原子接受这个质子,形成氧离子。
这个氧离子再与另一个醇分子中的亲电性中心结合,形成醚。
常用的酸催化剂有浓硫酸(H2SO4)、磷酸(H3PO4)和三氯化铁(FeCl3)等。
这些酸具有较高的酸性,可以有效促进醚化反应的进行。
此外,酸碱双催化也可以促进醚化反应的进行。
在催化剂存在的条件下,酸和碱可以很好地相互配合,使醚化反应速率更高。
以硫酸和氢氧化钠为例,硫酸具有酸性,可以从醇中提取质子;氢氧化钠具有碱性,可以中和产生的酸,并使体系的酸碱度维持在适当的范围内。
醚化反应的适用范围很广。
不同类型的醇可以进行醚化反应,包括脂肪醇、芳香醇、脂环醇和脂孤环醇等。
此外,醚化反应还可以针对不同类型的醇进行串联反应,生成三元醚和多元醚等高级醚。
醚化反应还可以用于合成药物、香料、染料和涂料等有机化合物。
醚具有较好的溶剂性,具有广泛的应用前景。
此外,醚还具有较好的化学稳定性和热稳定性,对于高温、高压等条件下的催化反应具有一定的优势。
总结起来,醇和醇反应生成醚是一种醚化反应,其机理主要包括质子转移和质子歧化两个步骤。

有机化学中的醇和醚醇和醚是有机化合物中常见的两类化合物,它们在化学性质和应用领域上具有一定的相似性和差别。
本文将对有机化学中的醇和醚进行详细的介绍和分析。
一、醇的概念和性质1.概念:醇是由一个或多个羟基(OH)取代碳原子而形成的有机化合物,通式一般为ROH,其中R代表烷基或芳基。
2.性质:醇具有以下几个特点:(1)醇分子中的羟基具有极性,导致醇具有较高的沸点、溶解度和比热容,同时也使醇能够与水分子形成氢键。
(2)醇可以和酸反应,形成醚、酯等化合物,这是醇的一个重要反应。
(3)醇可以进行氧化反应,形成醛、酮等化合物,这是醇的另一个重要反应。
二、醇的命名和分类1.命名:醇的命名遵循系统命名法,以确定主链和羟基的位置、取代基和官能团等因素,例如乙醇、异丙醇等。
2.分类:醇可以根据羟基所连接的碳原子个数进行分类,分为一元醇、二元醇等。
三、醇在有机合成中的应用1.醇的还原性:由于醇分子中含有极易离去的羟基,醇具有还原性,可以被氢化剂还原为饱和烃。
这一性质使得醇成为重要的还原试剂,在有机合成中用于还原醛、酮等化合物。
2.醇的亲核性:醇分子中的羟基具有较强的亲核性,可以与酰卤、烯烃等电子不足的化合物发生亲核取代反应,形成醚、酯等化合物。
这一反应在有机合成中十分常见。
3.醇的氧化性:醇可以通过氧化反应被氧化剂氧化为醛、酮等化合物,这一反应常用于有机合成中的氧化反应。
四、醚的概念和性质1.概念:醚是由两个有机基通过氧原子连接而成的化合物,通式一般为R-O-R'。
2.性质:醚具有以下特点:(1)醚是较稳定的化合物,具有较低的沸点和溶解度。
(2)醚分子中的氧原子不带电荷,因此醚没有和水分子形成氢键的能力。
(3)醚可以被酸催化下的水解反应,将醚分解为两个醇。
五、醚的命名和分类1.命名:醚的命名同样遵循系统命名法,以确定两个有机基的结构和官能团等因素,例如乙醚、二甲醚等。
2.分类:醚可以根据氧原子所连接的碳原子个数进行分类,分为二元醚、三元醚等。

醇和醚的沸点醇和醚是常见的有机化合物,它们的沸点是两种不同的物理性质。
本文将详细介绍醇和醚的沸点。
一、醇的沸点醇是一种含有羟基(-OH)官能团的有机化合物。
由于羟基与碳原子之间存在氢键,因此醇分子之间的相互作用力比较强,导致其沸点比相同分子量的烃要高。
另外,随着碳链长度增加,分子量也随之增加,因此其沸点也会随之升高。
例如,甲醇(CH3OH)和乙醇(C2H5OH)是两种常见的低级别醇。
甲醇的分子量为32.04 g/mol,其沸点为64.7℃;而乙醇的分子量为46.07 g/mol,其沸点为78.4℃。
可以看出,乙醇比甲醇分子大,因此其相互作用力更强,在室温下不易挥发。
二、醚的沸点与醛和羧酸等其他含氧官能团的有机化合物不同,由于缺少了氢键作用力,因此醚分子之间的相互作用力比较弱,导致其沸点比相同分子量的醇要低。
例如,二甲醚(CH3OCH3)和二乙醚(C2H5OC2H5)是两种常见的低级别醚。
二甲醚的分子量为46.07 g/mol,其沸点为-24.8℃;而二乙醚的分子量为74.12 g/mol,其沸点为34.6℃。
可以看出,由于缺少了氢键作用力,醚分子更容易挥发,在室温下就可以达到液态。
三、总结综上所述,由于醇和醚之间相互作用力不同,因此其沸点也有很大差异。
在实际应用中,我们可以利用这种差异来进行物质的分离和提纯等操作。
例如,在石油化工行业中,我们可以通过蒸馏等方法将原油中含有的不同碳链长度的烷烃、烯烃、芳香烃、酮类、羧酸等物质进行分离提纯。
总体来说,在化学领域中对于不同物质性质的认识是非常重要的。
对于有机化合物而言,了解其沸点等物理性质可以帮助我们更好地理解其分子结构和相互作用力,为后续的实验研究提供有力的支持。

有机化学中的醇与醚的合成有机化学作为化学的一个重要分支,研究的是碳氢化合物及其衍生物的结构、性质和反应。
其中,醇和醚是有机化合物中常见的两类官能团,它们在生物、药物、农药等领域具有重要的应用价值。
本文将重点讨论有机化学中醇与醚的合成方法。
一、醇的合成
醇是含有羟基(-OH)官能团的有机化合物,在合成中使用广泛。
下面介绍几种常见的醇合成方法:
1. 烷烃氧化法:烷烃氧化是醇的一种重要合成途径,其中最常见的是烷烃的氧化裂解反应。
例如,乙烷氧化可生成乙醇。
2. 烯烃水化法:烯烃通过水合反应可以生成醇。
例如,乙烯经过水合反应可以制备乙醇。
3. 羧酸还原法:羧酸的还原反应也是醇的常见合成方法。
例如,乙酸经过还原反应可以生成乙醇。
二、醚的合成
醚是含有氧桥(-O-)官能团的有机化合物,通常可以由醇和卤代烷基的缩合反应来合成。
下面介绍几种常见的醚合成方法:
1. 醇缩合法:醇和卤代烷基经过缩合反应可以生成醚。
例如,甲醇和溴乙烷经过缩合反应可以制备甲基乙基醚。
2. 醇脱水法:醇经过脱水反应也可以生成醚。
例如,乙醇在酸性条件下脱水反应可以生成乙醚。
3. 醇与醚之间转化法:醇可以通过醚化反应转化为醚。
例如,在酸催化条件下,乙醇可以与甲醇发生醚化反应生成乙基甲醚。
综上所述,有机化学中的醇与醚是重要的有机化合物,在实际合成中有着广泛的应用。
通过实验室合成或生物合成等方法,我们可以合成出各种类型的醇和醚化合物,为化学领域的发展和应用提供了有力支持。
希望本文对读者有所帮助,欢迎交流讨论。
醇和醚知识点详解醇和醚是有机化合物中常见的两类化合物。
它们在许多领域具有重要的应用,如有机合成、溶剂、药物和香料等。
本文将详细介绍醇和醚的定义、性质、制备方法和应用等知识点。
一、醇的定义和性质醇是一类含有氢氧基(-OH)的有机化合物。
根据氢氧基的位置,醇可以分为一次醇、二次醇和三次醇。
一次醇中,氢氧基连接在碳链上,如甲醇(CH3OH)和乙醇(C2H5OH)。
二次醇中,有两个氢氧基连接在碳原子上,如乙二醇(HOCH2CH2OH)。
三次醇则有三个氢氧基连接在碳原子上。
醇分子中的氢氧基使其具有一些特殊性质,如溶解性和酸碱性。
1. 溶解性:醇一般可溶于水。
较短的醇(一次醇和二次醇)溶解性较高,而较长的醇溶解性较差。
这是因为水分子能与醇分子的氢键形成氢键,使其能够相互溶解。
2. 酸碱性:醇可作为酸或碱。
在适当条件下,醇的氢氧基可以脱去质子成为负离子(醇的碱性),也可以接受质子成为正离子(醇的酸性)。
二、醇的制备方法1. 氢氧化物的还原:将醛或酮用还原剂(如氢气与催化剂)还原即可得到相应的醇。
2. 同分异构体的合成:对一些具有同分异构体的化合物,通过适当的反应条件,可以选择性地将其转化为某一种醇。
3. 环氧化合物的开环:将环氧化合物与酸或碱反应,使其开环而生成相应的醇。
4. 卤代烃的取代反应:醇也可以通过将卤代烃与水反应来获得。
三、醇的应用1. 溶剂:醇在许多化学反应中可以作为溶剂使用,如乙醇常用于制备药物和香料。
2. 酯的制备:醇与酸酐反应,通常可以生成酯。
酯在食品工业、香料工业和制药工业中有广泛的应用。
3. 脱水剂:由于醇分子中含有活泼的氢氧基,因此醇在一些有机合成反应中可以作为脱水剂使用。
四、醚的定义和性质醚是一类含有两个烷基或芳基团的有机化合物,其通式为R-O-R',其中R和R'可以是烷基或芳基团。
根据醚分子中氧原子在碳链上的位置,可以分为对称醚和非对称醚。
1. 对称醚:两个烷基或芳基团相同,例如乙醚(CH3OCH3),是最简单的醚。
有机化学基础知识点整理醇和醚的性质和反应醇和醚是有机化合物中常见的官能团,它们在化学反应中起着重要的作用。
了解其性质和反应对于有机化学的学习和应用非常重要。
本文将对醇和醚的性质和反应进行整理和总结。
一、醇的性质和反应1. 醇的结构和命名醇是含有羟基(-OH)官能团的化合物。
根据羟基上所连接的碳原子数目,醇可以分为一元醇(含有一个羟基),二元醇(含有两个羟基),三元醇(含有三个羟基)等。
醇的命名通常采用将烷烃命名法中的“烷”改为“醇”,同时在碳原子前面标记羟基所连接的位置。
2. 醇的物理性质醇具有许多与羟基相关的物理性质。
由于羟基可以形成氢键,醇的沸点和溶解度通常较高。
此外,醇还具有较大的极性,使得它们具有良好的溶剂性,尤其对于极性化合物。
3. 醇的酸碱性醇既可以表现出酸性,也可以表现出碱性。
醇的酸性主要体现在羟基上,它可以失去氢原子形成羟基阴离子。
同时,醇中的氧原子也能形成键合氢,表现出碱性。
4. 醇的氧化反应醇可以发生氧化反应,其中最常见的就是醇的燃烧反应。
醇在氧气的存在下可以燃烧,并释放出大量的热能和水。
此外,醇还可以被氧化剂如酸性高锰酸钾(KMnO4)氧化成酮或醛。
5. 醇的酯化反应醇与酸酐发生酯化反应,生成酯。
酯是一类常见的醇的衍生物,具有良好的香味和挥发性。
酯化反应是众多有机合成中常用的一种方法。
二、醚的性质和反应1. 醚的结构和命名醚是由两个碳原子通过一个氧原子连接形成的化合物。
根据氧原子所连接的碳原子的数目和位置,醚可以分为对称醚和不对称醚。
醚的命名通常采用将两个碳原子团按字母顺序排列,并在后面加上“醚”字。
2. 醚的物理性质醚具有较低的沸点和较好的挥发性,这使得它们广泛应用于溶剂和非极性反应介质中。
醚的极性较小,不溶于水,但溶于大部分有机溶剂。
3. 醚的裂解反应醚可以通过热或酸性条件下的裂解反应进行分解,生成相应的醇。
这是由于氧原子的带负电荷引发了裂解反应。
4. 醚的醚化反应醚还可以通过醇的酸性氢进行醚化反应。