乙醛的结构
- 格式:pptx
- 大小:195.65 KB
- 文档页数:14

乙醛【知识要点】1.乙醛的分子组成与结构乙醛的分子式是O H C 42,结构式是,简写为CHO CH 3。
注意 对乙醛的结构简式,醛基要写为—CHO 而不能写成—COH 。
2.乙醛的物理性质乙醛是无色、具有刺激性气味的液体,密度小于水,沸点为C 8.20。
乙醛易挥发,易燃烧,能与水、乙醇、氯仿等互溶。
注意 因为乙醛易挥发,易燃烧,故在使用纯净的乙醛或高浓度的乙醛溶液时要注意防火。
3.乙醛的化学性质从结构上乙醛可以看成是甲基与醛基()相连而构成的化合物。
由于醛基比较活泼,乙醛的化学性质主要由醛基决定。
例如,乙醛的加成反应(碳氧双键)和氧化反应(醛基氢),都发生在醛基上。
(1)乙醛的加成反应乙醛分子中的碳氧双键能够发生加成反应。
例如,使乙醛蒸气和氢气的混合气体通过热的镍催化剂,乙醛与氢气发生加成反应:说明:①在有机化学反应中,常把有机物分子中加入氢原子或失去氧原子的反应叫做还原反应。
乙醛与氢气的加成反应就属于还原反应。
②从乙醛与氢气的加成反应也属于还原反应的实例可知,还原反应的概念的外延应当扩大了。
(2)乙醛的氧化反应在有机化学反应中,通常把有机物分子中加入氧原子或失去氢原子的反应叫氧化反应。
乙醛易被氧化,如在一定温度和催化剂存在的条件下,乙醛能被空气中的氧气氧化成乙酸:注意 ①工业上就是利用这个反应制取乙酸。
②在点燃的条件下,乙醛能在空气或氧气中燃烧。
乙醛完全燃烧的化学方程式为: O H CO O CHO CH 22234452+−−→−+点燃乙醛不仅能被2O 氧化,还能被弱氧化剂(如银氨溶液和新制备氢氧化铜悬浊液)氧化。
银氨溶液的制备: 在洁净的试管里加入1 mL 2%的3AgNO 溶液,然后一边摇动试管,一边逐滴滴入2%的稀氨水,至最初产生的沉淀恰好溶解为止(此时得到的溶液叫做银氨溶液)。
再滴入3滴乙醛,振荡后把试管放在热水中温热。
实验现象 不久可以看到,试管内壁上附着一层光亮如镜的金属银。

《乙醛》讲义一、乙醛的基本信息乙醛,化学式为 C₂H₄O,结构简式为 CH₃CHO,是一种醛类有机化合物。
它在常温常压下是一种无色、易挥发、具有刺激性气味的液体。
乙醛能与水、乙醇、乙醚等多种有机溶剂混溶。
二、乙醛的物理性质1、外观与气味乙醛为无色透明液体,具有强烈的刺激性气味。
这股气味类似于水果熟透或者发酵的味道。
2、沸点和熔点乙醛的沸点约为 208℃,熔点约为-1235℃。
由于其沸点较低,所以在常温下容易挥发。
3、密度相对密度为 07834(水= 1),这意味着它比水的密度小。
4、溶解性乙醛能与水、乙醇、乙醚等有机溶剂以任意比例互溶。
三、乙醛的化学性质1、加成反应乙醛分子中的碳氧双键可以发生加成反应。
例如,在催化剂的作用下,乙醛可以与氢气发生加成反应,生成乙醇。
CH₃CHO + H₂ → CH₃CH₂OH2、氧化反应(1)乙醛可以被氧气氧化为乙酸。
2CH₃CHO + O₂ → 2CH₃COOH(2)乙醛也能被一些弱氧化剂氧化,比如银氨溶液和新制的氢氧化铜悬浊液。
与银氨溶液反应,会产生银镜现象,化学方程式为:CH₃CHO + 2Ag(NH₃)₂OH → CH₃COONH₄+2Ag↓ + 3NH₃+ H₂O与新制的氢氧化铜悬浊液反应,会产生砖红色沉淀,化学方程式为:CH₃CHO + 2Cu(OH)₂+NaOH → CH₃COONa + Cu₂O↓ +3H₂O3、缩合反应乙醛在一定条件下可以发生自身缩合反应,生成β羟基丁醛。
2CH₃CHO → CH₃CH(OH)CH₂CHO四、乙醛的制备方法1、乙醇氧化法乙醇在催化剂(如铜或银)的作用下,加热可以被氧化为乙醛。
这是工业上制备乙醛的常用方法之一。
2CH₃CH₂OH + O₂ → 2CH₃CHO + 2H₂O2、乙烯氧化法乙烯在催化剂(如钯盐)和氧气的作用下,可以被氧化为乙醛。
CH₂=CH₂+ 1/2 O₂ → CH₃CHO五、乙醛的用途1、化工原料乙醛是合成乙酸、乙酸酐、季戊四醇、丁醇、三氯乙醛等多种有机化工产品的重要原料。



乙醛化学式结构式及其相关性质和应用1. 乙醛的基本信息乙醛(英文名:acetaldehyde),又被称为醋醛,分子式为CH₃CHO,是一种醛类有机化合物。
乙醛是一种无色、易燃、易挥发的液体,具有辛辣、刺激性的臭味。
乙醛可溶于水,混溶于乙醇、乙醚、苯、甲苯、丙酮等有机溶剂。
由于乙醛含有羰基基团,且与羰基相连的碳上具有α氢,所以乙醛容易发生加成、氧化、还原等反应。
乙醛是一种重要的化工中间体,可通过氧化反应合成乙酸、乙酸酐等化合物,还可以通过缩合反应制得丁醇、季戊四醇等化合物,还可以合成乳酸、吡啶等化合物。
乙醛对人体的眼、鼻、呼吸道等有强烈的刺激作用,长时间接触可引发中毒。
2. 乙醛的化学结构乙醛是带有一个羰基的醛类化合物,乙醛分子由一个醛羰基和一个甲基构成。
乙醛甲基中的碳原子以sp杂化轨道成键,和所有的醛基化合物一样,乙醛羰基中的碳原子以三个sp杂化轨道形成三个σ键,其中一个是和氧形成的,这三个键处于同一平面,碳原子的一个p轨道和氧原子的一个p轨道重叠形成一个π键,与σ键所成的平面垂直,因此羰基的碳氧双键是由一个σ键和一个π键形成的。
羰基中氧原子的电负性大于碳原子,因此羰基是一个极性基团,具有偶极矩,偶极矩的负极在氧原子这一端,正极在碳原子这一端,因此羰基中的碳原子带有部分正电荷,氧原子带有部分负电荷。
3. 乙醛的理化性质3.1 物理性质乙醛是一种无色有刺激性臭味的液体,常温下密度为0.785 g/mL,沸点为20.8℃,熔点为-123.4 °C。
乙醛可以溶于水,混溶于乙醇、乙醚、苯、甲苯、丙酮等有机溶剂。
乙醛的闪点是-38 ℃,自燃温度为175 °C。
3.2 化学性质乙醛含有羰基,具有醛类化合物的某些化学性质,可以发生亲核加成、氧化、还原等反应。
乙醛的甲基与羰基相连,因此甲基碳上的氢原子具有一定的活泼性,可以发生卤代、卤仿等取代反应。
3.2.1 加成反应乙醛与格氏试剂加成有机镁试剂(格氏试剂)容易对含羰基的化合物进行亲核加成反应,在无水无氧的条件下,格氏试剂对乙醛的加成反应如下:CH₃CHO + CH₃MgBr → CH₃CH (OMgBr)CH₃ — H₃O⁺ → CH₃CH (OH)CH₃乙醛与亚硫酸氢钠加成亚硫酸氢钠与乙醛反应可以生成一种溶于水的盐。

乙醛的化学式和结构式-概述说明以及解释1.引言1.1 概述乙醛是一种重要的有机化合物,它在化工、医药、食品等领域都有着广泛的应用。
乙醛具有独特的化学性质和结构特征,其化学式为CH3CHO,结构式为CH3-CHO。
乙醛在化学反应中扮演着重要角色,其重要性不可忽视。
本文将深入探讨乙醛的定义、性质、化学式和结构式,以及乙醛在化学领域的应用和未来发展方向。
通过对乙醛的全面了解,可以更好地认识和利用这种重要的有机化合物。
文章结构部分的内容应包括对整篇文章的组织和安排进行说明。
在这篇关于乙醛的化学式和结构式的文章中,我们将按照以下结构展开讨论:1. 引言部分:1.1 概述:简要介绍乙醛的基本信息和重要性。
1.2 文章结构:介绍本文的组织结构和讨论内容。
1.3 目的:明确本文撰写的目的和意义。
2. 正文部分:2.1 乙醛的定义和性质:详细介绍乙醛的定义、性质和特点。
2.2 乙醛的化学式:分析乙醛的化学式及其组成元素。
2.3 乙醛的结构式:探讨乙醛的分子结构和构造特点。
3. 结论部分:3.1 总结乙醛的重要性:概括乙醛在化学领域的重要作用。
3.2 乙醛在化学领域的应用:列举乙醛在实际应用中的具体场景和用途。
3.3 展望乙醛的未来发展:展望乙醛在未来的应用前景和发展趋势。
通过以上结构安排,我们将全面深入地探讨乙醛的化学式和结构式,展示其重要性和潜在应用价值,为读者提供详尽的信息和知识内容。
1.3 目的本文的目的在于深入探讨乙醛这一化合物的化学式和结构式,并分析其定义、性质以及在化学领域的应用。
通过对乙醛的研究,我们可以更加全面地了解这一化合物的特点和重要性,为化学领域的研究提供更为深入的参考和理解。
同时,通过展望乙醛的未来发展,可以为相关研究的方向和发展趋势提供一定的参考和借鉴,促进乙醛在化学领域的更广泛应用和推广。
通过本文的研究,旨在为读者提供关于乙醛的详尽信息,增强对该化合物的理解和认识。
2.正文2.1 乙醛的定义和性质乙醛,化学式为CH3CHO,又称乙醛醛,是一种有机化合物,属于醛类化合物。


高二化学乙醛、醛类【本讲主要内容】乙醛、醛类乙醛的结构、物理性质、化学性质、制法和用途;醛类的结构、通性和检验方法;对照醛的内容简要了解其同分异构体酮的知识。
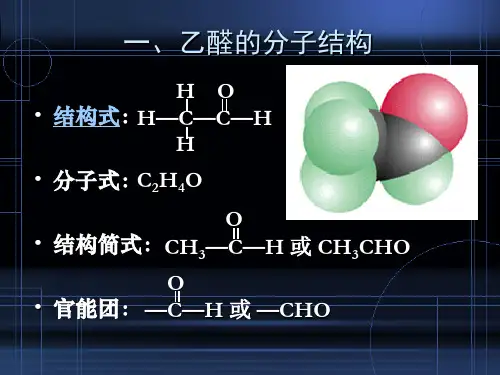
【知识掌握】 【知识点精析】 一. 乙醛1. 分子式结构式结构简式官能团 C 2H 4OC H HHCHOH 3C C H O或CH 3CHO醛基2. 物理性质 乙醛是无色、具有刺激性气味的液体,密度比水小,沸点很低(20.8℃,比乙醇低得多),易挥发,易燃烧,能跟水、乙醇、氯仿等互溶。
3. 化学性质 (1)加成反应NiOH CH 3-C+H 2CH 3CH 2OH注:① 该反应实质为加氢还原反应。
有机化学反应中,通常把有机物分子中加入氢原子或失去氧原子的反应叫做还原反应,而加氧去氢的反应称为氧化反应。
如乙醇的催化氧化。
② 醛基与H 2的加成是在分子中引入—OH 的一种方法。
但工业上并不用此法合成乙醇。
③ C =O 键和C =C 键不同,只能与H 2加成,但不能与溴水加成。
(2)氧化反应① 剧烈氧化——燃烧2CH 3CHO+5O 2点燃4CO 2+4H 2O② 催化氧化2CH 3CHO+O 2催化剂2CH 3COOH③ 被弱氧化剂氧化 a. 银镜反应 Ag ++NH 3·H 2O =AgOH ↓+NH 4+AgOH+2NH 3·H 2O =[23)(NH Ag ]++OH -+2H 2O CH 3CHO+223)(NH Ag ]++2OH-水浴2Ag ↓+CH 3COO -+NH 4++3NH 3+H 2O这个反应叫银镜反应。
银镜反应常被用于检验醛基的存在。
也常用于测定有机物中醛基的数目。
b. 与新制2)(OH Cu 悬浊液反应CuSO 4+2NaOH =2)(OH Cu ↓+Na 2SO 4 22)(OH Cu +CH 3CHOCu 2O ↓+CH 3COOH+2H 2O乙醛与新制2)(OH Cu 悬浊液的反应也可用于检验醛基的存在。

醛化学式及结构式醛是一类含有羰基(C=O)的有机化合物,通式为R-CHO。
其中R代表烃基,可以是烷基(含有烷基基团),也可以是芳基(含有芳族基团)。
醛的命名通常以醛作为词尾,如甲醛、乙醛等。
醛常见的结构式有以下几种:线性结构、环状结构和酸醛(醛羧酸)结构。
一、线性醛的结构式:1. 甲醛(HCHO):该化合物为最简单的醛,由单个碳原子和一个氢原子组成。
其结构式为:HCHO。
2. 乙醛(CH3CHO):该化合物由两个碳原子、四个氢原子和一个氧原子组成。
其结构式为:CH3CHO。
3. 丙醛(CHO-CH2-CH3):该化合物由三个碳原子、六个氢原子和一个氧原子组成。
其结构式为:CHO-CH2-CH3。
二、环状醛的结构式:1. 环戊醛(C5H8O):该化合物由一个五元环状结构和一个羰基组成。
其结构式为:O||CH2--CH-[CH2]-CH2 ||CH2--CH-[CH2]-CH2 2. 环己醛(C6H10O):该化合物由一个六元环状结构和一个羰基组成。
其结构式为:O||CH2-CH2-CH2-CH2-CH2-[CH2]三、酸醛(醛羧酸)的结构式:1. 甲酸(HCOOH):该化合物由一个羰基和一个羧基组成。
其结构式为:O||H-[C=O]-OH2. 乙酸(CH3COOH):该化合物由两个碳原子、两个羰基和一个羧基组成。
其结构式为:O||CH3-[C=O]-OH||CH3以上仅为醛的一些典型结构式示例,实际上醛具有很多不同的结构式。
因为醛以其独特的结构和性质在有机合成、药物化学、食品添加剂等领域有着广泛的应用。
通过研究醛的结构式,可以更好地理解其性质与反应机制。
乙醛的结构
乙醛(乙醛)是由两个氢原子和一个氧原子组成的有机化学物质,符号为CH3CHO或HCHO。
它在常温常压下是无色无味的液体。
它的分子结构如下
H–C–O–H
/
H H
这种结构形式是分子中的氢原子和氧原子通过单键双键形成的
单一碳原子,碳原子上有三个氢原子,一个氧原子,这种结构形式也称为碳氧式有机物。
它有一个氢原子的IUPAC名称是甲醛,分子式为CH3-CHO。
乙醛具有一个碳-氧双键(C=O),因此它也被称为一种碳氧双键化合物,并且乙醛在水溶液中具有极佳的溶解性,同时它也具有易挥发性。
- 1 -。
乙醛和丙醛的结构-概述说明以及解释1.引言1.1 概述概述乙醛和丙醛是两种常见的有机化合物,它们都属于醛类化合物。
醛类化合物是含有醛基(-CHO)的有机化合物,它们在许多化学和生物过程中具有重要的作用。
乙醛的结构简单而紧凑,由一个碳原子与一个醛基(-CHO)组成。
乙醛的分子式为C2H4O,它是一种无色液体,具有特殊的刺激性气味。
乙醛广泛应用于化学工业中,用于制备各种化学品,如有机合成中的中间体和溶剂。
此外,乙醛还可用作某些食品添加剂,例如味精的原料。
丙醛与乙醛相比稍复杂一些,它的结构由一个碳原子和一个醛基(-CHO)组成,加上一个甲基基团(-CH3)。
丙醛的分子式为C3H6O,它也是一种无色液体,具有特殊的气味。
丙醛在医药和农药工业中广泛应用,也可用于有机合成和溶剂。
乙醛和丙醛具有一些相似的物理性质和化学性质,但它们也存在一些差异。
通过比较它们的结构、物理性质和化学性质,我们可以更好地了解它们各自的特点和应用领域。
本文将从乙醛和丙醛的结构描述、物理性质、化学性质以及两者之间的区别等方面进行详细介绍和分析。
最后,我们将总结乙醛和丙醛的结构特点,并展望它们在未来的应用前景。
通过这篇文章,读者将能够更全面地了解乙醛和丙醛的结构和性质,以及它们在化学和工业领域的重要性。
1.2 文章结构文章结构部分的内容可以包括以下内容:文章结构部分是对整篇文章的组织和安排进行说明,主要是为读者提供一个清晰的导引,使读者能够更好地理解和把握文章的内容和逻辑结构。
本文采用以下结构:引言部分包括文章的概述、文章结构、文章的目的和总结。
在概述部分,将简要介绍乙醛和丙醛的结构以及它们在化学领域中的重要性和应用。
在文章结构部分,将详细介绍每个章节的内容和组织方式,以便读者能够清楚地了解整篇文章的结构。
在目的部分,说明文章撰写的目的是为了深入探讨乙醛和丙醛的结构,并对其进行比较分析。
最后,在总结部分,将简要总结乙醛和丙醛的结构特点和应用前景,以及本文的主要观点和结论。
乙醛的结构视图分析方法
乙醛的结构可以通过以下几种视图分析方法进行分析:
1. 线结构:乙醛的线结构表示乙醛的原子连接顺序和原子之间的键连接关系。
乙醛的线结构中包括一个碳原子和一个氧原子,碳原子与氧原子之间有一个双键,碳原子还与两个氢原子相连。
2. 键线结构:乙醛的键线结构表示乙醛中的化学键和原子之间的连接关系。
乙醛的键线结构中可以看到碳原子与氧原子之间的双键、碳原子与一个氢原子之间的单键、碳原子与另一个氢原子之间的单键。
3. 空间结构:乙醛的空间结构表示乙醛中原子的空间排列方式。
乙醛的空间结构是一个平面分子,氧原子和碳原子在同一个平面上,氢原子位于该平面之上。
4. 骨架结构:乙醛的骨架结构表示乙醛中的主要碳原子框架,即去除所有氢原子后的结构。
乙醛的骨架结构只包括碳原子和氧原子,无其他原子。
5. 分子式:乙醛的分子式表示乙醛中所有原子的数量和种类。
乙醛的分子式为C2H4O。
这些方法可以帮助我们全面了解乙醛的结构和组成,有助于进一步理解乙醛的性质和反应。