磺胺合成工艺的改进
- 格式:pdf
- 大小:50.08 KB
- 文档页数:1

广州大学化学化工学院本科学生综合性、设计性实验报告实验课程有机化学基础实验实验项目磺胺的合成-多步骤合成对氨基苯磺酰胺专业班级学号姓名指导教师开课学期至学年学期时间年月日磺胺的合成—多步骤合成对氨基苯磺酰胺姓名:摘要:对氨基苯磺酰胺作为一种简单的磺胺药,投入大量生产。
能抑制多种细菌和少数病毒的生长和繁殖,用于防治多种病菌感染。
本实验以苯为原料经过硝化、还原、酰胺化、氯磺化、氨置换、水解及中和等一系列反应,得到磺胺。
最后通过测定熔点和红外光谱图鉴定磺胺的结构。
关键词:对氨基苯磺酰胺、磺胺药物,红外光谱Abstract:As a simple sulfa drugs, Sulfanilamide put into mass production. Sulfa drugs can inhibit the growth and multiplication of certain kinds of bacteria and a few virus for the preventing bacteria infections. In this experiment, benzene was treated by nitration, reduction, acylation, chlorine, ammonia substitution, hydrolysis and a series of reactions to get sulfanilamide. The structure of sulfanilamide was characterized by melt point and IR spectra analysis.Key words: Ammonium p-aminobenzene sulfonic acid, sulfa drugs, IR前言:磺胺药物是含磺胺基团合成抗菌药的总称,能抑制多种细菌和少数病毒的生长和繁殖,用于防治多种病菌感染。


一、工艺设计阶段〔一〕、磺胺背景资料1、发展历程:磺胺类药物的发现,开创了化学治疗的新纪元,使死亡率很高的细菌性传染疾病得到了控制。
同时它的作用机制的阐明为药物研究提供了新的思路——代谢拮抗。
早在1908年,磺胺就被合成,但当时仅作为合成偶氮染料的中间体,无人注意到它的医疗价值。
直到1932年domagk发现了百浪多息,可以使鼠、兔免受链球菌和葡萄球菌的感染,次年报告了用百浪多息治疗由葡萄球菌引起败血症的第一病例,引起了世界范围的极大兴趣。
令人奇怪的是“百浪多息〞只有在体内才能杀死链球菌,而在试管内则不能。
而由于乙酰化是体内代谢的常见反应,因此推断百浪多息在体内代谢成磺胺,而产生抗菌作用。
然后证明磺胺在体内外均有抑菌作用。
从此之后,磺胺名字很快在医疗界广泛传播开来;磺胺类药物的研究工作发展极为迅速。
1937年制出“磺胺吡啶〞,1939年制出“磺胺噻唑〞,1941年制出了“磺胺嘧啶〞……至1946年共合成了5500余种磺胺类化合物,并有20余种作为合成抗菌药在临床上使用。
磺胺类药物在细菌性传染的化学治疗上,有卓越的功效。
它的发现以及随之而来的一系列新的磺胺药物合成上的研究成果,是医疗事业上一件有极重要意义的事。
人类依靠了磺胺类药物,在与病菌作战中,取得过空前的胜利。
许多严重的危机人们生命安全的疾病,诸如产褥热、丹毒、猩红热、败血症以及肺炎、骨髓炎、流行性脑膜炎、细菌性痢疾和各种创伤传染及眼耳鼻喉等的化脓性传染等,都纷纷低头;它的治疗功效,在化学治疗学上,写下了光辉的一页。
2、磺胺〔对氨基苯磺酰胺〕[结构式]:[化学名] 对氨基苯磺酰胺[中文通用名称] 磺胺[英文通用名称] Sulfanilamide[其他名称] 磺酰胺、对苯胺磺酰胺、对磺酰胺苯胺。
[性状] 从乙醇水溶液中析出者为白色叶片状结晶或结晶性粉末,无臭,味先微苦而后甜,遇光变色。
相对分子质量172.22。
相对密度1.08。
熔点165~166℃。


药物设计之磺胺类药物的改造磺胺类药物的发现,开创了化学治疗的新纪元,使死亡率很高的细菌性传染疾病得到了控制。
磺胺类药物的母体对氨基苯磺酰胺(sulfanilamide)又称为磺胺,早在1980年就被合成,但当时仅作为合成偶氮染料的中间体,无人注意到它的医疗价值。
直到1932年磺胺类化合物改造生成的百浪多息(prontosil)治疗了有葡萄球菌引起的败血症的第一病例,才引起了世界范围的极大兴趣。
磺胺类的药物的作用机制有许多学说,最为广泛被认可的胃Wood-Fields学说。
该学说认为磺胺类药物能与细菌生长所必须的对氨基苯甲酸(PABA)产生竞争性拮抗,干扰了细菌的酶系统对PABA的利用,PABA是叶酸的组成部分,叶酸为微生物生长中的必要物质,也是构成体内叶酸辅酶的基本原料。
PABA在二氢叶酸合成酶的催化下,与二氢蝶啶焦磷酸酯及谷氨酸或二氢蝶啶焦磷酸酯对氨基苯甲酰谷氨酸(PABG)合成二氢叶酸。
再在二氢叶酸还原酶作用下还原成四氢叶酸,为细菌合成核酸提供叶酸辅酶。
Bell-Roblin指出,磺胺类药物之所以能和PABA竞争性拮抗,是由于分子大小与电荷分布极为相似的缘故。
由于磺胺类药物和PABA的这种类似性,使得在PABG的生物合成中,磺胺类药物可以取代PABA的位置,生成无功能的化合物,妨碍了PABG的生物合成。
PABG 经二氢叶酸还原酶作用还原为四氢叶酸,后进一步合成辅酶F。
辅酶F为DNA合成中所必须的嘌呤、嘧啶碱基的合成提供一碳单位。
人体作为微生物的宿主,可以从食物中摄取PABG,因此,磺胺类药物不影响正常叶酸代谢,而微生物靠自身合成PABG,一旦叶酸代谢受阻,生命就不能继续,因此微生物对磺胺类药物都敏感。
通过查阅相关资料,得出磺胺类药物的构效关系如下:(1)对氨基苯磺酰胺结构是必要的结构。
即苯环上的氨基与磺酰胺基必须在对位,在邻位或间位无抑菌作用。
(2)芳氨基的氮原子上一般没有取代基,若有取代基则必须在体内易被酶分解或还原为游离的氨基才有效,否则无效。

磺胺醋酰钠合成路线改进一、本文概述本文旨在探讨磺胺醋酰钠合成路线的改进,以期提高生产效率、降低成本并减少环境污染。
磺胺醋酰钠作为一种重要的医药中间体,广泛应用于抗生素、磺胺类药物等领域。
然而,传统的合成路线存在诸多不足,如原料成本高、反应条件苛刻、废弃物产生量大等,这些问题限制了磺胺醋酰钠的大规模生产和应用。
因此,研究并改进磺胺醋酰钠的合成路线,具有重要的现实意义和经济价值。
本文首先回顾了磺胺醋酰钠的传统合成路线,分析了其存在的问题和不足。
在此基础上,提出了一种改进的合成路线,并对其进行了详细的实验验证。
新的合成路线采用了更为经济、环保的原料,优化了反应条件,减少了废弃物的产生。
本文还对新合成路线的经济效益和环境影响进行了评估,结果表明,改进后的合成路线在提高生产效率、降低成本和减少环境污染等方面均取得了显著的效果。
本文的研究不仅对磺胺醋酰钠的合成工艺具有指导意义,也为其他类似化合物的合成路线改进提供了有益的借鉴。
未来,我们将继续深入研究磺胺醋酰钠的合成机制,探索更为高效、环保的合成方法,为推动磺胺类药物的发展和应用做出更大的贡献。
二、现有合成路线分析磺胺醋酰钠,作为一种重要的医药中间体,其合成路线的优化对于提高生产效率、降低成本以及环保要求具有重要意义。
目前,磺胺醋酰钠的合成路线主要有以下几种。
传统的合成路线主要依赖于磺胺与醋酐的直接缩合反应。
该路线虽然操作简单,但存在原料利用率低、能耗高、产物纯度不高以及环境污染等问题。
由于反应过程中产生的副产物较多,后续分离提纯步骤繁琐,不利于工业化生产。
近年来,研究者们尝试了一些新的合成方法,如酶催化法、微波辅助法等。
这些方法在一定程度上提高了反应速度和产物纯度,但仍存在操作复杂、成本较高或设备投入大等限制。
酶催化法虽然环保,但酶的来源和稳定性问题限制了其工业化应用。
微波辅助法则需要特殊的设备,且对于反应条件的控制要求较高。
现有的磺胺醋酰钠合成路线在原料利用率、能耗、产物纯度以及环保等方面均存在一定的不足。

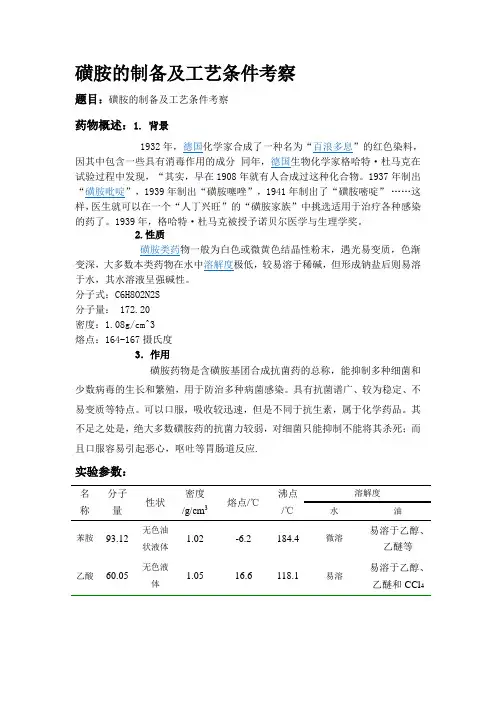
磺胺的制备及工艺条件考察题目:磺胺的制备及工艺条件考察药物概述:1. 背景磺胺类药物一般为白色或微黄色结晶性粉末,遇光易变质,色渐变深,大多数本类药物在水中溶解度极低,较易溶于稀碱,但形成钠盐后则易溶于水,其水溶液呈强碱性。
分子式:C6H8O2N2S分子量: 172.20密度:1.08g/cm^3熔点:164-167摄氏度3.作用磺胺药物是含磺胺基团合成抗菌药的总称,能抑制多种细菌和少数病毒的生长和繁殖,用于防治多种病菌感染。
具有抗菌谱广、较为稳定、不易变质等特点。
可以口服,吸收较迅速,但是不同于抗生素,属于化学药品。
其不足之处是,绝大多数磺胺药的抗菌力较弱,对细菌只能抑制不能将其杀死;而且口服容易引起恶心,呕吐等胃肠道反应.实验参数:名称分子量性状密度/g/cm3熔点/℃沸点/℃溶解度水油苯胺93.12 无色油状液体1.02 -6.2 184.4 微溶易溶于乙醇、乙醚等乙酸60.05 无色液体1.05 16.6 118.1 易溶易溶于乙醇、乙醚和CCl4乙酰苯胺氯磺酸对乙酰基苯磺酰氯对乙酰基苯磺酰胺对氨基苯磺酰胺135.17116.52233.64214.23172.21白色结晶或粉末无色或黄色液体白色或粉红色粉末白色粉末白色粉末1.221.08114.3151149219164.5-166.530480微溶于冷水,溶于热水溶微溶微溶微溶溶溶溶溶溶实验步骤:(一)苯胺乙酰化——乙酰苯胺的制备1. 乙酰化:用量筒取新蒸出的苯胺4.0mL于100mL的干净烧杯中,加水10mL,在不断搅拌下慢慢加入6mL醋酸酐,搅至晶体析出(可置于自来水或冰水中冷却),冷至室温即可得到白色的乙酰苯胺固体。
2. 抽滤收集:将上步所得固体与母液混合物抽滤分离,固体用少量冷水洗涤2次,抽干,于表面皿上用红外灯干燥,以便进行下步反应。
(二)乙酰苯胺氯磺化按图4-5装好反应装置,称取5.0g干燥的乙酰苯胺置于干燥的250mL 三颈瓶中,再在分液漏斗中加入20mL氯磺酸。


磺草胺合成路线-概述说明以及解释1.引言1.1 概述磺草胺是一种重要的草甘膦类除草剂,具有广谱、高效、低毒性等特点,被广泛应用于农业生产中的除草工作。
在农作物的生长过程中,杂草是一个常见的问题,它们竞争养分和光线资源,严重影响着农作物的生长发育和产量。
传统的除草方法主要是人工除草,但这种方法劳动密集、费时费力,无法满足大面积农田的需求。
磺草胺合成路线的研究和发展解决了这一问题。
磺草胺合成路线通过化学合成的方式,能够大量生产磺草胺,以满足农田除草的需要。
磺草胺合成路线的研究具有重要意义,不仅可以提高农作物产量和质量,还可以减少人力资源的浪费,提高农田作业效率。
本文将介绍磺草胺合成路线的重要性和应用,并对其发展前景进行展望。
通过对磺草胺合成路线的研究和了解,可以为农业生产提供科学、高效的除草方法,为农田生产保驾护航。
文章的目的是全面了解磺草胺合成路线的研究现状和发展趋势,为相关领域的科研人员和农业生产者提供参考和借鉴,推动磺草胺合成技术的进一步发展。
通过文章的撰写和阅读,希望能够加深对磺草胺合成路线的认识,为农业产业链的可持续发展做出积极贡献。
1.2 文章结构文章结构部分的内容,可以从以下几个方面展开讨论:1. 磺草胺合成路线相关研究历史回顾:介绍磺草胺合成路线研究的起源和发展过程,重点突出一些里程碑式的研究成果和突破,以及这些研究对磺草胺合成路线的意义和影响。
2. 磺草胺合成路线的现状和现有问题:概述当前已经建立的磺草胺合成路线,并简要介绍这些合成路线的优势和不足之处,指出目前存在的主要问题和待解决的难题。
3. 磺草胺合成路线的分析和评价:对已有的磺草胺合成路线进行系统分析和评价,主要从反应步骤的效率、选择性、原料的可获得性、环境友好性等方面进行综合考量,指出各个合成路线的优缺点,并探讨不同路线之间的比较。
4. 未来磺草胺合成路线的改进方向和展望:根据目前磺草胺合成路线存在的问题和需求,提出改进和优化的方向和思路,例如采用新的催化剂、反应条件和新型合成方法,以提高磺草胺的合成效率和质量,并探讨可能的创新点和发展趋势。

#技术与方法#药学专业学生实验教学磺胺醋酰钠合成工艺的改进李 零,胡伦香(贵阳医学院药学院药物化学教研室,贵州贵阳 550004)[摘 要]目的:优化磺胺醋酰钠合成工艺,以获取良好的实验教学效果。
方法:改变磺胺醋酰合成实验的反应温度、反应时间、控制反应过程中的p H 值,对滴加醋酐的加入方法也作了一定的改进,观察磺胺醋酰及磺胺醋酰钠的产量。
结果:延长交替滴加醋酐时间至9~13m i n 、反应温度60~65e 或延长反应时间至40~60m i n ,可提高磺胺醋酰的产量。
结论:改变滴加醋酐的方式、适当延长反应时间和提高反应温度,均有利于磺胺醋酰钠产率的提高。
[关键词]化学,药物;磺胺醋酰钠;工艺学,制药[中图分类号]R988.1 [文献标识码]B [文章编号]1000-2707(2010)06-0646-02 磺胺醋酰钠在临床上主要用于沙眼、结膜炎等眼科感染,其合成原料易得,反应步骤少,且疗效肯定,副反应小,是一种眼科常用药物。
磺胺醋酰钠的合成是药物化学实验教学中常规项目之一,在实验教学过程中发现,合成磺胺醋酰的产率较低,致使磺胺醋酰的成盐反应很难获取产品。
从2009年9月开始,在学生教学实验中对磺胺醋酰钠合成工艺进行了改进,报告如下。
1 材料和方法1.1 药品与仪器电动搅拌器、温度计(100e )、布氏漏斗,量杯10m l 、50m l 、球形冷凝管30c m 、250m l 三颈瓶、100m l 及250m l 吸滤瓶。
药用级磺胺,醋酐、盐酸、氢氧化钠及活性炭。
1.2 实验方法1.2.1 反应原理 合成原理见图1。
图1 反应原理路线图Fig .1 A sche m atic d iagra m sho w i n gthe princ i p le of reaction1.2.2 改进前磺胺醋酰钠合成的实验步骤[1]在装有搅拌子及温度计的100m l 三颈瓶中,加入磺胺17.2g ,22.5%氢氧化钠22m ,l 开动搅拌,并加热至50e 左右。
实验二磺胺醋酰钠的合成【药物概述】磺胺醋酰钠在临床上主要用于沙眼、结膜炎等眼科感染,其合成原料易得,反应步骤少,且疗效肯定,副反应小,是一种眼科常用药物.【1】本品为白色粉末,无臭.本品为短效磺胺类药物,具有广谱抑菌作用.因与对氨基苯甲酸竞争细菌的二氢叶酸合成酶,使细菌叶酸代谢受阻,无法获得所需嘌呤和核酸,致细菌生长繁殖受抑制.本品对大多数革兰氏阳性和阴性菌有抑制作用,尤其对溶血性链球菌、肺炎双球菌、痢疾杆菌敏感,对葡萄球菌、脑膜炎球菌及沙眼衣原体也有较好抑菌作用.对真菌有一定作用.而作为合成磺胺醋酰钠的原料——磺胺醋酰,可用于由敏感细菌引起的角膜炎、睑缘炎、结膜炎、泪囊炎等,也可用于沙眼衣原体感染的辅助治疗和眼外伤的治疗,还可在结膜、角膜及内眼手术前、后用于预防感染,非眼用制剂可用于细菌性阴道炎和寻常性痤疮.磺胺醋酰最初由K.A.Jense等以对硝基苯磺酰胺为原料制得.随后中国著名化学家黄鸣龙等用乙酸酐和乙酸对磺胺直接酰化,得二乙酰化物,经水解得磺胺醋酰,收率为77%.1949年日本学者以对乙酰氨基苯磺酰胺为原料,在NaOH存在下经醋酐酰化再水解,得到磺胺醋酰.1958年O.Leoveanu等提出了酸催化乙酰化方法.1989年Kravchenga N.A.提出选择性乙酰化制备磺胺醋酰的方法.【2】也有人提出用碱催化进行乙酰化的方法,收率为58.3%,尤启冬所编教材《药物化学实验指导》即采用此法.【3】2003年何黎琴等在文献方法基础上加入吡啶以提高醋酐的酰化能力,产率为63.5%.【4】2005年王淑月等通过相转移催化法合成了磺胺醋酰,产率为71.67%.【5】【目的和要求】1. 通过本实验,掌握磺胺类药物的一般理化性质,并掌握如何利用其理化性质的特点来达到分离提纯产品的目的.2. 通过本实验操作,掌握乙酰化反应的原理.【原理】【1】【仪器和试剂】仪器装置图2012~2013学年药物化学实验设计试剂总览原料名称规格用量摩尔数摩尔比磺胺CP 17.2g 0.1 1醋酐CP 13.6ml 0.142 1.42氢氧化钠22.5% 22ml 0.1125 1.13氢氧化钠77% 12.5ml 0.1925 1.9试剂主要性质试剂名称性质磺胺白色颗粒或粉末状结晶,无臭.味微苦.微溶于冷水、乙醇、甲醇、乙醚和丙酮,易溶于沸水、甘油、盐酸、氢氧化钾及氢氧化钠溶液,不溶于氯仿、乙醚、苯、石油醚.醋酐无色易挥发液体,具有强烈刺激性气味和腐蚀性.溶于冷水,溶于氯仿、乙醚和苯.氢氧化钠纯品是无色透明的晶体.易溶于水,同时强烈放热.并溶于乙醇和甘油;不溶于丙酮、乙醚.露放在空气中,最后会完全溶解成溶液.试剂主要理化常数物质分子量熔点/℃性质磺胺172.21 溶于氢氧化钠水溶液磺胺醋酰214.24 182-184 微溶于水(150:1),溶于无水乙醇(15:1)pK a1(芳伯氨基):1.8,pK a2(磺酰氨基):5.4磺胺醋酰钠236.23 257 易溶于水(1.5:1),微溶于96%乙醇【方法和步骤】【6】一、磺胺醋酰(SA)的制备1.在装有搅拌器、温度计和回流冷凝管的三颈瓶中投入磺胺17.2g及22.5%氢氧化钠溶液22ml,开始搅拌,于水浴上加热至50℃左右.2.待物料溶解后,滴加醋酐3.6 ml,隔5min后滴加77%氢氧化钠溶液2.5ml,并保持反应液pH在12~13之间.第2页实验二磺胺醋酰钠的合成3.随后每隔5min交替滴加醋酐及氢氧化钠溶液,每次2ml,加料期间反应温度维持在50~55℃及pH12~13.4.加料毕,继续保持温度搅拌反应30min,将反应液转入烧杯中,加水20ml稀释.用浓盐酸调pH至7,于水浴中放置1~2h,冷却析出固体.5.抽滤固体,用适量冰水洗涤.洗液与滤液合并后用浓盐酸调pH至4~5,滤取沉淀压干.6.沉淀用3倍量的10%盐酸溶解,放置30min,抽滤除去不溶物.滤液加少量活性炭室温脱色后,用40%氢氧化钠溶液调pH至5,得磺胺醋酰,抽滤.7.于红外灯下干燥得产品,熔点179~184℃.如熔点不合格,可用热水(1:15)精制.注:(1)本实验中使用氢氧化钠溶液有多种不同浓度.在试验中切勿用错,否则会导致实验失败.(2)滴加醋酐和氢氧化钠溶液是交替进行,每滴完一种溶液后,让其反应5min后,再滴加另一种溶液.滴加是用玻璃管滴加,滴加速度不宜过快.(3)反应中保持反应pH在12~13之间很重要,否则收率将会降低.(4)在pH7是析出的固体不是产物,应弃去,产物在滤液中.(5)在pH4~5析出的固体是产物.(6)本实验中,溶液pH的调节是反应能否成功的关键,应小心注意,否则实验会失败或收率降低.二、磺胺醋酸钠的制备将上步所得的磺胺醋酰投入烧杯中,滴加少量(0.5ml)水润湿.于水浴上加热至90℃,滴加40%氢氧化钠溶液至恰好溶解,溶液pH为7~8,趁热抽滤,滤液转至小烧杯中放冷析出晶体,抽滤,干燥,得磺胺醋酰钠.注:(1)加入水的量以磺胺醋酰略湿即可.0.5ml较难控制,可适当多加入一些,在析出晶体时在蒸发去一些水分.第3页2012~2013学年药物化学实验设计第4页(2)此步须趁热过滤漏斗应先预热.若滤液放置后较难析出晶体,可至电炉上略加热,使其挥发去一些水分,再放冷析晶.【其他合成路线和方法改进】1.用相转移催化法合成磺胺醋酰本实验改进方法以磺胺为原料以醋酐为酰化剂,以TEBA(三乙基卞基氯化铵)为相转移催化剂在氢氧化钠存在下进行反应,反应式如下:本实验改进方法学者通过正交实验探索出,保温温度过低,不利于乙酰化反应的进行,产率较低,故加料温度在30~50℃,保温温度应控制在50~55℃,加入相转移催化剂TEBA 0.2 g,ω(NaOH)为31%能明显增加磺胺醋酰的产率.(1)由于TEBA对水不稳定,故该路线加大了ω(NaOH),将TEBA和乙酸酐同时投入,减少了TEBA的分解.TEBA将磺胺阴离子带入底物——醋酐中,同时也将反应后的醋酸根阴离子带入水相,因此提高了产率,也加快了反应速率.(2)本路线对单、双乙酰化物的分离方法进行了改进,磺胺醋酰在体积分数为70%~75%的乙醇溶液中溶解度最大,而双乙酰化产物溶解度极小,故用乙醇溶解磺胺醋酰,分离出双乙酰化产物,然后蒸出乙醇和水,得到目标产物.其优点为不经过酸碱中和反应,直接利用待分离物的溶解性差异进行分离,减少了分离步骤,蒸出的乙醇可以套用,减少了对环境的污染,提高了产率.【5】2.以吡啶为催化剂;用NaOH乙醇液代替NaOH水溶液与磺胺醋酰成盐磺胺醋酰制备中,加少量吡啶做催化剂,可使醋酐酰化能力增强,磺胺利用率有明显提高,磺胺醋酰的收率也由原来的约50%提高到70%左右.在磺胺醋酰钠制备过程中,采用NaOH水溶液与磺胺醋酰成盐,操作繁琐,需要90%的水浴加热,调整到pH7~8后趁热过滤,在实验教学过程中,发现严格按上述步骤操作,仍很难得到产品,因磺胺醋酰钠易溶于水.根据磺胺醋酰钠略溶于乙醇的物理性质,用NaOH乙醇液取代NaOH 水溶液,并按计算量进行投料.通过实验验证,此步改进使操作简单化,避免了热水浴,只需在室温中进行,所用乙醇可通过蒸馏回收,重新利用,更为可贵的是,成盐一步收率可达98%以上,通过定性分析,与磺胺醋酰钠一致.【4】3.改变实验过程中的反应条件及投料方式反应中保持pH 12~13,必要时需补加碱液.滴加醋酐的方法对反应影响较大,慢滴快加搅拌是操作的关键,有两种方法有利于磺胺醋酰的生成:一是将交替滴加醋酐的时间由原来每次5min延长至10min左右(9~13min);二将原来交替滴加醋酐5次(每次2ml)改为交替滴加4次(每次2.5ml),并保持每次滴加醋酐的时间为10min.将反应温度提高到60~65℃,或延长反应时间至40~60min,均可提高磺胺醋酰的产率.【1】【问题和讨论】1.为什么在第一步反应中会生成副反应产物——磺胺双醋酰?答:因为磺胺中4-胺基的电子云密度大于1-磺酰胺基的电子云密度,1-磺酰胺基上的弱酸性加实验二磺胺醋酰钠的合成入强碱可生成盐,使得1-磺酰胺基的电子云密度增大.磺酰胺基成盐后N原子上具有强电负性,然后另一分子中硫原子具有强正电性,于是两分子发生缩合反应,生成磺胺双醋酰.2.磺胺醋酰钠的合成中为什么乙酐和氢氧化钠交替滴加?答:磺胺和乙酐反应生成主产物是我们需要的,该反应为放热反应,多次少量加入是为了便于控制温度;加入氢氧化钠是为了保持pH值,因为碱性环境下副产物少主产物多,交替反应也利于pH值的控制.3.酰化液处理的过程中,pH 7时析出的固体是什么?pH 5时析出的固体是什么?10% 盐酸中的不溶物是什么?答:pH=7时候析出的固体是未反应的磺胺;pH=5的时候析出的是磺胺醋酰;10%盐酸中不溶物是杂质和未反应的磺胺.4.为什么在10%盐酸中有不溶物析出?答:因为在10%盐酸溶液中磺胺醋酰生成盐酸盐而溶解,而磺胺双醋酰由于结构中无游离的芳伯胺基,不能和盐酸成盐故析出.5.磺胺醋酰钠的合成为什么调pH 7~8?答:滴加40%氢氧化钠溶液调pH7~8时可见溶液澄明,显示磺胺醋酰已生成磺胺醋酰钠,若有微量不溶物,可能是未除尽的副产物.氢氧化钠溶液切勿过量,因磺胺醋酰钠在强碱性溶液中和受热情况下,易氧化水解而致产量和质量下降.6.反应过程中,调节pH在12~13是非常重要的.若碱性过强,其结果是磺胺较多,磺胺醋酰次之,双乙酰物较少;碱性过弱其结果双乙酰物较多,磺胺醋酰次之,磺胺较少,为什么?答:因碱度过大,磺胺双醋酰易水解成磺胺,且易引起磺胺醋酰水解成磺胺;而因碱度过小时,反应过程中易生成较多的N-乙酰磺胺,且磺胺双醋酰分子结构中的N-乙酰基不易水解下来,所以该反应必须控制好pH 值.7.将磺胺醋酰制成钠盐时,为什么要严格控制22.5%NaOH溶液的用量?答:将磺胺醋酰制成钠盐时,必须要严格控制22.5%NaOH溶液的用量.因磺胺醋酰钠水溶性大,由磺胺醋酰制备其钠盐时若22.5%NaOH的量多,则损失很大.必要时可加少量丙酮,使磺胺醋酰钠析出.8.磺胺类药物有哪些理化性质?答:(1)酸碱性因本类药物分子中有芳香第一胺,呈弱碱性;有磺酰氨基,显弱酸性,故本类药物呈酸碱两性,可与酸或碱成盐而溶于水.(2)自动氧化反应本类药物含芳香第一胺,易被空气氧氧化.(3)芳香第一胺反应磺胺类药物含芳香第一胺,在酸性溶液中,与亚硝酸钠作用,可进行重氮化反应,利用此性质可测定磺胺类药物的含量.生成的重氮盐在碱性条件下,生成橙红色偶氮化合物,可作本类药物的鉴别反应.(4)与芳醛缩合反应芳香第一胺能与多种芳醛(如对二甲氨基苯甲醛、香草醛等)缩合成具有颜色的希夫碱.(5)铜盐反应磺酰氨基上的氢原子,可被金属离子(如铜、银、钴等)取代,生成不同颜第5页2012~2013学年药物化学实验设计色的难溶性沉淀,可用于鉴别.9.如何利用磺胺类药物的理化性质进行产品纯化?答:利用主产物和副产物的解离常数不同,在不同pH条件下分别令主产物溶于溶剂而副产物不溶,过滤后弃去固体;或者主产物不溶而副产物溶,过滤后弃去溶液.10.【综上所述】为何不能通过利用第一步反应直接得到产物磺胺醋酰钠而要将其转变为磺胺醋酰后再与NaOH反应生成磺胺醋酰钠?答:首先必须明确,第一步反应中,作为反应物的醋酐、NaOH等均过量,这使得第一步生成的磺胺醋酰钠中含有醋酸钠等杂质,另外第一步反应也会产生副反应产物——磺胺双醋酰.那么,我们可以通过调节pH等方法将这些杂质等去除后再将磺胺醋酰与NaOH反应生成较纯的磺胺醋酰钠.【参考文献】1.李零,胡伦香.药学专业学生实验教学磺胺醋酰钠合成工艺的改进.贵阳医学院学报,2010,35(6):646~647.2.袁干军,黎岳南,任兆平,焦亮.培养学生科学思维的头脑——浅谈药物化学实验中磺胺醋酰钠的合成.中国科教创新导刊,2009,11:65.3.尤启东主编.药物化学实验与指导.中国医药科技出版社,2000年3月第1版:113~115.4.何黎琴,完茂林.磺胺醋酰钠合成路线改进.安徽化工,2003,2:16~17.5.王淑月,张二巧,袁志法.磺胺醋酰合成技术研究.河北科技大学学报,2005,26(2):124~126,145.6.天津大学等编.制药工程专业药物化学实验指导.化学工业出版社,2005年8月第1版:33~37.第6页。
磺胺类抗菌素药物的合成方法改进熊非;李晋;陈圣赟;胡飞【摘要】磺胺类抗菌素药物对氨基苯磺酰胺的连续多步骤合成实验是大学有机化学实验教学中的一个常见经典实验,本文采用改进的合成策略对传统合成路线中乙酰苯胺的直接氯磺化这一关键反应过程进行合成方法优化,采用先磺化、再氯代的合成策略,巧妙的避免了剧毒、强腐蚀性氯磺化试剂氯磺酸的使用,提高了反应效率,消除了学生在实验操作过程中存在的安全隐患。
%The continuous multi-step synthesis of sulfonamide antibiotics is a classic teaching case of organic chemistry experiment in universities. An efficient total synthesis of sulfanilamide was described via an improved chlorosulfonation reaction with acetanilide as the key step, which included a novel synthetic strategy based upon the aromatic sulfonation and chlorination reaction. Some limitation ( using highly toxic and corrosive chlorosulfonation ) of other reported literature was overcome and improved the security of experimental process.【期刊名称】《广州化工》【年(卷),期】2016(011)010【总页数】2页(P192-193)【关键词】磺胺药物;抗菌素;对氨基苯磺酰胺;合成【作者】熊非;李晋;陈圣赟;胡飞【作者单位】上海理工大学化学系,上海 200093;上海理工大学化学系,上海200093;上海理工大学化学系,上海 200093;上海理工大学化学系,上海 200093【正文语种】中文【中图分类】G642磺胺类药物是一类能够抑制多种细菌和少数病毒的生长和繁殖,用于预防和治疗细菌感染性疾病的化学合成药[1-2],为对氨基苯磺酰胺的衍生物,它也是含有磺酰胺基团的合成抗菌药物的总称。
磺胺醋酰钠药物的合成工艺研究(一)已有的合成路线或相关合成路线1.2.改进后磺胺醋酰钠合成工艺.. 反应中保持pH 12~ 13, 必要时需补加碱液。
滴加醋酐的方法对反应影响较大, 慢滴快加搅拌是操作的关键, 有两种方法有利于磺胺醋酰的生成, 一是将交替滴加醋酐的时间由原来每次5 m in 延长至10 m in左右( 9~ 13 m in) , 或将原来交替滴加醋酐5 次(每次2m l)改为交替滴加4次(每次2. 5m l), 并保持每次滴加醋酐的时间为10 m in。
将反应温度提高到60~ 65 .. , 或延长反应时间至40~ 60 m in, 均可提高磺胺醋酰的产率。
3.将以上所得的磺胺醋酰投入50ml烧杯中,滴加少量水润湿(<0.5ml)(附注1)。
于水浴上加热至90 ℃,滴加40%氢氧化钠至恰好溶解,溶液pH为7~8,趁热抽滤,滤液转至小烧杯中放冷析出结晶(附注2),抽滤,干燥,得磺胺醋酰钠9g。
(二)确定合成路线及步骤1、磺胺醋酰的制备在装有搅拌棒及温度计的100 mL三颈瓶中,加入磺胺17.2 g,22.5%氢氧化钠22 mL,开动搅拌,于水浴上加热至50℃左右。
待磺胺溶解后,滴加醋酐3.6 mL,77% 氢氧化钠2.5 mL(首先,加入醋酐3.6 mL,77% 氢氧化钠2.5 mL;随后,每次间隔5 min,将剩余的77% 氢氧化钠和醋酐分5次交替加入,每次2 ml)。
加料期间反应温度维持在50~55℃及pH12~13;加料完毕继续保持此温度反应30 min。
反应完毕,停止搅拌,将反应液倾入100mL烧杯中,加水20 mL 稀释。
用36% 盐酸调至pH 7,于冰水浴中放置30 min,并不时搅拌析出固体,抽滤固体,用适量冰水洗涤。
洗液与滤液合并后用浓盐酸调至pH 4~5,抽滤,得白色粉末。
用3倍量(3 mL / g)10% 盐酸溶解得到的白色粉末,放置30min,不时搅拌,尽量使单乙酰物成盐酸盐溶解,抽滤除不溶物。
336.
4Eisner U,Kuthan J.The chemistry of dihydrophyridines.Chem Rev,1972,72B1.
收稿日期:1998-09-21
磺胺合成工艺的改进
李志裕林克江尤启冬李明富1(南京210009中国药科大学;1枣庄277000薛城人民医院)
磺胺是应用广泛的原料药及医药中间体,现生产磺胺的起始原料为乙酰苯胺[1],成本较高。
GI Braz[2]等报导了一条采用二苯脲作为起始原料的路线,该路线经氯磺化,氨化,水解三步反应制得,操作繁琐,收率低。
我们对其进行了改进,使之更适合于工业生产。
原文献中,氨化产物要经过吡啶溶解,脱色,再用热水处理,或用氢氧化钠溶解,盐酸酸化才进行下一步水解反应。
本文叙述了氨化产物不经提纯,直接水解,简化了操作,总收率由45%~50%提高到65.7%,同时,对二苯脲的合成工艺进行了改进。
原文献[3]中需用大量的醇或苯胺作为溶剂,本文革掉了溶剂,同时加入少量锌粉,采用氮气保护,以防高温下苯胺被氧化,且收率达到94.5%。
合成路线如下。
实验部分
1二苯脲的合成
苯胺(50g,0.54mol)与尿素(16.2g,0.27mol)混和,同时加入1g锌粉,氮气保护下缓慢升温,1h后,升至190e,5h后,达240e,继续反应1h,冷却,所得白色固体用0.01M HCl研磨,抽滤,水洗,得二苯脲54.2g(94. 5%),mp229~234e(文献[3]234~236e)。
2二苯脲二磺酰氯的合成
氯磺酸(47.3g,0.4mol)冷却至10e,于20e下分次加入二苯脲(10.6g,0.05mo l),全部加完后升温至50e,反应4h,冷却至室温,反应液倾入碎冰中,静置,抽滤,冰水洗,得蜡状固体。
3磺胺的合成
将上步反应制得的产品在10e下分次加到25ml 浓氨水中,搅拌,反应2h,抽滤,得蜡状固体为氨化物。
将氨化物加到30ml的50%氢氧化钠溶液中,回流4h 后降温到80e,滴加浓盐酸,调pH5~6,冷却,抽滤得粗品,用水重结晶,得白色磺胺结晶11.3g,mp164~ 165.3e,收率65.7%(以二苯脲计算)。
产品的红外光谱与文献[4]一致,并经元素分析及薄层层析鉴定。
参考文献
1李正化主编.有机药物合成原理.北京:人民卫生出版社, 1985B423.
2Braz GI,Lizgunova M U,Ch emerisskaya AA,et al.
Sulfanilamide from diph enylurea.J Applied Chem(USSR), 1946,19B379(CA,41:1215f,1947).
3Nagaraj R Ayyangar,Anil R Chowdhary,Uttam R Kalkote,et al.A non-phosgen e route for th e synthesis of sym-N,N c-diethyldiphenylurea.Chemis try and Industry,1988B599.
4中华人民共和国卫生部药典委员会编.药品红外光谱集.
北京:化学工业出版社,1995B560.
收稿日期:1998-05-25
醛糖还原酶抑制剂依帕司特的合成
姜晔张荣久麻凯旋任宇王德才梁淑芳(南京210009江苏省药物研究所)依帕司特(epalrestat,1),化学名5-[(1Z,2E)-2-甲
基-3-苯基-2-丙烯亚基]-4-氧代-2-硫代-3-噻唑烷乙酸,由日本小野药品工业株式会社1992年1月21日日本姜晔,男,32岁。
1990年毕业于中国药科大学药物化学专业,硕士学位
#
25
#
中国现代应用药学杂志1999年10月第16卷第5期。