2 钒的性质
- 格式:ppt
- 大小:552.00 KB
- 文档页数:19

二氧化钒折射率matlab-概述说明以及解释1.引言1.1 概述在概述部分,我们将介绍二氧化钒这种化合物的基本概念和特性。
二氧化钒是一种化学式为VO2的化合物,它由钒和氧两种元素组成。
与许多金属氧化物类似,二氧化钒具有多种物理和化学性质,使其在各种领域有广泛的应用。
二氧化钒的一个重要特性是其电子结构的可调节性。
在较低温度下,二氧化钒的结构为单斜晶系,具有半导体性质。
当温度升高到临界点(约68摄氏度)以上时,二氧化钒会发生相变,结构变为四方晶系,并呈现出金属特性。
这种结构调变现象使得二氧化钒成为电子器件、存储器件和光学器件等领域的研究热点。
除了电子性质,二氧化钒还具有磁性、光学和热学性质。
一些研究表明,二氧化钒在特定的条件下表现出磁性行为,这对于磁性存储器件和传感器等应用具有重要意义。
此外,二氧化钒在红外光波段具有较高的折射率,因此在光学材料和光电器件中有着潜在的应用价值。
在二氧化钒的制备方法方面,研究人员已经开发出多种化学、物理和生物合成方法。
这些方法旨在获得高纯度和可控性的二氧化钒材料,并进一步探索其特性和应用潜力。
总之,二氧化钒作为一种多功能化合物,在电子、光学、磁性和热学等领域都有重要的研究价值和应用前景。
随着对其性质和制备方法的深入研究,我们可以期待二氧化钒在新型器件和材料的开发中发挥更大的作用,并带来更多的科学和技术进展。
1.2 文章结构文章结构部分的内容可以编写如下:文章结构部分主要介绍了整篇文章的组成和章节安排。
本文共包括引言、正文和结论三个部分。
引言部分主要对本文的研究主题进行了概述,并介绍了文章的结构和目的。
接下来,正文部分将详细探讨二氧化钒的性质、制备方法和应用领域。
最后,结论部分对二氧化钒的重要性、潜在应用价值进行总结,并展望了二氧化钒研究的未来发展方向。
通过这样的结构布局,读者可以清晰了解文章的组成,同时也能更好地理解和掌握二氧化钒的相关知识。
接下来,我们将逐一介绍这些内容,为读者提供全面、系统的二氧化钒信息。


1.钒A.物理性质钒是一种单晶金属,呈银灰色,具有体心立方晶格,曾发现在1550℃以及-28~-38℃时有多晶转变。
钒的力学性质与其纯度及生产方法密切相关。
O、H、N、C等杂质会使其性质变脆,少量则可提高其硬度及剪切力,但会降低其延展性。
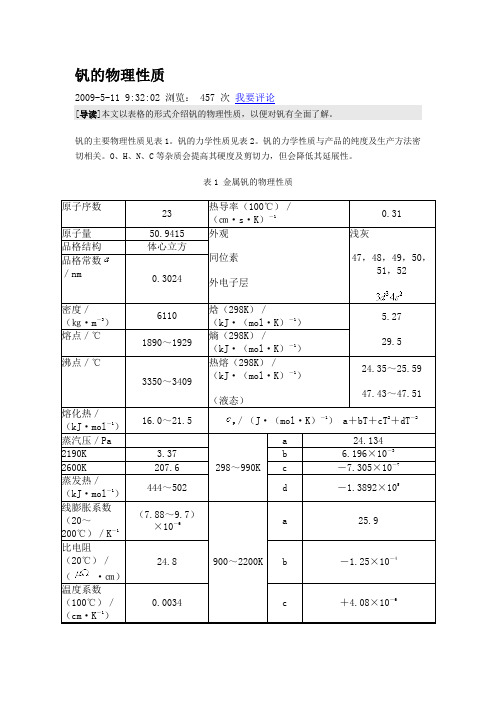
钒的主要物理性质见表2-1钒的力学性质如表2-2所示。
表2-1 金属钒的物理性质性质数值性质数值原子序数23 热导率(100℃)/J·(cm·s·K)-10.31原子量50.9415 外观浅灰晶格结构体心立方外电子层3d34s2晶格常数a/mm 0.3024 焓(298K)/kJ·(mol·K)-1 5.27密度/kg·m-36110 熵(298K)/J·(mol·K)-129.5熔点/℃1890~1929 热容c p(298K液态)/kJ·(mol·K)-124.35~25.59 47.43~47.51沸点/℃3350~3409熔化热/kJ·mol-116.0~21.5热容c p①(298~990K)/kJ·(mol·K)-1a.24.134b.6.196×10-3c.-7.305×10-7d.-1.3892×105蒸气压/Pa 1.3×10-6(1200℃)1.3(2067℃)3.73(2190K) 207.6(2600K)蒸发热/kJ·mol-1444~502热容c p②(900~2200K)/kJ·(mol·K)-1a.25.9b.-1.25×10-4c.4.08×10-6线膨胀系数(20~200℃)/K-1(7.88~9.7)×10-6比电阻(20℃)/μΩ·cm24.8 温度系数(100℃)/cm·K-10.0034钒同位素46V 47V 48V 49V 50V 51V 52V 53V 54V 半衰期0.426s 33min 16.0d 330d 6×1015a 稳定 3.75min 2.0min 55s 丰度/% 0.25 99.75①c p=a+b T+c T 2+d T -2;②c p=a+b T+c T 2,式中,T为温度,K。

钒的性质及用途简介钒是一种神奇的金属,化合价有2+、3+ 和5+ ,金属单质钒很少,其主要形态有:VO(氧化钒),V2O3(三氧化二钒),V2O5(五氧化二钒),FeV(钒铁)及偏钒酸铵等,工业上使用最多的是V2O5和FeV,主要用于冶金的添加剂,增强钢铁的强度和韧性。
一、性质1、钒的性质钒(Vanadium),化学符号V,元素周期表中序数为23,原子量为50.94。
钒是银白色略带蓝色的金属,具有延展性;含有氧、氮、氢时则变脆、硬。
钒在较高的温度下与原子量较小的非金属形成稳定的化合物;在低温下有良好的耐腐蚀性。
钒进入合金后可增强合金的强度,降低热膨胀系数。
钒在地壳中的丰度约为0.02%,比铜、锌、镍、铬都高。
按地壳中元素丰度排列第13位。
可以说,在地壳中含有非常丰富的钒金属。
但钒金属有一个特点,很难形成独立的矿床,伴生性非常明显,因此在自然界非常分散,通常和其他金属伴生,如:钒钛磁铁矿。
因此,不太容易单独对钒金属进行开采和提炼,钒产品多作为冶金业的副产品生产。
2、五氧化二钒的性质五氧化二钒(V2O5)为褐色固体,有两种形态:粉状和片状,因在富氧和缺氧的加热条件下而得到不同的形态。
五氧化二钒有毒性。
在国际化学剧毒品名录中排名第43位。
其毒性主要是对呼吸道有刺激,引起鼻粘膜充血。
如果过多的吸入了粉状的五氧化二钒,有头昏、恶心等感觉,擤鼻涕时可能会带有血丝。
如果五氧化二钒中毒,离开了现场症状自然缓解,休息一两天一般自然恢复,不需治疗。
在国内没有对五氧化二钒毒性检测的规程,但中华人民共和国国标中也明确列示其为剧毒物质,生产过程需要在省级安监部门办理安全生产许可证。
3 、偏钒酸铵偏钒酸铵(NH4VO3)为白色结晶体,既是一种独立的产品,也是制造五氧化二钒的上一道工序的中间产品,其性质与五氧化二钒相似,其生产也需要办理安全生产许可证。
4 、钒铁的性质工业上使用的钒,主要是元素钒。
五氧化二钒(V2O5)中,钒的原子量仅占56%,其余为氧原子量。

二价钒离子颜色钒是一种过渡金属,它的化学性质非常活泼,可以形成多种价态。
其中,二价钒离子是最常见的一种价态,在化学反应和化合物中都有广泛应用。
二价钒离子具有特殊的颜色,通常呈现出深蓝或紫色的色调,这是因为它们的电子结构和分子结构导致的。
二价钒离子的电子结构二价钒离子的电子结构为[d]3,其中d轨道填满了三个电子。
这意味着二价钒离子具有一个未成对电子,这个电子是从3d轨道中提升到4s轨道的。
这个未成对电子赋予了二价钒离子一些特殊的化学性质,比如它们很容易与其他物质发生化学反应,形成各种化合物。
二价钒离子的分子结构二价钒离子在化合物中通常呈现出八面体分子结构,这是因为它们的电子构型和价态所决定的。
在八面体分子结构中,钒离子处于八面体的中心位置,周围六个配位原子分别位于八面体的六个顶点。
这种分子结构是二价钒离子和其他物质发生化学反应的基础。
二价钒离子的颜色二价钒离子的颜色通常呈现出深蓝或紫色的色调,这是因为它们的电子结构和分子结构导致的。
在八面体分子结构中,二价钒离子的未成对电子可以吸收光子,从而发生能级跃迁。
这个能级跃迁所对应的光子通常是在红外和可见光谱范围内的,因此我们可以看到深蓝或紫色的颜色。
除了深蓝或紫色,二价钒离子还可以呈现出其他颜色,这取决于它们所处的化合物和化学环境。
比如,二价钒离子在硫酸钒(II)中呈现出黄绿色,而在氯化钒(II)中呈现出绿色。
这些颜色的产生也是由于能级跃迁所导致的。
总结二价钒离子是一种常见的钒离子,具有深蓝或紫色的颜色。
这种颜色的产生是由于它们的电子结构和分子结构所决定的。
二价钒离子在化学反应和化合物中有广泛应用,比如在钒酸盐和钒氧化物的生产中。
了解二价钒离子的颜色和化学性质有助于我们更好地理解它们的应用和反应过程。
钒元素的颜色之谜揭秘钒在玻璃和颜料中的奇妙应用钒元素的颜色之谜揭秘:钒在玻璃和颜料中的奇妙应用钒元素是一种重要的过渡金属,在自然界中以多种氧化态存在。
除了在钢铁、合金、化工等行业中的广泛应用外,钒元素还有着让人惊叹的颜色表现能力。
本文将揭秘钒在玻璃和颜料中的奇妙应用。
第一章:钒元素的基本特性钒(V)的原子序数为23,原子量为50.94,其5s、4d轨道的电子结构决定了其物理、化学性质。
钒元素在不同氧化态中呈现不同的颜色,正是由于这一特性,钒得以在玻璃和颜料中发挥其独特的应用。
第二章:钒在玻璃中的应用2.1 钒元素赋予玻璃颜色的原理在玻璃中添加不同氧化态的钒,可以赋予玻璃不同的颜色。
比如,加入钒的最低氧化态,可以使玻璃呈现蓝色或绿色,而加入更高氧化态的钒则可使玻璃呈现黄色、橙色或红色。
2.2 钒玻璃制品的应用领域钒玻璃广泛应用于建筑、艺术品和光学仪器等领域。
在建筑中,钒玻璃可以通过调控钒元素的氧化态而呈现不同的颜色,增加建筑的美观性。
在艺术品中,钒玻璃的独特颜色效果使得作品更加生动鲜明。
在光学仪器中,钒玻璃可以用于滤光片、摄像机镜头等器件的制造,以调节和改善光线的颜色。
第三章:钒在颜料中的应用3.1 钒颜料的种类及特点钒颜料主要包括氧化钒黄、氧化钒红、氧化钒绿等,这些颜料都以钒元素的不同氧化态为基础,拥有鲜艳的颜色和良好的耐光性。
钒颜料的应用广泛,可以用于绘画、印刷、塑料等行业。
3.2 钒颜料对环境和健康的影响尽管钒颜料有着出色的色彩表现力,但其对环境和健康也有一定的影响。
钒颜料在加工和使用过程中会释放出部分钒元素,当超过一定浓度时可能对环境产生污染,因此在生产和使用中需要采取适当的措施来减少钒元素的释放。
结论:通过深入分析钒元素在玻璃和颜料中的应用,我们可以更好地理解钒元素在颜色表现方面的奇妙能力。
钒元素所呈现的多样化颜色,不仅丰富了人们的日常生活,而且在建筑、艺术和光学仪器等领域发挥着重要的作用。
钒离子各价态颜色
钒元素是化学元素周期表中的第23号元素,具有多种不同的氧化态。
钒的主要氧化态分别为+2、+3、+4和+5。
每个氧化态对应着不同的电荷数和结构特征,因此在化学反应中展现出不同的性质和颜色。
+2价态的钒离子是钒的最低氧化态,也被称为亚钒离子。
这种离子是银白色的固体,溶于水后呈现出浅蓝色溶液。
在有机合成中,+2价的钒离子常被用作催化剂,在反应中发挥重要的作用。
+3价态的钒离子是常见的氧化态之一,也是最稳定的态势之一。
它是蓝色的固体,溶于水后溶液呈现深蓝色。
+3价钒离子在许多领域都具有重要的应用,例如作为染料、催化剂和电池材料。
+4价态的钒离子是一种黄色的固体,溶于水后呈现浅黄色溶液。
这种氧化态的稳定性相对较低,常需要在特定条件下才能得到。
它在化学反应中也扮演着重要的角色,常用于有机合成和催化剂制备。
+5价态的钒离子是钒的最高氧化态,通常被称为过钒酸盐。
它是黄色的晶体,溶于水后呈现橙黄色溶液。
+5价钒离子在化学反应中具有强氧化性,常用作催化剂、电池材料和化学分析试剂。
铜化学元素钒-概述说明以及解释1.引言1.1 概述概述部分:铜和钒都是重要的化学元素,具有广泛的应用价值。
铜是一种常见的金属元素,具有良好的导电性和导热性,被广泛用于制造电线、管道、电器等。
钒是一种稀有的过渡金属元素,具有良好的耐磨性和热稳定性,被广泛用于合金制品、汽车零部件等领域。
本文将深入探讨铜和钒的性质以及它们的化合物,探索其在各个领域的应用与前景展望。
1.2 文章结构本文将首先介绍铜和钒这两种元素的性质,包括它们的物理性质和化学性质。
随后将重点讨论铜和钒之间的化合物,探讨它们的合成方法、结构特点和应用领域。
最后,我们将总结铜和钒的化学性质,并展望它们在未来的应用前景。
通过对这两种元素的深入研究,我们可以更好地了解它们在化学领域的重要性和潜在价值。
1.3 目的:本文旨在深入探讨铜和钒这两种化学元素的性质,并重点介绍它们的化合物。
通过对铜和钒的化学性质进行分析和比较,可以帮助读者更好地理解这两种元素在化学反应中的作用和特点。
此外,文章还将探讨铜和钒在工业生产和科学研究中的应用,展望其在未来的发展前景。
通过阐述铜和钒的重要性和应用前景,可以帮助读者更全面地认识这两种元素的价值和重要性。
2.正文2.1 铜的性质铜是一种重要的化学元素,原子序数为29,原子量为63.55,元素符号为Cu,属于第一周期第一族的过渡金属元素。
铜具有良好的导电性和导热性,是一种黄色的金属,常用于制作导线、管道和各种器具。
以下是铜的一些主要性质:1. 物理性质:- 密度:铜的密度为8.96克/立方厘米,是一种密度较高的金属。
- 熔点和沸点:铜的熔点为1083摄氏度,沸点为2595摄氏度。
- 色泽:铜呈现黄色金属光泽,表面可因氧化而呈现绿色。
2. 化学性质:- 反应性:铜在常温下不会与空气和水反应,但是会与氧气和酸性物质反应,产生氧化铜。
- 氧化态:铜主要存在+1和+2的氧化态,+1氧化态的化合物为氧化亚铜(Cu2O),+2氧化态的化合物为氧化铜(CuO)。