第十三章 d区和ds区元素
- 格式:ppt
- 大小:3.22 MB
- 文档页数:76
1ds区元素1.1 本章学习要求(1)掌握铜和银的重要化合物的性质,Cu(Ⅰ)和Cu(Ⅱ)的相互转化。
(2)掌握锌和汞的重要化合物的性质,Hg(Ⅰ)和Hg(Ⅱ)的相互转化。
(3)了解镉的重要化合物性质。
(4)了解含汞、镉废水的处理。
ds区元素包括铜族元素(铜、银、金)和锌族元素(锌、镉、汞)。
这两族元素原子的价电子构型与其它过渡元素有所不同,为(n-1)d10n s1~2。
由于它们的次外层d能级有10个电子(全满结构),而最外层的电子构型又和s区相同,所以称为ds区。
1.2 铜族元素通性和单质1.2.1概述ⅠB族元素包括铜(Cu)、银(Ag)、金(Au)三种元素,通常称为铜族元素。
铜族元素原子的价电子构型为(n-1)d10n s1。
最外层与碱金属相似,只有1个电子,而次外层却有18个电子(碱金属有8个电子)。
因此与同周期的ⅠA族元素相比,铜族元素原子作用在最外层电子上的有效核电荷较多,最外层的s电子受原子核的吸引比碱金属元素原子要强得多,所以铜族元素的电离能比同周期碱金属元素显著增大,原子半径也显著减小,铜族元素单质都是不活泼的重金属,而相应的碱金属元素的单质都是活泼的轻金属。
表 1.2-1 碱金属与铜族元素比较自然界的铜、银主要以硫化矿存在,如辉铜矿(Cu2S),黄铜矿(CuFe S2),孔雀石[Cu2(OH)2C O3]等;银有闪银矿(Ag2S);金主要以单质形式分散在岩石或沙砾中,我国江南、甘肃、云南、新疆、山东和黑龙江等省都蕴藏着丰富的铜矿和金矿。
铜族元素密度较大,熔点和沸点较高,硬度较小,导电性好,延展性好,尤其是金。
1克金可抽3公里长的金丝,可压成0.1微米的金箔,500张的总厚度比头发的直径还薄些。
金易生成合金,尤其是生成汞齐。
铜是宝贵的工业材料,它的导电能力虽然次于银,但比银便宜得多。
目前世界上一半以上的铜用在电器、电机和电讯工业上。
铜的合金如黄铜(Cu-Zn)、青铜(Cu-Sn)等在精密仪器、航天工业方面都有广泛的应用。

d区ds区重要化合物的性质化合物是由不同元素组成的物质,其性质在科学研究和工业应用中具有重要的意义。
在d区和ds区,许多化合物由过渡金属元素和其他元素组成,具有特殊的性质和应用。
本文将探讨d区和ds区重要化合物的性质。
一、配合物的性质配合物是由一个或多个中心金属离子与配体(通常是有机分子或无机阴离子)形成的化合物。
在d区和ds区,配合物具有许多重要的性质。
1. 水合作用许多金属离子在溶液中结合水分子形成水合物。
这种水合作用使得配合物具有溶解度和溶解度的变化,因此在溶液中具有良好的稳定性。
2. 配合物的颜色由于d电子的存在和转移,许多配合物具有明显的颜色。
这是由于d电子的跃迁引起的电子的吸收和发射,从而产生可见光谱。
3. 配合物的磁性许多配合物具有不同的磁性。
在配合物中,d电子的自旋和轨道运动导致了不同的磁性行为,如顺磁性和反磁性。
4. 配合物的光谱性质配合物的d电子在吸收或发射光时,产生特定的吸收光谱或发射光谱。
这些光谱可以被用来研究配合物的结构和性质。
二、过渡金属氧化物的性质过渡金属氧化物是由过渡金属元素和氧元素组成的化合物。
它们在许多重要领域具有广泛的应用。
1. 磁性过渡金属氧化物中的过渡金属离子具有未成对的d电子,因此具有磁性。
这使得它们在磁性材料和磁性存储器中具有重要作用。
2. 催化性能由于过渡金属氧化物表面具有特殊的化学性质,因此它们在催化剂中起着重要作用。
它们能够促进化学反应,提高反应速率。
3. 电子导电性过渡金属氧化物具有良好的电子导电性,因此它们在电池和电子器件中被广泛应用。
4. 光催化性能一些过渡金属氧化物具有光催化性能,能够吸收光能,催化光化学反应。
这对于环境保护和能源开发具有重要意义。
三、金属盐的性质金属盐是由金属离子和阴离子组成的化合物,其性质在生活和工业中具有重要意义。
1. 溶解度金属盐在溶液中具有不同的溶解度。
这是由于金属的化合价和盐的晶体结构等因素所决定的。
2. 导电性金属盐在溶液中能够电离成金属离子和阴离子,从而具有良好的电导性。


元素的分区与原子结构
元素周期表中的元素可以根据其电子构型被划分到不同的区域。
这些区域包括s区、p区、d区、ds区和f区,其中除ds区外,区的名称来自按构造原理最后填入电子的能级符号。
s区元素包括氢之前的碱金属元素和氢,它们的价电子构型为ns1-2,电子分布在s能级上。
p区元素包括碱土金属元素、大部分非金属元素和卤素,它们的价电子构型为ns2np1-6,电子分布在s能级和p能级上。
d区元素包括过渡金属元素,它们的价电子构型为(n-2)d1-10ns2,电子分布在d能级上。
ds区元素是指8、9、10三个纵行对应的元素,它们的价电子构型为
ns2np6,电子分布在ds能级上。
f区元素是指镧系和锕系元素,它们的价电子构型为(n-2)f1-14ns2np6,电子分布在f能级上。
元素的分区与原子结构密切相关,不同区域的元素具有不同的电子构型和性质。


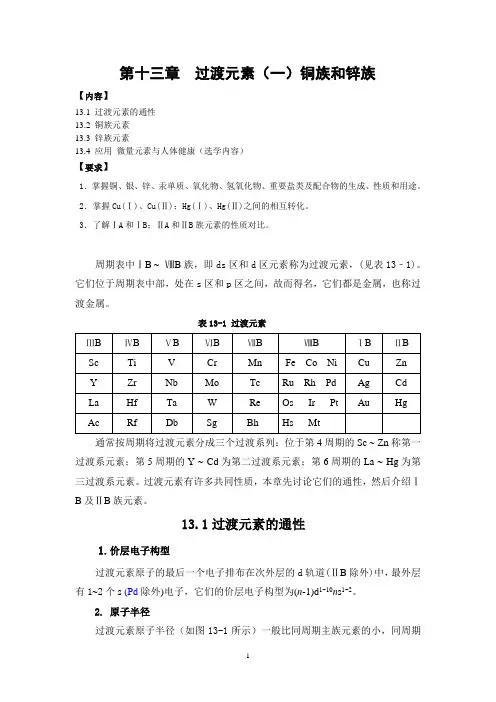
第十三章过渡元素(一)铜族和锌族【内容】13.1 过渡元素的通性13.2 铜族元素13.3 锌族元素13.4 应用微量元素与人体健康(选学内容)【要求】1.掌握铜、银、锌、汞单质、氧化物、氢氧化物、重要盐类及配合物的生成、性质和用途。
2.掌握Cu(Ⅰ)、Cu(Ⅱ);Hg(Ⅰ)、Hg(Ⅱ)之间的相互转化。
3.了解ⅠA和ⅠB;ⅡA和ⅡB族元素的性质对比。
周期表中ⅠB ~ⅧB族,即ds区和d区元素称为过渡元素,(见表13﹣1)。
它们位于周期表中部,处在s区和p区之间,故而得名,它们都是金属,也称过渡金属。
表13-1 过渡元素通常按周期将过渡元素分成三个过渡系列:位于第4周期的Sc ~ Zn称第一过渡系元素;第5周期的Y ~ Cd为第二过渡系元素;第6周期的La ~ Hg为第三过渡系元素。
过渡元素有许多共同性质,本章先讨论它们的通性,然后介绍ⅠB及ⅡB族元素。
13.1过渡元素的通性1.价层电子构型过渡元素原子的最后一个电子排布在次外层的d轨道(ⅡB除外)中,最外层有1~2个s (Pd除外)电子,它们的价层电子构型为(n-1)d1~10n s1~2。
2. 原子半径过渡元素原子半径(如图13-1所示)一般比同周期主族元素的小,同周期元素从左到右原子半径缓慢减小,到铜族前后又稍增大。
同族元素从上往下原子半径增大,但第二、第三过渡系(除ⅢB外)由于镧系收缩使同族元素原子半径十分接近,导致元素性质相似。
图13-1过渡元素原子半径3. 氧化态过渡元素有多种氧化态,因其最外层s电子和次外层部分或全部d电子都可作为价电子参与成键,一般可由+2依次增加到与族数相同的氧化态(Ⅷ族除Ru、Os外,其它元素尚无Ⅷ氧化态),这种氧化态的显著特征以第一过渡系最为典型。
表13-2第一过渡系元素的氧化数(下划线表示常见的氧化态)由13-2表可看出随着原子序数的增加,氧化数先是逐渐升高,后又逐渐降低。
这种变化主要是由于开始时3d轨道中价电子数增加,氧化数逐渐升高,当3d轨道中电子数达到5或超过5时,3d轨道逐渐趋向稳定。
s区、d区、ds区重要元素及其化合物(s Block, ds Block, d Block Elements and Compounds)9.1 s区元素s区元素中锂(Lithium)、钠(Sodium)、钾(Potassium)、铷(Rubidium)、铯(Cesium)、钫(Francium)六种元素被称为碱金属(alkali Metals)元素。
铍(Beryllium)、镁(Magnesium)、钙(Calcium)、锶(Strontium)、钡(Barium)、镭(Radium)六种元素被称为碱土金属(alkaline earth metals)元素。
锂、铷、铯、铍是稀有金属元素,钫和镭是放射性元素。
碱金属和碱土金属原子的价层电子构型分别为ns1和ns2,它们的原子最外层有1~2个电子,是最活泼的金属元素。
9.1.1 通性碱金属和碱土金属的基本性质分别列于表9-1和表9-2中。
表9-1碱金属的性质碱金属原子最外层只有1个ns电子,而次外层是8电子结构(Li的次外层是2个电子),它们的原子半径在同周期元素中(稀有气体除外)是最大的,而核电荷在同周期元素中是最小的,由于内层电子的屏蔽作用较显著,故这些元素很容易失去最外层的1个s电子,从而使碱金属的第一电离能在同周期元素中最低。
因此,碱金属是同周期元素中金属性最强的元素。
碱土金属的核电荷比碱金属大,原子半径比碱金属小,金属性比碱金属略差一些。
s区同族元素自上而下随着核电荷的增加,无论是原子半径、离子半径,还是电离能、电负性以及还原性等性质的变化总体来说是有规律的,但第二周期的元素表现出一定的特殊性。
例如锂的EΘ(Li+/Li)反常地小。
表9-2碱土金属的性质s区元素的一个重要特点是各族元素通常只有一种稳定的氧化态。
碱金属的第一电离能较小,很容易失去一个电子,故氧化数为+1。
碱土金属的第一、第二电离能较小,容易失去2个电子,因此氧化数为+2。
在物理性质方面,s区元素单质的主要特点是:轻、软、低熔点。
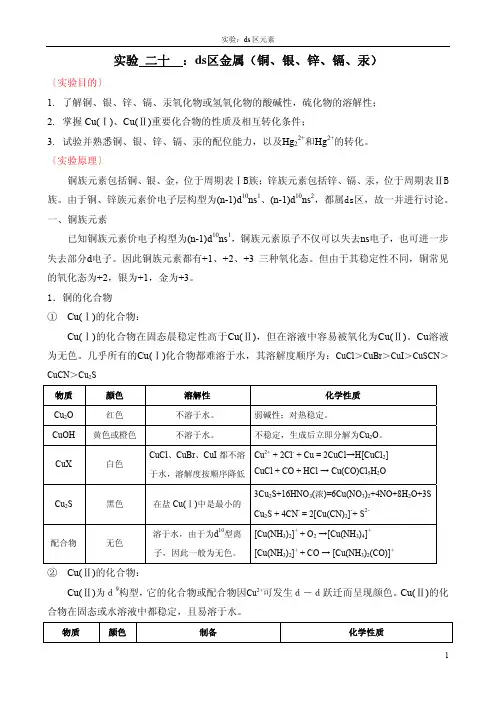
实验二十:ds区金属(铜、银、锌、镉、汞)〔实验目的〕1.了解铜、银、锌、镉、汞氧化物或氢氧化物的酸碱性,硫化物的溶解性;2.掌握Cu(Ⅰ)、Cu(Ⅱ)重要化合物的性质及相互转化条件;3.试验并熟悉铜、银、锌、镉、汞的配位能力,以及Hg22+和Hg2+的转化。
〔实验原理〕铜族元素包括铜、银、金,位于周期表ⅠB族;锌族元素包括锌、镉、汞,位于周期表ⅡB 族。
由于铜、锌族元素价电子层构型为(n-1)d10ns1、(n-1)d10ns2,都属ds区,故一并进行讨论。
一、铜族元素已知铜族元素价电子构型为(n-1)d10ns1,铜族元素原子不仅可以失去ns电子,也可进一步失去部分d电子。
因此铜族元素都有+1、+2、+3三种氧化态。
但由于其稳定性不同,铜常见的氧化态为+2,银为+1,金为+3。
1.铜的化合物①Cu(Ⅰ)的化合物:Cu(Ⅰ)的化合物在固态晨稳定性高于Cu(Ⅱ),但在溶液中容易被氧化为Cu(Ⅱ)。
Cu溶液为无色。
几乎所有的Cu(Ⅰ)化合物都难溶于水,其溶解度顺序为:CuCl>CuBr>CuI>CuSCN>CuCN>Cu2S物质颜色溶解性化学性质Cu2O 红色不溶于水。
弱碱性;对热稳定。
CuOH 黄色或橙色不溶于水。
不稳定,生成后立即分解为Cu2O。
CuX 白色CuCl、CuBr、CuI都不溶于水,溶解度按顺序降低Cu2+ + 2Cl- + Cu = 2CuCl→H[CuCl2] CuCl + CO + HCl → Cu(CO)Cl5H2OCu2S 黑色在盐Cu(Ⅰ)中是最小的3Cu2S+16HNO3(浓)=6Cu(NO3)2+4NO+8H2O+3SCu2S + 4CN- = 2[Cu(CN)2]-+ S2-配合物无色溶于水,由于为d10型离子,因此一般为无色。
[Cu(NH3)2]+ + O2→[Cu(NH3)4]+ [Cu(NH3)2]+ + CO → [Cu(NH3)2(CO)]+②Cu(Ⅱ)的化合物:Cu(Ⅱ)为d9构型,它的化合物或配合物因Cu2+可发生d-d跃迁而呈现颜色。


ds区元素(铜、银、锌、镉、汞)的性质【摘要】ds区元素是指元素周期表中的ⅠB、ⅡB两族元素,包括铜、银、金、锌、镉、汞6种自然形成的金属元素和Rg、Uub2种人工合成元素。
ds区的名称是因为它们的电子构型都是d10s1(ⅠB)或d10s2(ⅡB)。
ds区是d区元素的一部分,ds区元素都是过度金属。
但由于它们的d层是满的,所以体现的性质与其他过渡金属有所不同(比如说最高的氧化态只能达到+3)。
【关键字】元素过渡酸碱性;一、实验目的1、掌握铜、锌氢氧化物的酸碱性;2、掌握铜、银、锌、汞的配合物的生成和性质;6、掌握铜、银、锌、汞离子的分离与鉴定方法。
二、实验原理IB IIBCu Zn Cu(+2,+1)Zn(+2)Ag Cd Ag(+1)Cd(+2)Au Hg Au(+1,+3)Hg(+2,+1)蓝色的Cu(OH)2呈现两性,在加热时易脱水而分解为黑色的CuO。
AgOH在常温下极易脱水而转化为棕色的Ag2O。
Zn(OH)2呈两性,Cd(OH)2显碱性,Hg(I, II)的氢氧化物极易脱水而转变为黄色的HgO(II)和黑色的Hg 2O(I)。
易形成配合物是这两副族的特性,Cu 2+、Ag +、Zn 2+、Cd 2+与过量的氨水反应时分别生成[Cu(NH 3)4]2+、[Ag(NH 3)2]+、[Zn(NH 3)4]2+、[Cd(NH 3)4]2+。
但是Hg 2+和Hg 22+与过量氨水反应时,如果没有大量的NH 4+存在,并不生成氨配离子。
如:HgCl 2 + 2NH 3 = Hg(NH 2)Cl↓白+ 2 NH 4Cl Hg 2Cl 2 + 2NH 3 = Hg(NH 2)Cl↓白+ Hg↓黑+NH 4Cl(观察为灰色)Cu 2+具有氧化性,与I -反应,产物不是CuI 2,而是白色的CuI :Cu2++ I -= 2CuI↓白 + I 2将CuCl 2溶液与铜屑混合,加入浓盐酸,加热可得黄褐色[CuCl 2]-的溶液。