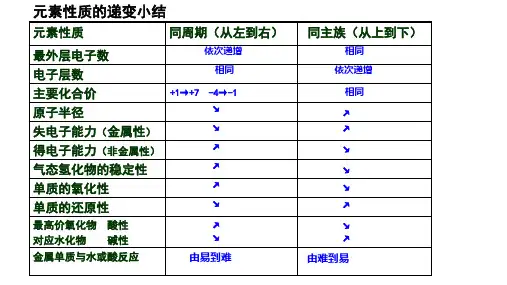
若同主族元素A、B、C在同一主族中从上往下排列,则可推知 A、B、C的单质的氧化性依次减弱顺序为? A、B、C
小试牛刀
3、运用元素周期律分析,下列推断中错误的是 D
A. 已知Ra是第七周期第IIA族元素,故Ra(OH)2的碱性比Mg(OH)2的碱 性强
B. 已知As是第四周期第VA族元素,故AsH3的稳定性比NH3的稳定性弱 C. 已知Cs是第六周期第IA族元素,原子半径比Na的原子半径大,故Cs
2.判断正误(正确的打“√”,错误的打“×”)。
如何变化?
(1)同周期元素从左到右,原子半径逐渐减小,离子半径也逐渐减小( × )
(2)第二周期元素从左到右,最高正价从+1递增到+7( ×) (3)元素的原子得电子越多,非金属性越强;失电子越多,金属性越强( ×) (4)Al(OH)3为两性氢氧化物,与氨水、盐酸均可反应( × ) (5)AlCl3溶液中加足量氨水可生成Al(OH)3沉淀( √ ) (6)元素的氧化物的水化物酸性越强,非金属性越强;碱性越强,金属性越强
1、X、Y、Z均是短周期元素,X、Y位于同一周期,X、Z的
最低价离子分别为X2-和Z-,且Y+和Z-离子具有相同的电子层结
构.下列说法正确的是(D )
X、Y、Z的位置是?
A. 原子最外层电子数:X>Y>Z 正确顺序?
B. 对应气态氢化物的稳定性:X>Z 如何比较?
C. 离子半径:X2->Y+>Z- 正确顺序?
同周期:递变性
一、元素“位置—结构—性质”之间的关系
1.结构与位置的互推 工具:(1)电子层数=周期数。
(2)质子数=原子序数。 (3)主族元素原子最外层电子数=主族序数。 (4)主族元素的最高正价=族序数(氧、氟除外),最低负价=主族序数-8。