§1.1从古典原子论到原子结构的行星模型
- 格式:ppt
- 大小:703.00 KB
- 文档页数:24


1.1从葡萄干面包原子模型到原子结构的行星模型(第二课时)1.1从葡萄干面包原子模型到原子结构的行星模型(第二课时)课前自主预习【基础梳理】1.将科学家与其对应的贡献连线汤姆孙德谟克利特卢瑟福伦琴道尔顿贝克勒尔X射线元素的放射性行星模型葡萄干面包模型近代原子论古典原子论【自我测评】α射线是指_________________,β射线是指___________,γ射线是指_______________。
课堂互动探究【核心突破】1.α粒子散射实验探究(1)介绍:α粒子散射实验装置和原理图1.4(2)请同学们根据汤姆孙原子模型对实验结果进行预测。
①α粒子通过时遇到电子后会发生怎样变化?(已知:α粒子的质量约是电子的7000倍)α粒子通过时原子正电部分对它产生的库仑斥力的影响是怎样的?②请同学们在图1.5汤姆孙原子模型中画出α粒子可能的运动轨迹。
(据推算:根据汤姆孙原子模型α粒子穿过金箔时产生大角度散射的几率是10-3500,最大散射角不超过10°)图1.5(3)根据α粒子散射实际实验结果推测:绝大多数α粒子能直线穿过金箔说明:__________________;极少数的α粒子能被金箔偏转,有的还被直接弹回说明:__________________;(4)描述:卢瑟福的行星模型2.思考:回顾当初人类对原子的认识过程,科学家们曾使用了不少科学研究方法,请至少说出两种。
课后巩固归纳【自主练习】基础题一. 选择题(每小题只有一个选项符合题意)1.中国古代哲学家提出:物质的分割是有条件的,如果物质不存在分割的条件,物质就不能被分割。
这种不能再分割的部分,称之为“端”。
这位哲学家是( )A.惠施B.孔子C.墨子D.老子2.卢瑟福提出原子的行星模型的实验依据是( )A.α粒子散射实验B.铀盐晶体实验C.X射线管实验D.14C放射性实验3.下列关于放射性元素的说法正确的是( )①所有元素都具有放射性;②只有铀元素具有放射性;③元素具有放射性是由原子内部结构变化引起的;④放射性元素的放射现象是在一定条件下发生的。

第一章 打开原子世界的大门§1-1从葡萄干面包模型到原子结构的行星模型一、从古典原子论到葡萄干面包原子模型1、古典原子论2、道尔顿的原子学说3、葡萄干面包原子模型二、从X 射线的发现到元素放射性的发现1、X 射线的发现2、元素放射性的发现3、α、β和γ射线的发现⑴一部分辐射偏向连接电源负极的极板~带正电荷的微粒~α辐射~α粒子是He 2+ ⑵另一部分辐射偏向连接电源正极的极板~带负电荷的微粒~β辐射~β射线是电子流 ⑶第3种辐射~不带电荷~γ射线~波长很短的电磁波结论:原子是可分的,并且具有复杂的结构。
三、原子结构的行星模型α粒子轰击金箔即α粒子的散射实验现象1:绝大部分α粒子都穿过了金箔 说明:原子是中空的现象2:极少数α粒子穿过金箔时发生了偏转,个别α粒子偏转了180°,弹了回来。
说明:原子中存在一个体积很小,正电荷集中,质量很大的核。
§1-2考古断代 同位素和相对原子量一、原子核构成原子的微粒及其性质:课本P11/表格关系式:(1)电性守恒:核电荷数=核内质子数=核外电子数=原子序数(2)质量数=质子数+中子数 (A=Z+N )元素符号角标意义:例题:35 17Cl 16 O 24 12Mg 2+ 32 16S 2- 3717Cl 2二、同位素 ±a A Z X c b ±1、 定义:具有相同质子数而不同中子数的原子互称为同位素。
2、 性质:(1)同位素的化学性质基本相同(2)对存在等同位素的元素,不论这种元素是处于化合态还是游离态,各种同位素原子所占的百分比是不变的。
三、碳-14测定考古年代1、 半衰期2、 原理3、年代的计算方法:C K =C 0(1/2)xC K —文物中C-14的浓度 C 0—大气中C-14的浓度 x —半衰期个数四、相对原子质量的求算1、同位素的相对原子质量2、元素的(精确)平均相对原子质量(即元素的相对原子质量)——该元素所含各同位素的相对原子质量按丰度(原子百分比)计算的平均值例题2:根据下列实测数据计算氧的平均相对原子质量同位素 丰度(%) 相对原子质量16 O 99.759 15.99517 O 0.037 16.99118 O 0.204 17.9913、元素的近似相对原子质量例题3:氯元素在自然界有两种同位素35 17Cl 与37 17Cl ,它们的相对原子质量分别为34.969和36.966,氯元素的相对原子质量为35.453,求35 17Cl 与37 17Cl 的丰度。

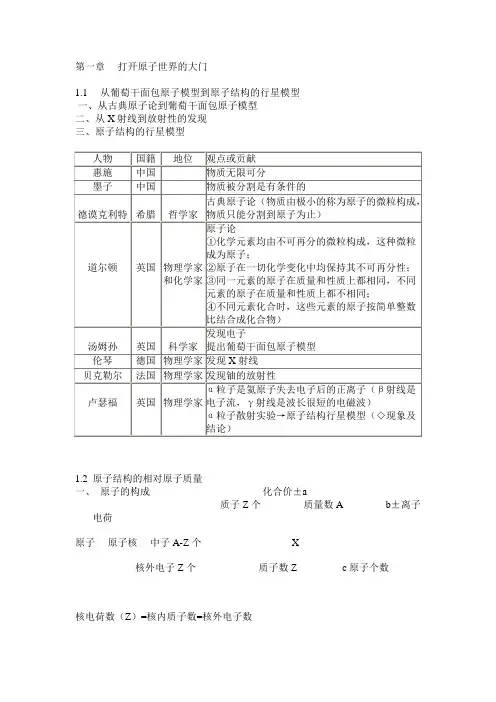
第一章打开原子世界的大门1.1 从葡萄干面包原子模型到原子结构的行星模型一、从古典原子论到葡萄干面包原子模型二、从X射线到放射性的发现三、原子结构的行星模型1.2 原子结构的相对原子质量一、原子的构成化合价±a质子Z个质量数A b±离子电荷原子原子核中子A-Z个X核外电子Z个质子数Z c原子个数核电荷数(Z)=核内质子数=核外电子数质量数(A)=质子数(Z)+中子数(N)二、同位素元素:具有相同核电荷数(质子数)的同一类原子叫做元素同位素:具有相同质子数和不同中子数的同一种元素的原子互称为同位素(同位素原子核内的质子数、化学性质相同;中子数、原子的质量数不同)例:氢原子的同位素(1个质子):氕(H)无中子;氘(D、重氢)1个中子;氚(T、超重氢)2个中子大多数天然元素都有同位素,各种同位素所占的原子百分率一般是不变的。
放射性同位素的应用:探测金属器件缺陷、研究化学反应机理、育种、保存食物、治疗肿瘤三、相对原子质量相对原子质量:以一个碳—12原子质量的1/12作为标准,任何一个原子的真是质量跟一个碳—12原子质量的1/12的比值,成为该原子的相对原子质量。
元素的相对原子质量:它的各种同位素的相对原子质量,根据其所占的原子百分率(丰度)计算而得的平均值(A=A1*a1%+A2*a2%+…+An*an%)近似平均相对原子质量:用各种原子的质量数替换各种同位素的相对原子质量◇十字交叉法1.3 揭开原子核外电子运动的面纱一、原子结构示意图与电子式核外电子按能量高低由内层至外层分层排布(近核低、远核高),这种分层排布情况可用原子结构示意图来表示。
(◇熟记1到20号元素)第一电子层称为K层,依次为、L、M、N、O、P、Q。
元素的化学性质主要由原子的最外层电子数决定,常用小黑点或叉来表示元素原子的最外层上的电子,这种图式被称为电子式。
二、初步认识核外电子排布的规律1、各电子层最多可容纳的电子书为2n^2个(n表示电子层序数)。


第一章打开原子世界大门§1.1 从葡萄干面包模型到原子结构的行星模型一、从古典原子论到葡萄干面包原子模型:1、古代对物质的认识:惠施:物质是无限可分的。
墨子:物质分割是有条件的,当物质不能被分割时,这种不能分割的部分称为“端”。
古希腊德谟克利特:物质只能分割到原子,提出原子是构成物质的最小微粒。
2、近代对原子的认识:(1)19世纪初,英国物理化学家道尔顿提出原子论:①化学元素由不可再分的微粒构成,这种微粒称为原子。
(不正确)②原子在一切化学变化中均保持其不可再分性。
(不正确)③同种元素的原子质量和性质相同,不同种元素的原子质量和性质不同。
(不正确)④构成化合物的原子按简单整数比结合。
(正确)注:③中,“同种元素的原子化学性质是相同的”这一句正确。
④中,“原子与原子之间结合时,都是以简单的整数比化合的”。
(2)20世纪初,汤姆孙发现电子,指出:原子中正电荷(当时没有质子概念)所带的电量与电子所带的负电荷电量相等。
提出葡萄干面包原子模型,认为原子中的正电荷均匀地分布在整个原子的球形体内,电子则均匀地分布在这些正电荷之间。
二、从X射线到元素放射性发现:1、德国物理学家伦琴发现X射线:X射线穿透力强。
2、法国物理学家贝克勒尔发现放射性:说明原子有一定结构。
3、英国物理学家卢瑟福发现两种辐射:α辐射和β辐射。
①α辐射是粒子流,是氦正离子(He2+)。
穿透力弱。
②β射射是电子流。
穿透力弱,穿透力较强。
③γ射线是电磁波。
穿透力强,穿透力很强。
三、原子结构的行星模型:单位换算:1纳米(nm)=10-9m英国物理学家卢瑟福提出原子结构行星模型:①实验现象和结果:绝大部分粒子能直线穿过金箔,说明原子一定是中空的,极少数的粒子能被金箔偏转,有的还被直接弹回来,说明在原子中存在着很小的带正电荷的核。
②行星模型:原子是由带正电荷的质量很集中的很小的原子核和在它周围运动着的带负电荷的电子组成。
§1.2 原子结构和相对原子质量一、原子的构成:1、原子的构成:原子(原子核+核外电子);原子核(质子+中子)a)氢原子(氕、 1 1H)核内无中子,它的其它同位素都有中子( 2 1H有1个中子, 3 1H有2个中子)。

×loading...
退出客服电话:4008980910[全国]首页优课展示排行榜我晒的课我的已晒20077421课
本年度3102074课我要晒课高中化学>沪科课标版>高一上册>1
打开原子世界的大门
>
1.1从葡萄干面包原子模型到原子结构的行星模型
...从古典原子论到葡…高中化学沪科课标版2019年度王晓燕指导教师:无地区:甘肃省
-
白银市
-
平川区学校:白银市平川中学发布时间:2019-06-29
16:36
(0次点评)教学设计教学资源我要点评第一学时共1学时top1
/
1bottomzoom
inzoom
out点评全部(0)
教师(0)
教研员(0)
其他人员(0)我要点评暂无评论教学设计【设计】古典原子教学资源【资源】第一学时主办单位:中华人民共和国教育部
运行维护:中央电化教育馆国家教育资源公共服务平台
版权所有京ICP备09059518号-3。
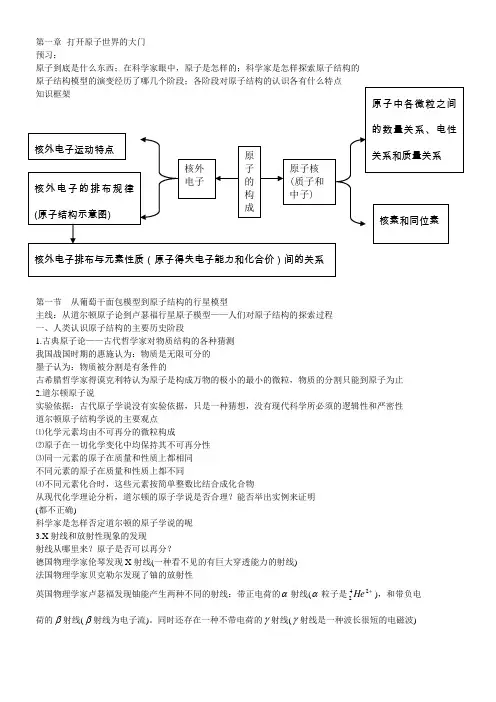
第一章 打开原子世界的大门预习:原子到底是什么东西;在科学家眼中,原子是怎样的;科学家是怎样探索原子结构的原子结构模型的演变经历了哪几个阶段;各阶段对原子结构的认识各有什么特点第一节 从葡萄干面包模型到原子结构的行星模型主线:从道尔顿原子论到卢瑟福行星原子模型——人们对原子结构的探索过程一、人类认识原子结构的主要历史阶段1.古典原子论——古代哲学家对物质结构的各种猜测我国战国时期的惠施认为:物质是无限可分的墨子认为:物质被分割是有条件的古希腊哲学家得谟克利特认为原子是构成万物的极小的最小的微粒,物质的分割只能到原子为止2.道尔顿原子说实验依据:古代原子学说没有实验依据,只是一种猜想,没有现代科学所必须的逻辑性和严密性 道尔顿原子结构学说的主要观点⑴化学元素均由不可再分的微粒构成⑵原子在一切化学变化中均保持其不可再分性⑶同一元素的原子在质量和性质上都相同不同元素的原子在质量和性质上都不同⑷不同元素化合时,这些元素按简单整数比结合成化合物从现代化学理论分析,道尔顿的原子学说是否合理?能否举出实例来证明(都不正确)科学家是怎样否定道尔顿的原子学说的呢3.X 射线和放射性现象的发现射线从哪里来?原子是否可以再分?德国物理学家伦琴发现X 射线(一种看不见的有巨大穿透能力的射线)法国物理学家贝克勒尔发现了铀的放射性英国物理学家卢瑟福发现铀能产生两种不同的射线:带正电荷的α射线(α粒子是+242He ),和带负电荷的β射线(β射线为电子流)。
同时还存在一种不带电荷的γ射线(γ射线是一种波长很短的电磁波)汤姆孙发现了电子电子带负电,单原子是电中性的,表明原子中存在带正电荷的微粒汤姆孙提出葡萄干面包模型原子中的正电荷均匀地分布在整个原子的球形体内,电子均匀地分布在这些正电荷之间,就像葡萄干面包一样合理之处:原子不是坚硬、实心的球体,是可以分割的不合理之处:原子的质量分布是均匀的,原子中的电荷分布也是均匀的4.用α粒子轰开原子世界的大门卢瑟福用α粒子轰击金箔——α粒子散射实验⑴α粒子散射实验的装置介绍放射源——放射性元素放出α粒子,α粒子是氦的核,带2e正电荷,质量是氢原子的4倍,具有较大的动能。