氨基酸的常见化学反应
- 格式:doc
- 大小:26.00 KB
- 文档页数:3

有机化学基础知识氨基酸的合成和反应有机化学基础知识——氨基酸的合成和反应氨基酸是构成蛋白质的基本单元,对于理解生命活动的基础过程和分子结构具有重要意义。
本文将介绍氨基酸的合成和反应,帮助读者进一步了解有机化学中的氨基酸相关知识。
一、氨基酸的合成氨基酸可以通过多种途径合成,其中最主要的方法有以下几种:1. 斯特莱克合成法斯特莱克合成法是合成α-氨基酸的一种常用方法。
这种方法以碳酸和胺为原料,在存在催化剂的条件下,发生酰胺的羰基活化,得到氨基酸。
2. 格布斯合成法格布斯合成法是一种通过氨基酸的脱水缩合反应合成新的氨基酸的方法。
该方法通过两个不同的氨基酸分子间的羧基和氨基的反应,生成新的氨基酸,反应需要在酸性条件下进行。
3. 氨基化合物的合成此外,还可以通过合成氨基化合物,再将其转化为氨基酸。
例如,通过胺与酸酐反应生成酰化胺,再通过水解反应将酰化胺转化为相应的氨基酸。
二、氨基酸的反应氨基酸在有机化学中具有丰富的反应性,主要表现在以下几个方面:1. 缩合反应氨基酸的缩合反应是指多个氨基酸在酸性或碱性条件下,通过酯键或酰胺键的形成缩合为多肽。
这种反应在生物体内形成蛋白质的过程中尤为重要。
2. 氨化反应氨基酸可以与氨基化合物反应,发生氨化反应生成新的氨基酸衍生物。
这种反应可通过调整反应条件和反应物的选择,实现氨基酸结构的改变和扩展。
3. 酸碱性反应氨基酸中的氨基和羧基具有酸碱特性,可发生与酸或碱的反应,形成相应的盐类。
当氨基酸在碱性溶液中时,氨基接受H+生成氨离子,氨离子极易溶解于水中。
4. 氧化还原反应氨基酸中的羧基和氨基都可以参与氧化还原反应。
例如,氨基酸的羧基可以被氧化生成相应的羧酸,而氨基则可以被还原生成相应的胺。
三、氨基酸的应用氨基酸作为生物体内重要的生物分子,在医药、食品、化妆品等领域具有广泛的应用价值。
1. 医药领域氨基酸作为药物的原料,可以合成多种药物,如抗生素、抗肿瘤药物等。
此外,氨基酸还可以作为体外代谢工程和靶向药物传递的载体。


1.氨基的反应(1)酰化氨基可与酰化试剂,如酰氯或酸酐在碱性溶液中反应,生成酰胺。
该反应在多肽合成中可用于保护氨基。
(2)与亚硝酸作用氨基酸在室温下与亚硝酸反应,脱氨,生成羟基羧酸和氮气。
因为伯胺都有这个反应,所以赖氨酸的侧链氨基也能反应,但速度较慢。
常用于蛋白质的化学修饰、水解程度测定及氨基酸的定量。
(3)与醛反应氨基酸的α-氨基能与醛类物质反应,生成西佛碱-C=N-。
西佛碱是氨基酸作为底物的某些酶促反应的中间物。
赖氨酸的侧链氨基也能反应。
氨基还可以与甲醛反应,生成羟甲基化合物。
由于氨基酸在溶液中以偶极离子形式存在,所以不能用酸碱滴定测定含量。
与甲醛反应后,氨基酸不再是偶极离子,其滴定终点可用一般的酸碱指示剂指示,因而可以滴定,这叫甲醛滴定法,可用于测定氨基酸。
(4)与异硫氰酸苯酯(PITC)反应α-氨基与PITC在弱碱性条件下形成相应的苯氨基硫甲酰衍生物(PTC-AA),后者在硝基甲烷中与酸作用发生环化,生成相应的苯乙内酰硫脲衍生物(PTH-AA)。
这些衍生物是无色的,可用层析法加以分离鉴定。
这个反应首先为Edman用来鉴定蛋白质的N-末端氨基酸,在蛋白质的氨基酸顺序分析方面占有重要地位。
(5)磺酰化氨基酸与5-(二甲胺基)萘-1-磺酰氯(DNS-Cl)反应,生成DNS-氨基酸。
产物在酸性条件下(6NHCl)100℃也不破坏,因此可用于氨基酸末端分析。
DNS-氨基酸有强荧光,激发波长在360nm左右,比较灵敏,可用于微量分析。
(6)与DNFB反应氨基酸与2,4-二硝基氟苯(DNFB)在弱碱性溶液中作用生成二硝基苯基氨基酸(DNP氨基酸)。
这一反应是定量转变的,产物黄色,可经受酸性100℃高温。
该反应曾被英国的Sanger用来测定胰岛素的氨基酸顺序,也叫桑格尔试剂,现在应用于蛋白质N-末端测定。
(7)转氨反应在转氨酶的催化下,氨基酸可脱去氨基,变成相应的酮酸。
2.羧基的反应羧基可与碱作用生成盐,其中重金属盐不溶于水。
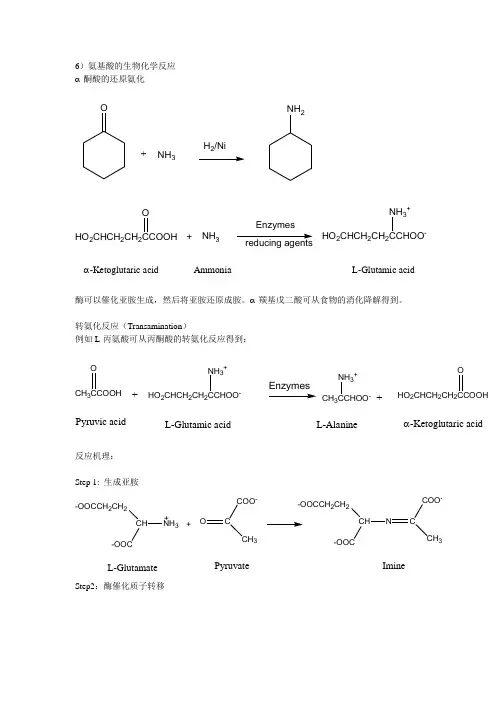
6)氨基酸的生物化学反应 α-酮酸的还原氨化ONH 2H 2/NiNH 3HO 2CHCH 2CH 2CCOOH O+NH 3+HO 2CHCH 2CH 2-NH 3+Enzymesα-Ketoglutaric acidAmmoniaL-Glutamic acid酶可以催化亚胺生成,然后将亚胺还原成胺。
α-羰基戊二酸可从食物的消化降解得到。
转氨化反应(Transamination )例如L-丙氨酸可从丙酮酸的转氨化反应得到:CH 3CCOOHHO 2CHCH 2CH 2-NH 3+Pyruvic acidL-Glutamic acid O +EnzymesHO 2CHCH 2CH 2CCOOHOCH 3CCHOO -NH 3+α-Ketoglutaric acidL-Alanine+反应机理:Step 1: 生成亚胺-OOCCH 2CH 2NH 3++COCOO -CH 3CH-OOCCH 2CH 2CCOO -CH 3NL-GlutamatePyruvate ImineStep2:酶催化质子转移C-OOCCH 2CH 2-OOCC-CH 3Imine from step 1H C-OOCCH 2CH 2-OOCCCOO -CH 3NRearranged imineHStep 3:重排的亚胺的水解C-OOCCH 2CH 2CCOO -3NRearranged imineH H 2OC-OOCCH 2CH 2O+H 2NCOO -CH 3-Ketoglutarate L-Alanine苯丙氨酸转化CH 2CHCOO -NH 3+CH 2-NH 3+CH 2-NH 3+OO EnzymeEnzymeHOL-PhenylalanineArene oxide intermediateL-TyrosineCH 2CHCOO -NH 3+CH 2CCOOHOEnzymeL-PhenylalaninePhenylpyruvic acid苯丙氨酸可以按照不同的消化途径转化。

氨基酸与甲酸反应-概述说明以及解释1.引言1.1 概述概述:氨基酸与甲酸反应是一种重要的有机化学反应,在生物化学和工业化学领域具有广泛的应用。
氨基酸是构成蛋白质的基本单元,是生命体内重要的有机分子之一。
而甲酸是一种简单的有机酸,常用于防腐剂、药物和化学合成中。
在本文中,将深入探讨氨基酸与甲酸之间的反应机理及其产物,分析反应的结果和可能的应用前景。
通过对这一反应的研究,可以更好地理解有机化学反应的原理和应用,为相关领域的研究和生产提供理论支持和实践指导。
1.2 文章结构文章结构:本文主要分为引言、正文和结论三个部分。
在引言部分,将介绍氨基酸与甲酸反应这一主题的概要和背景,说明文章的目的和意义。
在正文部分,将分别介绍氨基酸和甲酸的基本概念、性质和用途,以及详细探讨氨基酸与甲酸反应的机理和过程。
在结论部分,将分析反应结果,展望氨基酸与甲酸反应的应用前景,并对整篇文章进行总结。
通过这样的结构安排,读者可以清晰地了解氨基酸与甲酸反应的相关知识,并对其应用和发展方向有所了解。
1.3 目的本文的目的在于探讨氨基酸与甲酸反应的机理以及可能产生的产物,以帮助读者深入了解这一化学反应过程。
通过对氨基酸和甲酸反应的研究,不仅可以拓展对氨基酸和甲酸的理解,还有助于发现新的应用领域和生产方法。
同时,通过对反应过程的分析,可以为相关领域的科研和工业生产提供一定的参考和指导。
希望本文能够为读者提供有益的知识和启发,促进对氨基酸与甲酸反应的深入研究与应用。
2.正文2.1 氨基酸的基本概念氨基酸是构成蛋白质的基本单位,是生命体内最基本的有机分子之一。
每个氨基酸分子都包含一个氨基(NH2)和一个羧基(COOH),以及一个特定的侧链。
目前已知的氨基酸共有20种,它们在生物体内起着重要的功能和作用。
氨基酸不仅是蛋白质的构成单位,还参与许多重要的生物化学反应。
在细胞内,氨基酸可作为合成酶和激素的前体,参与代谢过程和物质传递,是维持生命活动所必需的重要物质之一。


氨基酸的四个重要化学反应原理及应用氨基酸是构成蛋白质的基本组成单元,对于生物体的生长和代谢至关重要。
在生物体内,氨基酸参与了许多重要的化学反应,这些反应不仅在生物体内起着关键作用,也在医学和生物化学领域有着广泛的应用。
本文将介绍氨基酸的四个重要化学反应原理及其在生物体内和医学领域中的应用。
一、酸碱中和反应酸碱中和反应是氨基酸在生物体内起着关键作用的一种重要化学反应。
氨基酸分子中的氨基和羧基均可与其他分子中的酸性或碱性基团进行中和反应,形成盐和水。
这种反应对于维持生物体内部的酸碱平衡至关重要。
当氨基酸在胃部被蛋白酶分解而产生的羧基和氨基离子进入肠道时,它们会与肠道中的盐酸进行中和反应,使酸碱平衡得以维持。
酸碱中和反应也在体外试管实验中被广泛应用,例如在酶反应体系中调节pH值,以促进酶的活性。
二、氨基酸脱羧反应氨基酸脱羧反应指的是氨基酸分子中的羧基被氨基所脱去的过程。
这种反应在生物体内参与了许多重要的代谢途径,例如氨基酸的降解和合成。
在氨基酸的降解过程中,氨基酸通过脱羧反应生成相应的醛、酮或其他代谢产物,参与能量产生或其他生物化学途径。
在生物体内的代谢途径研究中,氨基酸脱羧反应也被广泛地应用。
在肝脏中,氨基酸脱羧反应参与了尿素循环的代谢途径,调节体内氮代谢平衡。
三、氧化还原反应氨基酸分子中的氨基和羧基均可参与氧化还原反应,这些反应对于氨基酸的功能和代谢至关重要。
在肝脏中,氨基酸的氨基可被氧化为酮酸,而氨基酸的羧基可被还原为醇,这些反应参与了氨基酸的代谢途径。
氨基酸分子中的硫氢基还可参与氧化还原反应,形成二硫键或参与其他重要的生物化学反应。
在医学领域,氨基酸的氧化还原反应被广泛地应用于氨基酸代谢异常的诊断和治疗。
四、氨基酸的缩合反应氨基酸的缩合反应是指两个或多个氨基酸分子通过缩合作用形成肽键的过程。
这种反应在蛋白质的合成过程中起着关键作用,通过氨基酸的缩合反应,氨基酸分子可以串联成长链状的多肽或蛋白质分子。

氨基酸的茚三酮反应名词解释
茚三酮反应:
1. 概念:
茚三酮反应是一种有机化学反应,是将含氨基酸官能团的酸性脱氢物
与含有亚磷酰腙的有机物通过催化剂的作用,在低温下进行的反应。
这种反应可反映出氨基酸的酸性,可测定氨基酸的含量,也可以用来
鉴定氨基酸、比较氨基酸种类和含量。
2. 条件:
茚三酮反应一般要求反应温度低于80℃,最常用的温度一般很低,在25℃-60℃之间。
反应中所用催化剂一般都是硫酸钴和硫酸铝等酸性催
化剂,其中以硫酸钴为主。
3. 原理:
茚三酮反应的原理是氨基酸与含亚磷酰腙基团的有机反应制备茚三酮
类衍生物的反应机理。
该反应利用亚磷酰腙基团与氨基酸中苯丙氨酸
基团发生构象,dNAA及其他一般氨基酸发生酰脱氢作用,从而生成
茚三酮类衍生物,并在反应过程中形成一定量的硝酸盐、磷酸二氢钙,从而形成茚三酮衍生物。
4. 特点:
(1)反应过程简单,可以迅速完成。
(2)这种反应具有一定的特异性,只有酸性氨基酸和亚磷酰腙正确结合才能发生反应。
(3)反应过程可以温和控制,反应时间相对比较短,能有效地避免氨基酸的酶分解。
(4)还可以用于鉴定、定量分析复杂的氨基酸和蛋白质。
(5)反应产物可以通过波长廓线谱识别和酸度测定,可快速准确地测定含氨基酸的含量。

氨基酸反应
氨基酸是一类含有氨基和羧基的有机化合物,它们参与了许多生物合成的反应和代谢过程。
以下是一些与氨基酸相关的常见化学反应:
1. 脱氨反应:氨基酸在室温下与亚硝酸反应会发生脱氨,生成羟基羧酸和氮气。
这个反应可以用于氨基酸的化学修饰和氨基酸的定量分析。
2. 酰化反应:氨基酸的氨基可以与酰化试剂如酰氯或酸酐在碱性溶液中反应,生成酰胺。
这个反应在多肽合成中常被用来保护氨基。
3. 磺酰化反应:氨基酸可以与丹磺酰氯(DNS-Cl)发生磺酰化反应,生成DNS-氨基酸。
此外,氨基酸还可以与异硫氰酸苯酯(PITC)反应,生成苯氨基硫甲酰衍生物(PTC-AA),用于蛋白质测序(Edman降解)。
4. 烃基化反应:氨基酸的氨基可以与桑格尔试剂(2,4-二硝基氟苯,DNFB)发生烃基化反应,生成二硝基苯基氨基酸(DNP-氨基酸)。
5. 转氨酶催化反应:氨基酸在转氨酶的催化下可以脱去氨基,生成相应的酮酸。
6. 席夫碱的生成:氨基酸的α-氨基上的氢可以与醛或酮羰基上的氧脱水缩合,生成含碳氮双键(-C=N-)的亚胺,称为席夫碱(Schiff base)。
这些反应显示了氨基酸在生物体内的重要性和多样性,但请注意,这些反应仅作为示例列出,每个反应的具体细节和条件可能会有所不同。
氨基酸的化学方程式氨基酸的化学方程式是指一种由氨基酸小分子分子组成的化学反应,它是大多数有机物质的基本结构。
氨基酸是一类特殊的有机分子,它们之间可以通过化学反应来形成不同的化合物。
由于氨基酸的分子结构特殊,所以在所有的有机物中都有出现,它们既可以直接参与反应,也可以作为催化剂来加速反应过程。
因此,研究氨基酸的化学反应方程式对于了解和设计有机反应有着非常重要的意义。
首先,任何一种氨基酸的化学反应方程式都可以分为两个部分:一部分是氨基酸分子本身,另一部分是其他有机物质(如小分子、大分子小分子、脂肪酸等)的反应性物质。
比如,在一般的氨基酸反应中,常常会有一种氨基酸——谷氨酸,它的一个完整反应方程式可以写作:C2H4O2 + NH4+ → C2H4O2 + NH4OH上面的反应方程式清晰地表明,在氨基酸反应中,氨基酸与其他有机物质之间建立了反应性结合。
其次,氨基酸反应同样根据它们的化学特性来分类,有酯化反应、羧基化反应、硫化反应、硝化反应等。
酯化反应是由氨基酸和碳酸酯组成的有机反应,它们可以形成类似于脂肪酸的物质,比如乙酰化反应:R-NH2 + H-COOR' → RCOOH + R'NH3+羧基化反应是指氨基酸与羧酸反应,它的反应方程式如下:R-NH2 + HOOC-R' → RCOOH + R'NH2在硫化反应中,氨基酸与硫酸盐之间发生反应,生成硫酸酯:R-NH2 + H2SO4 → RCOOH + (NH4)2SO4而硝化反应则是氨基酸与硝酸盐发生结合,生成硝酸酯:R-NH2 + HNO3 → RCOOH + NH4NO3最后,可以指出,不同的氨基酸往往会发生不同的化学反应,而这些反应又有着各自独特的化学方程式。
所以,要想全面和深入地了解氨基酸的化学反应,就需要借助于化学方程式来进行研究。
氨基酸的常见化学反应⏹ -氨基的反应⏹亚硝酸反应⏹范围:可用于Aa定量和蛋白质水解程度的测定(Van slyke法)⏹注意:生成的氮气只有一半来自于Aa,ε氨基酸也可反应,速度较慢.⏹与酰化试剂的反应⏹Aa+酰氯,酸酐-→Aa被酰基化⏹丹磺酰氯用于多肽链末端Aa的标记和微量Aa的定量测量.⏹烃基化反应⏹Aa的氨基的一个氢原子可被羟基(包括环烃及其衍生物)取代.⏹与2,4-二硝基氟苯(DNFB,FDNB)反应⏹最早Sanger用来鉴定多肽或蛋白质的氨基末端的Aa⏹与苯异硫氰酸酯(PITC)的反应⏹Edman用于鉴定多肽或蛋白质的N末端Aa.在多肽和蛋白质的Aa顺序分析方面占有重要地位(Edman降解法)⏹形成西佛碱反应⏹Aa的α-NH2能与醛类化合物反应生成弱碱,即西佛碱(schiff ‘sbase)⏹前述甲醛滴定:甲醛与H2N-CH2-COO-结合,有效地减低了后者的浓度,所以对于加入任何量的碱, [H2N-CH2-COO- ]/[+H3N-CH2-COO- ]的比值总要比不存在甲醛的情况下小得多。
加入甲醛的甘氨酸溶液用标准盐酸滴定时,滴定曲线B并不发生改变。
⏹脱氨基反应⏹Aa在生物体内经Aa氧化酶催化即脱去α-NH2而转变成酮酸⏹α-COOH参加的反应⏹成盐和成酯反应⏹Aa + 碱-→盐⏹Aa + NaOH -→氨基酸钠盐(重金属盐不溶于水)⏹Aa-COOH + 醇-→酯⏹Aa+ EtOH ---→氨基酸乙酯的盐酸盐⏹当Aa的COOH变成甲酯,乙酯或钠盐后,COOH的化学反应性能被掩蔽或者说COOH被保护,NH2的化学性能得到了加强或活化,易与酰基结合。
Aa酯是制备Aa的酰氨or酰肼的中间物⏹⏹成酰氯反应⏹当氨基酸的氨基用适当的保护基保护以后,其羧基可与二氯亚砜作用生成酰氯⏹用于多肽人工合成中的羧基激活⏹叠氮反应⏹氨基酸的氨基通过酰化保护后,羧基经酯化转变为甲酯,然后与肼和亚硝酸变成叠氮化合物⏹用于多肽人工合成中的羧基激活⏹脱羧基反应⏹α-氨基和α-羧基共同参与的反应⏹与茚三酮反应⏹茚三酮在弱酸性溶液中与α-氨基酸共热,引起氨基酸氧化脱氨、脱羧反应,最后茚三酮与反应产物中的氨和还原茚三酮发生作用生成紫色物质⏹Pro与hyPro(羟脯氨酸)不释放氨,而直接生成黄色化合物⏹定性,定量测定各种Aa,蛋白质⏹测定CO2 的量,从而可计算参加反应的Aa的量⏹成肽反应⏹一个Aa的NH2+另一个Aa的COOH可以缩合成肽,形成的键称肽键⏹侧链R基参加的反应⏹R功能基:⏹羟基,酚基,巯基(二硫键),吲哚基,咪唑基,胍基,甲硫基,非α-NH2,非α-COOH⏹酪氨酸的酚基在3和5位上容易发生亲电取代反应⏹二碘酪氨酸或一硝基酪氨酸和二硝基酪氨酸⏹酪氨酸的酚基可以与重氮化合物(对氨基苯磺酸的重氮盐)生成桔黄色的化合物。
氨基酸的化学反应
氨基酸的化学反应是其基团的特征性反应。
重要的有:
1、茚三酮反应。
所有具有自由α-氨基的氨基酸与过量茚三酮共热形成蓝紫色化合物(脯氨酸和羟脯氨酸与茚三酮反应产生黄色物质)医|学教|育网搜集整理。
用分光光度法可定量测定微量的氨基酸。
蓝紫色化合物的最大吸收峰在570nm波长处,黄色在440nm波长下测定。
吸收峰值的大小与氨基酸释放的氨量成正比。
2、与2,4-二硝基氟苯(DNFB)的反应。
在弱碱性溶液中,氨基酸的α-氨基很容易与DNFB作用生成稳定的黄色2,4-二硝基苯氨基酸(DNP-氨基酸),这一反应在蛋白质化学的研究史上起过重要作用,Sanger等人应用它测定胰岛素一级结构。
多肽顺序自动分析仪是根据相类似的原理设计的,即利用多肽链N端氨基酸的α-氨基与异硫氰酸苯酯PITC反应(Edman降解法)。
化学反应中的氨基酸的酸碱中和反应化学反应是化学领域中不可或缺的研究内容,其中氨基酸的酸碱中和反应更是广泛应用于生物化学、医学等领域。
本文将着重介绍氨基酸的酸碱中和反应过程以及其在生物化学中的应用。
一、氨基酸的结构与性质在化学领域中,氨基酸是指含有羧基(COOH)和胺基(NH2)的有机化合物。
根据侧链不同,氨基酸可以分为20种,其中人体中常见的氨基酸有丝氨酸、半胱氨酸、甘氨酸、赖氨酸等。
与一般有机化合物不同,氨基酸具有明显的酸碱性质。
当氨基酸在溶液中时,可根据其的羧基和胺基上的游离质子(即H+)含量分为三类:酸性氨基酸、碱性氨基酸和中性氨基酸。
二、氨基酸的酸碱中和反应过程当氨基酸分子中的游离质子数等于负离子数时,氨基酸表现出中性性质。
例如,丝氨酸(Ser)分子式为HO2CCH(NH2)CH2OH,当其处于中性状态时,其游离质子数等于负离子数,即:HO2CCH(NH2)CH2OH ⇌ H+ + O2CCH(NH2)CH2OH-当氨基酸处于酸性条件下,即游离质子(H+)的浓度高于胺基(NH2)的浓度时,氨基酸表现出酸性性质。
此时,质子(H+)会与胺基(NH2)中的自由电子形成NH3+,羧基(COO-)中的电子会往外挤,形成COOH。
例如,在酸性环境下,丝氨酸会发生如下的反应:HO2CCH(NH2)CH2OH ⇌ H+ + HO2CCH(NH3+)CH2OHHO2CCH(NH3+)CH2OH ⇌ HO2CCH(NH2)CH2OH + H+当氨基酸处于碱性条件下,即游离质子(H+)的浓度小于或等于胺基(NH2)的浓度时,氨基酸表现出碱性性质。
此时,胺基(NH2)会接受水分子中的质子(H+),形成NH3+。
例如,在碱性环境下,丝氨酸会发生如下的反应:HO2CCH(NH2)CH2OH ⇌ HO2CCH(NH)CH2OH- + H+HO2CCH(NH)CH2OH- + H2O ⇌ HO2CCH(NH3+)CH2OH三、氨基酸的酸碱中和反应在生物化学中的应用人体内有许多重要的物质,例如各种酶、激素和细胞膜等都是由氨基酸组成的。
氨基酸与碘的反应摘要:I.引言- 简要介绍氨基酸和碘的反应II.氨基酸与碘的基本性质- 氨基酸的定义和结构- 碘的定义和性质III.氨基酸与碘的反应类型- 亲核取代反应- 亲电加成反应- 消除反应IV.反应机理- 亲核取代反应的机理- 亲电加成反应的机理- 消除反应的机理V.氨基酸与碘反应的应用- 生物体内碘的作用- 氨基酸碘化物的应用VI.结论- 总结氨基酸与碘的反应及其重要性正文:氨基酸与碘的反应在生物化学和有机化学领域具有重要意义。
氨基酸是生命体内构成蛋白质的基本组成单位,而碘是一种卤素元素,具有很高的化学活性。
本文将详细介绍氨基酸与碘的反应类型、反应机理及其在生物化学和有机化学中的应用。
首先,我们简要了解一下氨基酸和碘的基本性质。
氨基酸是一类含有氨基(-NH2)和羧基(-COOH)的有机化合物,它们通过脱水缩合反应形成肽键,进而构成蛋白质。
碘是一种卤素元素,原子序数为53,具有较强的氧化性,在化学反应中易得电子。
氨基酸与碘的反应主要分为三类:亲核取代反应、亲电加成反应和消除反应。
在亲核取代反应中,氨基酸的亲核基团(如氨基、羟基等)取代碘的离去基团,生成新的化合物。
在亲电加成反应中,氨基酸的π电子对与碘的卤素原子形成共价键,生成新的化合物。
在消除反应中,氨基酸与碘发生加成反应后,通过消除一个小分子(如水分子)生成新的化合物。
反应机理方面,以亲核取代反应为例,首先,氨基酸的亲核基团攻击碘的离去基团,形成一个中间体。
接着,离去基团离去,生成新的化合物。
在这个过程中,氨基酸的亲核基团会发生构象变化,从而完成反应。
氨基酸与碘的反应在生物化学和有机化学领域具有广泛的应用。
在生物体内,碘作为甲状腺激素的重要组成部分,对维持生物体正常代谢具有重要作用。
此外,氨基酸碘化物在医药、农业等领域也有广泛应用,如合成抗病毒药物碘苷等。
综上所述,氨基酸与碘的反应在生物化学和有机化学领域具有重要意义。
氨基酸与茚三酮反应原理1.引言引言部分是文章的开篇,用于引出文章的主题并提供背景信息。
在概述部分,我们可以简要介绍氨基酸和茚三酮的相关概念,并为读者概括性地解释它们的特性和重要性。
以下是可能的概述部分内容:引言1.1 概述氨基酸是生物体内构成蛋白质的基本组成单位之一。
它们由氨基基团、羧基和一个侧链组成,而侧链的不同确定了每种氨基酸的特性。
氨基酸不仅参与蛋白质的合成,还在细胞内发挥着其他重要的生理作用。
因此,对于了解氨基酸的性质和其在生物体中的功能至关重要。
茚三酮是一种有机化合物,它具有茚环和酮基的结构特征。
茚三酮是一种重要的芳香化合物,在药物、材料科学等领域具有广泛的应用。
它的结构特性赋予了它良好的稳定性和反应活性。
因此,深入研究茚三酮的反应原理将有助于我们理解其与其他物质的相互作用和应用领域。
本文旨在探讨氨基酸与茚三酮的反应原理。
通过研究氨基酸与茚三酮的反应机制,我们可以更好地理解它们之间的相互作用,并为相关领域的研究提供重要的理论基础。
文章将介绍氨基酸和茚三酮的概念和特性,并深入探讨它们之间的反应原理。
接下来,我们将进行结果的分析,以期为相关领域的进一步研究和应用提供有益的参考。
在本文的正文部分,我们将详细介绍和分析氨基酸的概念和特性,以及茚三酮的概念和特性。
随后,我们将进一步探讨氨基酸与茚三酮的反应原理,并对实验结果进行分析。
通过这一研究,我们希望为进一步的科学研究和相关领域的应用提供有益的信息和指导。
请注意,以上内容仅供参考,具体的概述部分可以根据你自己的写作需求进行调整和修改。
文章结构部分的内容可以包括以下几个方面:1.2 文章结构本文将按照以下结构展开讨论氨基酸与茚三酮的反应原理:第2章:正文2.1 氨基酸的概念和特性介绍氨基酸的定义、组成以及其在生物体中的重要性。
阐述氨基酸的分类、结构特点以及常见的氨基酸的例子。
重点介绍与反应有关的氨基酸的特性。
2.2 茚三酮的概念和特性介绍茚三酮的定义、结构特点以及其在化学领域中的应用。
氨基酸的常见化学反应
⏹ -氨基的反应
⏹亚硝酸反应
⏹范围:可用于Aa定量和蛋白质水解程度的测定(Van slyke法)
⏹注意:生成的氮气只有一半来自于Aa,ε氨基酸也可反应,速度较
慢.
⏹与酰化试剂的反应
⏹Aa+酰氯,酸酐-→Aa被酰基化
⏹丹磺酰氯用于多肽链末端Aa的标记和微量Aa的定量测量.
⏹烃基化反应
⏹Aa的氨基的一个氢原子可被羟基(包括环烃及其衍生物)取代.
⏹与2,4-二硝基氟苯(DNFB,FDNB)反应
⏹最早Sanger用来鉴定多肽或蛋白质的氨基末端的Aa
⏹与苯异硫氰酸酯(PITC)的反应
⏹Edman用于鉴定多肽或蛋白质的N末端Aa.在多肽和蛋白
质的Aa顺序分析方面占有重要地位(Edman降解法)
⏹形成西佛碱反应
⏹Aa的α-NH2能与醛类化合物反应生成弱碱,即西佛碱(schiff ‘s
base)
⏹前述甲醛滴定:甲醛与H2N-CH2-COO-结合,有效地减低了后者的
浓度,所以对于加入任何量的碱, [H2N-CH2-COO- ]/
[+H3N-CH2-COO- ]的比值总要比不存在甲醛的情况下小得多。
加入
甲醛的甘氨酸溶液用标准盐酸滴定时,滴定曲线B并不发生改变。
⏹脱氨基反应
⏹Aa在生物体内经Aa氧化酶催化即脱去α-NH2而转变成酮酸
⏹α-COOH参加的反应
⏹成盐和成酯反应
⏹Aa + 碱-→盐
⏹Aa + NaOH -→氨基酸钠盐(重金属盐不溶于水)
⏹Aa-COOH + 醇-→酯
⏹Aa+ EtOH ---→氨基酸乙酯的盐酸盐
⏹当Aa的COOH变成甲酯,乙酯或钠盐后,COOH的化学反
应性能被掩蔽或者说COOH被保护,NH2的化学性能得到
了加强或活化,易与酰基结合。
Aa酯是制备Aa的酰氨or
酰肼的中间物
⏹成酰氯反应
⏹当氨基酸的氨基用适当的保护基保护以后,其羧基可与二氯亚砜作
用生成酰氯
⏹用于多肽人工合成中的羧基激活
⏹叠氮反应
⏹氨基酸的氨基通过酰化保护后,羧基经酯化转变为甲酯,然后与肼
和亚硝酸变成叠氮化合物
⏹用于多肽人工合成中的羧基激活
⏹脱羧基反应
⏹α-氨基和α-羧基共同参与的反应
⏹与茚三酮反应
⏹茚三酮在弱酸性溶液中与α-氨基酸共热,引起氨基酸氧化脱氨、脱
羧反应,最后茚三酮与反应产物中的氨和还原茚三酮发生作用生成
紫色物质
⏹Pro与hyPro(羟脯氨酸)不释放氨,而直接生成黄色化合物
⏹定性,定量测定各种Aa,蛋白质
⏹测定CO2 的量,从而可计算参加反应的Aa的量
⏹成肽反应
⏹一个Aa的NH2+另一个Aa的COOH可以缩合成肽,形成的键称肽
键
⏹侧链R基参加的反应
⏹R功能基:
⏹羟基,酚基,巯基(二硫键),吲哚基,咪唑基,胍基,甲硫基,非
α-NH2,非α-COOH
⏹酪氨酸的酚基在3和5位上容易发生亲电取代反应
⏹二碘酪氨酸或一硝基酪氨酸和二硝基酪氨酸
⏹酪氨酸的酚基可以与重氮化合物(对氨基苯磺酸的重氮盐)生成桔
黄色的化合物。
——Pauly反应
⏹组氨酸的咪唑基可以发生类似反应但产物颜色为棕红色。
⏹精氨酸的侧链胍基在硼酸钠缓冲液(pH 8-9, 25-35︒C)中,与1.2-环已二酮
反应,生成缩合物。
该缩合物在羟胺缓冲液中,重新生成Arg
⏹色氨酸的侧链吲哚基在温和条件下可被N-溴代琥珀酰亚胺
(N-bromosuccinimide)氧化。
此反应可用于分光光度法测定蛋白质中色氨
酸的含量,并能在色氨酸和酪氨酸残基处选择性化学断裂肽键。
⏹蛋氨酸侧链上的甲硫基是一个很强的亲核基团,与烃化试剂如甲基碘容易形
成锍盐(sulfonium salt)
⏹此反应可被硫基试剂逆转。
在逆转反应中,原有的甲基和新加入的
甲基除去的机会是相等的,因此当用14C标记的甲基碘处理时,获
得的蛋氨酸将有50%是同位素标记的。
⏹半胱氨酸侧链上的巯基(-SH)有很强的反应活性,可参与很多反应
⏹二硫键的形成和打开
⏹2R-SH + 1/2 O2-→R-S-S-R + H2O ;Cu2+,Fe2+ ,
Co2+和Mn2+存在下,巯基的空气氧化将显著提高。
⏹胱氨酸中的二硫键在稳定蛋白质的构象上起很大的作用。
氧
化剂和还原剂都可打开二硫键。
过甲酸可以定量地打开二硫
键,生成磺基丙氨酸(cysteic acid)残基。
还原剂如巯基化
合物(R-SH)也能打开二硫键,生成半胱氨酸残基及相
应的二硫化物
⏹二硫苏糖醇(dithiothreitol,缩写为DTT),与胱氨酸中的二
硫键反应形成一个含分子内二硫键的稳定六元环
⏹巯基能和各种金属离子形成稳定程度不等的络合物e.g. 对氯汞苯甲
酸(p-chloromercuribenzoic acid)
⏹由于许多蛋白质,如SH酶,其活性中心涉及-SH基,当遇
到重金属离子而生成硫醇盐时,将导致酶的失活,因此制备
这类蛋白质时应避免进入重金属离子
⏹半胱氨酸可与二硫硝基苯甲酸(dithionitrobenzoic acid,缩写为
DTNB)或称Ellman氏试剂发生硫醇-二硫化物交换反应
⏹反应中1分子的半胱氨酸引起1分子的硝基苯甲酸的释放。
它在pH8.0时,在412nm波长处有强烈的光吸收,因此可利
用比色法定量测定-SH基。