3387高一化学电解质测试题
- 格式:doc
- 大小:179.50 KB
- 文档页数:5
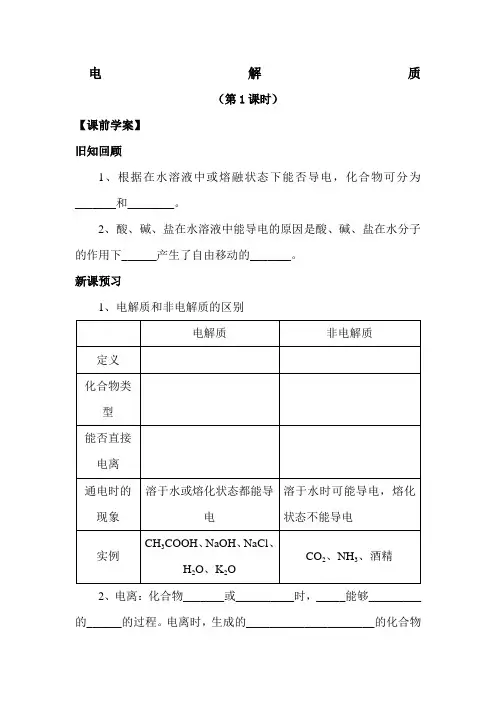
电解质(第1课时)【课前学案】旧知回顾1、根据在水溶液中或熔融状态下能否导电,化合物可分为_______和________。
2、酸、碱、盐在水溶液中能导电的原因是酸、碱、盐在水分子的作用下______产生了自由移动的_______。
新课预习1、电解质和非电解质的区别2、电离:化合物_______或__________时,_____能够_________的______的过程。
电离时,生成的______________________的化合物称为酸;生成的__________________的化合物称为碱;能生成________和_____________的化合物称为盐。
写出下列化合物的电离方程式:H2SO4:KOH:BaCl2:3、电解质按照其在水溶液中能否完全电离分为______________和____________。
强电解质溶液的导电能力_____________弱电解质溶液的导电能力,电解质溶液的导电能力取决于溶液中的自由移动的离子浓度的大小。
溶液中的自由移动的离子浓度越大,其导电性_________;浓度越小,其导电性__________。
如:硝酸是强电解质,但如果浓度很小,溶液中自由移动的离子浓度就很小,其导电性就___________较浓的醋酸溶液。
【课堂学案】重难点突破:一、电解质和非电解质电解质是指在水溶液中或熔化状态下能够导电的化合物。
酸、碱、盐都是电解质。
如NaOH、HCl、NaCl、CaCO3等等。
非电解质是指在水溶液和熔化状态都不导电的化合物。
如CO2、NH3、绝大多数有机物如酒精等。
温馨提示:(1)电解质、非电解质是对化合物的一种分类。
单质既不是电解质,也不是非电解质。
(2)电解质溶液导电必须是化合物本身电离产生的离子导电,否则该化合物属于非电解质。
如CO2、SO2、NH3等是非电解质。
二、强电解质和弱电解质在电解质中,按照它们在水溶液中的电离程度,把它们分为强电解质和弱电解质。

高一化学电解质试题1.下列说法正确的是()A.硫酸钡不溶于水,所以硫酸钡是非电解质B.氨气溶于水可以导电,所以氨气是电解质C.固态磷酸是电解质,所以磷酸在熔化时和溶于水时都能导电D.液态氯化氢不能导电,但氯化氢是电解质【答案】D【解析】硫酸钡虽不溶于水,但它是电解质;氨气溶于水可以导电,但氨气不是电解质;磷酸是电解质,它溶于水时能导电,但熔化时不导电;液态氯化氢不能导电,但在水溶液中能导电,所以氯化氢是电解质。
【考点】非电解质、电解质2.把0.05 mol NaOH固体加入到100 mL下列液体中,溶液的导电能力变化最小的是() A.自来水B.0.5 mol·L-1盐酸C.0.5 mol·L-1NaOH溶液D.0.5 mol·L-1KCl溶液【答案】B【解析】自来水中离子浓度很小,当加入NaOH固体后,溶液中离子的浓度明显增加,溶液导电能力明显增强;含0.1 L×0.5 mol·L-1=0.05 mol HCl的盐酸中,当加入0.05 mol NaOH固体,反应后生成0.05 mol NaCl和H2O,溶液中的离子浓度基本不变;而在NaOH、KCl溶液中加入NaOH固体后,都会使100 mL溶液中离子的物质的量增加,浓度增大,导电性增强。
【考点】电解质3.下表中有关物质的分类正确的是【答案】C【解析】A、二氧化碳不是电解质,错误;B、铜既不是电解质也不是非电解质,错误;C、碳酸钙属于盐类,是电解质,酒精属于非电解质,正确;D、水是电解质,错误,答案选C。
【考点】考查电解质、非电解质的概念4.下列有关叙述正确的是A.溶于水后能电离出H+的化合物都是酸B.BaSO4不溶于水,故BaSO4不是电解质C.CO2溶于水能导电,故CO2是电解质D.尽管NaCl固体不导电,但NaCl是电解质【答案】D【解析】A、水、硫酸氢钠等溶于水后能电离出H+,但它们不是酸,错误;B、硫酸钡等难溶盐是电解质,错误;C、CO2本身不能电离,属于非电解质,错误;D、NaCl溶于水或熔融后能够导电,正确。

高一化学电解质题目
一、电解质是什么?
电解质是指在特定条件下,在溶液中能够进行电解并且分离出正
负离子的化学物质。
电解质可以随着溶解度的不同而溶解于液体或汽体,有时也可以溶解于固体中,因此有液态电解质、气态电解质和固
体电解质之分。
二、高一化学电解质的相关内容
1.电解质的种类
正电解质:钠、钾、铝、碳酸钙等;负电解质:氯化物(氯、氢
氟酸钠、硫酸钠、氯化钡)、硫酸根离子等。
2.电解质的溶解度
电解质的溶解度是指在一定温度下,把一定量电解质溶解在单位
体积的溶液中所需要的电解质质量,也就是说,电解质的溶解度越大,溶液中所含的电解质的量也就越多。
3.电解质的极化
溶液电解质受到极化作用,极化作用引起溶液中的正负电解质的
分布不均,即在极化方向上电解质的浓度比另一方向的浓度高,称为
极化电解质。
4.电解质的电离
当一种电解质在溶液中处于一定的条件时,例如某些电压施加,
它会分解成离子并将其在溶液中分散,这种现象称为电解质的电离,
也即电解质的离子化过程。
5.电解质的电解
电解是一个物理和化学综合的反应,它通过电解将电解质分解成正电解质和负电解质,这两种电解质形成了单离子溶液,因此也称为单离子电解质。

高一化学上学期电解质离子方程式综合练习题(附答案)-CAL-FENGHAI-(2020YEAR-YICAI)_JINGBIAN高一化学上学期电解质离子方程式综合练习题学校:___________注意事项: 2、请将答案正确填写在答题卡上第1卷一、单选题( )A .熔融的NaOHB .铜C .KOH 溶液D .液氨 2.下列说法正确的是( )A. 铜、石墨均导电,所以它们均是电解质B. NH 3、CO 2的水溶液均导电,所以NH 3、CO 2均是电解质C. 液态HCl 、固体NaCl 均不导电,所以HCl 、NaCl 均是非电解质D.蔗糖、酒精在水溶液和熔融状态下均不导电,所以它们均是非电解质 3.下列离子方程式表达不正确的是( )A.向3FeCl 溶液中滴加HI 溶液:223++2I =2Fe Fe =2I -++B.向223Na S O 溶液中滴加盐酸:222+322H ==S O S SO H O -++↓↑+ C.向2NaA1O 溶液中通入过量2CO 制()3A1OH :()-33222A12O==A1OH O O C H H O C -+↓++D.向()442NH A1SO 溶液中滴加少量()2Ba OH 溶液:+2--442+4322NH SO 2OH BaBaS =O H =O 2N H ↓++⋅++ 4.常温下,相同物质的量浓度的下列溶液,导电能力最强的是(?? ) A.盐酸???????B.氨水???????C.醋酸???????D.碳酸钠5.某100mL 溶液中含H 2SO 4 ,加入下列物质,溶液导电性增强的是( ) A . Ba(OH)2B .100mL 水C .酒精D . Na 2SO 4固体6.如图点滴板上四种溶液间的反应对应的离子方程式书写正确的是( )反应:+-2H OH H O +== 反应:22+3+l 2l Fe C Fe C -+==+反应:2+422-+-4SO H O Ba BaSO H O H +=↓+++=反应:()3++3243A13NH H O A1OH 3NH =↓+=+⋅7.下列各项的两组物质在溶液中的反应,可用同一离子方程式表示的是( ) A .氢氧化钠与盐酸;氢氧化钠与碳酸B .BaCl 2溶液与Na 2SO 4溶液;Ba(OH)2溶液与H 2SO 4溶液C .Na 2CO 3溶液与硝酸溶液;CaCO 3溶液与硝酸溶液D .石灰石与硝酸反应;石灰石与盐酸 8.下列解释事实的方程式不正确的是( )A.用食醋清洗水垢:233CO 2CH COOH -+3222CH COO H O CO -++↑消毒液与洁厕灵混用产生有毒气体:ClO Cl 2H --+++ 22Cl H O ↑+C.用氢氧化铝治疗胃酸过多:()3Al OH 3H ++ 32Al 3H O ++ D.用硫化钠除去废水中的汞离子:22Hg +S +-HgS ↓9.能用离子方程式H ++OH -=H 2O 表示的反应是(?? ) A.?稀醋酸和稀氨水反应 B.?稀硫酸和烧碱溶液反应 C.?稀盐酸和氢氧化铜反应 D.?稀硫酸和氢氧化钡溶液反应10.下列离子方程式的书写及评价,均合理的是( )11.能发生离子反应,但是不会产生沉淀的是( )A .澄清石灰水中通入CO 2B .NaHCO 3溶液中滴加NaOH 溶液C .Na 2CO 3溶液中滴加NaOH 溶液D .氯化钠溶液中滴加硝酸银溶液 12.下列化学反应的离子方程式正确的是(?? )A.氯化铝溶液与过量的氨水反应:Al 3++4NH 3·H 2O=-2AlO +4+4NH +2H 2OB.小苏打溶液中加入过量的澄清石灰水:Ca 2++2OH -+2-3HCO =CaCO 3↓+ 2-3CO +H 2O C.纯碱溶液中滴加少量盐酸: 2-3CO +H +=-3HCO D.用FeCl3溶液腐蚀铜电路板:Fe 3++Cu?= Fe 2++ Cu 2+13.下列按电解质、非电解质、酸性氧化物、碱性氧化物的组合,正确的是( ) A.?切开的金属Na 暴露在空气中,光亮表面逐渐变暗:2Na +O 2=Na 2O 2 B.?金属钠比通金属铜活泼,金属钠放入CuSO 4溶液:CuSO 4+2Na=Cu +Na 2SO 4 C.?Na 2O 2在潮湿的空气中放置一段时间,变成白色粘稠物:2Na 2O 2+2CO 2=2Na 2CO 3+O 2 D.?将Na 块放入水中,产生气体:2Na +2H 2O=2NaOH +H 2↑ 15.关于反应过程中的先后顺序,下列评价正确的是( )A .向浓度都为L 的FeCl 3和CuCl 2的混合溶液中加入铁粉,溶质CuCl 2首先与铁粉反应B .向过量的Ba(OH)2溶液中滴加少量的KAl(SO 4)2溶液,开始没有白色沉淀生成C .向浓度都为L 的Na 2CO 3和NaOH 的混合溶液通入CO 2气体,NaOH 首先反应D .向浓度为L 的FeCl 3溶液中,加入质量相同、颗粒大小相同的铁和铜,铜单质首先参加反应 16.下列反应属于离子反应的是( ) A .氢气还原氧化铜生成水和铜B .石灰石高温分解生成氧化钙和二氧化碳C .盐酸滴加到石灰石固体上D .实验室加热高锰酸钾制氧气二、填空题(1)按要求写出方程式:①HNO 3(电离方程式) 。

高一化学 第六单元 电解质单元测试题1.下列关于电解质的说法正确的是 A.液态HCl 不导电,所以HCl 不是电解质B.NH 3溶于水形成的溶液能导电,所以NH 3是电解质C.SO 2溶于水能导电,所以SO 2是电解质D.BaSO 4在水溶液中难导电,但熔融下能导电所以.BaSO 4是电解质 2.下列物质属于强电解质的是A.H 2CO 2B.Cl 2C.CaCO 3D.NH 33.在下列化合物中,只有在溶液状态下才能导电的电解质是 A.NaCl B.酒精 C.H 2SO 4 D.Fe4.下列各组均为两种化合物溶于水时电离出的离子,其中由酸电离的是 A.Na +、OH -、SO 42- B.H +、Cl -、SO 42- C.Na +、K +、OH -D.Na +、K +、NO 3-5.要使溶液中存在大量的K +、Na +、H +、NO 3-和SO 42-五种离子,则在蒸馏水中至少溶解几种物质A.2种B.3种C.4种D.5种6.在某溶液中仅存在Na +、Fe 3+、SO 42-三种离子,已知Na +和SO 42-个数比为3:2,则Na +、Fe 3+和SO 42-三种离子的个数比为A.9:1:6B.3:1:2C.1:1:1D.6:1:9 7.下列说法正确的是A.电离时生成的阳离子全部是氢离子的单质叫做酸B.只有酸电离时,阳离子才是氢离子C.电离时生成的阴离子全部是氢氧根离子的化合物叫做碱D.所有的盐电离时都生成金属离子和酸根离子 8.能用H ++OH - = H 2O 表示的化学方程式为A.稀H 2SO 4和Ba(OH)2溶液反应B.氢氧化铜和稀盐酸反应C.氢氧化钾和稀H 2SO 4反应D.氢氧化钠和醋酸反应 9.下列离子方程式书写正确的是 A.Na 与水反应:Na+H 2O=Na ++OH -+H 2↑ B.Fe 与盐酸反应:2Fe+6H +=2Fe 3++3H 2↑ C.Cu 和AgNO 溶液反应:Cu+Ag +=Cu 2++Ag +D.石灰石与盐酸反应:CaCO 3+2H +=Ca 2++H 2O+CO 2↑ 10.无色溶液中能大量共存的是 A.K +、Na +、Cl -、NO 3-B.Cu 2+、NO 3-、OH -、Cl -C.MnO 4-、OH -、Cl -、K +D.CO 32-、K +、H +、Cl -二、非选择题。

高一化学电解质试题1.(1)写出下列物质在溶液中的电离方程式:3⑦CaCO3、⑧二氧化碳,根据表格内容进行填写。
【答案】(1)HCl====H++Cl-H2SO4====2H++SNaOH====Na++OH-Ca(OH)2====Ca2++2OH-KHSO4====K++H++SNaHCO3====Na++HC(2)①②⑥⑦⑤⑧③④【解析】(1)根据酸碱盐的定义书写相应的电离方程式,注意碳酸氢钠电离出碳酸氢根离子和钠离子,硫酸氢钾电离出钾离子、氢离子和硫酸根离子。
(2)单质铁、混合物氨水既不是电解质,也不是非电解质;二氧化碳、蔗糖是非电解质;酸、碱、盐是电解质。
【考点】物质的分类2.下列属于电解质并能导电的物质是A.淀粉B.KNO3溶液C.FeCl3晶体D.熔融的NaCl【答案】D【解析】A、淀粉是非电解质,错误;B、是电解质溶液,错误;C、是电解质但没有电离不能导电,错误;D、正确。
【考点】考查电解质概念及性质有关问题。
3.下列电离方程式书写错误的是()A.CaCl2=Ca2++2Cl—B.H2CO3H++HCO3-C.NaHCO3=Na++H++CO32-D.NaClO=Na++Cl O—【答案】C【解析】A、CaCl2电离生成Ca2+、Cl‾,正确;B、H2CO3为弱酸电离生成H+、HCO3‾,正确;C、NaHCO3电离生成H+、HCO3‾,错误;D、NaClO电离生Na+和ClO‾。
【考点】本题考查电离方程式的书写。
4.按要求完成下列填空(1)写出下列物质的电离方程式:Fe2(SO4)3_____________________________________________,NaHCO3______________________________________________;(2)写出下列反应的离子方程式:稀盐酸与碳酸钙反应___________________________________,氢氧化钡溶液与稀硫酸反应_______________________________;【答案】(1)Fe2(SO4)3=2Fe3++3SO42-,NaHCO3=Na++HCO3-(2)CaCO3+2H+=Ca2++CO2↑+ H2O Ba2++2OH-+2H++SO42-=BaSO4↓+ 2H2O【解析】(1)表示电解质电离出离子的式子属于电离方程式,则硫酸铁与碳酸氢纳的电离方程式分别是Fe2(SO4)3=2Fe3++3SO42-、NaHCO3=Na++HCO3-。

高一化学电解质题目和答案1. 下列状态的物质,既能导电又属于电解质的是( )a. mgcl2 晶体b. nacl 溶液c. 液态氯化氢d. 熔融的koh2. 下面关于电解质电离的描述恰当的就是( )a. caco3在水中溶解度很小,其导电能力很弱,所以 caco3是弱电解质b. caco3在水中溶解度不大,但熔化的 caco3全部电离,所以 caco3就是强电解质c. 氯气和氨气的水溶液导电性都很好,所以它们是强电解质d. 水难电离,纯水几乎不导电,水就是非电解质3. 下列物质中,导电性能最差的是( )a. 石墨棒b. 盐酸溶液c. 熔融的氢氧化钠d. 液态氯化钾4. 下列物质的水溶液能导电,但其本身属于非电解质的是( )a. 乙酸b. 酒精c. 食盐d. 氨气5. 正确书写离子方程式时,下列各项中,应使等式两边相等的是( )①离子数目成正比②粒子总数成正比③原子数目成正比④阳离子所带正电荷总数跟阴离子所带负电荷总数成正比⑤分子数目成正比⑥各元素原子数目成正比a. 只有①⑤b. 只有②④c. 只有③⑥d. 只有④⑥6. 向饱和状态石灰水中不断灌入二氧化碳,其溶液导电性的变化就是( )a. 由弱变强b. 由强变弱c. 由弱弱化,再变d. 由弱变强,再弱化7. 下列各组中的离子,相互间不发生离子反应的是( )a. na+、mg2+、cl-、oh-b. h+、ca2+、co32-、no3-c. cu2+、k+ 、so42-、no3-d. na+、hco3-、oh-、ca2+8. 电解质在人体内的促进作用就是十分广为和十分关键的,当电解质紊乱时,人体就要发生一系列呼吸困难症状,甚至可以损害生命。
为保持人体内电解质均衡,在大量流汗后应当及时补足的离子就是( )a. mg2+b. ca2+c. fe 3+d. na+9. 以下离子方程式中恰当的就是( )a. 稀硫酸滴在铜片上:cu + 2h+ = cu2+ +h2↑c. 硝酸几滴在石灰石上:caco3+ 2h+= ca2+ +h2co3d. 氧化铜与硫酸混和: cu2+ + so42-= cuso410. 以下描述恰当的就是( )a. naoh 溶液能导电,所以 naoh 溶液是电解质b. 液态kcl 不导电,但kcl 就是电解质c. 氯化氢的水溶液能导电,所以hcl 是电解质d. co2 的水溶液能够导电,所以co2 就是电解质二、填空题11. 在以下条件下若想出现离子反应?对能出现的写下离子方程式,无法出现的表明理由(1)ch3coona溶液与hcl溶液混和_________________________(2)ca(oh)2 的回应溶液与na2so4叶唇柱溶液复合____________________(3)ca(oh)2 的澄悬浊液与na2so4浓溶液混和____________________(4)cucl2 溶液与h2so4溶液复合__________________________12. (1)向nahso4 溶液中逐滴加入ba(oh)2溶液至中性,请写出发生反应的离子方程式____________________________(2)在上述溶液中继续滴加ba(oh)2溶液,请写出此步反应的离子方程式_____________________________13. 将hcl、h2so4、ba(no3)2 三种溶液,按一定顺序滴入到na2co3溶液中至恰好完全反应有以下现象:(1)加入a时有白色沉淀;(2)往(1)中结晶里重新加入b时结晶熔化,并存有气体逸出;(3)往(2)中溶液里加入c时,又有白色沉淀生成。

高一化学(必修一)《第一章 电解质的电离》练习题及答案班级:___________姓名:___________考号:___________一、单选题1.下列说法中正确的是A .液态HCl 、固态NaCl 均不导电,所以HCl 、NaCl 均不是电解质B .蔗糖、酒精在水溶液或熔化时均不导电,所以它们是非电解质C .铜、石墨均导电,所以它们是电解质D .NH 3、CO 2的水溶液均导电,所以NH 3、CO 2均是电解质 2.下列说法正确的是A .水导电性很差,所以水是非电解质B .电解质与非电解质的本质区别,是在一定条件下能否电离C .酸、碱和盐都属于电解质,其他化合物都是非电解质D .NaCl 和HCl 都是电解质,所以它们在熔融状态下都能导电 3.下列电离方程式中,正确的是A .NaHCO 3=Na ++3HCO -B .KClO 3=K ++Cl -+3O 2-C .Ca(NO 3)2=Ca 2++2(NO)23-D .熔融状态下,NaHSO 4=Na ++H ++SO 24-4.下列说法正确的是A .氨水能导电,所以氨气是电解质B .盐酸是强电解质,所以导电能力比醋酸溶液强C .氯化银难溶于水,所以氯化银是非电解质D .蔗糖溶液和熔融的蔗糖都不能导电,所以蔗糖是非电解质5.下列物质中,①碘化氢 ②KF ③液氨 ④KClO ⑤液氯 ⑥浓H 2SO 4 ⑦干冰 ⑧NH 4NO 3 ⑨澄清石灰水 ⑩CaCO 3 ⑪酒精。
是强电解质的一组物质是 A .②④⑥⑧⑩B .①②④⑧⑩C .①②④⑥⑧D .①④⑥⑧⑩6.在水溶液中,下列电离方程式不正确的是( )A .2244H SO 2H SO +-+═B .44NaHSO Na HSO +-+═C .2233Na CO 2Na CO +-+═D .()22Ba OH Ba 2OH +-+═7.下表中物质的分类组合完全正确的是( )A .AB .BC .CD .D8.下列说法正确的是A .石墨有较好的导电性,所以石墨属于电解质B .实验可知NH 3的水溶液具有一定的导电性,所以NH 3是电解质C .液态HCl 、固态NaCl 均不能导电,所以HCl 、NaCl 均不是电解质D .蔗糖在水溶液中和熔融状态下均不能导电,所以蔗糖不是电解质 9.下列物质中含有自由移动的Cl -的是 A .KClO 3溶液B .MgCl 2溶液C .液态HClD .固态NaCl10.在以下各种情形下,下列电离方程式书写正确的是A .熔融状态下NaHSO 4的电离:NaHSO 4=Na ++H ++SO 24-B .水溶液中Ba(OH)2的电离:Ba(OH)2=Ba 2++OH -C .水溶液中NaHCO 3的电离:NaHCO 3=Na ++HCO 3-D .水溶液中Al 2(SO 4)3的电离: Al 2(SO 4)3=3Al 3++3SO 24-11.下列叙述正确的是( )A .NaCl 、MgCl 2等物质熔融状态时都导电,因此它们都是电解质B .HCl 、H 2SO 4液态时都不导电,因此它们都是非电解质C .易溶于水的化合物都是电解质D .浓溶液的导电能力一定强12.下列物质中既能导电,又属于强电解质的一组物质是( )A.石墨、醋酸溶液、食盐晶体B.熔融状态的KOH、熔融状态的NaClC.稀H2SO4、NaOH溶液、纯HNO3D.液氨、石灰水、水银13.某学生利用如图所示装置对电解质溶液导电性进行实验探究。

高一化学电解质练习题1.正确选项为C,含有自由移动的Cl-的是KCl溶液。
2.正确选项为B,石墨棒导电性最差。
3.正确选项为C,AgNO3属于强电解质。
4.正确选项为B,BaSO4在熔化状态下不能导电,因为存在固态离子晶体结构。
5.正确选项为A,能自身电离出自由移动离子的化合物是电解质。
6.正确选项为D,NaOH的电离方程式为NaOH=Na+ + OH-。
7.正确选项为D,只有KCl在溶液中才能导电。
8.正确选项为C,固态磷酸是电解质,可以在熔融时或溶于水时导电。
9.正确选项为D,KCl本身是非电解质,但其水溶液可以导电。
10.1) Ba(OH)2 → Ba2+ + 2OH-2) NH4HSO4 → NH4+ + H+ + SO42-3) NaHCO3 → Na+ + HCO3-4) BaSO4不溶于水,不能电离。
11.正确选项为A,电解质与非电解质的本质区别是在水溶液或熔化状态下能否电离。
12.正确选项为B,NaCl既不属于电解质也不属于非电解质,但其水溶液可以导电。
13.在下列四种物质的溶液中,哪一种物质所含的离子种类最多?选项包括:A。
盐酸B。
硫酸C。
氢氧化钡D。
醋酸。
14.某种化合物易溶于水,但其水溶液不导电,那么该化合物是什么类型的?选项包括:A。
弱电解质B。
强电解质C。
非电解质 D。
无法确定。
15.在 KHSO4 的溶液和熔融态 KHSO4 中都存在哪种离子?选项包括:A。
H+ B。
HSO4- C。
SO42- D。
K+。
16.向下列各溶液中加入少量 NaOH 固体后,哪个溶液的导电能力变化最小?选项包括:A。
水 B。
盐酸 C。
醋酸溶液D。
NaCl 溶液。
13.在以下四种物质的溶液中,哪一种所含的离子种类最多?选项包括:A。
盐酸 B。
硫酸 C。
氢氧化钡 D。
醋酸。
14.某种化合物可以轻易溶于水,但其水溶液却不具备导电性。
那么这种化合物属于哪种类型?选项包括:A。
弱电解质 B。
强电解质 C。
![{高中试卷}高一化学电解质测试题1[仅供参考]](https://uimg.taocdn.com/32c53c9cfe4733687f21aaab.webp)
20XX年高中测试高中试题试卷科目:年级:考点:监考老师:日期:测试题1.下列关于电解质的说法正确的是A.液态HCl不导电,所以HCl不是电解质B.NH3溶于水形成的溶液能导电,所以NH3是电解质C.SO2溶于水能导电,所以SO2是电解质D.BaSO4在水溶液中难导电,但熔融下能导电所以.BaSO4是电解质2.下列物质属于强电解质的是A.H2CO2B.Cl2C.CaCO3D.NH33.在下列化合物中,只有在溶液状态下才能导电的电解质是A.NaClB.酒精C.H2SO4D.Fe4.下列各组均为两种化合物溶于水时电离出的离子,其中由酸电离的是A.Na+、OH-、SO42-B.H+、Cl-、SO42-C.Na+、K+、OH-D.Na+、K+、NO3-5.要使溶液中存在大量的K+、Na+、H+、NO3-和SO42-五种离子,则在蒸馏水中至少溶解几种物质A.2种B.3种C.4种D.5种6.在某溶液中仅存在Na+、Fe3+、SO42-三种离子,已知Na+和SO42-个数比为3:2,则Na+、Fe3+和SO42-三种离子的个数比为A.9:1:6B.3:1:2C.1:1:1D.6:1:97.下列说法正确的是A.电离时生成的阳离子全部是氢离子的单质叫做酸B.只有酸电离时,阳离子才是氢离子C.电离时生成的阴离子全部是氢氧根离子的化合物叫做碱D.所有的盐电离时都生成金属离子和酸根离子8.能用H++OH-= H2O表示的化学方程式为A.稀H2SO4和Ba(OH)2溶液反应B.氢氧化铜和稀盐酸反应C.氢氧化钾和稀H2SO4反应D.氢氧化钠和醋酸反应9.下列离子方程式书写正确的是A.Na与水反应:Na+H2O=Na++OH-+H2↑B.Fe与盐酸反应:2Fe+6H+=2Fe3++3H2↑C.Cu和AgNO溶液反应:Cu+Ag+=Cu2++Ag+D.石灰石与盐酸反应:CaCO3+2H+=Ca2++H2O+CO2↑10.无色溶液中能大量共存的是A.K+、Na+、Cl-、NO3-B.Cu2+、NO3-、OH-、Cl-C.MnO4-、OH-、Cl-、K+D.CO32-、K+、H+、Cl-二、非选择题。

高一化学电解质试题1. 下列电离方程式中,正确的是 A .H 2SO 4=H 2++SO 42-B .Ba(OH)2=Ba 2++OH -C .NaNO 3=Na ++NO 3-D .HClO =H ++Cl -+O 2-【答案】C【解析】A 、硫酸是强酸,在水溶液中完全电离,产生2H +,而不是H 2+,错误;B 、Ba(OH)2是强碱,完全电离产生2OH -,错误;C 、NaNO 3是易溶易电离的盐,完全电离,正确;D 、次氯酸是弱酸,不完全电离产生H +和ClO -,错误,答案选C 。
【考点】考查电解质的电离方程式的书写2. 下列叙述正确的是( )A .BaSO 4溶于水的部分能够电离,所以BaSO 4是电解质B .SO 2的水溶液能够导电,所以SO 2是电解质C .液态Cl 2不导电,所以Cl 2是非电解质D .液态HCl 不导电,所以HCl 是非电解质【答案】A【解析】A .正确。
D 虽然液态HCl 不导电,但是HCl 溶于水能导电,故HCl 是电解质。
B 电解质必须是其本身能电离出离子导电,错误。
电解质和非电解质必须是化合物,C 错误。
【考点】本题考查电解质和非电解质的判断。
3. 下列物质的水溶液能导电,但属于非电解质的是 A .H 2SO 4 B .Cl 2 C .NaAlO 2 D .SO 2【答案】D【解析】H 2SO 4、NaAlO 2都是电解质。
Cl 2是单质,既不是电解质,也不是非电解质。
SO 2+H 2O=H 2SO 3,H 2SO 3H ++ HSO 3-。
水溶液能导电。
故符合题意的物质是SO 2选项为D . 【考点】考查电解质、非电解质等概念的知识。
4. 下列物质属于电解质的一组是( ) A .CO 2、NH 3、HCl B .H 2SO 4、HNO 3、BaCl 2 C .H 3PO 4、H 2O 、Cu D .液态KNO 3、NaOH 溶液、C 2H 5OH【答案】B【解析】CO 2属于非电解质;A 选项不正确;Cu 属于单质,C 选项正确;NaOH 溶液属于混合物、C 2H 5OH 属于非电解质,D 选项不正确。
高一化学电解质试题答案及解析1.向一定体积的Ba(OH)2溶液中逐滴加入稀硫酸,溶液的导电性(以电流I表示)和滴入的稀硫酸的体积(用V表示)之间的关系正确的是()【答案】A【解析】向Ba(OH)2溶液中逐滴滴入稀硫酸,发生如下反应:Ba(OH)2+H2SO4====BaSO4↓+2H2O,所以随H2SO4溶液的不断加入,溶液中Ba2+和OH-的浓度越来越小,导电性越来越弱,当恰好完全反应时,溶液中离子浓度近乎为0,导电性最弱。
若此时继续滴加硫酸,因为H2SO4====2H++S,所以自由移动的离子浓度逐渐增大,导电性逐渐增强,当滴加到一定量时,随着H2SO4的加入,自由移动的离子浓度变化不大,其导电能力基本不再发生变化。
【考点】离子反应2.某化合物的化学式为(NH4)2Fe(SO4)2,它在水溶液里电离时生成两种阳离子和一种酸根离子。
(1)写出(NH4)2Fe(SO4)2的电离方程式。
(2)该化合物中氮元素与铁元素的质量比为。
(3)若向该化合物的水溶液中通入氯气,一种离子很容易被氧化,该离子将变成(用离子符号表示)。
(4)若向该溶液中加入过量的氨水,只能发生一个离子反应,则该反应的离子方程式为。
【答案】(1)(NH4)2Fe(SO4)2====2+Fe2++2(2)1∶2(3)Fe3+(4)Fe2++2NH3·H2O====Fe(OH)2↓+2【解析】(1)(NH4)2Fe(SO4)2在溶液中能够电离出、Fe2+两种阳离子和一种酸根离子;(2)其中氮元素与铁元素的质量比为(2×14)∶56=1∶2;(3)向溶液中通入氯气时,Fe2+被氧化成Fe3+;(4)氨水是弱碱,电离出的OH-与Fe2+发生离子反应生成Fe(OH)2沉淀,其反应的离子方程式为Fe2++2NH3·H2O====Fe(OH)2↓+2。
【考点】离子反应3.下列说法正确的是()A.硫酸钡不溶于水,所以硫酸钡是非电解质B.氨气溶于水可以导电,所以氨气是电解质C.固态磷酸是电解质,所以磷酸在熔化时和溶于水时都能导电D.液态氯化氢不能导电,但氯化氢是电解质【答案】D【解析】硫酸钡虽不溶于水,但它是电解质;氨气溶于水可以导电,但氨气不是电解质;磷酸是电解质,它溶于水时能导电,但熔化时不导电;液态氯化氢不能导电,但在水溶液中能导电,所以氯化氢是电解质。
高一化学电解质试题答案及解析1.向一定体积的Ba(OH)2溶液中逐滴加入稀硫酸,溶液的导电性(以电流I表示)和滴入的稀硫酸的体积(用V表示)之间的关系正确的是()【答案】A【解析】向Ba(OH)2溶液中逐滴滴入稀硫酸,发生如下反应:Ba(OH)2+H2SO4====BaSO4↓+2H2O,所以随H2SO4溶液的不断加入,溶液中Ba2+和OH-的浓度越来越小,导电性越来越弱,当恰好完全反应时,溶液中离子浓度近乎为0,导电性最弱。
若此时继续滴加硫酸,因为H2SO4====2H++S,所以自由移动的离子浓度逐渐增大,导电性逐渐增强,当滴加到一定量时,随着H2SO4的加入,自由移动的离子浓度变化不大,其导电能力基本不再发生变化。
【考点】离子反应2.离子的摩尔电导率可用来衡量电解质溶液中离子导电能力的强弱,摩尔电导率越大,离子在溶液中的导电能力越强。
已知Ca2+、OH-、HC的摩尔电导率分别为0.60、1.98、0.45,据此可判断,往饱和的澄清石灰水中通入过量的CO2,溶液导电能力随CO2通入量的变化趋势正确的是()【答案】D【解析】向澄清石灰水中通入CO2,当CO2适量时Ca(OH)2+CO2====CaCO3↓+H2O,其反应的离子方程式为Ca2++2OH-+CO2====CaCO3↓+H2O,当CO2过量时CaCO3+CO2+H2O====Ca(HCO3)2,其反应的离子方程式为CaCO3+CO2+H2O====Ca2++2HC。
所以向澄清石灰水中通入过量的CO2,先生成碳酸钙沉淀,钙离子、氢氧根离子浓度减小,溶液导电能力减弱,后沉淀溶解生成碳酸氢钙溶液,钙离子、碳酸氢根离子的浓度增大,钙离子的浓度与原来相等,碳酸氢根离子的浓度与原来氢氧根离子浓度相等,但OH-的摩尔电导率大于HC的摩尔电导率,所以最后溶液的导电性小于原来的导电性,最后CaCO3全部溶解后,溶液中离子的浓度不再发生变化,即导电能力不再发生变化。
20XX年高中测试高中试题试卷科目:年级:考点:监考老师:日期:电解质(第二课时)学习目标:1. 了解离子反应的概念,掌握离子反应的条件(复分解类型)2. 掌握简单离子反应方程式的书写3. 进一步学会用实验法进行研究和学习学习过程:二、电解质在水溶液中的反应1、电解质在水溶液中反应的实质【实验·探讨】实验:向Ba(OH)2溶液中滴加几滴酚酞,测其导电性,然后逐滴加入稀H2SO4,观察溶液中的现象和导电情况(看电流表指针的变化)。
现象:①②③。
分析原因:(1)写出H2SO4和Ba(OH)2的电离方程式(2)说明出现上述现象的原因:结论:该反应的实质为练习:分析下列化学反应的实质:①盐酸与氢氧化钠溶液的反应②氯化钠与硝酸银溶液的反应③碳酸钠与稀盐酸的反应2、离子反应概念:条件:①②③3、离子方程式的书写(1)概念:(2)离子方程式的书写有两种书写思路:一是从溶液中所含离子的角度分析如何发生反应;二是根据化学方程式改写。
①从溶液中所含离子的角度分析:以Ba(OH)2与H2SO4混合为例,其书写步骤为:ⅰ、分析各反应物在水溶液里的存在形式:Ba(OH)2溶于水后存在、离子,H2SO4溶于水后得、。
规律:易溶于水的强电解质(强酸、强碱、可溶性盐)在水中完全电离写离子,难溶于水的物质,气体物质,弱电解,单质,氧化物写化学式。
微溶物的处理:在反应物中,若为溶液写离子,若为浊液写化学式,若在生成物中写成化学式ⅱ、按离子反应发生的条件判断上述微粒是否结合:故与结合为沉淀,与结合为 (弱电解质)iii、综合i、ii写出离子方程式,对前后未变化的离子不写,只写实际参加反应的离子。
Ⅳ、检查是否配平既注意质量守恒(微粒的种类和数量的守恒),又要注意电荷守恒。
离子方程式为:②根据化学方程式改写:以Na2CO3与盐酸反应为例i、写先正确写出化学方程式(必须配平):ii、拆易溶的强电解质写离子符号,难溶物及弱电解质,气体,单质,氧化物仍写化学式,上述反应改写为:iii、删把前后未发生变化的离子删去,只剩下变化的离子,即用实际参加反应的离子的符号表示出该反应的离子方程式。
3388高一化学电解质测试题第二节电解质(第2节)【课前学案】旧知回顾1.电离的含义。
2.强电解质和弱电解质的本质区别。
3.写出以下物质的电离方程式:H2SO4 __________________________________一.一般书写离子方程式时可分四步:① 写——写正确的。
②拆――把易溶于水且易电离的物质写成_____________形式,把难溶于水的物质或难电离的物质以及气体、单质、氧化物仍用___________表示。
③ 删除-对于方程式两侧的相同离子,不参与反应的离子应“按数字”删除。
④ 检查——检查书写的离子方程式是否符合前三项的规定,是否同时符合质量守恒和电荷守恒,即方程式两侧各元素的原子数是否相等,以及方程两边每个离子携带的电荷总数是否相等。
注:要想正确书写离子方程式,需掌握住难溶、微溶以及难电离的物质。
2.学习离子反应需注意的问题:(1)为了判断一个化学反应是否是离子反应,我们必须先看看这个反应是否在_______________________。
(2)在离子方程式里,把易溶、易电离的物质写成______________,把难溶的或难电离的物质以及气体物质等,写成它们的_______________。
(3)为了平衡离子方程式,我们不仅要平衡每个元素的原子或离子的数量,还要平衡________________________。
(4)离子方程式表示所有___________________的离子反应。
3、如何证明硫酸溶液和ba(oh)2溶液的反应是离子反应?hclo________________;。
【课堂学案】重点难点突破:1、指出下列离子方程式的错误:(1) Na放入水中Na+2H2O==Na+OH+2h2↑-(2)硫酸铜溶液与氢氧化钡溶液Ba2+SO24=baso4的反应↓+-+(3)cl2与水反应cl2+h2o===2h+cl+clo+++--2-(4)caco3中加入盐酸ca2+co2+h2o+co2↑3+2h===ca+(5)al与盐酸反应al+2h===al3+h2↑++(6)铁与盐酸2Fe+6h==2fe3+3h2的反应↑++-(7)naoh溶液中通入过量的co22oh+co2===co23+h2o- 2. 下列反应的离子方程式不能用Ba2++SO24==BaSO4表示↓, 这是()-a、硝酸钡溶液和稀硫酸C、碳酸钡和稀硫酸B、稀硫酸和氯化钡溶液d、氯化钡溶液与硫酸钠溶液+-3.硫酸氢钠(NaHSO4)在水溶液中可以完全电离成Na和hso-4,而HSO4被稀释(例如1-4)moll-1以下)的溶液中,可完全电离为h+so24。
夯实基础1.下列物质中含有自由移动的―()Cl 的是A .KClO 3溶液B.液态 HCl C.KCl 溶液D. NaCl 晶体2.下列物质中,导电性能最差的是()A .熔融氢氧化钠B.石墨棒C.盐酸D.氯化钾固体3.下列物质中,属于强电解质的是()A .醋酸B. Fe(OH)3C.AgNO 3D.H2O 4.BaSO4在熔化状态下能导电,其本质原因是()A .是电解质B.存在自由移动的离子C.存在电子D.存在离子5.下列叙述正确的是()A.在水溶液中能自身电离出自由移动的离子的化合物是电解质B.凡是在水溶液里和熔化状态下都不能导电的物质叫非电解质C.能导电的物质一定是电解质D.某物质若不是电解质,就一定是非电解质6.下列电离方程式中,正确的是()A.NH32O NH 4++ OH -·HB. KClO 3=K ++Cl- +3O2-C.H2S=2H++S2-D.NaOH=Na ++OH -7.下列化合物中,只有在溶液中才能导电的电解质是()A .NaCl B.酒精C.H2SO4D. KCl8.下面的说法正确的是()A.硫酸钡不溶于水,所以硫酸钡是非电解质B.二氧化碳溶于水可以导电,所以二氧化碳是电解质C.固态磷酸是电解质,所以磷酸在熔融时或溶于水时都能导电D.液态氯化氢不能导电,但氯化氢是电解质9.下列物质的水溶液能导电,但本身属于非电解质的是()A .Cl 2B. NH3C.HCl D. KCl10.写出下列物质在水溶液中的电离方程式。
(1)Ba(OH) 2(2)NH4HSO4(3)NaHCO 3(4)BaSO4能力提升11.下列说法正确的是()A.电解质与非电解质的本质区别是在水溶液或熔化状态下能否电离B.强电解质与弱电解质的本质区别是其水溶液导电性的强弱C.酸、碱和盐类都属于电解质,其他化合物都是非电解质D.常见的强酸、强碱和大部分盐都是强电解质,其他化合物都是弱电解质12.下列物质中既不属于电解质,也不属于非电解质,但其水溶液能导电的是()A .C12B. Na C.Na2CO3D.C2H5OH13.下列四种物质的溶液中所含分子.离子种类最多的是()A .盐酸B.硫酸C.氢氧化钡D.醋酸14.某化合物易溶于水,但其水溶液不导电,则该化合物是()A .弱电解质B.强电解质C.非电解质D.不能确定15.在 KHSO 4的溶液中和熔融态的KHSO 4中都存在的离子是()A .H+B. HSO4-C.SO42-D.K+16.分别向下列各溶液中加入少量NaOH 固体,溶液的导电能力变化最小的是()A .水B.盐酸C.醋酸溶液D. NaCl 溶液17.下列关于酸.碱.盐元素组成的说法中,正确的是()A.酸、碱一定含氢,盐一定不含氢B.酸、碱、盐可能都不含金属元素C.碱、盐可能含氧,酸一定含氧D.盐一定含金属元素,酸、碱不一定含金属元素18.现有以下物质:①NaCl 晶体②液态SO2③液态醋酸④汞⑤固体BaSO4⑥纯蔗糖(C12H22O11)⑦酒精 (C2H5OH) ⑧熔化的 KNO 3。
化学电解质练习题高一化学电解质练习题1.下列物质中含有自由移动的Cl ―的是 ( )A.KClO3溶液B.液态 HClC.KCl溶液D.NaCl晶体2.下列物质中,导电性能最差的是 ( )A.熔融氢氧化钠B.石墨棒C.盐酸D.氯化钾固体3.BaSO4在熔化状态下能导电,其本质原因是 ( )A.是电解质B.存在自由移动的离子C.存在电子D.存在离子4.下列叙述正确的是 ( )A.在水溶液中能自身电离出自由移动的离子的化合物是电解质B.凡是在水溶液里和熔化状态下都不能导电的物质叫非电解质C.能导电的物质一定是电解质D.某物质若不是电解质,就一定是非电解质5.下列化合物中,只有在溶液中才能导电的电解质是 ( )A.NaClB.酒精C.H2SO4D.KCl6.下面的说法正确的是 ( )A.硫酸钡不溶于水,所以硫酸钡是非电解质B.二氧化碳溶于水可以导电,所以二氧化碳是电解质C.固态磷酸是电解质,所以磷酸在熔融时或溶于水时都能导电D.液态氯化氢不能导电,但氯化氢是电解质9.下列物质的水溶液能导电,但本身属于非电解质的是 ( )A.Cl2B.NH3C.HClD.KCl能力提升7.下列说法正确的是 ( )A.电解质与非电解质的本质区别是在水溶液或熔化状态下能否电离B.强电解质与弱电解质的本质区别是其水溶液导电性的强弱C.酸、碱和盐类都属于电解质,其他化合物都是非电解质D.常见的强酸、强碱和大部分盐都是强电解质,其他化合物都是弱电解质8.下列物质中既不属于电解质,也不属于非电解质,但其水溶液能导电的是 ( )A.C12B.NaC.Na2CO3D.C2H5OH9.现有以下物质:①NaCl晶体②液态SO2③液态醋酸④汞⑤固体BaS O4⑥纯蔗糖(C12H22O11)⑦酒精(C2H5OH)⑧熔化的KNO3。
请回答下列问题。
(填相应序号)(1)以上物质能导电的是____________;(2)以上物质属于电解质的是___________;(3)以上物质属于非电解质的是______________________;(4)以上物质中溶于水后形成的水溶液能导电的是______________________。
第二节电解质
(第1课时)
【课前学案】
旧知回顾
1、根据在水溶液中或熔融状态下能否导电,化合物可分为_______和________。
2、酸、碱、盐在水溶液中能导电的原因是酸、碱、盐在水分子的作用下______产生了自由移动的_______。
新课预习
时,生成的______________________的化合物称为酸;生成的__________________的化合物称为碱;能生成________和_____________的化合物称为盐。
写出下列化合物的电离方程式:
H2SO4:KOH:
BaCl2:
3、电解质按照其在水溶液中能否完全电离分为______________和____________。
强电解质溶液的导电能力_____________弱电解质溶液的导电能力,电解质溶液的导电能力取决于溶液中的自由移动的离子浓度的大小。
溶液中的自由移动的离子浓度越大,其导电性_________;浓度越小,其导电性__________。
如:硝酸是强电解质,但如果浓度很小,溶液中自由移动的离子浓度就很小,其导电性就___________较浓的醋酸溶液。
【课堂学案】
重难点突破:
一、电解质和非电解质
电解质是指在水溶液中或熔化状态下能够导电的化合物。
酸、碱、盐都是电解质。
如NaOH、HCl、NaCl、CaCO3等等。
非电解质是指在水溶液和熔化状态都不导电的化合物。
如CO2、NH3、绝大多数有机物如酒精等。
温馨提示:(1)电解质、非电解质是对化合物的一种分类。
单质既不是电解质,也不是非电解质。
(2)电解质溶液导电必须是化合物本身电离产生的离子导电,否则该化合物属于非电解质。
如CO2、SO2、NH3等是非电解质。
二、强电解质和弱电解质
在电解质中,按照它们在水溶液中的电离程度,把它们分为强电解质和弱电解质。
因此(1)划分强、弱电解质的唯一标准是看电解质能否完全电离。
(2)电解质的强弱与其溶解性无关。
(3)电解质的强弱与溶液的导电性没有必然联系,强电解质溶液的导电性不一定强。
导电性的强弱取决于溶液中自由移动的离子的浓度。
常见的强电解质:强酸、强碱、绝大多数盐;
常见的弱电解质:弱酸、弱碱、水等。
三、电解质的电离和电离方程式
电解质溶于水或受热熔化时,离解成能够自由移动的离子的过程称为电离。
1、电离的条件:溶于水或受热熔化。
注意:与是否通电无关。
2、电离方程式:强电解质的电离方程式用“=”,弱电解质的电离方程式用“”。
【例题解析】
【例题1】现有九种物质:①铝线②石墨③氯气④硫酸钡晶体⑤纯硫酸⑥金刚石⑦石灰水⑧乙醇⑨熔化的硝酸钾。
其中能导电的是__________,属于电解质的是__________,既不是电解质也不是非电解质的是__________。
【例题2】下列说法正确的是()
A.硫酸钡难溶于水,其水溶液导电能力极弱,所以硫酸钡是弱电解质
B.CO2溶于水得到的溶液能导电,所以CO2是电解质
C.强电解质溶液的导电能力不一定比弱电解质溶液的导电能力强
D.氯化银难溶于水,故其水溶液不导电
【例题3】下列电离方程式书写正确的是()
A.H2SO4=2H++SO2-
4B.Ba(OH)2=Ba2++(OH)-
2
C.FeCl3=Fe2++3Cl-D.NaHCO3=Na++H++CO2-
3知识归纳
1.概念:
电解质
非电解质
强电解质
弱电解质
2.电解质导电的原因:
3.电离及电离方程式:
【课后学案】
夯实基础
1.下列物质中含有自由移动的Cl―的是()A.KClO3溶液B.液态HCl C.KCl溶液D.NaCl晶体2.下列物质中,导电性能最差的是()A.熔融氢氧化钠B.石墨棒
C.盐酸D.氯化钾固体
3.下列物质中,属于强电解质的是()A.醋酸B.Fe(OH)3C.AgNO3D.H2O 4.BaSO4在熔化状态下能导电,其本质原因是()A.是电解质B.存在自由移动的离子
C.存在电子D.存在离子
5.下列叙述正确的是()A.在水溶液中能自身电离出自由移动的离子的化合物是电解质
B.凡是在水溶液里和熔化状态下都不能导电的物质叫非电解质
C.能导电的物质一定是电解质
D.某物质若不是电解质,就一定是非电解质
6.下列电离方程式中,正确的是()
+OH-
A.NH 3·H2O NH+
4
B.KClO3=K++Cl-+3O2-
C.H2S=2H++S2-
D.NaOH=Na++OH-
7.下列化合物中,只有在溶液中才能导电的电解质是()A.NaCl B.酒精C.H2SO4D.KCl
8.下面的说法正确的是()A.硫酸钡不溶于水,所以硫酸钡是非电解质
B.二氧化碳溶于水可以导电,所以二氧化碳是电解质
C.固态磷酸是电解质,所以磷酸在熔融时或溶于水时都能导电
D.液态氯化氢不能导电,但氯化氢是电解质
9.下列物质的水溶液能导电,但本身属于非电解质的是()A.Cl2B.NH3C.HCl D.KCl
10.写出下列物质在水溶液中的电离方程式。
(1)Ba(OH)2
(2)NH4HSO4
(3)NaHCO3
(4)BaSO4
能力提升
11.下列说法正确的是()A.电解质与非电解质的本质区别是在水溶液或熔化状态下能否电离
B.强电解质与弱电解质的本质区别是其水溶液导电性的强弱
C.酸、碱和盐类都属于电解质,其他化合物都是非电解质
D.常见的强酸、强碱和大部分盐都是强电解质,其他化合物都是弱电解质
12.下列物质中既不属于电解质,也不属于非电解质,但其水溶液能导电的是()A.C12B.Na C.Na2CO3D.C2H5OH
13.下列四种物质的溶液中所含分子.离子种类最多的是()A.盐酸B.硫酸C.氢氧化钡D.醋酸
14.某化合物易溶于水,但其水溶液不导电,则该化合物是()A.弱电解质B.强电解质C.非电解质D.不能确定
15.在KHSO4的溶液中和熔融态的KHSO4中都存在的离子是()
A.H+B.HSO-
4C.SO2-
4
D.K+
16.分别向下列各溶液中加入少量NaOH固体,溶液的导电能力变化最小的是()A.水B.盐酸C.醋酸溶液D.NaCl溶液
17.下列关于酸.碱.盐元素组成的说法中,正确的是()
A.酸、碱一定含氢,盐一定不含氢
B.酸、碱、盐可能都不含金属元素
C.碱、盐可能含氧,酸一定含氧
D.盐一定含金属元素,酸、碱不一定含金属元素
18.现有以下物质:①NaCl晶体②液态SO2③液态醋酸④汞⑤固体BaSO4⑥纯蔗糖(C12H22O11)
⑦酒精(C2H5OH)⑧熔化的KNO3。
请回答下列问题。
(填相应序号)
(1)以上物质能导电的是______________________;
(2)以上物质属于电解质的是______________________;
(3)以上物质属于非电解质的是______________________;
(4)以上物质中溶于水后形成的水溶液能导电的是______________________。
第一课时
【例题1】【解析】导电并不是电解质在任何状态下都具有的性质,电解质导电必须通过外因――加热至熔融状态或水分子的作用。
电解质和非电解质必须是化合物。
某化合物溶于水能导电但不一定是电解质,这是因为只有该化合物在水溶液中能直接电离出自由移动的离子才能判定其是电解质。
【答案】①②⑦⑨④⑤⑨①②③⑥⑦
【例题2】〖解析〗硫酸钡是强电解质,电解质的强弱与化合物的溶解性无关,也与其溶液的导电能力无关。
溶液的导电能力强弱与溶液中自由移动的离子的浓度以及所带的电荷有关,氯化银虽难溶于水但为强电解质,氯化银电离产生的银离子、氯离子,故其水溶液导电。
而CO2本身在水溶液中不能电离,能电离的为碳酸。
〖答案〗C
【例题3】〖解析〗B中Ba(OH)2在水中电离出Ba2+与OH-,但不能写成(OH)2-的形式。
C中FeCl3在溶液中电离出Fe3+、Cl-,而不是Fe2+,电荷也不守恒。
D中NaHCO3在溶液中电离出的HCO3-不能拆开写。
〖答案〗A
A组夯实基础答案:
1.D
2.D
3.C
4.B
5.A
6.AD
7.C
8.D
9.B
10.(1)Ba(OH)2=Ba2++2OH-(2)NH4HSO4=NH4++HSO4-
(3)NaHCO3=Na++HCO3-(4)BaSO4=Ba2++SO42-
B组能力提升答案:
11.A 12.A 13.D 14.C 15.D 16.D 17.B
18.(1)④⑧(2)①③⑤⑧(3)②⑥⑦(4)①②③⑤⑧。