[热点新题]金属与酸反应的图象题
- 格式:doc
- 大小:182.00 KB
- 文档页数:7

一、中考初中化学金属与酸反应的图像1.向一定量的稀盐酸中,分别加入足量的水、金属铁、氢氧化钙溶液、硝酸银溶液,下列图示正确的是A.B.C.D.【答案】D【解析】【分析】铁和稀盐酸反应生成氯化亚铁和氢气,稀盐酸和氢氧化钙反应生成氯化钙和水,稀盐酸和硝酸银反应生成氯化银和硝酸。
【详解】A、向一定量的稀盐酸中加入足量的水时,酸性减弱,pH升高,但不会变成中性或碱性,pH只会接近7,故A不正确;B、活泼金属和酸接触就会放出氢气,铁和稀盐酸反应生成氯化亚铁和氢气,起点应该从零开始,故B不正确;C、一定量的稀盐酸和氢氧化钙反应生成氯化钙和水,随着反应的进行,溶液的质量增加,反应完全后溶液质量不变,故C不正确;D、稀盐酸和硝酸银反应生成氯化银和硝酸,随着反应的进行,沉淀的质量增加,反应完全,质量不变,故D正确。
故选D。
2.下列四个图像中分别表示四个化学兴趣小组活动中的数据及处理情况,其中错误的是A.图甲:加水稀释氢氧化钠溶液B.图乙:足量的锌和铁分别加入等质量同浓度的稀硫酸中C.图丙:加热一定质量的KMnO4 固体D.图丁:往饱和石灰水加入少量生石灰【答案】B【解析】【分析】【详解】A.氢氧化钠溶液呈碱性,pH大于7,加水稀释氢氧化钠溶液,pH不断减小至无限接近于7,故A正确;B.足量的锌和铁分别加入等质量同浓度的稀硫酸,产生氢气质量相等,故B错误;C.一定质量的KMnO4固体在加热条件下生成锰酸钾、二氧化锰和氧气,固体质量不断减少,当完全分解时固体质量达到最小值,之后不再变化,故C 正确;D、往饱和石灰水中加入少量生石灰,生石灰与水反应放热,温度升高,氢氧化钙的溶解度减小,溶质质量分数减小,当完全反应后温度降低到室温时,溶解度不变,饱和溶液的溶质质量分数不变,故D正确。
答案选B。
【点睛】本题考查物质的性质的图象题,注意起点、拐点与终点的含义。
3.下列图象不能正确反映对应变化关系的是()A.某温度时,向一定量的饱和石灰水中加入少量生石灰B.加热氯酸钾与二氧化锰的混合物制氧气C.向等质量、等质量分数的稀硫酸中分别加入镁、铝至过量D.向氯化钠的饱和溶液中不断地加入硝酸钾【答案】D【解析】【分析】【详解】A、某温度时,向一定量的饱和石灰水中加入少量生石灰时,氧化钙和水反应生成氢氧化钙,同时放热,温度恢复至室温时,由于溶剂水减小,部分溶质析出,因此溶质质量减小,故正确;B、氯酸钾在二氧化锰的催化作用下加热生成氯化钾和氧气,生成的逸散到空气中,所以固体中氧元素的质量分数减小,由于二氧化锰中含有氧元素,所以最终氧元素质量分数不为0,故正确;C、足量的金属与等质量、等质量分数的稀硫酸反应时生成氢气的质量是相等的,因为质量相等的同浓度的稀硫酸中氢元素的质量相等,根据化学方程式:2Al+3H2SO4═Al2(SO4)3+3H2↑、Mg+H2SO4═MgSO4+H2↑,完全反应参加反应的镁的质量大于铝的质量,故正确;D、向氯化钠的饱和溶液中不断地加入硝酸钾,硝酸钾会溶解,溶液质量增加,氯化钠的质量不变,根据溶液的质量分数=100% 溶质的质量溶液的质量,所以氯化钠的质量分数会不断减小,直至硝酸钾在溶液中达到饱和,故错误。

一、中考初中化学金属与酸反应的图像1.下列图像能正确反映其对应关系的是()A.向等质量、等浓度的稀硫酸中分别加入过量的Zn和FeB.向含有少量NaOH的Na2CO3溶液中逐滴加入稀盐酸C.用等质量、等浓度的过氧化氢溶液在有、无催化剂条件下制取氧气D.向盛有稀硫酸的烧杯中不断加水稀释【答案】B【解析】【分析】【详解】A、酸质量相等,金属过量,最终产生氢气质量相等,产生相同质量的氢气时,消耗的锌的质量应大于铁的质量,与图像不符;B、向含有少量NaOH的Na2CO3溶液中逐滴加入稀盐酸,稀盐酸会先和氢氧化钠反应生成氯化钠和水,再和碳酸钠反应生成二氧化碳氯化钠和水,与图像相符,故选B;C、催化剂只能改变反应速率,不能改变生成物的多少,用等质量、等浓度的过氧化氢溶液在有、无催化剂条件下制取氧气,生成氧气质量应该相等,与图像不符;D、加水稀释只会使稀硫酸酸性减弱,不可能pH大于7,变为碱性,与图像不符。
【点睛】该题是一道图像题,图像题的难点在于图像信息和文字信息的转化,然后和实际反应情况对应是否相符。
2.下列图像能正确反应其对应关系的是()A.向一定体积的稀硫酸中逐滴加入足量的氢氧化钠溶液B.向足量的镁和铁中加入等质量、等质量分数的稀硫酸C.向硫酸镁和硫酸的混合溶液中逐渐加入氢氧化钠溶液D.某温度下,向一定量饱和硝酸钾溶液中加入硝酸钾晶体【答案】B【解析】【详解】A、向一定体积的稀硫酸中逐滴加入足量的氢氧化钠溶液,pH应该是由小于7逐渐升高,直至等于或大于7,该选项对应关系不正确;B、向足量的镁和铁中加入等质量、等质量分数的稀硫酸,最终生成氢气质量相等,由于镁比铁活泼,反应需要时间短,该选项对应关系正确;C、向硫酸镁和硫酸的混合溶液中逐渐加入氢氧化钠溶液,氢氧化钠先和硫酸反应生成硫酸钠和水,后和硫酸镁反应生成氢氧化镁沉淀和硫酸钠,该选项对应关系不正确;D、某温度下,向一定量饱和硝酸钾溶液中加入硝酸钾晶体,硝酸钾不能溶解,溶质质量分数不变,该选项对应关系不正确。
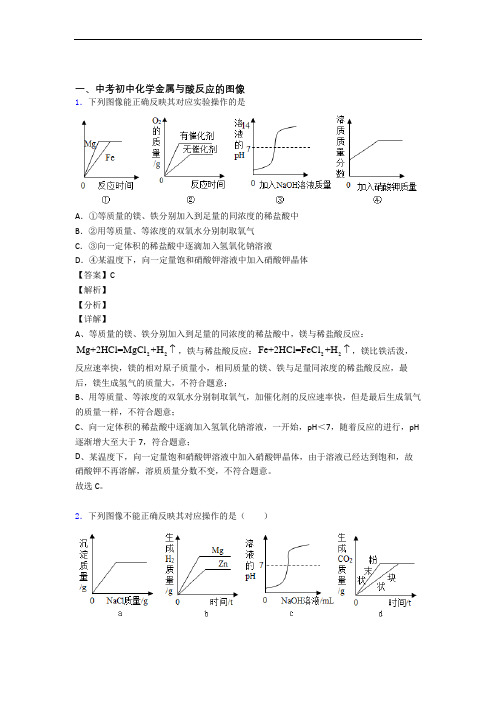
一、中考初中化学金属与酸反应的图像1.下列图像能正确反映其对应实验操作的是A .①等质量的镁、铁分别加入到足量的同浓度的稀盐酸中B .②用等质量、等浓度的双氧水分别制取氧气C .③向一定体积的稀盐酸中逐滴加入氢氧化钠溶液D .④某温度下,向一定量饱和硝酸钾溶液中加入硝酸钾晶体【答案】C【解析】【分析】【详解】A 、等质量的镁、铁分别加入到足量的同浓度的稀盐酸中,镁与稀盐酸反应:22Mg+2HCl=MgCl +H ↑,铁与稀盐酸反应:22Fe+2HCl=FeCl +H ↑,镁比铁活泼,反应速率快,镁的相对原子质量小,相同质量的镁、铁与足量同浓度的稀盐酸反应,最后,镁生成氢气的质量大,不符合题意;B 、用等质量、等浓度的双氧水分别制取氧气,加催化剂的反应速率快,但是最后生成氧气的质量一样,不符合题意;C 、向一定体积的稀盐酸中逐滴加入氢氧化钠溶液,一开始,pH <7,随着反应的进行,pH 逐渐增大至大于7,符合题意;D 、某温度下,向一定量饱和硝酸钾溶液中加入硝酸钾晶体,由于溶液已经达到饱和,故硝酸钾不再溶解,溶质质量分数不变,不符合题意。
故选C 。
2.下列图像不能正确反映其对应操作的是( )A.a图在一定量的AgNO3溶液中逐滴加入NaCl溶液B.b图足量的Zn和Mg分别与一定量的等体积等质量分数的稀硫酸反应C.c图向稀盐酸中逐滴加入NaOH溶液D.d图等质量块状和粉末状CaCO3分别与足量等体积等质量分数的稀盐酸反应【答案】B【解析】【分析】【详解】A、在一定量的AgNO3溶液中逐滴加入NaCl溶液,不断产生白色沉淀,当恰好完全反应时沉淀达到最大值,对应关系正确;B、镁比锌活泼,镁和稀硫酸的反应速率较快,足量的Zn和Mg分别与一定量的等体积等质量分数的稀硫酸反应,镁的活动性比锌强,反应速率快,反应时间短;镁和锌过量,盐酸完全反应,最终生成氢气的质量相等,对应关系不正确;C、向稀盐酸中逐滴加入NaOH溶液时,稀盐酸和氢氧化钠反应生成氯化钠和水,随着反应的进行,pH升高,当恰好完全反应时,溶液的pH等于7,继续加入氢氧化钠溶液时,溶液的pH大于7,对应关系正确;D、首先粉末状碳酸钙和盐酸反应速率大于块状的,所以对应图象斜率要大,同时由于碳酸钙质量相同,所以二者图象的终点也相同,对应关系正确。

一、中考初中化学金属与酸反应的图像1.下列图像能正确反映其对应实验操作的是A .①等质量的镁、铁分别加入到足量的同浓度的稀盐酸中B .②用等质量、等浓度的双氧水分别制取氧气C .③向一定体积的稀盐酸中逐滴加入氢氧化钠溶液D .④某温度下,向一定量饱和硝酸钾溶液中加入硝酸钾晶体【答案】C【解析】【分析】【详解】A 、等质量的镁、铁分别加入到足量的同浓度的稀盐酸中,镁与稀盐酸反应:22Mg+2HCl=MgCl +H ↑,铁与稀盐酸反应:22Fe+2HCl=FeCl +H ↑,镁比铁活泼,反应速率快,镁的相对原子质量小,相同质量的镁、铁与足量同浓度的稀盐酸反应,最后,镁生成氢气的质量大,不符合题意;B 、用等质量、等浓度的双氧水分别制取氧气,加催化剂的反应速率快,但是最后生成氧气的质量一样,不符合题意;C 、向一定体积的稀盐酸中逐滴加入氢氧化钠溶液,一开始,pH <7,随着反应的进行,pH 逐渐增大至大于7,符合题意;D 、某温度下,向一定量饱和硝酸钾溶液中加入硝酸钾晶体,由于溶液已经达到饱和,故硝酸钾不再溶解,溶质质量分数不变,不符合题意。
故选C 。
2.下列图像能正确反映其对应关系的是A .表示向一定量的稀硫酸中加入足量的锌粒B.表示向一定量稀盐酸和氯化钡的混合液中滴加硝酸银溶液C.表示向一定量的氢氧化钠溶液中滴加稀硫酸至恰好完全反应D.表示将等质量的大理石分别与足量的等质量等溶质质量分数的稀盐酸反应【答案】A【解析】【分析】【详解】A、向一定量的稀硫酸中加入足量的锌粒时,反应生成氢气,当稀硫酸完全反应后不再产生气体,正确;B、向一定量稀盐酸和氯化钡的混合液中滴加硝酸银溶液时,立即产生白色沉淀,错误;C、向一定量的氢氧化钠溶液中滴加稀硫酸时,氢氧化钠和稀硫酸反应生成硫酸钠和水,随着反应进行,pH不断减小,恰好完全反应时pH=7,错误;D、将等质量的大理石分别与足量的等体积等溶质质量分数的稀盐酸反应时,最终生成二氧化碳的质量相等,错误。

一、中考初中化学金属与酸反应的图像1.向一定量的稀盐酸中,分别加入足量的水、金属铁、氢氧化钙溶液、硝酸银溶液,下列图示正确的是A.B.C.D.【答案】D【解析】【分析】铁和稀盐酸反应生成氯化亚铁和氢气,稀盐酸和氢氧化钙反应生成氯化钙和水,稀盐酸和硝酸银反应生成氯化银和硝酸。
【详解】A、向一定量的稀盐酸中加入足量的水时,酸性减弱,pH升高,但不会变成中性或碱性,pH只会接近7,故A不正确;B、活泼金属和酸接触就会放出氢气,铁和稀盐酸反应生成氯化亚铁和氢气,起点应该从零开始,故B不正确;C、一定量的稀盐酸和氢氧化钙反应生成氯化钙和水,随着反应的进行,溶液的质量增加,反应完全后溶液质量不变,故C不正确;D、稀盐酸和硝酸银反应生成氯化银和硝酸,随着反应的进行,沉淀的质量增加,反应完全,质量不变,故D正确。
故选D。
2.如图表所示4个图象中,能正确反映变化关系的是A.足量镁和铝分别放入等质量、等浓度的稀盐酸中B.镁在空气中加热C .加热一定质量的高锰酸钾固体D .向一定质量的二氧化锰中加入过氧化氢溶液【答案】B【解析】【分析】【详解】A 、根据反应的化学方程式及其质量关系:22Mg+2HCl=24MgCl +3H 72↑,325421961872Al +6HCl =2AlCl +3H 32↑可知 ,足量的镁和铝分别放入等质量、等浓度的稀盐酸中,酸能完全反应,因此反应生成的氢气质量相同,产生相同质量的氢气,消耗镁的质量大于 铝的质量,图像不能正确反映变化关系,不符合题意;B 、镁与空气中的氧气反应生成氧化镁,根据质量守恒定律,反应物质量应该等于生成物质量,因此固体的质量不断增加,图像能正确反映变化关系,符合题意;C 、高锰酸钾受热分解生成了锰酸钾、二氧化锰和氧气,固体的质量减小,锰元素的质量不变,因此固体中锰元素的质量分数应当增加,图像不能正确反映变化关系,不符合题意;D 、向一定质量的二氧化锰中加入过氧化氢溶液,二氧化锰是该反应的催化剂,质量不变,图像不能正确反映变化关系,不符合题意。

初中化学图像试题1.下列图像与所述实验相符的是A B C DA .向一定量锌粒中加入过量稀硫酸B .向一定量氯化钠饱和溶液中不断加水C .向一定量氢氧化钠和碳酸钠的混合溶液中加入过量的石灰水D .20℃时,向一定量不饱和的硝酸钾溶液中加入过量的硝酸钾晶体2某兴趣小组为探究活泼金属与酸反应的规律,将质量相等的甲、乙两种金属分别放入到质量分数相同的足量稀盐酸中,经实验测定并绘制出生成氢气的质量与反应时间的关系(见右图)。
分析图像得到的以下结论中, 一定正确的是:( )A .金属甲比金属乙活泼B .金属甲比金属乙的相对原子质量大C .金属乙比金属甲的反应速率大D .金属乙比金属甲的化合价高3.用质量相等的锌粉和铁粉,分别与溶质质量分数相同、等质量的稀盐酸充分反应,产生氢气的质量和反应所用时间的关系如右图所示。
则下列说法中不正确的是( )A.曲线a 、b 分别表示锌、铁的反应情况 B.盐酸均反应完,锌、铁有剩余C.盐酸均反应完,锌恰好完全反应,铁有剩余 D.锌、铁都反应完,盐酸有剩余4.某校化学活动小组为探究X 、Y 、Z三种金属与酸的反应情况,进行了如下实验:取等质量的X 、Y 、Z 分别与足量的溶质质量分数相等的稀硫酸反应,都生成+2价金属的硫酸盐,反应情况如右图所示。
下列对该图象理解的叙述中,正确的是[相对原子质量Mg-24 Zn-65 Fe-56 Al-27 Na-23]A .金属活动性由强到弱:X 、Z 、YB .金属活动性由强到弱:X 、Y 、ZC .X 、Y 、Z 依次可能是Mg 、Zn 、FeD .相对原子质量的大小:Z>Y>X5.等质量的A 、B 两种金属,分别与质量分数相同的足量稀盐酸反应(已知,A 、B 在生成物中均为+2价),生成氢气的质量和反应时间的关系如图所示,则下列判断正确的是( ) A .金属A 比金属B 活泼 B .相对原子质量:A>BC .A 、B 均消耗完时,所得溶液的质量均比反应前各自酸溶液的质量大D .A 、B 均消耗完时,产生氢气的质量:A<B6.用相同质量的锌和铁分别跟足量稀盐酸反应,反应情况见图(横坐标t 表示反应时间,纵坐标m 表示生成氢气的质量),其中符合实际的是ZnSO /gKNO 质量分数氢气质量37、室温下,等质量的镁片和铝片分别与足量的稀硫酸反应,产生氢气的质量(m)与时间(t)的关系图正确的是( )A 、B 、C 、D 、8.(09湖北鄂州)某研究性学习小组的同学为探究实验室制取氢气的方案,分别用等质量的金属A 、B 跟质量相同、溶质质量分数相同的稀硫酸反应,反应生成氢气的质量与时间的关系如下图所示。





一、中考初中化学金属与酸反应的图像1.下列图像能正确反映其对应关系的是()A.向等质量、等浓度的稀硫酸中分别加入过量的Zn和FeB.向含有少量NaOH的Na2CO3溶液中逐滴加入稀盐酸C.用等质量、等浓度的过氧化氢溶液在有、无催化剂条件下制取氧气D.向盛有稀硫酸的烧杯中不断加水稀释【答案】B【解析】【分析】【详解】A、酸质量相等,金属过量,最终产生氢气质量相等,产生相同质量的氢气时,消耗的锌的质量应大于铁的质量,与图像不符;B、向含有少量NaOH的Na2CO3溶液中逐滴加入稀盐酸,稀盐酸会先和氢氧化钠反应生成氯化钠和水,再和碳酸钠反应生成二氧化碳氯化钠和水,与图像相符,故选B;C、催化剂只能改变反应速率,不能改变生成物的多少,用等质量、等浓度的过氧化氢溶液在有、无催化剂条件下制取氧气,生成氧气质量应该相等,与图像不符;D、加水稀释只会使稀硫酸酸性减弱,不可能pH大于7,变为碱性,与图像不符。
【点睛】该题是一道图像题,图像题的难点在于图像信息和文字信息的转化,然后和实际反应情况对应是否相符。
2.如图表所示4个图象中,能正确反映变化关系的是 A .足量镁和铝分别放入等质量、等浓度的稀盐酸中B .镁在空气中加热C .加热一定质量的高锰酸钾固体D .向一定质量的二氧化锰中加入过氧化氢溶液【答案】B【解析】【分析】【详解】A 、根据反应的化学方程式及其质量关系:22Mg+2HCl=24MgCl +3H 72↑,325421961872Al +6HCl =2AlCl +3H 32↑可知 ,足量的镁和铝分别放入等质量、等浓度的稀盐酸中,酸能完全反应,因此反应生成的氢气质量相同,产生相同质量的氢气,消耗镁的质量大于 铝的质量,图像不能正确反映变化关系,不符合题意;B 、镁与空气中的氧气反应生成氧化镁,根据质量守恒定律,反应物质量应该等于生成物质量,因此固体的质量不断增加,图像能正确反映变化关系,符合题意;C、高锰酸钾受热分解生成了锰酸钾、二氧化锰和氧气,固体的质量减小,锰元素的质量不变,因此固体中锰元素的质量分数应当增加,图像不能正确反映变化关系,不符合题意;D、向一定质量的二氧化锰中加入过氧化氢溶液,二氧化锰是该反应的催化剂,质量不变,图像不能正确反映变化关系,不符合题意。

一、中考初中化学金属与酸反应的图像 1.如图表所示4个图象中,能正确反映变化关系的是A .足量镁和铝分别放入等质量、等浓度的稀盐酸中B .镁在空气中加热C .加热一定质量的高锰酸钾固体D .向一定质量的二氧化锰中加入过氧化氢溶液【答案】B【解析】【分析】【详解】A 、根据反应的化学方程式及其质量关系:22Mg+2HCl=24MgCl +3H 72↑,325421961872Al +6HCl =2AlCl +3H 32↑可知 ,足量的镁和铝分别放入等质量、等浓度的稀盐酸中,酸能完全反应,因此反应生成的氢气质量相同,产生相同质量的氢气,消耗镁的质量大于 铝的质量,图像不能正确反映变化关系,不符合题意;B 、镁与空气中的氧气反应生成氧化镁,根据质量守恒定律,反应物质量应该等于生成物质量,因此固体的质量不断增加,图像能正确反映变化关系,符合题意;C、高锰酸钾受热分解生成了锰酸钾、二氧化锰和氧气,固体的质量减小,锰元素的质量不变,因此固体中锰元素的质量分数应当增加,图像不能正确反映变化关系,不符合题意;D、向一定质量的二氧化锰中加入过氧化氢溶液,二氧化锰是该反应的催化剂,质量不变,图像不能正确反映变化关系,不符合题意。
故选B。
2.下列所示的四个图像,能正确反映对应变化关系的是A.向一定量的硝酸铜和硝酸镁的混合溶液中加入铁粉B.等质量的镁和铁分别与等质量、等浓度足量的稀硫酸反应C.向一定量的氢氧化钠溶液中滴加pH=3的稀盐酸D.向一定量的含有盐酸的氯化铜溶液中滴加氢氧化钠溶液【答案】B【解析】【分析】【详解】A、铁的金属活动性比铜强,比镁弱,向一定量的硝酸铜和硝酸镁的混合溶液中加入铁粉,铁不能与硝酸镁溶液反应,铁能与硝酸铜溶液反应生成硝酸亚铁溶液和铜,参加反应的铁的质量小于生成铜的质量,则溶液的质量应减少,故错误;B、等质量的镁和铁分别与等质量、等浓度足量的稀硫酸反应,横坐标是硫酸的量,故等量的硫酸产生氢气的质量相等,当金属全部参加反应,生成氢气的质量与金属的相对原子质量成反比(+2价的金属),则镁产生的氢气的质量大于铁,故正确;C、向一定量氢氧化钠溶液中滴加pH=3的稀盐酸,稀盐酸和氢氧化钠反应生成氯化钠和水,随着反应进行,溶液碱性减弱,pH减小,恰好完全反应时pH=7,继续加入稀盐酸时,溶液pH小于7,但是不能减小到3,更不能小于3,故错误;D、向含有盐酸的氯化铜溶液中滴加烧碱溶液时,氢氧化钠先和稀盐酸反应,后和氯化铜反应,因此开始不能产生沉淀,故错误。



金属与酸反应(讲义)➢知识点睛1.图象题(1)氢气质量与反应时间的关系a.等质量的镁、铝、锌、铁和足量的酸反应(图1),金属反应完,酸有剩余,生成氢气的质量不等,产生氢气的质量由多到少为:____、____、____、____,产生氢气由快到慢为____、____、____、____。
b.足量的镁、铝、锌、铁和等量的酸反应(图2),酸反应完,金属有剩余,生成氢气的质量相等,消耗金属的质量由少到多为:____、____、____、____,产生氢气由快到慢为____、____、____、____。
注:四种金属的产氢能力由强到弱为:___、___、___、___。
(2)氢气质量与反应物质量的关系a.向等质量的镁、铝、锌、铁中加入足量酸(图3),最初酸不足,产生氢气的质量相等,最终酸过量,金属不足,产生的氢气质量不等,产生氢气的质量由多到少为:____、____、____、____。
b.向等质量的酸中加入足量的镁、铝、锌、铁(图4),最初金属不足,等质量的金属参与反应产生氢气的质量不等,产生氢气的质量由多到少为:____、____、____、____,最终酸不足,产生的氢气质量相等。
注:此类图象中斜率的大小不再表示产生氢气的快慢。
2.天平问题天平两边加入金属和酸的量均相等,天平偏转情况:(1)天平首先偏向放出氢气较慢的一侧,即金属活动性较弱的一侧。
(2)天平最终偏向放出氢气的量较少的一侧,即产氢能力弱的一侧。
若两边放出氢气的质量相等,则天平最终平衡。
注:天平最终不可能偏向产氢能力强的一侧。
3.根据金属混合物与酸反应判断金属混合物的成分(1)平均值法计算出金属混合物的平均相对原子质量Ar,利用平均值法,推测金属混合物的成分(将Al的相对原子质量折算成18,氢后金属的相对原子质量折算成无穷大)。
A r(A)<Ar< A r(B)(2)极端假设法假设金属混合物中只含已知的该金属,计算此时应产生的氢气质量,比较其与实际产生的氢气质量的大小关系,根据金属产氢能力,推测金属混合物的成分。

一、中考初中化学金属与酸反应的图像1.如图表所示4个图象中,能正确反映变化关系的是A .足量镁和铝分别放入等质量、等浓度的稀盐酸中B .镁在空气中加热C .加热一定质量的高锰酸钾固体D .向一定质量的二氧化锰中加入过氧化氢溶液【答案】B 【解析】 【分析】 【详解】A 、根据反应的化学方程式及其质量关系:22Mg+2HCl=24MgCl +3H 72↑,325421961872Al +6HCl =2AlCl +3H 32↑可知 ,足量的镁和铝分别放入等质量、等浓度的稀盐酸中,酸能完全反应,因此反应生成的氢气质量相同,产生相同质量的氢气,消耗镁的质量大于 铝的质量,图像不能正确反映变化关系,不符合题意;B 、镁与空气中的氧气反应生成氧化镁,根据质量守恒定律,反应物质量应该等于生成物质量,因此固体的质量不断增加,图像能正确反映变化关系,符合题意;C 、高锰酸钾受热分解生成了锰酸钾、二氧化锰和氧气,固体的质量减小,锰元素的质量不变,因此固体中锰元素的质量分数应当增加,图像不能正确反映变化关系,不符合题意;D 、向一定质量的二氧化锰中加入过氧化氢溶液,二氧化锰是该反应的催化剂,质量不变,图像不能正确反映变化关系,不符合题意。
故选B 。
2.如图所示四个图像,分别对应四个过程,其中不正确的是A .向一定量的锌中加入足量的稀盐酸B .向一定量硫酸铜溶液中加入足量的铁C .足量锌、铁中分别加入等质量、等质量分数的稀硫酸D .等质量的锌和铁中分别加入足量等质量分数的稀硫酸【答案】B 【解析】 【分析】 【详解】A 、向一定量的锌中加入足量的稀盐酸,锌完全反应后质量为0,不符合题意;B 、向一定量硫酸铜溶液中加入足量的铁,铁和硫酸铜反应生成硫酸亚铁和铜,44=Fe+CuSO FeSO +Cu ,每56g 固体铁加入置换出64g 铜单质,反应后固体质量增加,溶液的质量减小,反应完后不再减小,符合题意;C 、足量锌、铁中分别加入等质量、等质量分数的稀硫酸,锌的活动性强,在相同的时间内生成的氢气多,稀硫酸的质量相同,完全反应后生成的氢气相同,不符合题意;D、等质量的锌和铁中分别加入足量等质量分数的稀硫酸,相同的酸反应,生成的氢气质量相同,根据反应方程式:22Zn+2HCl=ZnCl+H↑22Fe+2HCl=FeCl+H↑每生成2g氢气需要锌的质量为65g,需要铁的质量为56g,等质量的锌和铁中分别加入足量等质量分数的稀硫酸,完全反应后,铁生成的氢气多,不符合题意。

一、中考初中化学金属与酸反应的图像1.下列图像能正确反映其对应关系的是()A.向等质量、等浓度的稀硫酸中分别加入过量的Zn和FeB.向含有少量NaOH的Na2CO3溶液中逐滴加入稀盐酸C.用等质量、等浓度的过氧化氢溶液在有、无催化剂条件下制取氧气D.向盛有稀硫酸的烧杯中不断加水稀释【答案】B【解析】【分析】【详解】A、酸质量相等,金属过量,最终产生氢气质量相等,产生相同质量的氢气时,消耗的锌的质量应大于铁的质量,与图像不符;B、向含有少量NaOH的Na2CO3溶液中逐滴加入稀盐酸,稀盐酸会先和氢氧化钠反应生成氯化钠和水,再和碳酸钠反应生成二氧化碳氯化钠和水,与图像相符,故选B;C、催化剂只能改变反应速率,不能改变生成物的多少,用等质量、等浓度的过氧化氢溶液在有、无催化剂条件下制取氧气,生成氧气质量应该相等,与图像不符;D、加水稀释只会使稀硫酸酸性减弱,不可能pH大于7,变为碱性,与图像不符。
【点睛】该题是一道图像题,图像题的难点在于图像信息和文字信息的转化,然后和实际反应情况对应是否相符。
2.下列图像能正确反映其对应实验操作的是A .①等质量的镁、铁分别加入到足量的同浓度的稀盐酸中B .②用等质量、等浓度的双氧水分别制取氧气C .③向一定体积的稀盐酸中逐滴加入氢氧化钠溶液D .④某温度下,向一定量饱和硝酸钾溶液中加入硝酸钾晶体【答案】C【解析】【分析】【详解】A 、等质量的镁、铁分别加入到足量的同浓度的稀盐酸中,镁与稀盐酸反应:22Mg+2HCl=MgCl +H ↑,铁与稀盐酸反应:22Fe+2HCl=FeCl +H ↑,镁比铁活泼,反应速率快,镁的相对原子质量小,相同质量的镁、铁与足量同浓度的稀盐酸反应,最后,镁生成氢气的质量大,不符合题意;B 、用等质量、等浓度的双氧水分别制取氧气,加催化剂的反应速率快,但是最后生成氧气的质量一样,不符合题意;C 、向一定体积的稀盐酸中逐滴加入氢氧化钠溶液,一开始,pH <7,随着反应的进行,pH 逐渐增大至大于7,符合题意;D 、某温度下,向一定量饱和硝酸钾溶液中加入硝酸钾晶体,由于溶液已经达到饱和,故硝酸钾不再溶解,溶质质量分数不变,不符合题意。

一、中考初中化学金属与酸反应的图像1.下列图象分别与选项中的操作项对应,其中不合理的是()A.往一定量的NaOH溶液中滴加稀盐酸至过量B.某温度下,将KNO3固体不断地加入水中C.向一定量CuSO4溶液和稀硫酸的混合溶液中滴加NaOH溶液D.持续不断地加热一定质量的碳酸氢钠固体【答案】D【解析】【详解】A、向一定量的NaOH溶液滴加盐酸中至过量,碱性逐渐变弱,酸性逐渐增强,pH值的变化是从大于7逐渐的减小到小于7,故选项图象与选项中的操作项对应合理;B、某温度下,将KNO3固体不断地加入水中,所得溶液的溶质的质量分数由0不断增大,当达到饱和时溶质质量分数不再增大,故选项图象与选项中的操作项对应合理;C、向一定量CuSO4溶液和稀硫酸的混合溶液中滴加NaOH溶液,先与硫酸反应,开始时不会生成沉淀,硫酸消耗完后再与硫酸铜反应会生成氢氧化铜沉淀,故沉淀的质量先是零,再不断上升,最后形成一条水平直线,故选项图象与选项中的操作项对应合理;D、持续不断地加热一定质量的碳酸氢钠固体,碳酸氢钠受热分解生成了碳酸钠、水和二氧化碳,剩余固体的质量不为0,故选项图象与选项中的操作项对应不合理。
故选D。
2.下列图像能正确反映其对应变化关系的是A .常温下,相同质量的锌和铁分别与足量的溶质质量分数相同的稀硫酸反应B .镁条在氧气中燃烧C .加热氯酸钾和二氧化锰的混合物D .用一氧化碳气体还原一定质量的氧化铁【答案】C【解析】【分析】【详解】A 、在金属活动性顺序中,锌的活动性强于铁,故锌的反应速率大于铁,根据化学反应方程式2442=F Fe+H SO SO +H e ↑2442=Z Zn+H SO SO +H n ↑,每生成2g 氢气,需要消耗的锌、铁的质量分布为65g 、56g ,所以相同质量的锌和铁分别与足量的溶质质量分数相同的稀硫酸,最终是铁产生的氢气的质量大于锌产生的氢气的质量,故选项错误;B 、镁燃烧生成氧化镁,随着反应的进行,固体质量不断增大,但是开始时固体质量不是0,故选项错误;C 、加热氯酸钾和二氧化锰的混合物制取氧气,反应中二氧化锰作催化剂,反应前后质量不变,故选项正确;D 、一氧化碳气体还原一定质量的氧化铁粉末除了生成二氧化碳外还会生成一定质量的铁,最终固体的质量不会为0,故选项错误。
[热点新题]金属与酸反应的图象题山东省高密市李家营中学刘常德一般情况下,活泼金属可以与稀盐酸、稀硫酸等稀酸溶液发生反应生成氢气。
涉及金属与酸反应问题的图像题,侧重于考查金属的活动性、金属的相对原子质量、氢气的质量(或体积)、溶液的质量、溶质质量分数等相关量的变化关系。
解答这类题的关键是,读懂图像本意,审清图像内涵。
准确理解并应用图像中的相关信息,正确解题。
如图1,图中横坐标代表时间,纵坐标代表生成氢气的质量。
当金属与稀酸溶液反应时,随着反应的进行,生成氢气的质量越来越大,此时在图像上表现为一条上升的直线(如图1中OA段所示),且生成氢气越快,这条直线的斜率越大(即“坡度越陡”)。
因此,从图像上看生成氢气的快慢只须看“坡度陡、坡度缓”,“坡度越陡”表示生成氢气越快,线段OA的斜率与金属的活动性强弱有关。
金属活动性越强,线段斜率越大。
“坡度越缓”表示生成氢气越慢,金属活动性越弱,线段斜率越小。
当金属与稀酸溶液充分反应后,生成氢气的质量将不再变化,此后在图像上表现为一条水平直线(如图1中的AB段所示)。
生成氢气越多,这条直线表现在图像上就越高。
因此,从图像上看生成氢气的多少,只须看“线高、线低”,“线越高”表示生成氢气越多,“线越低”表示生成氢气越少。
综上所述,解决这类问题时,一般需要用到下列规律:1.在温度、金属颗粒大小和稀酸溶液溶质质量分数一定的条件下,金属的活动性越强,生成氢气就越快;生成氢气越快,说明金属的活动性就越强。
2.当金属的化合价相同时,对于相同质量的金属,金属的相对原子质量越大,生成的氢气越少;生成的氢气越多,金属的相对原子质量越小。
例1.锌和稀硫酸反应生成氢气,几次实验的锌的用量不等,但稀硫酸的用量相同。
锌的用量(X轴),生在氢气的体积(Y轴)(在同温同压下测定)关系如图2,下列关于实验结果描述错误的是()A.线段AB(包括A点)表示锌过量、硫酸已耗尽B.线段AB(不包括A点)表示锌过量、硫酸已耗尽C.线段OA(包括A点)表示锌和过量的硫酸反应D.线段OA(不包括A点)表示锌和过量的硫酸反应解析:一定质量的锌与足量的稀硫酸充分反应,图2中A点表示某一时刻,反应刚好停止。
线段OA(包括点A)表示金属和过量的稀硫酸反应。
线段AB(不包括点A)表示金属已经反应完,而稀硫酸过量。
不过,值得我们注意的是,如果是足量的锌与一定量的稀硫酸充分反应时,那么线段OA(包括点A)则表示过量的金属和稀硫酸反应。
线段AB(不包括点A)表示稀硫酸已经消耗完,而锌过量。
解答:B、D如图3,金属A的活动性要比金属B的活动性强。
如果金属A、B与相同质量分数的酸溶液反应后生成的化合物中元素化合价相同(如同为+2价等)那么,生成氢气的体积越多或质量越大,则该金属的相对原子质量越小。
图3中金属B的相对原子质量小于金属A的相对原子质量。
足量的A、B两种金属同时分别放入两份溶质质量分数相同的少量稀盐酸中,如果反应后出现一种金属有剩余或两种金属都有剩余,而稀盐酸完全消耗了,那么它们生成氢气的体积(或质量)相等,如图4所示。
练一练将物质的量相等的铝粉和铁粉分别与同体积、同浓度的稀硫酸反应。
反应情况如图5所示。
有关叙述中正确的是()A.铝粉、铁粉和硫酸均有剩余B.铝粉、铁粉均反应完,硫酸有剩余C.硫酸、铝粉均反应完,铁粉有剩余D.硫酸、铁粉均反应完,铝粉有剩余例2. 某探究小组的同学对金属的性质很感兴趣,探究金属的活泼性。
取等质量的A、B 金属,分别投入溶质质量分数相同的足量的盐酸中,生成氢气的质量(m)与时间(t)的关系如图6(已知A、B元素在生成物中的化合价相同)1.由图6分析,甲、乙、丙三位同学的对话正确的是()时,产生氢气的质量A<B甲:时间t1时,金属均有剩余乙:到时间t2丙:两种金属原子的相对原子质量A<B2.结论:金属A、B的活泼性强弱关系是()解析:金属与酸反应涉及的量有:①金属的质量;②金属元素在反应中显示的化合价;③金属的相对原子质量;④金属的活动性;⑤产生氢气的量;⑥产生氢气的时间;⑦酸的量。
这些量之间存在如下关系:1.当金属的化合价相同时,对于相同质量的金属,金属的相对原子质量越大,生成的氢气越少;生成的氢气越多,金属的相对原子质量越小。
2.在温度、金属颗粒大小和稀酸溶液溶质质量分数一定的条件下,金属的活动性越强,生成氢气就越快;生成氢气越快,说明金属的活动性就越强。
可通过曲线的斜率来判断金属的活动性,斜率越大,反应的速率越快,则金属的活动性越强。
解决这类问题有时要讨论两种情况:1.如果酸足量,由于A、B的相对原子质量不同,则产生氢气的量不同;2.如果酸不足,产生氢气的量相同,相对原子质量小的金属一定过量,相对原子质量较大的金属可能过量,也可能正好完全反应。
本题中等质量的A、B金属,分别投入溶质质量分数相同的足量的盐酸中。
由图示产生氢气的量不相等,属于第一种情况。
解答:1、甲、丙 2、 A<B练一练等质量的镁、锌、铁分别跟足量的稀硫酸在室温下起反应,图7中能够正确反映产生氢气质量m与反应时间t关系的图像为()练一练将质量相等的A、B、C三种金属,同时分别放入三份溶质质量分数相同的质量与反应时间的关系如图8所示。
根据图中所且足量的稀盐酸中,反应生成H2提供的信息,得出的结论正确的是()(A、B、C在生成物中均为+2价)的质量是A>B>CA.放出H2B.金属活动性顺序是A>B>CC.反应速率最大的是AD.相对原子质量是C>B>A练一练将等质量的镁、铁、锌,分别放入三份溶质质量分数相同的稀盐酸中,反应生成的H质量与反应时间的关系如图9所示。
根据图中的信息,作出的判断不正确的是()2A.图线x表示镁的反应情况B.铁消耗的稀盐酸质量最大C.镁、锌一定过量,铁可能反应完D.镁一定过量,锌、铁可能反应完我们在讨论金属与酸反应的图像问题时,一定要分清图像中X、Y轴所表示的具体含义,因为变换了X、Y轴的内容,所对应的图像就会出现不同的情形。
如果X轴表示参加反应的金属的质量, Y轴表示生成的氢气的质量,一定量的不同金属与足量的酸进行反应,如图10所示。
假设三种金属分别为铝、镁、铁,你能找出其中代表铁的线条吗?这时,我们可采取以下方法:1、在图像上画一条平行于X轴的直线与三个线条交于不同的三个点,比较这三个点的横坐标数值的大小,数值越大,表示产生等质量的氢气时,消耗的金属质量越多,数值越小,表示产生等质量的氢气时,消耗的金属质量越少;2、在图像上画一条平行于Y轴的直线与三个线条交于不同的三个点,比较这三个点的纵坐标数值的大小,数值越大,表示相等质量的金属完全反应后,产生的氢气越多;数值越小,表示相等质量的金属完全反应后,产生的氢气越少。
通过以上分析,我们不难看出,线条C表示的金属是铁。
练一练图11表示Fe、Zn、Mg、Al分别跟稀盐酸反应制取氢气的质量(m)与所用的金属质量(M)之间的关系图,其中正确的是()刚才提到,我们在讨论金属与酸反应的图像问题时,一定要分清图像中X、Y轴所表示的具体含义,因为变换了X、Y轴的内容,所对应的图像就会出现不同的情形。
进行变式训练时,有时还会出现如下的情况。
例3.向一定量的铁粉中逐滴加入稀硫酸至过量,图12是反应过程中某种物质的质量Y 随加入稀硫酸的质量变化的关系,则Y不可能表示()A.消耗铁粉的质量 B.生成硫酸亚铁的质量C.溶液的总质量 D.生成氢气的质量解析:根据金属与酸反应的原理与过程,图中确定了X轴的含义,表示稀硫酸的质量,那么一段时间后,消耗铁粉的质量从无到有,渐渐增多,完全消耗后,不再变化。
生成硫酸亚铁的质量也是从无到有,渐渐增多,反应停止后,不再变化。
生成氢气的质量也是从无到有,渐渐增多,反应停止后,不再变化。
而溶液的质量一开始不应该是0,并且反应后溶液的质量一直在增加。
所以Y轴有可能是消耗铁粉的质量、生成硫酸亚铁的质量、生成氢气的质量,Y轴不可能表示溶液的总质量。
解答:C练一练如图13表示等质量的金属Mg和Al分别与足量且质量分数相等的稀硫酸反应,下列叙述正确的是()A.X表示反应所用时间,Y表示生成氢气的质量B.X表示生成氢气的质量,Y表示反应所用时间C.X表示滴加稀硫酸的质量,Y表示生成氢气的质量D.X表示参加反应的金属的质量,Y表示生成氢气的质量提示:质量相等的Mg和Al与足量且质量分数相等的稀硫酸反应,Al产生氢气的质量比Mg产生氢气的质量多,同时Al消耗的硫酸质量也比Mg消耗的硫酸质量多。
因为两种金属的活动性不相同,所以它们反应所需的时间也不相同。
例4.白铁是镀锌的铁,将白铁投入到稀硫酸溶液中,反应产生氢气的质量和反应时间的关系如图14,写出不同时间的化学方程式:1.0-t1间不产生氢气:2.t1-t2间产生氢气速度快:3.t2后产生氢气较慢:解析:因为白铁是镀锌的铁,白铁最外层的锌与空气中的氧气反应生成致密的氧化锌。
将白铁投入到稀硫酸中,刚开始应是氧化锌与硫酸反应,此时没有气泡产生。
反应的化学方程式是:ZnO+H2SO4=ZnSO4+H2O ,除去氧化锌后,锌与稀硫酸接触,快速反应产生氢气,化学方程式是:Zn+H2SO4=ZnSO4+H2↑,镀锌层消耗后,铁与稀硫酸接触,缓慢地产生氢气,反应的化学方程式是:Fe+H2SO4=FeSO4+H2↑。
解答:1.ZnO+H2SO4=ZnSO4+H2O 2.Zn+H2SO4=ZnSO4+H2↑ 3.Fe+H2SO4=FeSO4+H2↑练一练将相等质量的锌粒(X)与锌粉(Y)投入到相同体积相同质量分数的足量稀盐酸中,充分反应。
图15中能正确表示产生氢气的质量与反应的时间的关系的是()提示:等质量的锌粒与锌粉与足量的稀盐酸充分反应后,生成的氢气的质量应该项相等。
反应物的颗粒大小影响了反应的速率,也就是反应所需的时间有区别,颗粒越小反应就越快,所需要的时间就越短。
练一练:1、C 2、A 3、A D 4、C 5、D 6、C 7、A。