镁和铝
- 格式:ppt
- 大小:700.50 KB
- 文档页数:30
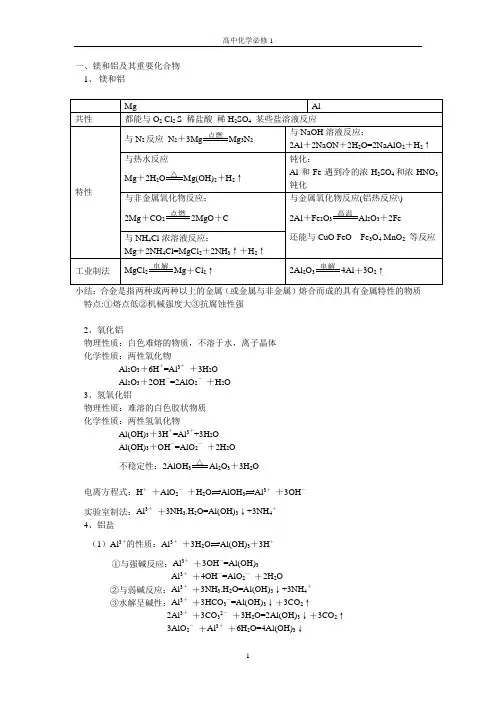
一、镁和铝及其重要化合物1、镁和铝特点:①熔点低②机械强度大③抗腐蚀性强2、氧化铝物理性质:白色难熔的物质,不溶于水,离子晶体化学性质:两性氧化物Al2O3+6H+=Al3++3H2OAl2O3+2OH-=2AlO2-+H2O3、氢氧化铝物理性质:难溶的白色胶状物质化学性质:两性氢氧化物Al(OH)3+3H+=Al3++3H2OAl(OH)3+OH-=AlO2-+2H2O△不稳定性:2AlOH3Al2O3+3H2O电离方程式:H++AlO2-+H2O33++3OH-实验室制法:Al3++3NH3.H2O=Al(OH)3↓+3NH4+4、铝盐(1)Al3+的性质:Al3++3H2O Al(OH)3+3H+①与强碱反应:Al3++3OH-=Al(OH)3Al3++4OH-=AlO2-+2H2O②与弱碱反应:Al3++3NH3.H2O=Al(OH)3↓+3NH4+③水解呈碱性:Al3++3HCO3-=Al(OH)3↓+3CO2↑2Al3++3CO32-+3H2O=2Al(OH)3↓+3CO2↑3AlO2-+Al3++6H2O=4Al(OH)3↓总结:AlCl 3溶液滴加到NaOH 溶液中开始无沉淀后有沉淀NaOH 溶液滴加到AlCl 3溶液中先出现沉淀后沉淀溶解 (2)AlO 2-的性质AlO 2- +2H 2O=Al(OH)3↓+OH - ① 与强酸反应: AlO 2- +H +(少量) +H 2O=Al(OH)3↓ AlO 2-+4H + (过量)=Al 3+ +H 2O②与弱酸反应:AlO 2-+CO 2+2H 2O=Al(OH)3↓+HCO 3-③与水解呈酸性的物质反应:3AlO 2- +Al 3+ +6H 2O=4Al(OH)3↓3AlO 2- +Fe 3+ + 6H 2O=3Al(OH)3↓+Fe(OH)3↓总结:将HCl 滴加到NaAlO 2中先出现沉淀后溶解 将NaAlO 2滴加到HCl 中开始无沉淀后有沉淀 (3)明矾2KAl(SO 4)2+3Ba(OH)2=2Al(OH)3↓+3BaSO 4+K 2SO 4 KAl(SO 4)2+2Ba(OH)2=2BaSO 4↓+KAlO 2+H 2O小结:Al 3+AlOH 3AlO 2AlOH 3Al 3+ 未知溶液白色沉淀白色沉淀溶解,从而未知溶液中含Al 3+未知溶液白色沉淀白色沉淀溶解,从而未知溶液含AlO 2-二、铁及其重要化合物1、铁:第四周期第Ⅷ族 26号元素 各层电子数为2 8 14 2 常见价态+2和+3(1)与弱氧化剂反应 Fe Fe 2+ S +Fe I 2+Fe 2(2)与强氧化剂反应Fe Fe 3+ 3Cl 2+2Fe=2FeCl 3 3Br 2+2Fe 3稀硝酸:Fe +4HNO 3=Fe(NO 3)3+2NO ↑+2H 2O 3Fe +8HNO 3=3Fe(ON 3)3+2NO 2↑+4H 2O特殊:3Fe +2O 23O 4 3Fe +4H 2O 3O 4+4H 2↑2、 氧化物 FeO :黑色固体不溶于水,在空气中加热会生成Fe 3O 4Fe 2O 3:红棕色固体不溶于水,俗称铁红、铁锈,可做红色染料 Fe 3O 4:黑色固体不溶于水,俗称磁性氧化铁3、 氢氧化物Fe(OH)2 白色沉淀迅速变成灰绿色,最后变成红褐色 4Fe(OH)2+O 2+2H 2O=4Fe(OH)3Fe(OH)3:红褐色沉淀 具有不稳定性,受热易分解2FeOH 3Fe 2O 3+3H 2O4、Fe 2+ Fe 3+的盐 (1)Fe 2+的性质 ①颜色:浅绿色△高温点燃△△△过量HClHCl 过量NaOH H +H +OH - OH -②易水解:Fe2++2H2O2+2H+如何保存FeSO4溶液:加几滴稀硫酸或加铁粉③强还原性:与O2Cl2Br2HNO3浓H2SO4KMnO4酸性溶液反应Fe2+检验:①加碱法(NaOH或氨水)②先加KSCN溶液,无现象再加氨水会出现血红色(2)Fe3+的性质①颜色:棕黄色②易水解:Fe3++3H2O3+3H+Fe3++3HCO3-=Fe(OH)3↓+3CO2↑(与CO32-AlO2-也双水解) ③强氧化性:氧化S2-I-SO2SO32-Cu Fe2Fe3++2S2-=2Fe2++2S↓2Fe3++2I-=2Fe2++I2 (Fe3+能使湿润的淀粉KI试纸变蓝)2Fe3++Cu=2Fe2++Cu2+④络合性:KSCN溶液--血红色Fe3++3SCN-=Fe(SCN)3↓⑤制Fe(OH)3胶体:FeCl3+3H2O=Fe(OH)3胶体+3HCl⑥与苯酚显紫色⑧Fe3+检验:溶液加碱法加苯酚法。
高三化学镁和铝知识精讲一. 本周教学内容:镁和铝二. 重点、难点:1. 了解镁和铝的原子结构、物理性质的比较。
2. 了解铝的物理性质以及用途和两性。
3. 掌握镁和铝的化学性质。
4. 了解铝的几种重要化合物。
5. 理解与铝及其化合物两性有关的计算和图像分析。
6. 初步了解合金及其特点。
三. 具体内容:(一)Mg、Al的位置和结构镁、铝元素在元素周期表中的位置、原子结构、元素金属性的评价Mg:在元素周期表中的第三周期、ⅡA族,原子结构示意图为Al:在元素周期表中的第三周期、ⅢA 族,原子结构示意图为根据镁、铝在元素周期表中的位置、原子结构特点和元素周期律进行分析可知,镁铝两种元素都是金属性较强的金属元素,镁比铝金属性略强。
镁、铝在金属活动顺序中的位置,单质活泼性的评价Mg、Al在金属活动顺序中的位置是:……Na Mg Al Zn Fe Sn Pb (H)……根据镁、铝在金属活动顺序中的位置和金属活动顺序的意义进行分析可知,镁、铝都是比较活泼的金属,镁比铝金属活泼性略强。
(二)镁和铝的物理性质与用途1. 镁和铝的物理性质镁、铝具有金属共有的物理性质,也有一些不同于其他金属的物理性质,对其列表说明如下:元素名称元素符号单质的物理性质颜色和状态硬度密度/g·cm-3熔点/℃沸点/℃镁Mg 银白色固体很软 1.738 645 1090铝Al 银白色固体较软 2.70 660.4 2467小结:①由表可知,镁和铝都是密度较小、熔点较低、硬度较小的银白色金属,但镁和铝比较,铝比镁的硬度稍大,熔点和沸点都是铝比镁的高。
②在元素周期表中,同一主族的金属从上到下熔点降低,硬度减小;同一周期的主族金属从左到右熔点升高,硬度增大。
2. 镁和铝的重要用途铝由其优良的物理性质所决定的重要用途,主要有:(1)延展性——铝线、铝箔、多种容器(2)导电性——做电的导体。
铝的导电性仅次于铜,是优良的导体之一。
(3)导热性——做热的导体。



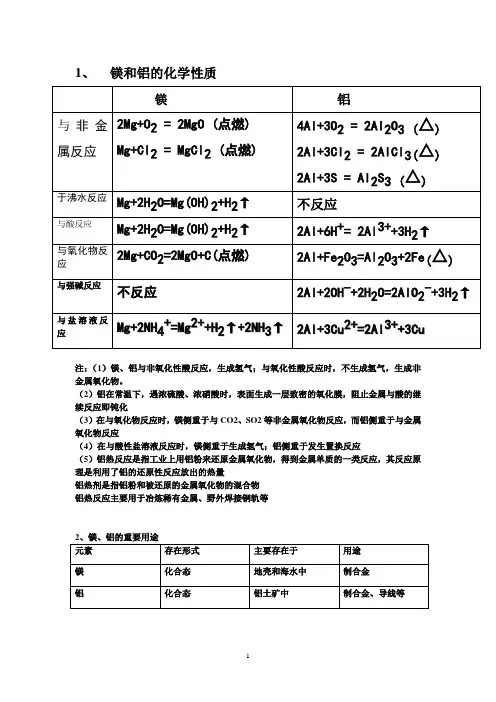
1、镁和铝的化学性质注:(1)镁、铝与非氧化性酸反应,生成氢气;与氧化性酸反应时,不生成氢气,生成非金属氧化物。
(2)铝在常温下,遇浓硫酸、浓硝酸时,表面生成一层致密的氧化膜,阻止金属与酸的继续反应即钝化(3)在与氧化物反应时,镁侧重于与CO2、SO2等非金属氧化物反应,而铝侧重于与金属氧化物反应(4)在与酸性盐溶液反应时,镁侧重于生成氢气;铝侧重于发生置换反应(5)铝热反应是指工业上用铝粉来还原金属氧化物,得到金属单质的一类反应,其反应原理是利用了铝的还原性反应放出的热量铝热剂是指铝粉和被还原的金属氧化物的混合物铝热反应主要用于冶炼稀有金属、野外焊接钢轨等4、氢氧化镁和氢氧化铝(1)Mg(OH)2是一种难溶于水的中强碱,能使酚酞溶液变为浅红色①跟酸反应M g(O H)2+2H ++=M g22+++2H2O②热稳定性差M g(O H)2=M g O+H2O(△)③可溶于铵盐溶液中M g(O H)2+2N H4++=M g22+++2N H3↑+2H2O(2)AI(OH)3是一种难溶的白色胶状物质,不能使酚酞变色,它是典型的两性氢氧化物A I(O H)3+3H+=A I3++3H2OA I(O H)3+O H-=A I O2-+2H2O总:Al3++3OH- Al(OH)3 H++AlO2-+H2O练习:1、为除去镀在铝表面的铜镀层,可选用的试剂是()。
A 稀硝酸B 浓硝酸C 浓硫酸D 浓盐酸2、用铝盐制取氢氧化铝最好加___________,离子反应方程式为_______________________用偏铝酸盐制氢氧化铝最好通入___________,离子反应方程式为____________________________。
3、将氯化铝和氢氧化钠溶液等体积混合,得到的沉淀物中铝元素的质量与溶液中所含铝元素的质量相等,则氯化铝和氢氧化钠溶液的物质的量浓度之比可能为()A 1:3B 2:3C 1:4D 2:74、用稀硫酸、氢氧化钠溶液和铝为原料制取氢氧化铝,甲、乙、丙三个学生制备途径分别是:甲:Al→Al2(SO4)3→Al(OH)3乙:Al →NaAlO2→ Al(OH)3丙:Al→Al2(SO4)3Al →NaAlO2 A l(O H)3若要得到等质量的Al(OH)3,则 ( )A 三者消耗的原料相等B 甲消耗的原料最多C 乙消耗的原料最少D 丙消耗的原料最少答案:1: B2:氨水或偏铝酸盐,Al3++3NH3 H2O =Al(OH)3↓+3NH4+ CO2或铝盐,2AlO2-+CO2+2H2O=2Al(OH)3↓+CO32-3:B、D4:B、D5、明矾①化学式:KAl(SO4)2 12H2O②电离方程式KAl(SO4)2=K++Al3++2SO42-③属类:复盐(两种不同的金属离子和一种酸根离子组成的化合物)④净水原理Al3++3H2O Al(OH)3+3H+胶体吸附杂质—净水⑤化学性质兼有Al3+和SO42-的性质向明矾溶液中滴入Ba(OH)2溶液,当Al3+恰好完全沉淀时,此时沉淀的物质的量最大;向明矾溶液中滴入Ba(OH)2溶液,当SO42-完全沉淀时,此时沉淀的质量最大2Al3++3SO42-+3Ba2++6OH- = 2Al(OH)3↓ +3BaSO4↓2Al3++4SO42-+4Ba2++8OH- = 2AlO2- ↓ +4BaSO4↓+2H2O 练习:把Ba(OH)2溶液滴入明矾溶液中,使SO42-全部转化成BaSO4沉淀,此时铝元素的主要存在形式是( C )A、Al3+B、Al(OH)3C、AlO2-D、Al3+和Al(OH)36、几个基本图象1)向铝盐中加入强碱离子反应方程式 :Al 3++3OH -=Al(OH)3↓Al(OH)3+OH - = AlO 2-+2H 2O总离子反应方程式: Al 3++4OH - = AlO 2-+ 2H 2O(2)向强碱中滴入铝盐离子反应方程式 Al 3++4OH -=AlO 2-+2H 2Al 3++ 3AlO 2- +6H 2总离子反应方程式Al 3++3OH - = Al(OH)3↓(3)向偏铝酸盐中滴入强酸离子反应方程式AlO2-+H++H2O=Al(OH)3↓Al(OH)3+3H+ = Al3++3H2O总离子反应方程式AlO2-+4H+ = Al3++2H2(4)向盐酸中滴入偏铝酸盐离子反应方程式AlO2-+4H+ = Al3++2H2O3AlO2-+Al3++6H2O=4Al(OH)3↓总离子反应方程式AlO2-+H++H2O = Al(OH)3↓1 3以生成沉淀的物质的量为纵坐标,以加入的物质的物质的量为横坐标画出下列反应的图象:①向氯化铝溶液中逐渐滴加氨水至过量②向偏铝酸钠溶液中通入二氧化碳至过量③向氯化镁、氯化铝和盐酸的混合溶液中逐滴加入氢氧化钠溶液至过量④向明矾溶液中滴加氢氧化钡溶液至过量⑤向氯化镁、氯化铝混合溶液中先加氢氧化钠溶液,后加盐酸(氢氧化钠和盐酸等体积)(阿妹:d图自己画下拉差唔多成点钟家姐眼训了~~整得满意吗?我尽力了哦你要加油哦o(∩_∩)o…)。

高二化学第二册第四章镁和铝知识点
1.镁知识点
(1)物理性质:镁,化学符号Mg,相对原子质量为24,银白色金属;熔点
648.8deg;C,沸点1107deg;C,密度1.74克/厘米
sup3;.
(2)化学性质:能与卤族元素反应,例
如:Mg+Cl2---(点燃)MgCl2
能与氧气反应:Mg+O2MgO
能与稀酸反映:H2SO4+Mg==MgSO4+H2(气体)
能与沸水反映:Mg+2H2O==Mg(OH)2+H2(气体)
注:镁位于第三周期第二主族,所以你可以找和他相邻的元素,他们的结构性质都相似
2生物方面:是生物生活的必须元素,不能缺.在植物体内,以离子态存在.新叶含的镁比老叶多.
2.铝的知识点
Al(OH)3是一种两性氢氧化物,三元弱碱.也可以看作是HAlO2+H2O,这样,它也可以看成是一元弱酸.
Al(OH)3只能和强酸强碱反应,与弱酸弱碱(如
CO2+H20,NH3.H2O)都不反应
关于Al+ 和AlO-的问题也比较简单,把Al(OH)3看成是对应的酸碱就行了
第四章镁和铝知识点的全部内容就是这些,更多精彩内容请持续关注。

镁铝合金反应
镁铝合金是一种经过特殊处理的复合材料,它由镁和铝制成,能够发生反应。
因为镁与铝本身在空气中有腐蚀性,所以当它们结合起来时,其腐蚀性更加剧烈。
镁铝合金反应可以通过化学反应或合金化学反应实现。
通常情况下,当镁与铝发生反应时,他们会形成一种新的合金,称为双金属硅酸盐。
这种双金属硅酸盐很容易溶解,可以获得鞣剂或增韧剂,这些物质能够扩展或强化金属材料的性能。
镁铝合金反应还可以用来制备各种金属材料,比如铝合金、磷酸铝和氧化铝等。
在镁铝合金反应中,电解质起着重要作用,可以加速镁和铝的反应,使产物更快更好地分解。
另外,镁铝合金的反应十分有趣,因为它们可以发生化学反应。
例如,在氯气存在下,当镁与铝发生反应时,会产生氯化镁和氯化铝,从而产生酸式的氢氧化物。
这种化学反应还可以用来生产热力学反应,以便获得更多的能量。
总之,镁铝合金反应是一种十分有趣的反应,可用来获取各种不同的物质,比如鞣剂、增韧剂、氧化物等。
此外,它还能够发生化学反应,从而获得热力学反应,获得更多的能量。
因此,镁铝合金的反应具有重要的意义,能够为许多应用领域提供积极的贡献。
- 1 -。

有关镁铝的化学方程式镁和铝是两种常见的金属元素,它们在化学反应中可以生成各种化合物。
以下是一些常见的镁铝化学方程式:1.镁与稀硫酸反应:Mg + H2SO4 → MgSO4 + H2↑这个反应是金属与酸反应的典型例子。
镁与稀硫酸反应生成硫酸镁和氢气。
这是一个放热反应,可以观察到反应物迅速产生气泡并放出热量。
2.铝与稀盐酸反应:2Al + 6HCl → 2AlCl3 + 3H2↑铝与稀盐酸反应生成氯化铝和氢气。
这个反应也是一个放热反应,可以观察到反应物迅速产生气泡并放出热量。
3.镁与氧气反应:2Mg + O2 → 2MgO镁与氧气在点燃条件下反应生成氧化镁。
这是一个重要的金属氧化反应,可以观察到镁在氧气中燃烧发出耀眼的白光。
4.铝与氧气反应:4Al + 3O2 → 2Al2O3铝与氧气在点燃条件下反应生成氧化铝。
这个反应也是金属氧化反应之一,可以观察到铝在氧气中燃烧发出明亮的白光。
5.镁与水反应:Mg + 2H2O → Mg(OH)2 + H2↑镁与水在加热条件下反应生成氢氧化镁和氢气。
这个反应可以用于制备氢氧化镁和氢气。
6.铝与氢氧化钠反应:2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2↑铝与氢氧化钠反应生成偏铝酸钠和氢气。
这个反应可以用于制备氢气和偏铝酸钠。
以上这些化学方程式涵盖了镁和铝的一些重要化学反应。
这些反应不仅存在于化学实验室中,也在工业生产和日常生活中有广泛应用。
例如,镁铝的合金被广泛应用于航空航天、汽车和建筑等领域,因为它们具有高强度、轻质和防腐蚀等优点。
此外,镁和铝的化合物也被广泛应用于医药、陶瓷和玻璃等领域。
在实际操作中,需要注意的是化学反应的条件和注意事项,以确保实验安全和得到正确的产物。
例如,在进行金属与酸的反应时,需要使用适当的酸、控制反应温度和时间,并注意防止金属与酸产生大量热量导致温度升高和可能的安全问题。
同时,在操作过程中要注意个人安全防护措施,如戴手套、防护眼镜等,以防止可能的化学伤害。


镁和铝的性质二. 重点、难点1. 镁和铝的原子结构比较。
2. 镁和铝的单质物理性质比较(色、态、熔沸点、硬度、密度、延展性等)。
3. 合金及其特点(定义、熔点等),镁、铝的重要用途。
4. 镁、铝的化学性质(与氧气、硫、卤素的反应,与非氧化性酸、某些氧化物的反应,铝的钝化,铝与碱反应),铝热反应的有关知识,铝的两性。
三.知识分析:(一)金属的物理性质有金属光泽、不透明、有导电性、导热性有延展性、多数具有较高熔点、较大硬度金属可以根据其颜色、密度、存在形式可把金属分为以下几类:从颜色分:黑色金属(Fe、Cr、Mn)有色金属(除以上金属外)从密度分:轻金属(d <4.5g/cm-3)重金属(d > 4.5g/cm-3)从存在分:常见金属(Fe、Al、Cu)稀有金属以上同学们对金属应有一定的认识,下面我们通过学习镁和铝的性质来深入了解金属的性质及用途。
(二)合金1. 定义——由两种或两种以上的金属(或金属与非金属)熔合在一起形成的具有金属特性的物质,合金属于混合物。
2. 合金的性质特点一般说来,合金的熔点比其成分金属都低,而在硬度、韧性等方面却往往有其成分金属所不具有的独特的性质。
3. 镁、铝的合金简介(三)镁和铝1. 原子结构(1)原子结构示意图(2)电子式2. 物理性质(1)共同点:均为银白色,属于轻金属,熔点较低,硬度较小、有良好的导电性、导热性。
(2)不同点:密度:铝>镁熔点、硬度:铝>镁思考:a. 镁和铝分别位于元素周期表的第几周期,第几族?b. 分别画出镁和铝的原子结构示意图,它们的原子结构有哪些特点?c. 为什么镁的化学性质比铝活泼?举出几个能说明镁的化学性质比铝活泼的实验事实。
3. 化学性质:(1)与非金属反应: a. 镁条在空气中的燃烧2Mg + O 2 = 2MgO 3Mg + N 2 = Mg 3N 2 b. 铝在氧气中的燃烧4Al + 3O 2 = 2 Al 2O 3 (2)与酸的反应: a. 与非氧化性酸反应: Mg + 2H + = Mg 2+ + H 2↑ 2Al + 6H + = 2Al 3+ + 3H 2↑b. 与氧化性酸反应:镁与浓硫酸、浓硝酸的反应: Mg + 2 H 2SO 4(浓)= MgSO 4 + SO 2 ↑+ 2H 2O Mg + 4HNO 3(浓)= 23)Mg(NO +2NO 2↑ + 2H 2O 铝与浓硫酸、浓硝酸发生钝化 (3)镁与水的反浓应:Mg +2 H 2O (沸水)=↑+↓22H Mg(OH)(4)铝与碱的反应:2Al + 2NaOH + 6H 2O = 2NaAlO 2 +3H 2↑+ 4H 2O 还原剂:Al 氧化剂: H 2O(5)镁、铝与某些氧化物的反应:镁条在二氧化碳里燃烧:2 Mg + CO 2 = 2MgO + C 铝热反应:2Al + Fe 2O 3 = Al 2O 3 +2Fe铝热剂:铝粉和某些金属氧化物组成的混合物运用:焊接钢轨;可以用于冶炼工业,冶炼难熔金属。
第50节镁和铝的性质镁和铝都是第三周期的金属元素。
镁、铝原子的价电子数都比较少,因此都有较强的金属性。
但由于结构不同,性质上又有一定的区别。
一、物理性质表10-1镁和铝的原子和单质的一些性质从上表可以知道,镁和铝都是密度较小、熔点较低、硬度较小的银白色金属。
但镁和铝相比铝的硬度、熔点、沸点都比镁高。
其原因是镁和铝的金属键的强弱不同,铝原子的价电子数比镁原子的多,核电荷数也比镁的大,但它的原子半径却比镁原子小,所以在铝的晶体中金属键较强,因此铝的硬度、熔点和沸点都比镁的高。
铝的导电性很好,可以代替铜作导线和电缆。
铝的延展性很大,能抽成丝,也能压成铝箔。
铝可以与许多元素形成合金,其主要用途也是制造各种轻合金。
合金是指两种或两种以上的金属(或金属与非金属)熔合而成的具有金属特性的物质。
由于组成不同,合金的性质有特殊性。
主要表现如下:1.合金的延展性、导电性和导热性,一般比组成它的成分的金属低。
2.大多数合金的熔点比组成合金中任何一种金属的熔点低。
例如,铝硅合金(含Si13.5%)的熔点为564℃,比纯铝或纯硅的熔点都低,而且它在凝固时收缩率又很小,很适合铸造。
3.大多数合金的硬度比组成它的金属的硬度要大。
例如,硬铝(含Cu4%,Mg0.5%,Mn0.5%,Si0.7%)的强度和硬度都比纯铝大,几乎相当于钢材,而密度又小。
例如,镁与铝、铜、锡等元素形成的合金,密度只有1.8g/cm3左右,但硬度和强度都较大。
因此,镁合金也是汽车、飞机制造业的重要原料。
二、化学性质镁和铝都是比较活泼的金属,能与非金属、酸等物质起反应,铝还能与强碱溶液反应。
1.与非金属的反应先用砂纸除去铝片表面的氧化膜,再插入Hg(NO3)2溶液中浸泡几秒钟,取出铝片,用滤纸吸干后,放在一干燥的滤纸上,静置,观察铝片表面发生的变化。
在常温下,铝与空气中氧气反应,生成一层致密的氧化物薄膜,从而阻止了金属的继续氧化。
①把铝箔的一端固定在粗铁丝上,另一端系上一根火柴。
镁和铝其化合物性质知识点归纳一Mg的化学性质1.与非金属反应(1)与O2反应。
常温下与空气中的O2反应生成一层致密的氧化物薄膜,所以镁、铝都有抗腐蚀的性能。
镁、铝都能在空气中燃烧:2Mg+O22MgO。
4Al+ 3O 22Al2O3(2)与卤素单质、硫等反应。
Mg+ Cl 2MgCl2 2Al+ 3Cl22AlCl32Al+ 3S Al2S3 (用于工业制备)Mg+ S MgS[特别提醒]:①镁在空气中用酒精灯火焰点燃即可燃烧,而铝在空气中需要高温点燃才能燃烧。
镁在空气中燃烧时有三个反应发生:2Mg+O22MgO 3Mg+N2Mg3N22Mg+CO22MgO+C②燃烧时都放出大量的热,发出耀眼的白光。
利用镁的这种性质来制造照明弹。
③集气瓶底部都要放一些细纱,以防止集气瓶炸裂。
2.与H2O反应Mg、A1和冷水都不反应,但在加热条件下与水反应生成氢氧化物和氢气Mg+2H2O Mg(OH)2+H2↑2A1+6H2O2A1(OH)3+3H2↑3.与酸反应置换出H2Mg、A1与浓、稀盐酸、稀硫酸、磷酸等酸反应置换出H2,其中铝在冷浓H2SO4,冷浓硝酸中发生钝化现象。
所以可用铝制容器贮存冷的浓硫酸或浓硝酸。
4.与某些氧化物反应(1)镁与二氧化碳反应:2Mg+CO22MgO+C[特别提醒]:“CO2不能助燃”的说法是不全面的,CO2对绝大多数可燃物是良好的灭火剂,而对K、Ca、Na、Mg等可燃物却是助燃剂。
(2)铝热反应:2Al+ Fe2O32Fe+ Al2O3铝热反应可用于焊接钢轨和冶炼某些难熔金属,如:V、Cr、等。
[特别提醒]:①铝热剂是指铝粉和某些金属氧化物的混合物,金属氧化物可以是:Fe2O3、FeO、Fe3O4、Cr2O3、V2O5、MnO2等。
②铝热反应的特点是反应放出大量的热,使生成的金属呈液态。
③要使用没有氧化的铝粉,氧化铁粉末要烘干。
④KClO3作为引燃剂,也可以用Na2O2代替。
实验时可以不用镁条点燃,而用在氯酸钾和白糖的混合物上滴加浓硫酸的方法来点燃。
相同质量镁和铝所含原子个数比镁和铝是常见的金属元素,它们在我们的日常生活中有着广泛的应用。
然而,这两种金属元素的性质并不完全相同,其中一个重要的区别是每个元素的原子个数。
那么,相同质量的镁和铝到底含有多少个原子呢?首先,我们来了解一下镁和铝的基本情况。
镁的原子序数为12,其原子量为24.3050吨/摩尔;铝的原子序数为13,其原子量为26.9815吨/摩尔。
可以看出,每个镁原子的质量为24.3050/6.02214076×10^23 = 4.0369×10^-23吨,每个铝原子的质量为26.9815/6.02214076×10^23 = 4.4804×10^-23吨。
假设我们有相同质量的镁和铝。
由于镁的原子质量较轻,相同质量的镁所含的原子个数将多于铝。
具体来说,假设我们有X克的镁和X克的铝,两者原子个数的比值可以通过以下计算得到:镁的原子个数 = X / (4.0369×10^-23)铝的原子个数 = X / (4.4804×10^-23)由此可得,镁和铝所含原子个数的比值为:(X / (4.0369×10^-23)) / (X / (4.4804×10^-23)) = (4.4804×10^-23) / (4.0369×10^-23) ≈ 1.1097即相同质量的镁和铝所含原子个数的比值约为1.1097。
这意味着,相同质量的镁比铝所含的原子个数多约10.97%。
这个结果对于我们理解金属元素的性质和应用具有一定的重要性。
镁和铝在实际应用中有着诸多不同的特点。
例如,镁具有较低的密度和较好的导电性能,因此常用于制造轻量化的结构材料和电子产品。
而铝则具有较高的强度和良好的耐腐蚀性,常用于制造航空器、汽车和建筑材料等。
通过了解镁和铝所含原子个数的比值,我们可以更好地理解它们的物理性质,并合理选择适用于不同场合的金属材料。
镁和铝的性质一、单质镁和铝金属项目镁(Mg)铝(Al)原子结构化合价+2 +3 晶体结构金属晶体金属晶体单质物理性质镁和铝都是密度较小、熔点较低、硬度较小的银白色金属,但镁和铝相比较,铝的硬度比镁的稍大,熔点和沸点都是铝比镁的高抗腐蚀性在空气中都能跟氧气反应,表面覆盖一层致密而坚硬的氧化物薄膜,都具有搞腐蚀性能与O2反应与酸反应与碱反应与水反应与氧化物反应结论镁、铝均为较活泼的金属,但镁的金属性强于铝解释核电荷数镁小于铝,而原子半径镁大于铝,故核对最外层的电子引力镁小于铝,即Al比Mg难失电子,金属性弱于Mg主要用途镁合金汽车、飞机制造、照明弹等铝合金汽车、船舶、飞机制造、防锈油漆、导线、电缆等注:镁在空气中点燃共发生三个反应:二、MgO与Al2O3的比较MgO Al2O3物理性质均为白色粉末,不溶于水,熔点高(MgO>Al2O3),是优良的耐火材料化学性质与热水反应与水不反应碱性氧化物两性氧化物三、Mg(OH)2与Al(OH)3的比较Mg(OH)2Al(OH)3物理性质均为白色固体,不溶于水化学性质不稳定性不稳定性碱性两性制备Mg2++2OH-= Mg(OH)2↓Mg2++2NH3·H2O =Mg(OH)2↓+2NH4+Al3++3NH3·H2O=Al(OH)3↓+3NH4+不用强碱AlO2-+CO2+2H2O= Al(OH)3↓+HCO3-不用强酸1.镁及其化合物转化关系2.铝及其化合物转化关系3、铝三角4、试剂的滴加顺序不同产生的现象不同(1)NaOH和AlCl3向AlCl3溶液中滴加NaOH溶液,先出现白色沉淀后消失:Al3++3OH-=Al(OH)3↓Al(OH)3+OH-=AlO2-+2H2O向NaOH溶液中滴加AlCl3溶液,开始无现象后出现白色沉淀:(2)NaAlO2和盐酸向NaAlO2溶液中滴加盐酸,先出现白色沉淀后消失:向盐酸中滴加NaAlO2溶液,开始无现象后出现白色沉淀:(3)Na2CO3和盐酸向Na2CO3溶液中滴加盐酸,开始无现象,后产生气泡向盐酸中滴加Na2CO3溶液,立即产生气泡。
镁铝合金反应镁铝合金是一种常见的金属合金,主要由镁(Mg)和铝(Al)两种金属元素构成。
它具有良好的耐腐蚀性和力学性能,被广泛用于飞机,建筑胶等工业中。
同时,它也是一种重要的化学物质,可以用于工业制造和实验室研究。
镁铝合金的反应温度很高,通常不低于1200°C。
在高温下,镁和铝的原子可以发生反应,产生金属间化合物,如MgAl2O4等。
此外,高温下还可以发生其他的反应,如金属氧化反应和金属降解反应。
在将镁和铝的原子混合溶液中,可以观察到金属氧化反应,铝原子会发生氧化还原反应,即铝(Al)损失电子,形成Al3+而镁(Mg)会增加电子,形成Mg2+ 。
此外,在高温下,金属降解反应也可以发生,即Mg和Al的原子可以相互取代,如Mg+Al→MgAl3。
除了高温的反应,低温下的镁铝合金也具有一定的化学性质。
例如,当镁铝合金中添加水以及氯离子,可以产生一种氧化物,称为Mg(Cl)2。
它是一种白色粉末,具有较高的热稳定性,可以用于制作火灾报警器等电子设备,也可以用于实验室中的化学研究。
镁铝合金反应是研究金属合金的重要一环,它有着独特的化学效应,可以为金属材料的开发和利用提供借鉴。
通过研究镁铝合金的反应温度,制备不同的金属氧化物,可以为金属材料的多种应用提供新的材料。
同样,对镁铝合金中的氧化反应以及金属降解反应进行研究,也可以使用更多可行的方法改善金属的耐腐蚀性和力学性能。
综上所述,镁铝合金反应是一种重要的金属化学反应。
不仅可以为工业和实验室研究制备各种金属氧化物,还可以为金属材料的多种应用提供新方法。
因此,镁铝合金反应得到了广泛的应用,为研究金属材料的性能提供了重要的研究依据。