不合格药品报告单
- 格式:doc
- 大小:28.50 KB
- 文档页数:1

本文部分内容来自网络整理,本司不为其真实性负责,如有异议或侵权请及时联系,本司将立即删除!== 本文为word格式,下载后可方便编辑和修改! ==药品不合格报告单201X篇一:不合格药品报告单不合格药品报告表篇二:03不合格药品报告单不合格药品通知单篇三:201X新版GSP整改报告篇一:201X年新版gsp整改报告唐山xxxxxxxxxxxxxxxxxxgsp认证现场检查缺陷项目整改报告唐山市食品药品监督管理局:我药房于201X年12月向我市食品药品监督管理局提交药品gsp认证申请资料,经审核,唐山市食品药品监督管理局于201X年3月20日派检查组对本药店进行了现场检查.通过这次认证现场检查,检查组对本企业经营管理上存在的不足,给予指出,并予以指导、建议和提出整改意见,对本店树立良好的社会形象起到了促进作用,本店将按照gsp管理的要求,针对gsp认证小组现场检查发现的问题,做出认真、详细,着实有效的整改。
整改落实到各责任人,专人专项进行纠正,对存在的缺陷问题已逐步整改完毕,如还有不足之处恳请专家组予以指正。
今后我企业将继续按gsp的要求,搞好企业的规范化管理,把实施gsp工作做得更好!现将检查的缺陷项目情况和整改落实的情况汇报如下:二、缺陷项目的整改篇二:201X年新版gsp整改报告景宁**平价大药房文件丽景*药字(201X)第3号药品gsp认证现场检查缺陷项目整改报告**县食品药品监督管理局:****平价大药房于201X年*月*日向**县食品药品监督管理局提交药品gsp认证申请资料,经审核,**县食品药品监督管理局于201X年*月*日派检查组对本药店进行了现场检查,现场检查发现严重缺陷0项,主要缺陷4项,一般缺陷7项,现将检查的缺陷项目情况和整改落实的情况汇报如下:一、缺陷项目的情况:二、缺陷整改措施:******大药房201X年5月26日篇三:201X药品零售企业gsp认证方案201X药品零售企业gsp认证方案一、职责分工行政法规科(纪检监察室)负责认证资料的受理、打证发证和认证过程中的纪检监督。

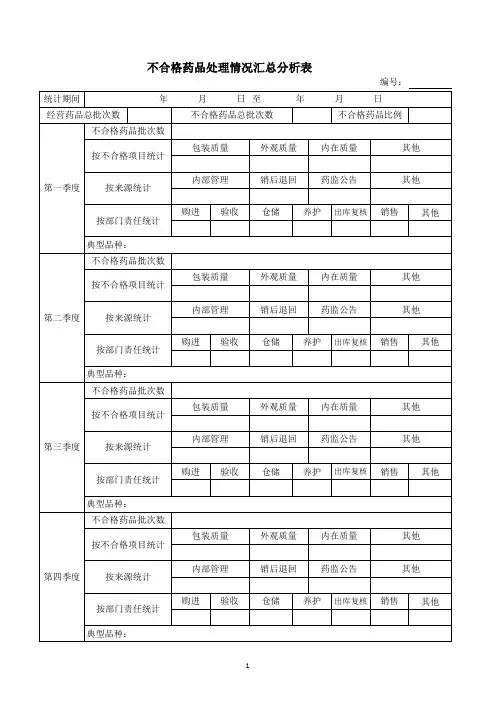
不合格药品汇总分析报告1. 引言本报告旨在对不合格药品进行总结和分析,以便了解不合格药品的种类、原因和应对措施,从而提高药品质量和保障公众健康。
2. 背景近年来,不合格药品问题引起了广泛关注。
不合格药品的存在对人们的健康和生命安全构成威胁,因此有必要对这些问题进行深入研究和分析。
3. 数据收集我们收集了大量有关不合格药品的数据,并按照药品类型、生产地区和不合格原因进行了分类整理。
3.1 药品类型根据药品类型的不同,我们将不合格药品分为以下几类: - 化学药品 - 中药材 - 生物制品 - 药用辅料3.2 生产地区我们对不同地区生产的不合格药品进行了统计,并发现以下地区存在较多不合格药品: - 北京市 - 上海市 - 广东省3.3 不合格原因我们对不合格药品的原因进行了细致的分析,并得出以下结论: - 药品生产过程中存在质量控制不严格的问题,导致不合格药品的产生。
- 生产企业可能存在生产设备老化、操作不规范等问题,需要加强管理和技术培训。
- 部分药品生产企业可能存在追求利益最大化的心态,不合格药品流入市场。
4. 分析结果与讨论根据我们的数据分析,可以得出以下结论:4.1 不合格药品种类分布根据我们的数据统计,化学药品是不合格药品中占比最大的类型,其次是中药材和生物制品。
4.2 地区分布北京市、上海市和广东省是不合格药品的集中地区。
这些地区的药品生产企业应加强质量管理,提高药品生产的合规性。
4.3 不合格原因分析从不合格原因来看,药品生产过程中质量控制不严格是主要原因之一。
生产企业应加强质量控制,确保药品符合国家标准。
5. 总结与建议根据以上的分析结果,我们得出以下总结和建议:•药品生产企业应加强质量管理,提高药品生产过程的合规性和质量控制水平。
•相关监管部门应加强对药品生产企业的监督和检查力度,确保药品质量符合国家标准。
•消费者在购买药品时应选择有信誉和合法资质的销售渠道,避免购买不合格药品。
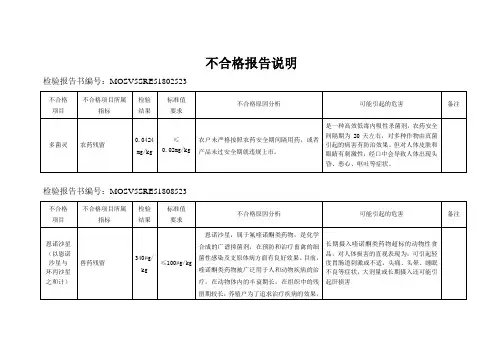

不合格药品分析报告背景介绍药品作为保护人们健康和治疗疾病的重要物品,在市场上的质量和安全问题备受关注。
不合格药品的存在对公众健康造成了极大的威胁。
为了保障人们的健康和权益,我们进行了一项不合格药品的分析研究。
研究目的本研究旨在分析不合格药品的原因和对人体健康的潜在危害,以提供给药品监管部门和公众相关信息,促进合格药品的生产和使用。
研究方法我们采取了以下步骤来进行不合格药品的分析:1. 数据收集我们收集了国内外相关的药品质量监测数据和相关文献,以获取足够的样本进行分析。
2. 样品筛选根据采集到的数据,我们对不合格药品进行筛选和分类,确保研究的准确性和可靠性。
3. 实验分析我们对不合格药品进行了实验室分析,包括成分分析、质量测定、微生物检测等,以了解其不合格的原因和潜在危害。
研究结果经过实验和分析,我们得出了以下结论:1. 药品成分不足或过量部分不合格药品的主要问题是成分不足或过量。
这可能是由于生产过程中的操作失误或质量控制不严格所致。
这些药品可能无法达到预期的疗效,甚至对人体健康产生不可预知的风险。
2. 药品污染一些不合格药品存在微生物污染或其他污染物,如重金属、农药残留等。
这些污染物可能会对人体造成严重的健康问题,包括过敏反应、中毒等。
3. 伪劣产品少数不合格药品可能是伪劣产品,也就是仿冒的药品,其成分与标签上标注的不符。
这些伪劣产品的使用可能导致治疗失败或产生其他不良反应。
结论与建议不合格药品对人体健康和公众利益造成了严重威胁。
为了保障人们的权益和健康,我们提出以下建议:1. 加强药品监管药品监管部门应加强对药品生产和销售环节的监管力度,确保药品质量和安全。
2. 提高生产质量控制药品生产企业应加强质量控制,确保药品成分和质量符合标准,避免不合格药品的产生。
3. 加强消费者教育公众应加强对药品质量和安全的认知,提高警惕性,避免购买和使用不合格药品。
结语本研究通过实验和分析,揭示了不合格药品存在的问题和潜在危害。

本文部分内容来自网络整理,本司不为其真实性负责,如有异议或侵权请及时联系,本司将立即删除!== 本文为word格式,下载后可方便编辑和修改! ==药品不合格项报告篇一:关于GSP认证现场检查不合格项目的整改报告XXXX关于GSP认证现场检查不合格项目的整改报告XX食品药品监督管理局:按照XX食品药品监督管理局药品评审认证中心的安排,GSP认证现场检查组于XXXX年XX月XX日至XX日对我公司的药品经营质量管理情况进行了现场检查。
经过检查,认为我公司的药品经营质量管理工作基本符合GSP的要求,但存在2个一般缺陷项目。
一、不合格项目情况1903 企业个别仓库有自来水设施(北一楼仓库有水槽)2102 企业外用药仓库无通风设施(缺换气扇)检查组要求限期整改,并将整改结果报省认证中心。
二、整改情况公司董事长XXX立即召开了质量管理领导小组会议,认真研究和分析检查中发现的问题及发生问题的原因,针对存在问题制订了整改措施,由质管科监督落实。
现将我公司的整改情况报告如下:1903 企业个别仓库有自来水设施(北一楼仓库有水槽)问题分析:由于我们对仓库与生活区有效隔离的理解存在误区,特别是没有考虑到仓库设置上下水的潜在危险。
只图仓库清洁和加湿器用水方便,在库内安装了水槽。
虽然与药品货垛的距离在六米以上,但无法避免一旦下水道堵塞,溢水污染药品储存环境而可能造成的危害。
整改措施:立即拆掉自来水水嘴,封闭管道。
整改责任人:XXX整改时间:XX月XX日整改结果:已经完成(见照片)2102 企业外用药仓库无通风设施(缺换气扇)问题分析:由于我公司现存药品数量很少,所有外用药都放在一间仓库里。
养护人员和公司管理人员对于另一间备用仓库都没有进行认真检查,因而出现了此问题。
整改措施:安装换气扇。
整改责任人:XXX整改时间:XX月XX日整改结果:已经完成(见照片)在进行整改的同时,我们还对相关责任人给予批评教育,要求相关的部门和部门负责人加强对所属人员的指导、帮助、督促和检查,使GSP的相关规定和公司质量管理制度得到不折不扣的执行,避免今后再出现此类认识不到位,管理不到位的问题。


本文部分内容来自网络整理,本司不为其真实性负责,如有异议或侵权请及时联系,本司将立即删除!== 本文为word格式,下载后可方便编辑和修改! ==药品不合格项报告篇一:关于GSP认证现场检查不合格项目的整改报告XXXX关于GSP认证现场检查不合格项目的整改报告XX食品药品监督管理局:按照XX食品药品监督管理局药品评审认证中心的安排,GSP认证现场检查组于XXXX年XX月XX日至XX日对我公司的药品经营质量管理情况进行了现场检查。
经过检查,认为我公司的药品经营质量管理工作基本符合GSP的要求,但存在2个一般缺陷项目。
一、不合格项目情况1903 企业个别仓库有自来水设施(北一楼仓库有水槽)2102 企业外用药仓库无通风设施(缺换气扇)检查组要求限期整改,并将整改结果报省认证中心。
二、整改情况公司董事长XXX立即召开了质量管理领导小组会议,认真研究和分析检查中发现的问题及发生问题的原因,针对存在问题制订了整改措施,由质管科监督落实。
现将我公司的整改情况报告如下:1903 企业个别仓库有自来水设施(北一楼仓库有水槽)问题分析:由于我们对仓库与生活区有效隔离的理解存在误区,特别是没有考虑到仓库设置上下水的潜在危险。
只图仓库清洁和加湿器用水方便,在库内安装了水槽。
虽然与药品货垛的距离在六米以上,但无法避免一旦下水道堵塞,溢水污染药品储存环境而可能造成的危害。
整改措施:立即拆掉自来水水嘴,封闭管道。
整改责任人:XXX整改时间:XX月XX日整改结果:已经完成(见照片)2102 企业外用药仓库无通风设施(缺换气扇)问题分析:由于我公司现存药品数量很少,所有外用药都放在一间仓库里。
养护人员和公司管理人员对于另一间备用仓库都没有进行认真检查,因而出现了此问题。
整改措施:安装换气扇。
整改责任人:XXX整改时间:XX月XX日整改结果:已经完成(见照片)在进行整改的同时,我们还对相关责任人给予批评教育,要求相关的部门和部门负责人加强对所属人员的指导、帮助、督促和检查,使GSP的相关规定和公司质量管理制度得到不折不扣的执行,避免今后再出现此类认识不到位,管理不到位的问题。
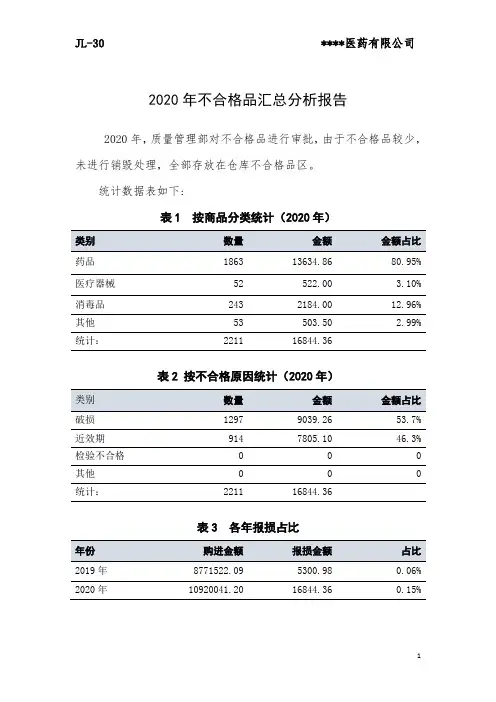
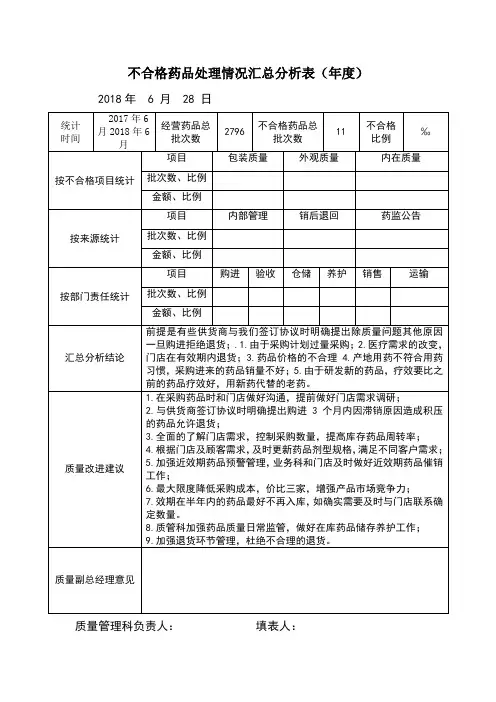
2020年不合格品汇总分析报告2020年,质量管理部对不合格品进行审批,由于不合格品较少,未进行销毁处理,全部存放在仓库不合格品区。
统计数据表如下:表1 按商品分类统计(2020年)药品1863 13634.86 80.95% 医疗器械52 522.00 3.10% 消毒品243 2184.00 12.96% 其他53 503.50 2.99% 统计:2211 16844.36表2 按不合格原因统计(2020年)破损1297 9039.26 53.7% 近效期914 7805.10 46.3% 检验不合格0 0 0 其他0 0 0 统计:2211 16844.36表3 各年报损占比2019年8771522.09 5300.98 0.06% 2020年10920041.20 16844.36 0.15%12072211100020002019年度2020年度报损数量(增长83.2%)5300.9816844.3650001000015000200002019年度2020年度报损金额(增长218%)2019年与2020年报损对比1夏枯草颗粒2铝碳酸镁颗粒3胃力胶囊4参苓口服液5匹多莫德胶囊6红花逍遥胶囊7复方大红袍止血片8碳酸钙胶囊9克林霉素磷酸酯片10维生素AD 滴剂11复方桔梗枇杷糖浆12盐酸氨溴索糖浆13苯酰甲硝唑分散片14布洛芬混悬滴剂15妇乐胶囊金额3139.22821.11035.61013990900690592374.9333.8314305.962551451203139.22821.11035.61013990900690592374.9333.8314305.962551451205001000150020002500300035002020年药品报损图表(单品超100元)1086.861.962444.82331429.5369.3730.42462.525.54289.543251.65001000150020002500300035004000450050001月2月3月4月5月6月7月8月9月10月11月12月2020年各月药品报损金额图表分析结论如下:1、2020年相比于2019年报损增长明显。