工业氯化铵灼烧残渣测定 共23页
- 格式:ppt
- 大小:955.50 KB
- 文档页数:23
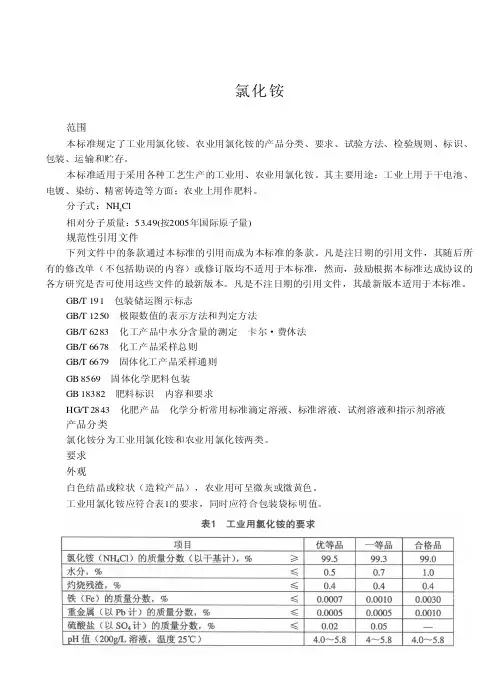
范围规范性引用文件产品分类要求外观本标准规定了工业用氯化铵、农业用氯化铵的产品分类、要求、试验方法、检验规则、标识、包装、运输和贮存。
本标准适用于采用各种工艺生产的工业用、农业用氯化铵。
其主要用途:工业上用于干电池、电镀、染纺、精密铸造等方面;农业上用作肥料。
分子式:NH Cl相对分子质量:53.49(按2005年国际原子量)下列文件中的条款通过本标准的引用而成为本标准的条款。
凡是注日期的引用文件,其随后所有的修改单(不包括勘误的内容)或修订版均不适用于本标准,然而,鼓励根据本标准达成协议的各方研究是否可使用这些文件的最新版本。
凡是不注日期的引用文件,其最新版本适用于本标准。
GB/T 191 包装储运图示标志GB/T 1250 极限数值的表示方法和判定方法GB/T 6283 化工产品中水分含量的测定 卡尔·费休法GB/T 6678 化工产品采样总则GB/T 6679 固体化工产品采样通则GB 8569 固体化学肥料包装GB 18382 肥料标识 内容和要求HG/T 2843 化肥产品 化学分析常用标准滴定溶液、标准溶液、试剂溶液和指示剂溶液氯化铵分为工业用氯化铵和农业用氯化铵两类。
白色结晶或粒状(造粒产品),农业用可呈微灰或微黄色。
工业用氯化铵应符合表1的要求,同时应符合包装袋标明值。
4氯化铵 农业用氯化铵应符合表2要求,同时应符合包装袋标明值。
本标准中所用试剂、水和溶液的配制,在未注明规格和配制方法时,均应符合HG/T 2843之规定。
氯化铵在碱性溶液中蒸馏出氨,用过量硫酸标准溶液吸收,在指示剂存在下,用氢氧化钠标准滴定溶液回滴过量的硫酸。
硫酸:c(1/2H SO )=0.5mol/L ,其浓度应小于氢氧化钠标准滴定溶液的浓度;氢氧化钠:450g/L ;氢氧化钠标准滴定溶液:c(NaOH)=0.5mol/L ;甲基红-亚甲基蓝混合指示剂;通用实验室仪器,以及蒸馏仪器:按GB/T2441.1配备;防暴沸颗粒或防暴沸装置:后者由一根长约100mm ,直径约5mm 玻璃棒连接在一根长约25mm 聚乙烯管上;加热装置:1000W ~1500W 电炉,置于升降台架上,可自由调节高度;也可使用调温电炉或能够调节供热强度的其它形式热源。


炽灼残渣检查法检验操作规程1.目的:规范炽灼残渣检验操作,保证检验的质量。
2.适用范围:适于本公司原辅料、成品检验。
3.责任者:质量保证部经理、化验室主任、化验员。
4.检验依据:《中国兽药典》2010年版一部附录。
5. 内容:5.1 原理:有机药物经高温加热分解或挥发后遗留下的不挥发的无机物(多为金属的氧化物、碳酸盐、磷酸盐、硅酸盐和氯化物等)。
经加硫酸并炽灼(700~800℃)后所得的硫酸盐即炽灼残渣(亦称为硫酸盐灰分,因为这个条件下,无机物质是转变成硫酸盐形式存在的),如不用硫酸处理,则“炽灼残渣”可能是金属氧化物、碳酸盐或氯化物等无机物质。
动植物生药经烧灼后的灰烬称为灰分。
5.2 仪器与用具5.2.1 高温炉、坩锅、坩锅钳、通风柜。
5.3 试药与试液:硫酸(分析纯)5.4 操作方法5.4.1 空坩锅恒重取坩锅置于高温炉内,将盖子斜盖在坩锅上,经700~800℃炽灼约30~60分钟,取出坩锅,稍冷片刻,移置干燥器内并盖上盖子,放冷至室温(一般约需60分钟),精密称定坩锅重量。
再在上述条件下炽灼约30分钟,取出,置干燥器内放冷、称重、重复数次直到恒重。
5.4.2 称取供试品取供试品1.0~2.0g或各该药品项下规定的重量,置已炽灼恒重的坩锅内,精密称定;5.4.3 炭化将盛有供试品的坩锅斜置电炉上(避免供试品骤然膨胀而逸出),炽灼至供试品完全产生炭化呈黑色,并不冒浓烟,放冷至室温。
“炭化”操作应在通风柜内进行。
5.4.4 灰化除另有规定外,滴加硫酸0.5~1.0ml,使灰化物全部湿润,继续在电炉或煤气灯上加热至硫酸蒸气除尽,白烟完全消失(以上操作应在通风柜内进行),将坩锅移置高温炉内,盖子斜盖于坩锅上,在700~800℃炽灼约60分钟,使供试品完全灰化;5.4.5 恒重按操作方法(5.4.1)自“取出坩锅”稍冷片刻起,依法操作,直至恒重。
5.5 注意事项5.5.1 供试品的取量应根据炽灼残渣限度来决定,一般规定炽灼残渣限度为0.1~0.2%,应使炽灼残渣的量在1~2mg之间,故供试品取量多为1.0~2.0g。


FNCPFL0029 氯化铵 氯化铵或氮含量的测定 蒸馏后滴定法F_NCP_FL_ 0029氯化铵-氯化铵或氮含量的测定-蒸馏后滴定法1 范围本方法适用于工、农业用氯化铵中氯化铵含量或氮含量的测定。
2 原理氯化铵在碱性溶液中蒸馏出氨,用过量硫酸标准溶液吸收,在指示液存在下,用氢氧化钠标准滴定溶液回滴过量的硫酸。
3 试剂3.1 氢氧化钠溶液,450g/L3.2 硫酸溶液,c (1/2H 2SO 4)=0.5mol/L量取15.0mL 硫酸(ρ约1.84 g/mL )慢慢注入盛有400 mL 水的600mL 烧杯内,混匀。
冷却后转移至1L 容量瓶中,用水稀释至刻度,混匀。
贮存于密闭的玻璃瓶内。
其浓度应小于氢氧化钠标准滴定溶液的浓度。
3.3 氢氧化钠标准滴定溶液,c (NaOH)=0.5mol/L3.3.1 无二氧化碳水的制备3.3.2 将水注入烧瓶中(水量不超过烧瓶体积的2/3),煮沸10min ,放置冷却,用装有碱石灰干燥管的橡皮塞塞紧。
3.3.3 制备10L~20L 较大体积的不含二氧化碳的水,可插一玻璃管到容器底部,往水中通氮气1h~2h ,以除去被水吸收的二氧化碳。
3.3.4 饱和氢氧化钠溶液的配制溶解162g 氢氧化钠于150mL 无二氧化碳水中,冷却至室温。
通过合格的介质(例如:玻璃毛)过滤,清液贮存于密闭的聚乙烯容器内;或溶液贮存于密闭的聚乙烯容器,放置至上层溶液清澈(放置时间一周),使用时吸取清液。
3.3.5 氢氧化钠标准滴定溶液的配制量取27.2mL 氢氧化钠饱和溶液清液,用无二氧化碳的水稀释至1L ,混匀,贮存在带有碱石灰干燥管的密闭的聚乙烯瓶中,防止吸入空气中的二氧化碳。
3.3.6 标定用玛瑙研钵将10g ~20g 基准邻苯二甲酸氢钾(KHC 8H 4O 4)研碎至粉状,置于120℃干燥箱内干燥2h ,在干燥器内冷却。
配制酚酞指示剂溶液(10g/L):称取1.0g 酚酞,溶于95%(V /V )乙醇,用95%(V /V )乙醇稀释至100mL 。


硅的测定(氯化铵重量法)
准确称取试样0.5克,置于200ml烧杯中,加1-2克氯化铵拌匀,盖上表面皿,沿皿口滴加2ml浓盐酸,2-3滴浓硝酸,拌匀,使试样充分溶解。
然后,置于电炉上垫石棉网加热至干,同时烧好沸水。
取下稍冷,加2ml浓盐酸,少许热水,拌匀过滤,滤液收集在250ml容量瓶中。
用热水洗烧杯7-8次,直至无氯离子。
沉淀连同滤纸取下放于磁坩埚中,在电炉上烘干灰化后,移至950℃马弗炉中灼烧30分钟,取出冷却,称重。
Si=G1×100%/G2
式中
G1——残渣的量
G2——试样重
滤液冷却,稀释至刻度,各吸取25ml测钙、镁、铁。
此时,钙、镁、铁不用加盐酸。
氟化钾,测法同一般组分分析。
钙的测法稍有不同:
吸取25ml滤液置于250ml烧杯中,用水稀释至150ml左右,加5ml三乙醇胺1+2,加MTB指示剂,用20%氢氧化钾滴定使溶液出现绿色荧光,过加5-7ml,用0.025N的EDTA标准溶液滴至溶液由酒红色变为蓝灰色为终点。
另外,测铝时,过加的0.015N的EDTA体积为8ml。

1 什么是炽灼残渣② ③ ④ ⑤ ⑥ ⑦ ⑧ ⑨ ⑩ ≤ ≥ < > ±① 其定义 :①指将药品(多为有机化合物)经加热灼烧至完全灰化, ②再加硫酸0.5~1.0ml ,并炽灼(700~800℃ )至恒重后遗留的金属氧化物或其硫酸盐(化学实验的残余物)②炽灼残渣检查法 检查不含金属的有机药物或挥发性无机药物中混入非挥发性的无机杂质(金属氧化物或无机盐类),③原理:样品炭化后+ H 2SO 4湿润→700~800℃炽灼至恒重→炽灼残渣(硫酸灰分) 残渣限量一般为0.1%~0.2%2. 操作方法一:主要仪器与试剂(1)高温电阻炉 (2 )坩埚( 瓷坩埚、铂坩埚、石英坩埚)(3)坩埚钳(普通坩埚钳、尖端包有铂层的铂坩埚钳) (4)通风柜。
(5).硫酸(分析纯) (6)电子天平0.1mg 即0.0001g(7)干燥器 (8)箱式电阻炉二.操作方法1.空坩埚恒重① .取 洁净 坩埚置于高温炉内,坩埚盖斜盖于坩埚上 ,经700~800℃炽灼约30~60分钟, ② 取出坩埚,稍冷片刻(或使高温炉停止加热,待冷却至300℃左右,取出坩埚), ③ 移置干燥器内,盖好坩埚盖,放冷至室温(一般约需60分钟),精密称定坩埚重量W 0 。
④ 再在上述条件下炽灼约30分钟,取出,置干燥器内,放冷,称重W 1 ;⑤ 重复数次,直至恒重(连续两次称量的重量差异在0.3mg 以下,即0.0003g ),备用。
残渣(恒重)蒸气除尽至放冷至全部黑色、无烟雾,炽灼至恒重的坩埚样品℃高温灼烧~湿润,直火加热~直火缓缓加热−−−−−−→−−−−−−−−−−→−−−−−→−+8007004215.0SO H SO H 42ml2称取供试品(剪碎)取供试品1.0~2.0g或各品种项下规定的重量,置已炽灼至恒重的坩埚内,精密称定。
3炭化:(上操作应在通风柜内进行)将盛有供试品的坩埚置电炉上缓缓灼烧(应避免供试品受热骤然膨胀或燃烧而逸出),炽灼至供试品全部炭化呈黑色,并不再冒烟,放冷至室温。

氯化铵检测分析方法1.目的明确氯化铵的质量控制方法和氯化铵的质量标准2. 职责质检部、试验室2.职责4.检验方法本标准所用水应符合GB\T6682—92中三级水的规格所列试剂,除特殊规定外,均指分析纯试剂。
试验中所需标准溶液,按GB、T601—88规定制备4.1含量测定方法甲:蒸馏后滴定法4.1.1原理氯化铵属铵盐,用蒸馏法测定含量的原理参见“WYN—030硫酸铵”中“氮的测定”部分4.1.2仪器蒸馏仪器与“WYN—030硫酸铵”中“氮的测定”所用蒸馏仪器相同。
≤0.8 4.1.3应用试剂氢氧化钠溶液(450g/L);氢氧化钠标准滴定溶液[A(NaOH)=0.5mol/L]硫酸标准滴定溶液[A(1/2H2SO4)=0.5mol/L];其浓度应小于氢氧化钠标准滴定溶液的浓度);甲基红—次甲基蓝混合指示液。
4.1.4测定手续称取9g样品(精确至0.001g),溶于少量水中,移至500ml容量瓶中,用水稀释到刻度,摇匀,准确吸取50ml于蒸馏瓶(A)中,加约350ml水,并加少量防爆沸石。
准确吸取50ml硫酸标准滴定[A(1/2H2SO4)=0.5mol/L]于吸收瓶E中,并加约80ml水(以水封除双连球与瓶连接口为准),加4~6滴甲基红-次甲基蓝混合指示液,然后将装置按图连接,各连接处涂以硅脂并固定,以确保蒸馏装置的严密性,然后将冷却水通入装置中,经滴液漏斗(A)往蒸馏瓶(A)中注入30ml 氢氧化钠溶液(450g/L),当漏斗(A)中流存2ml溶液时,关闭活塞。
加热蒸馏直至吸收瓶(E)中收集到250ml馏出液(蒸馏时间约45min)。
停止加热,打开漏斗(A)上活塞,拆下防溅球管(B),仔细冲洗冷凝管(D)将洗液并入馏出液中,最后拆下吸收瓶(E),用氢氧化钠标准滴定溶液[A(NaOH)=0.5mol/L]至溶液呈现灰色即为终点,同时作一空白试验。
4.1.5计算氯化铵(以NH4AL干基计) %(V1-V2)×A×0.05349×100=m×50÷500×(100-X)或氮(以N 干基计) % =(V1-V2)×A×0.01401×100=m×50÷500×(100-X)式中V1—空白试验耗用氢氧化钠标准滴定溶液体积,ml;V2—样品耗用氢氧化钠标准滴定体积,ml,A—氢氧化钠标准滴定溶液实际浓度,mol/L;m —称取样品质量,g;0.05349—与1.00ml氢氧化钠标准滴定溶液[A(NaOH)=1.0mol/L]相当的以克表示的氯化铵的质量;0.01401—与1.00ml氢氧化钠标准滴定溶液[A(NaOH)=1.0mol/L] 相当的以克表示的氮的质量;X—水分,%乙方法:银量法A:原理在NH4AL的中性或弱碱性溶液中,加入K2ArO4作指示剂,用Ag2ArO4标准溶液进行滴定,由于AgAl的溶解度(1.34×10-5mol/L)小于Ag2ArO4的溶解度(6.5×10-5mol/L),所以在滴定过程中AgAl首先沉淀出来,待滴定到终点附近,由于银离子浓度迅速增大,达到Ag2ArO4的浓度积,立即形成砖红色的Ag2ArO4沉淀,借此指示滴定终点。

工业氯化铵一、介绍工业氯化铵是一种常用的无机化学品,化学式为NH4Cl。
它是一种白色结晶固体,可溶于水。
工业氯化铵可以用于多种应用,包括金属表面处理、冶金、烟花制造、医药和化肥等领域。
在本文中,我们将对工业氯化铵的制备方法、性质、应用领域等进行全面、详细、完整且深入地探讨。
二、制备方法2.1 盐湖矿石法1.从含氯化铵的盐湖矿石中提取氯化铵。
2.将提取得到的氯化铵溶解在水中。
3.过滤溶液,去除杂质。
4.蒸发溶液,得到氯化铵结晶。
5.干燥和粉碎氯化铵结晶,得到工业氯化铵。
2.2 氨、盐酸反应法1.将氨气通入盐酸中,生成氯化铵。
2.过滤溶液,去除杂质。
3.蒸发溶液,得到氯化铵结晶。
4.干燥和粉碎氯化铵结晶,得到工业氯化铵。
三、性质3.1 外观和物理性质工业氯化铵是一种白色结晶固体,透明无色。
它具有吸湿性,易溶于水,在水中呈酸性。
工业氯化铵在高温下可以分解,产生氨气和盐酸。
3.2 化学性质工业氯化铵可以与一些金属进行反应,生成对应的金属氯化物。
它还可以与碳酸钠反应,生成氯化钠和碳酸氨。
工业氯化铵在高温下可以与氢氟酸反应,生成氟化铵和氯化氢。
四、应用领域4.1 金属表面处理工业氯化铵可以用于金属表面处理,以去除表面的氧化物和污垢,提高金属的表面质量和粗糙度。
它可以作为酸洗剂使用,清洁金属表面并去除氧化层。
4.2 冶金工业氯化铵在冶金领域也有应用。
它可以作为焊剂使用,用于铜、银等金属的焊接。
它还可以作为铅酸蓄电池的电解液添加剂,提高电池的性能。
4.3 烟花制造工业氯化铵是烟花制造中常用的化学品之一。
它可以用作烟花的氧化剂,提供氧气以支持燃烧。
通过控制工业氯化铵的添加量和配方,可以控制烟花的颜色和效果。
4.4 医药工业氯化铵在医药领域也有一定的应用。
它可以用于制备盐酸铵,进而制备药物。
盐酸铵可以用于治疗呼吸系统疾病,具有消炎和镇咳的作用。
4.5 化肥工业氯化铵还可以作为一种氮肥使用。
它可以提供植物所需的氮元素,促进植物的生长和发育。
制氯化铵与氮含量测定目的1制20g氯化铵2定性检验氯化铵3测定氮含量原理1制氯化铵(NH4)2SO4 + 2NaCl == Na2SO4 + 2NH4ClM 132.13 116.88 142.04 107m X Y 40 30解得X=37.13 Y=32.85(生成氯化铵按20克计算,最后无需的得到20克,)第一次操作溶液中理论剩余量如下表溶液/ml H2O/g NH4Cl/g Na2SO4/g120 85 60 25 100 65 46 27 80 45 32 19 70 35 25 15 故蒸发到80ml之后在80ml时温度/°C NH4Cl/g Na2SO4/g60 24 19(20)40 21 19(22)30 19 18 故冷却到接近35°C理论产出约10g第二次操作溶液中剩余量溶液/ml H2O/g NH4Cl/g Na2SO4/g80 45 21(32)1970 35 21(25)1560 25 18 11 可蒸发至70ml之后在70ml时温度/°C NH4Cl/g Na2SO4/g60 20 15(16)40 16 15(17)30 14 14 故冷却到接近35°C理论产出5g一共理论产出15g第三次操作溶液中剩余量 溶液/mlH 2O/g NH 4Cl/g Na 2SO 4/g70 35 14(25) 15 60 25 14(18) 1150 15 11 7可蒸发至60ml 之后在60ml 时 温度/°CNH 4Cl/g Na 2SO 4/g60 14 7(11) 40 11 7(12) 30 10 7(10)20 9 5 故冷却到接近30°C 理论产出5g 一共理论产出20g2定性检验氯化铵(氯化铵加热分解,而其他盐不会分解,所以用灼烧检验) NH4Cl+NaOH=NH3↑+NaCl+H2O 氨气在水中溶解度高氨水显碱性(加了NaOH ,任何溶液都会有碱性) NH4Cl+AgNO3=AgCl ↓+NH4NO3生成白色沉淀(NaCl 不会有此现象吗??)3测定氮含量NH4Cl =NH3↑+HCl↑加热使只有杂质残留,称量质量可算出NH4Cl 质量,进而算出产率=实验流程图123步骤与预期现象一、制氯化铵1取37.13g 硫酸铵与32.85g 氯化钠溶于120ml 水中2蒸发浓缩至80ml ,趁热过滤 3降温至35度,过滤 4反复2、3二、定性检验氯化铵 改灼烧实验1铵根离子:(1) 取少量产品于试管中,滴加适量(可过量)NaOH ,振荡(2) 溶解后,直接加热。
药品名称氯化铵拼⾳名 Lühua’an英⽂名 AMMONIUM CHLORIDE来源(分⼦式)与标准本品按⼲燥品计算,含NH4Cl 不得少于99.5%。
性状 本品为⽆⾊结晶或⽩⾊结晶性粉末;⽆臭,味咸、凉;有引湿性。
本品在⽔中易溶,在⼄醇中微溶。
检查 酸度 取本品2.0g,加⽔10ml使溶解,依法测定(附录Ⅵ H),pH值应为4.0 ~6.0 。
钡盐 取本品4.0g,加⽔20ml溶解后,滤过,滤液分为两等份,⼀份中加稀硫酸 2 ml,另⼀份中加⽔2ml ,静置15分钟,两液应同样澄清。
⼲燥失重 取本品,置硫酸⼲燥器中⼲燥⾄恒重,减失重量不得过0.5 %(附录Ⅷ L)。
炽灼残渣 不得过0.1 %(附录Ⅷ N)。
铁盐 取本品1.0g,⽤⼩⽕加热,俟氯化铵全部挥散,放冷,残渣中加⽔25ml,依法检查(附录Ⅷ G),与标准铁溶液5.0ml 制成的对照液⽐较,不得更深(0.005%) 。
重⾦属 取本品2.0g,加醋酸盐缓冲液(pH3.5)2ml与⽔适量使溶解成25ml,依法检查(附录Ⅷ H第⼀法),含重⾦属不得过百万分之⼗。
砷盐 取本品0.40g,加⽔23ml溶解后,加盐酸5ml,依法检查(附录Ⅷ J第⼀法),应符合规定(0.0005%)。
鉴别 本品的⽔溶液显铵盐与氯化物的鉴别反应(附录Ⅲ)。
含量测定 取本品约0.12g ,精密称定,加⽔50ml使溶解,再加糊精溶液(1→ 50)5ml、荧光黄指⽰液8 滴与碳酸钙0.10g ,摇匀,⽤硝酸银滴定液(0.1mol/L)滴定。
每1ml 的硝酸银滴定液(0.1mol/L)相当于5.349mg 的NH4Cl 。
类别祛痰药、辅助利尿药。
剂量⼝服祛痰 ⼀次0.3 ~0.6g ⼀⽇0.9 ~1.8g 利尿 ⼀次0.6 ~2g ⼀⽇1.8 ~6g注意肝、肾功能不全及溃疡病患者慎⽤。
贮藏密封,在⼲燥处保存。
制剂氯化铵⽚。
标准操作规程范围:适用于药品中微量不挥发性无机物的限度检查。
责任者:质量控制部主任、化验员。
规程:1。
本品引自《中国药典》2000年版附录。
1.1。
概述:药品(多为有机化合物)经高温加热分解或挥发后遗留下不挥发的无机物,经加硫酸并炽灼(700—800℃)恒重后生成金属氧化物或其硫酸盐即为炽灼残渣.2. 仪器与用具:高温炉、坩埚(瓷坩埚、铂坩埚、石英坩埚等)、长柄不锈钢坩埚钳、通风柜、干燥器、万分之一分析天平等。
3. 试药:硫酸(分析纯)、变色硅胶等。
4。
操作方法4。
1。
空坩埚的恒重:取坩埚置于高温炉内,将盖子斜盖在坩埚上,经700—800℃炽灼约30-60分钟,取出坩埚,稍冷片刻,移置干燥器内并盖上盖子,放冷至室温(一般约需60分钟),精密称定钳锅重量。
再在上述条件下炽灼30分钟,取出,置干燥器内,放冷,称重;直至恒重,备用.4。
2。
称取供试品:取供试品1。
0—2。
0g,或各该药品项下规定的重量,置已炽灼至恒重的坩锅内,精密称定。
4.3。
炭化:将盛有供试品的坩锅斜置电炉上缓缓灼烧(避免供试品骤然膨胀而逸出),炽灼至供试品全部炭化呈黑色,并不冒浓烟,放冷至室温.“炭化”操作应在通风柜内进行.4。
4。
灰化:除另有规定外,滴加硫酸0.5—1.0ml,使炭化物全部湿润,继续在电炉上加热至硫酸蒸汽除尽,白烟完全消失(以上操作应在通风柜中进行),将坩锅移至高温炉内,盖子斜盖于坩锅上,在700—800℃炽灼约60分钟,使供试品完全灰化。
标准操作规程4。
5. 恒重:按操作方法(4。
1)自“取出坩锅稍冷片刻"起,•依法操作,直至恒重。
5. 注意事项5.1. 供试品的取用量应根据炽灼残渣限度来决定,•一般规定炽灼残渣限度为0。
1-0。
2%,应使炽灼残渣的量在1-2mg 之间,故供试品取量多为1。
0-2.0g 。
炽灼残渣较高或较低的药品,可酌情减少或增加供试品的取量。
5.2。
炽灼残渣检查同时做几份时,钳锅应预先编码标记,盖子与钳锅应编码一致。