
趋化因子及其受体在免疫细胞中的作用研究概述
趋化因子是目前成员最多的细胞因子家族,在人和小鼠中大概有50个内源性趋化因子。这些因子大约结合20多个跨膜受体。趋化因子的主要作用是控制免疫细胞的迁移模式,对细胞运动至关重要。趋化因子系统在初始T细胞产生,决定细胞的分化(如效应细胞和记忆细胞),影响调节性T细胞的功能,调节免疫细胞迁移和定位,已达到体内平衡。趋化因子在急性炎症和淋巴系统中对免疫反应的产生和调节具有重要作用。趋化因子在炎性疾病及癌症中的作用使其成为新的药物靶点。
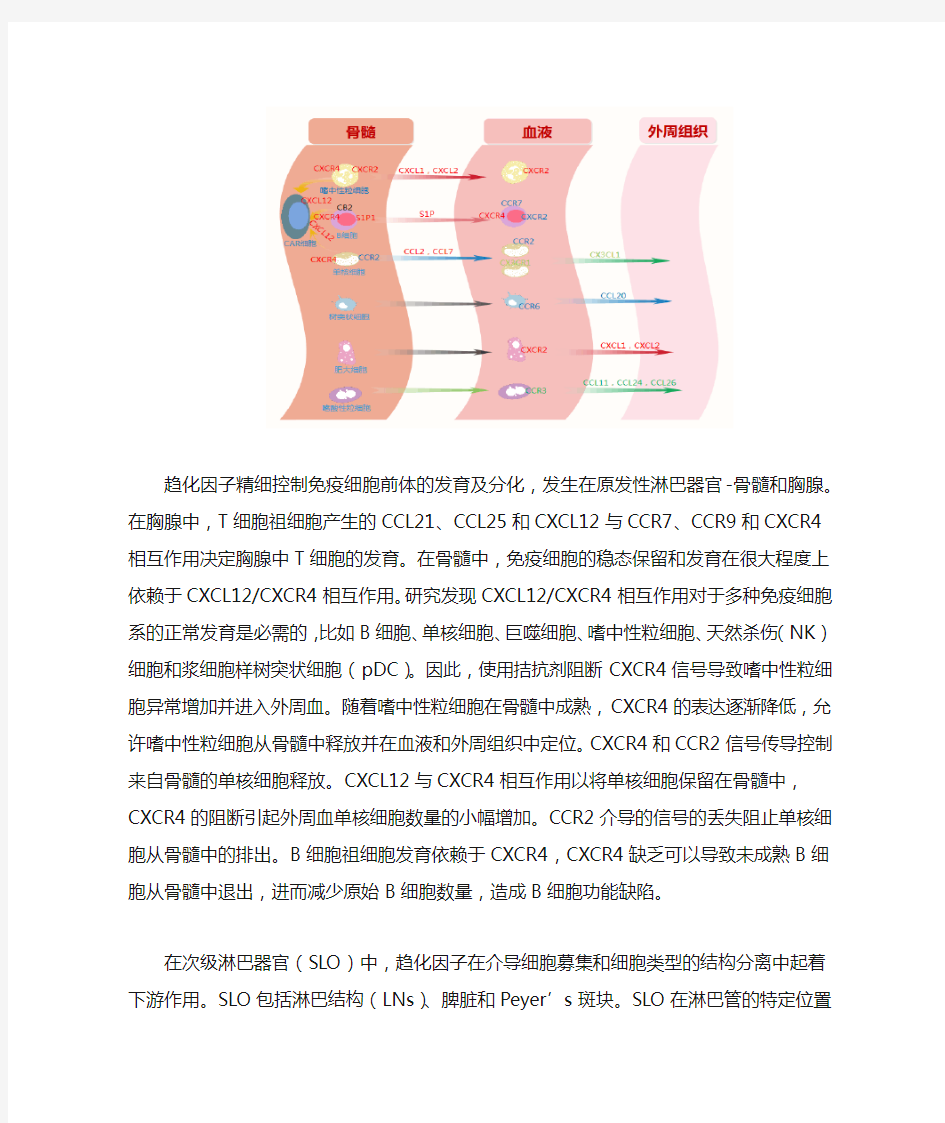
趋化因子可以控制骨髓、血液及外周组织中的免疫细胞运输。CXCL12由CAR细胞产生,可以使发育中的中性粒细胞、B细胞和单核细胞保留在骨髓中。DC前体、肥大细胞前体和发育中的嗜酸性粒细胞通过未知机制保留在骨髓中。在没有CXCR4信号传导或CXCR2信号传导的情况下,嗜中性粒细胞离开骨髓并进入血液。B细胞通过CB2信号进入骨髓,并通过S1P1信号传导进入血液。B细胞可以使用CCR7、CXCR4和CXCR5信号进入淋巴结构。单核细胞响应CCR2信号进入血液以及CXCR4信号传导减少。单核细胞分化为促炎症(CCR2+)和抗炎(CX3CR1+)单核细胞。抗炎单核细胞可以通过CX3CL1进入外周组织。DC前体通过未知机制进入血液,并可以通过CCL20离开外周组织。在人类中,CXCL14也可能在抗炎单核细胞和DC前体迁移到外周组织中起作用。肥大细胞前体通过未知机制离开骨髓,并在CXCR2介导的信号后迁移至肠道。CCR3信号通过CCL11和CCL24(人和小鼠)以及CCL26(人)后,嗜酸性粒细胞进入血液并离开外周组织。
趋化因子精细控制免疫细胞前体的发育及分化,发生在原发性淋巴器官-骨髓和胸腺。在胸腺中,T细胞祖细胞产生的CCL21、CCL25和CXCL12与CCR7、CCR9和CXCR4相互作用决定胸腺中T细胞的发育。在骨髓中,免疫细胞的稳态保留和发育在很大程度上依赖于CXCL12/CXCR4相互作用。研究发现CXCL12/CXCR4相互作用对于多种免疫细胞系的正常发育是必需的,比如B细胞、单核细胞、巨噬细胞、嗜中性粒细胞、天然杀伤(NK)细胞和浆细胞样树突状细胞(pDC)。因此,使用拮抗剂阻断CXCR4信号导致嗜中性粒细胞异常增加并进入外周血。随着嗜中性粒细胞在骨髓中成熟,CXCR4的表达逐渐降低,允许嗜中性粒细胞从骨髓中释放并在血液和外周组织中定位。CXCR4和CCR2信号传导控制来自骨髓的单核细胞释放。CXCL12与CXCR4相互作用以将单核细胞保留在骨髓中,CXCR4的阻断引起外周血单核细胞数量的小幅增加。CCR2介导的信号的丢失阻止单核细胞从骨髓中的排出。B细胞祖细胞发育依赖于CXCR4,CXCR4缺乏可以导致未成熟B细胞从骨髓中退出,进而减少原始B细胞数量,造成B细胞功能缺陷。
在次级淋巴器官(SLO)中,趋化因子在介导细胞募集和细胞类型的结构分离中起着下游作用。SLO包括淋巴结构(LNs)、脾脏和Peyer’s斑块。SLO在淋巴管的特定位置发展,通过CXCL13聚集。在成熟的SLO中,趋化因子的稳态生成可以维持SLO的结构。CXCL13和CXCR5相互作用促进B细胞的体内平衡定位。在脾脏中,边缘区域B细胞依赖于CXCR7表达用于其稳态定位。用CXCR7拮抗剂治疗小鼠,导致脾边缘区B细胞数量减少。同时,成纤维细胞网状细胞(FRCs)产生CCL19、CCL21和CXCL12,通过受体CCR7和CXCR4,促进T 细胞和树突状细胞(DCs)进入和定位。因此,即使在没有免疫应答的情况下,初始淋巴细胞和抗原呈递细胞(APC)也主动迁移并保留在SLO中。
在三级淋巴器官(TLOs)中,趋化因子的作用机制尚不清楚。炎性细胞因子诱导淋巴细胞吸收趋化因子CXCL13和CCL19的表达,一起作用促进淋巴细胞进入TLO。在通过淋巴毒素、CXCL13、CCL19或CCL21的异位表达研究TLO发展实验中,强调了无细胞因子阳性反馈环的存在。鉴于TLO在感染和病理性自身免疫应答中的局部免疫激活中的作用,该趋化因子反馈环可以呈现出有效的靶向和减弱自身免疫应答的区域。
在天然T细胞中,趋化因子受体CCR7和CXCR4得以表达。CCR7结合由HEV产生并呈现在腔内皮上的CCL21,以及由FRC网络产生的CCL19,并跨越HEV穿过腔内皮细胞。天然T细胞上的CXCR4还通过结合CXCL12促进LN进入,CXCL12由FRC产生并转染,呈递在HEV 腔上。一旦进入LN,T细胞将CCL19和CCL21跟踪到T细胞区域,这使得它们能够作用于DC。
在天然B细胞中,趋化因子受体CCR7、CXCR4和CXCR5得以表达。天然B细胞还表达CXCR5,其结合由FDC产生的CXCL13,并且可以通过HEV转胞吞素后呈递。CXCR5缺陷型B 细胞在很大程度上受到Peyer’s斑块的限制,但是似乎几乎不发挥作用。一旦进入LN,B细胞迁移到卵泡以响应CXCL13。
Foxp3 +调节性T细胞(Tregs)是免疫反应的重要介质。在没有感染或炎症的情况下,Treg广泛分布在大多数淋巴组织和非淋巴组织中。在小鼠中,趋化因子受体表达的破坏可以改变这种广泛的分布并导致致病性炎症反应。例如,Treg中CCR4的缺失可防止其在皮肤和肺中的稳态积累,并导致这些特定器官发炎。在人类中,趋化因子受体在Treg细胞中表达随发育生长而变化。在新生儿脐带血中,趋化因子受体CCR7、CXCR4和L-选择蛋白以及去神经受体CCR9得以表达。在三周岁以前,人类血清中的Treg大多数似乎具有记忆表型,使得肠道CCR9表达下调,而皮肤、肺部及炎症归巢的趋化因子受体获得表达,如CXCR3、CCR2、CCR4、CCR5、CCR6和CCR8。
趋化因子控制炎症中骨髓、血液和外周组织之间的先天免疫细胞运输。在炎症期间,G-CSF导致骨髓中CXCL12的产生减少,并通过嗜中性粒细胞增殖降低CXCR4的表达。CXCR4介导减少,CXCR2介导的出血信号的丧失,促进中性粒细胞释放到血液中。人类中的BLT1、CCR1(或CXCR1)和嗜中性粒细胞上的CXCR2受体与其配体结合,促进嗜中性粒细胞进入外周组织。在组织中,嗜中性粒细胞可能受到CCR1(小鼠)、CXCR1(人)、CXCR2和BLT1信号传导影响,而产生到感染或损伤。单核细胞通过全身病原体相关分子模式(如TLR配体)产生的CCL2迁移出骨髓,通过CXCR2信号粘附于发炎的内皮,并通过CCR2信号转移到外周。肥大细胞前体能够通过CXCR2、BLT1或CYSLT1信号转导到外周。嗜酸性粒细胞离开骨髓并通过CCR3信号迁移到外周组织。最后,成熟的组织DCs上调CCR7并通过CCL21迁移到淋巴管中以排出外周组织。
肥大细胞在急性炎症中起重要作用,因为它们表达多种模式识别受体(PRR)并含有预先形成的炎症介质的大颗粒。已有研究结果表明肥大细胞释放CCL1,诱导CCR8表达。肥大细胞脱颗粒是促进嗜中性粒细胞募集的趋化因子的重要直接来源。肥大细胞受到刺激可以产生多种趋化因子,如CCL2、CCL3、CCL4、CCL5、CCL11、CCL20、CXCL1、CXCL2、CXCL8、CXCL9、CXCL10和CXCL11。组织中趋化因子产生的另一个来源是响应于局部免疫细胞释放的炎性细胞因子。除了趋化因子,激活的肥大细胞、DC和巨噬细胞释放急性炎症细胞因子如TNF和IL-1。这些细胞因子可刺激其他局部免疫细胞或激活局部上皮细胞。细胞因子活化的上皮可以产生许多趋化因子,包括CCL2、CCL3、CCL4、CCL5、CXCL1、CXCL2、CXCL3、CXCL5和CXCL8。同时,细胞因子可以通过局部内皮细胞改变趋化因子的产生和表达。在实验性自身免疫性脑炎(EAE)中,脑内皮细胞的IL-17刺激导致CXCR7的外膜表达,CXCL12表达。在没有内皮CXCL12的情况下,白细胞可以进入脑并诱发疾病发病。
急性炎症趋化因子靶向的最早的细胞之一是嗜中性粒细胞。嗜中性粒细胞表达许多趋化因子受体,包括CXCR2和CCR1(和人类中的CXCR1)。趋化因子在介导中性粒细胞释放中发挥重要作用。在发炎的环境中,G-CSF的全身水平增加,这促进嗜中性粒细胞生成以及骨髓出血的增加。G-CSF降低骨髓中的CXCL12产生和中性粒细胞上的CXCR4表达,从而中断了基于CXCL12 / CXCR4的中性粒细胞滞留。活化的嗜中性粒细胞产生CCL3、CCL4、CCL5、CCL20、CXCL1、CXCL8、CXCL9和CXCL10。因此,它们可以通过促进额外的免疫细胞的流入来促进和扩大初始的急性炎症反应。
炎性单核细胞表达许多的趋化因子受体,其可能在粘附和迁移中发挥特异性和非冗余作用。例如,单核细胞表达CXCR2,但它们不会响应于CXCL8而迁移。相反,CXCL8/CXCR2相
互作用被证明是在动脉粥样化模型中单核细胞对血管内皮的牢固粘附所必需的。除CXCR2外,CCR1和CCR5可以促进单核细胞在体外内皮细胞粘附和迁移。最后,转移实验表明,CCR6是免疫后将炎性单核细胞迁移到皮肤组织中所必需的。尽管如此,CCR6的配体CCL20在体外不诱导单核细胞迁移,因此CCL20/CCR6在单核细胞迁移中的作用仍不清楚(16)。
嗜酸性粒细胞表达趋化因子受体CCR1和CCR3,使其能够响应多种趋化因子,包括嗜酸性粒细胞趋化因子(CCL11、CCL24和CCL26)。在哮喘模型中,CCL11、CCL24和CCL26在暴露于IL-4和IL-13时在肺中强烈诱导。CCR3和CCL11都能促进嗜酸性粒细胞向周围组织的迁移。CCL24和CCL26也诱导嗜酸性粒细胞迁移。
如上所述,天然淋巴细胞在稳态条件下表达炎性趋化因子受体,这使得它们能够快速迁移并对炎症刺激作出反应。趋化因子介导的细胞迁移可以促进先天和适应性免疫细胞之间重要的细胞相互作用。
趋化因子起初被认为是天然免疫细胞的重要化学引诱物,如嗜中性粒细胞和巨噬细胞。随着研究的深入,趋化因子系统对于产生原发性肝炎所需的T细胞、B细胞和DC的贩运模式、迁移行为、细胞相互作用和定位也是至关重要。趋化因子通过影响其在淋巴组织中的细胞相互作用和定位在起始初始T细胞中起重要作用,也在适应性免疫应答的中枢细胞命运决定中起重要作用,如效应和记忆分化。此外,Treg不仅受趋化因子的影响,而且也影响趋化因子表达,这是发挥其抑制功能的一种方式。
附图:趋化因子表达细胞及其靶细胞图
注释:: Macrophages, : Monocytes, : Fibroblasts, : Neutrophils, : Megakaryocytes, : T Cells, : Epithelial Cells, : Endothelial Cells, : Eosinophils, : Basophils, : B Cells, :Melanocytes, : Myeloid cell, : DCs;更多内容请关注我们近期在官网分享的细胞因子海报(Post of human cytokine and chemokine-Cell sources, cell targets and major funcetions)。
趋化因子SDF-1及受体CXCR4研究进展 第23卷第1期 2OO6年2月 生物学杂志 JOURNALOFBIOLOGY V o1.23No.1 Feb,2006 趋化因子SDF一1及受体CXCR4研究进展 储子彦,陈晓萍,方晶晶 (浙江工业大学生物与环境工程学院,杭州I310014) 摘要:趋化因子(chenmklne)是一类一级结构相似,以对白细胞等多种细胞具有趋化定向运动作用为特征的小分子蛋白.功 能研究表明,趋化因子在胚胎发育,血管生成,炎症,肿瘤,史滋病等机体多种生理和病理过程中发挥重要作用,部分趋化 因子的衍生物或抑制物具有潜在的临床应用前景.不久的将来,趋化因子及其受体可能成为疾病治疗的分子靶点. 关键词:趋化因子;SDF一1;CXCR4 中图分类号:4文献标识码:A文章编号:1008—9632(2006)Oi一0011—03 趋化因子是一类重要的免疫调节因子,直接引导 自细胞,包括多种免疫活性细胞进行有方向性迁移,不 仅能精确地调节免疫系统的反应,还对组织,器官形 成,造血系统功能有调节作用. 1趋化因子与受体的结构 趋化因子分子结构中有4个保守的半胱氨酸,形 成2对二硫键,可分成4个亚类:(1)CC亚类,2对二硫 键间无其它氨基酸间隔;(2)CXC亚类,间隔1个氨基 酸;(3)Cx3C亚类,间隔3个氨基酸;(4)C亚类,仅有1
对二硫键. SDF一1(stromalcell—derivedfactor1)基质细胞来源 因子,属于趋化因子CXC亚家族,编码区含267bp,编码89个氨基酸残基多肽. CXCR4为SDF一1受体,高度保守,a螺旋跨膜7 次,由352个氨基酸组成,在人体内,编码基因位于人染 色体2q21,有一个胞外N端,3个胞内环,3个胞外环和 1个胞内C端,SDF—l与CXCR4的N端结合,并与CX—CR4和第二胞外环ECI_2(secondextracelluarloop)相互作用才能启动下游信号通路. 2SDF一1/CXCR4生物学意义 2.1与HW病毒感染的关系 CXCR4为嗜T细胞性SI株辅助受体,能与CD4协 同作用,参与CD4抗原与HW表面糖蛋白gpl20结合 介导病毒吸附侵入的过程,CXCR4的N端结构参与病 毒结合,有多个CXCR4结构域特别是第二细胞外环结 构能与HⅣ相互作用.趋化因子与受体的结合能阻断 受体与HⅣ的结合位点防治HⅣ进入细胞,同时趋化 因子对受体的封闭和下调作用也成为一个有效的防治 手段,故趋化因子及其衍生物是辅助受体拮抗剂主要 成分之一. Fig1Representationof313modelforSDF—ld(NMR} 围1SDF一1n的3D模型 除了SDF一1的衍生物,还发现CXCR4的其他抑制剂,如:AMD一3100通过与CXCR4的第二膜外环的负电荷区域结合,成为迄今为止与CXCR4结合最有效的 非肽类抑制剂. 2.2与造血细胞的关系 2.2.1SDF一1对造血于/祖细胞增殖和分化的影响
1 对于Ⅲ-Ⅳ度骨髓抑制,或发热性粒细胞缺乏患者,短效还是长效升白药的起效时间更快,持续时间更长? 短效重组人粒细胞刺激因子的药代动力学资料显示皮下注射的半衰期为2.5-5.8小时,而长效制剂的的药代动力学资料显示其平均半衰期依据剂量不同而波动于27-47小时之间。且资料显示,常规剂量给予短效制剂1天后嗜中性细胞成熟(不给药状态下一般需要5-7天),从骨髓进入血液,这样似乎短效制剂起效相对迅速。 短效制剂主要由肾小球滤过排出,而长效制剂由于其独特的PEG链上的环氧乙烷单元高度水合形成的环状结构能够避免其蛋白成分被相关酶水解或被巨噬细胞吞噬,同时避免其被肾小球滤过,所以其进入人体后主要由中性粒细胞表面的RHG-CSF受体介导清除,随着外周血中性粒细胞绝对计数(ANC)的升高,血浆中的长效制剂浓度呈现与ANC负相关表现。这样既可以达到持续有效改善白细胞缺乏,同时也能减少ANC过高风险。 在石远凯教授组织的关于聚乙二醇化长效制剂的临床Ⅰ期临床耐受性实验,以及徐兵河教授组织的关于聚乙二醇化长效制剂预防化疗后中性粒细胞减少的多中心随机对照Ⅱ期临床研究中,也得到了支持上述观点的相关结论(分别发表于2006年《癌症》及2016年《中国肿瘤临床与康复》)。 2影响G-CSF疗效的原因有哪些? 患者的治疗依从性,药物副反应(包括罕见但严重的副反应如脾破裂/毛细血管渗漏综合症等),患者一般体力状态/既往化疗方案及次数/年龄因素(间接反映患者的骨髓储备功能水平)。 对于短效制剂还应当考虑到作为大肠埃希菌的表达产物,其免疫原性和抗原性导致机体产生中和性抗体导致药效减退的因素。
3放疗状态下出现的粒细胞减少,G-CSF如何使用? 参考ASCO建议,对于致死剂量全身放射治疗或意外全身照射的患者应考虑在终止放射暴露后G-CSF应用治疗(该推荐基于美国放射事故登记中心的辐射急症救援中心的病例观察资料而提出)。 2012年美国放疗协会推荐在大剂量放疗后24-48小时应用长效聚乙二醇化制剂。 而2016年发表的由CSCO联合中国抗淋巴瘤联盟/中国抗癌协会乳腺癌专业委员会/中华医学会血液学分会白血病及淋巴瘤学组/中国抗癌协会血液肿瘤专业委员会共同做出的《聚乙二醇化重组人粒细胞刺激因子临床应用中国专家共识》明确指出:建议对暴露于≥2GY和/或总粒细胞计数明显减少或预期中性粒细胞计数<0.5×10~9/L,且持续时间≥7天的患者考虑细胞因子治疗,并推荐开始治疗时间为治疗暴露后24小时。 4长效集落细胞刺激因子会增加病人的经济负担,国内外的背景有何不同? 1长效制剂目前不在我省医保目录范围,属于全自费药物,在目前国内形势下存在一定不足。 2从改善骨髓抑制状态从而减少并发感染导致非计划性住院治疗方面考虑,在一定程度上节约了医疗资源,减少了患者在并发症治疗方面的经济支出和家庭社会压力。 3截至2016年8月,原研长效聚乙二醇化制剂的核心专利在美国/日本/欧洲及中国均全部到期。随着辉瑞等厂家仿制药进入市场,能否通过竞争模式改善其市场定位及表现有待进一步观察。
趋化因子及其受体在免疫细胞中的作用研究概述 趋化因子是目前成员最多的细胞因子家族,在人和小鼠中大概有50个内源性趋化因子。这些因子大约结合20多个跨膜受体。趋化因子的主要作用是控制免疫细胞的迁移模式,对细胞运动至关重要。趋化因子系统在初始T细胞产生,决定细胞的分化(如效应细胞和记忆细胞),影响调节性T细胞的功能,调节免疫细胞迁移和定位,已达到体内平衡。趋化因子在急性炎症和淋巴系统中对免疫反应的产生和调节具有重要作用。趋化因子在炎性疾病及癌症中的作用使其成为新的药物靶点。 趋化因子可以控制骨髓、血液及外周组织中的免疫细胞运输。CXCL12由CAR细胞产生,可以使发育中的中性粒细胞、B细胞和单核细胞保留在骨髓中。DC前体、肥大细胞前体和发育中的嗜酸性粒细胞通过未知机制保留在骨髓中。在没有CXCR4信号传导或CXCR2信号传导的情况下,嗜中性粒细胞离开骨髓并进入血液。B细胞通过CB2信号进入骨髓,并通过S1P1信号传导进入血液。B细胞可以使用CCR7、CXCR4和CXCR5信号进入淋巴结构。单核细胞响应CCR2信号进入血液以及CXCR4信号传导减少。单核细胞分化为促炎症(CCR2+)和抗炎(CX3CR1+)单核细胞。抗炎单核细胞可以通过CX3CL1进入外周组织。DC前体通过未知机制进入血液,并可以通过CCL20离开外周组织。在人类中,CXCL14也可能在抗炎单核细胞和DC前体迁移到外周组织中起作用。肥大细胞前体通过未知机制离开骨髓,并在CXCR2介导的信号后迁移至肠道。CCR3信号通过CCL11和CCL24(人和小鼠)以及CCL26(人)后,嗜酸性粒细胞进入血液并离开外周组织。
第六章表皮生长因子受体抑制剂常见不良反应及其处理 表皮生长因子及其受体信号通路在非小细胞肺癌(NSCLC)发生发展中发挥了重要作用,它调控肿瘤细胞增殖、生存和凋亡、血管生成、肿瘤转移等多个生物学过程,是NSCLC治疗的重要靶点之一。针对表皮生长因子受体(EGFR)的靶向药物包括小分子抑制剂(如吉非替尼和厄洛替尼)和单克隆抗体(如西妥昔单抗等)。小分子药物已作为晚期NSCLC的二、三线治疗方案广泛用于临床,EGFR单抗联合化疗一线治疗晚期NSCLC同样也取得了较好的疗效。 EGFR抑制剂(EGFR TKIs)无论是小分子药物还是单克隆抗体,均具有良好的安全性和耐受性,常见不良反应有皮肤毒性和腹泻,罕见不良反应有间质性肺炎、肝功能异常、口腔炎、脱发、口腔干燥等,无威胁患者生命的血液学毒性。与化疗毒副反应的处理措施不同,应用此类药物出现不良反应并非停药的指征,反而是肿瘤对靶向药物敏感的临床信号。许多研究发现皮疹与EGFR TKIs治疗的疗效相关,中重度皮疹患者总体生存明显优于轻度或无皮疹的患者。因此,正确处理EGFR TKIs 引起的不良反应具有十分重要的临床意义。 第一节皮肤毒性 皮肤毒性是最常报道的不良反应,发生率在2/3左右,常见反应包括痤疮样皮疹、甲沟炎及甲裂、毛发改变、皮肤干燥、超敏反应、粘膜炎等(表1)。EGFR TKIs的皮肤毒性/皮疹不属于过敏反应,而是皮肤EGFR受到抑制的结果。正常上皮和滤泡角细胞存在EGFR表达,EGFR在上皮细胞增殖分化等方面发挥重要作用,它可以剌激表皮细胞生长,抑制其分化,保护细胞抵抗紫外线相关损伤,抑制炎症并加速创面愈合。有证据提示EGFR表达或活性改变可伴有上皮异常增生和分化;皮肤毒性的机制还包括上皮角化过度和滤泡阻塞或炎症性反应。 表1 EGFR TKIs相关性皮肤毒性反应 EGFR TKIs引起的皮疹通常为痤疮样皮疹,呈丘疹脓疱样改变。皮疹的发生率随研究和药物而异,在BR.21研究中,皮疹发生率为79%,多为轻中度,3级和4级皮疹发生率分别为8%和1%。单抗皮疹发生率相对较高,在FLEX研究中,接受西妥昔单抗治疗的患者痤疮样重度皮疹的发生率
趋化因子及其受体的研究进展 摘要:趋化因子( chemokine)是一类一级结构相似小分子细胞因子,能够趋化细胞定向移动的,而且在免疫细胞和器官的发育、免疫应答过程、炎症反应、病原体感染、创伤修复及肿瘤形成和转移等方面发挥广泛的生理和病理作用。本文综述了对趋化因子及其受体的结构、分类和生物学功能的研究进展。 关键词: 细胞因子;趋化因子;趋化因子受体;趋化作用 Abstract:chemokine is similar to the primary structure of a class of small molecule cytokine, chemokine cell directional movement, but also in the development of immune cells and organs, immune response, inflammatory response, pathogen infection, wound healing andplay a wide range of physiological and pathological roles of tumor formation and metastasis. This paper reviews the progress on the study of the structure, classification and biological function of chemokines and their receptors. Keywords: cell factor; chemokines; chemokine receptor; chemotactic effect 免疫细胞的定向迁移是集体免疫应答发生和完成的必须条件。趋化因子是一类控制细胞定向迁移的细胞因子。其功能行使由趋化因子受体介导。趋化因子与其受体的相互作用控制着各种免疫细胞在循环系统和组织器官间定向迁移,使之到达感染、创伤和异常增殖部位,执行清除感染源、促进创伤愈合和消灭异常增殖细胞,维持组织细胞的平衡的功能。因此,趋化因子系统在免疫系统功能行使的各个环节中处于关键地位,并由此在病原体的清除、炎症反应、病原体感染、细胞及器官的发育、创伤的修复、肿瘤的形成及其转移、移植免疫排斥等方面都起着重要的作用。以趋化因子及其受体为控制靶点,通过激活或拮抗趋化因子受体的信号传导来调控趋化因子系统的功能,可
趋化因子及其受体与大肠癌的关系 摘要 越来越多的研究表明肿瘤的微环境在肿瘤的发生发展中起着至关重要的作用,而趋化因子及其受体作为肿瘤微环境中关键信号分子,在肿瘤的发生发展中发挥着不可或缺的作用。关键词:趋化因子大肠癌趋化因子受体 大肠癌包括结肠癌与直肠癌,是消化系统最常见的恶性肿瘤。近年来,大肠癌的发病呈逐年上升趋势,给社会和家庭带来沉重负担。大量研究资料表明,大肠肿瘤是一个复杂的混合体,除癌细胞外还有炎症细胞、免疫细胞、内皮细胞、成纤维细胞等,这些基质细胞构成了肿瘤细胞的基本的微环境,并通过分子信号通路为肿瘤提供生存所需要的物质。而趋化因子及其受体作为肿瘤微环境中关键信号分子,在肿瘤的发生发展中发挥着不可或缺的作用。本文就这一方面进行综述。 1.趋化因子及其受体的分类结构 趋化因子是一类结构功能相似、具有趋化吸引和活化作用的碱基肝素结合性的小分子分泌蛋白,相对分子质量为8 000~10 000。目前研究发现并克隆出的趋化因子达50多种[1]。根据其分子结构中N端半胱氨酸的不同可分为CXC、CC、C和CX3C四个亚家族[2]。目前认为CXC亚家族主要作用于中性粒细胞、淋巴细胞和单核细胞。CC亚家族主要作用于单核细胞、淋巴细胞、嗜酸性粒细胞和嗜碱性粒细胞。CX3C亚家族主要作用于中性粒细胞和单核细胞。C亚家族仅作用于淋巴细胞。CXC趋化因子根据结构功能区第一个Cys前有无ELR (Glu-Leu-Arg)序列分为ELR+和ELR-两类。常见的ELR+CXC趋化因子有IL-8、上皮细胞嗜中性粒细胞活性蛋白(ENA-78)、中性粒细胞趋化蛋白-2(GCP-2)、肿瘤生长相关因子α/β/γ(GRO-α/β/γ)、中性粒细胞活化蛋白-2(NAP-2)等[3]。根据功能可把趋化因子分为2类[4]:一类称为炎症型趋化因子,主要趋化单核细胞、中性粒细胞和效应T细胞等效应细胞迁移至炎症发生部位,如RANTES/CCL5和IL-8/CCL2;另一类为自稳型趋化因子,趋化自稳免疫系统中的一些细胞,如SDF-1/CXCL12。 趋化因子受体是表达在中性粒细胞、淋巴细胞、巨噬细胞等炎症细胞和上皮细胞、成纤维细胞等结构细胞表面上的具有七次跨膜域的受体,属G蛋白偶联受体超家族成员,是介导相应趋化因子发挥生物学功能的关键受体。依据其结合的配体不同可分为CXCR、CCR、CR、CX3CR四类。 2.趋化因子及其受体的一般功能 趋化因子在正常和非正常生理状况下起着重要作用:1、促进细胞迁移;2、诱导和整合蛋白的活化;3、诱导细胞的呼吸爆发;4、诱导细胞因子的转录,促使多种淋巴因子的释放; 5、诱导次级淋巴器官的发育; 6、刺激血管的生成; 7、刺激骨髓细胞的生成并抑制干细胞的功能; 8、参与肿瘤细胞的移动、侵袭和转移; 9、作为免疫调节剂上调T细胞和抗原提呈功能;10、促进细胞增殖;11、促进抗原特异性Th1和Th2克隆活化[5]。不同类型的趋化因子通过与相应受体结合而发挥作用。但部分趋化因子与受体结合的特异性不强,及一种趋化因子可与多种受体结合,而一种趋化因子受体也可与多种趋化因子结合,不过亲和力有所不同[6]。 3.趋化因子及其受体在肿瘤中的双向调节作用
白介素IL-17细胞因子及其受体家族研究进展 白介素-17(IL-17)主要由T辅助细胞TH17产生。IL-17可以直接或间接诱导多种细胞因子、趋化因子、炎症因子与抗微生物蛋白来识别介导自身免疫与慢性感染的靶基因,最近的研究已经证明,IL-17与肿瘤的发生密切相关。 白介素-17(IL-17)已经发现的成员有6个,分别就是:IL-17A、IL-17B、IL-17C、IL-17D、IL-17E(也被称为IL-25)与IL-17F。随着研究的深入,IL-17产生细胞除了TH17细胞外,还有很多其它类型的细胞可以产生,比如:巨噬细胞、树突状细胞、CD-T细胞、自然杀伤T(NKT)细胞、CD8+ T细胞、调节性T细胞(Tregs)、嗜中性粒细胞、肥大细胞、骨髓源性抑制细胞(MDSCs)与淋巴组织诱导物(LTi)细胞等,在上皮细胞、周细胞、平滑肌细胞与肿瘤细胞中也可产生白介素IL-17。在IL-17家族的6个成员中,IL-17A就是IL-17家族的原型,IL-17F与之同源性最高(50%),并且编码基因定位于染色体的同一区域6p12,其它与IL-17A同源性较差,只有16%-30%,且定位在不同的染色体上。但这些细胞因子在人、鼠种属间的保守性较高(62-80%)。IL-17家族成员以同源二聚体或异源二聚体的形式发挥功能。IL-17A、IL-17E、IL-17F就是重要的促炎症因子,而IL-17B、IL-17C、IL-17D的功能还尚待研究。 白介素IL-17受体(IL-17R)家族由5个成员组成:IL-17RA、IL-17RB、IL-17RC、IL-17RD、IL-17RE。IL-17R由27个氨基酸的N-末端信号肽、293氨基酸胞外结构域、21个氨基酸的跨膜结构域与525个氨基酸异常长的胞质尾巴构成的单程跨膜蛋白。IL-17受体家族成员之间可以组合成不同的复合物,如IL-17RA与IL-17RC复合体介导细胞对IL-17A与IL-17F的反应,IL-17RA与IL-17RB复合体介导细胞对IL-17E的反应。IL-17RA作为这个家族迄今为止最大的分子,编码的基因位于染色体22上,就是至少4个配体传递信号的通用亚基。其她受体的编码基因位于染色体3上。L-17RA广泛表达,特别就是在造血组织中表达水平高。 IL-17RB能结合IL-17B与IL-17E,它主要表达于各种内分泌组织及肾、肝与TH2细胞。 IL-17RD负调控FGF介导的Ras-MAPK及PI3K信号通路。人的IL-17RD也能抑制FGF依赖的ERK激活与FGF依赖的增殖,但鼠的IL-17RD却能结合TAK1激活MAP2K4-JNK信号通路。IL-17受体家族中被了解最少的成员就是IL-17RE,近来研究表明IL-17C可能就是它的配体。
趋化因子家族及其受体基础研究进展 趋化因子(Chemokine)是一类小分子碱性蛋白,主要的功能是能够趋化细胞定向移动。 目前已经发现的趋化因子有50多种,随着研究的深入,趋化因子及其受体的结构、功能及在体内的作用已经被众多的研究者发现。趋化因子及其受体的相互作用,可以参与多种生理功能,比如细胞的生长、发育、分化、凋亡和分布等,在病理过程中也具有重要作用,如炎症反应、病原体感染、创伤修复及肿瘤形成和转移等。 趋化因子一般由70-125个氨基酸组成,分子量较小(6-14KD)。按照一级肽链结构特点,其N端半胱氨酸残基的位置和数目可将趋化因子分为4个亚族:CC、CXC、C和CX3C(C为半胱氨酸,X为任意氨基酸)。四类趋化因子结构相似性较高,氨基酸序列具有一定的同源性。根据趋化因子的表达方式以及其在免疫系统中的作用,可以将他们分为两类:内环境稳定性趋化因子和炎症性趋化因子。内环境稳定性趋化因子主要在归巢场所表达,有着维持内环境稳态的功能,并且对淋巴细胞归巢及成熟有着明确的作用。炎症性趋化因子由受到刺激的细胞表达,如炎性细胞因子的诱导、细菌毒素或其它破坏内环境稳定的因素的刺激,主要功能是募集效应细胞,在协调天然和获得性免疫反应中起重要作用。 大多数的趋化因子属于CC和CXC两个亚族族。其中CC亚族有28个成员(CCL1-CCL28),主要对中性粒细胞、单核细胞、肥大细胞、树突细胞、NK细胞、T和B淋巴细胞等具有强 大趋化活性,比较重要的有:单核细胞趋化蛋白(MCP-1/CCL2)、巨噬细胞炎症蛋白(MIP/CCL3)、正常T细胞表达和分泌,活化时表达下降的因子(RANTES/CCL5)等;CXC亚族有17个成员(CXCL1-CXCL17),CXC亚家族主要作用于中性粒细胞,这个亚族比较重要的趋化因子有: 白细胞介素-8(IL-8/CXCL8)、γ干扰素诱生的单核因子(Mig/CXCL9)、γ干扰素诱生蛋白10(IP-10/CXCL10)、基质细胞来源因子1(SDF-1/CXCL12)等。另外,CXC亚家族根据其第1 个半胱氨酸前有无谷氨酸-亮氨酸-精氨酸序列(Glu-Leu-Arg)进一步分为ELR+和ELR-两类, 前者具有促进血管新生作用。C亚家族包含两个趋化因子XCL1和XCL2,主要表达于胸腺,作用于CD8+ T淋巴细胞。CX3C亚家族只有一个趋化因子CX3CL1,也称为不规则趋化因子(fractalkine)或神经元趋化因子(neurotactin),是唯一膜结合性趋化因子,主要作用于单核细胞和中性粒细胞。 趋化因子要发挥生物学作用,必须与相应的受体结合才行。趋化因子受体(Chemokine Receptor)属于G蛋白偶联受体,具有7个富含疏水氨基酸的α螺旋穿膜区结构,主要表达
第三章免疫细胞 Chapter 3 Immunocytes 第一部分教学内容和要求 一、目的要求 掌握:淋巴细胞的种类、T、B细胞膜表面分子及功能,T、B细胞的功能、抗原提呈细胞的种类和功能,NK细胞的功能;熟悉:淋巴细胞的分化发育,单核-巨噬细胞和NK细胞的表面受体;了解:TCR基因和重排。 二、教学内容 1.T淋巴细胞的分化发育、膜表面分子、亚群及其功能。 2.B淋巴细胞的分化发育、膜表面分子、亚群及其功能。 3.NK细胞的膜表面分子、功能;NK细胞识别和杀伤靶细胞的机制。 4.巨噬细胞、树突状细胞、B细胞和非专职性抗原提呈细胞的分布及其在免疫中所发挥的作用。 5.中性粒细胞、嗜酸粒细胞、嗜硷粒细胞、肥大细胞、红细胞和血小板等细胞在免疫应答中的作用。 第二部分测试题 一、选择题 (一)单项选择题(A型题) 1.可刺激B淋巴细胞增殖转化的刺激物 A.PWM B.PHA C.ConA D.MHC E.BCG 2.中性粒细胞在血循环中存活的时间 A.数小时 B.十几小时 C.数天 D.数周 E.数月 3.可刺激T细胞增殖的刺激物是 A.ConA B.MHC C.SPA D.AFP E.LPS 4.具有特异性杀伤功能的细胞 https://www.doczj.com/doc/041408252.html,K 细胞 B.巨噬细胞 C.中性粒细胞 D.细胞毒性T细胞 E.NK细胞 5.淋巴细胞增殖试验可用来检测 A.细胞免疫功能 B.体液免疫功能 C.淋巴细胞数量 D.抗原提呈功能 E.补体功能 6.既具有抗原加工提呈作用又具有杀菌作用的细胞 A.树突状细胞 B.巨噬细胞 C.中性粒细胞 D.B细胞 E.T细胞 7.NK细胞表面的杀伤细胞抑制受体可识别 A.自身组织细胞表面的糖类配体复合物 B.肿瘤细胞表面的糖类配体 C.自身组织细胞表面的MHC-Ⅰ类分子 D.自身组织细胞表面的MHC-Ⅱ类分子 E.表达于感染细胞表面的病毒蛋白 8.具有SRBC受体的细胞是 A.T 细胞 B.B细胞 C.肥大细胞 D.NK 细胞 E.巨噬细胞 9.含有T细胞百分率最高的部位是 A.胸导管 B.胸腺 C.脾脏 D.外周血 E.扁桃体 10.参与非特异性免疫作用的细胞是 A.CD4+Th1细胞 B.CD4+Th2细胞 C.γδT细胞 D.αβT细胞 E.CD8+Tc细胞 11.B细胞识别抗原的表面分子是 A.C3 受体 B.mIg C.SRBC 受体 D.EB病毒受体 E.HIV受体
15 细胞因子及其受体 免疫受体是由一个由固有免疫系统和适应性免疫系统叠加而成的免疫系统,又是一个弥散系统,在体内往复循环的免疫细胞之间没有固定的有线”连接。这样的一个系统有效运转有赖于不同细胞之间的有序分工合作,信息交换与密切协调。细胞因子(cytokine)是免疫细胞之间以及免疫细胞与其他组织之间相互交换的语言。所谓细胞因子是指是有免疫细胞或非免疫细胞(如血管内皮细胞,表皮细胞和成纤维细胞等)经刺激而合成分泌的一类生物活性分子,他们之间的信息交换与相互调节,参与免疫应答和炎症反应过程。15-1细胞因子的主要特点(General Characteristics Of Cytokines)内分泌素也具有相对分子质量小,浓度低等特点,能够远距离调解组织器官的功能。细胞因子与与内分泌素不同,他们不由专门腺体分泌,而是来自多种不同的组织和细胞,以近距离调节为主。虽然已经发现200余种细胞因子,从人类基因组计划的测序结果来看,还有更多的细胞因子将被发现,他们具有如下一些基本特征: (1)半衰期短,不在细胞内储存而是在被活化
后开始合成并且分泌的。 (2)多效(重叠)性(pleiotropism):多种细胞可以产生同一种细胞因子,一种细胞因 子可以对不同细胞发挥不同作用。 (3)丰裕性(redundant):两种以上的的细胞因子具有相同的或者相似的生物学作用的 现象比较常见。 (4)协同性(synergy):两种细胞因子同时作用于一个靶细胞的效应大于他们单独效应 之和,即为协同作用。 (5)拮抗性(antagonism):有是有两种细胞因子有相互抑制的作用,即为拮抗性。(6)网络性:细胞因子能够诱导或抑制其他细胞因子的合成,形成细胞因子功能和调节 网络。 (7)效应延迟:靶细胞对细胞因子的反应通常发生在几个小时内,需要新mRNA和蛋白质 分子的原位合成。 (8)效应范围:近距离作用为主。多数细胞因子在血液中是检测不到的,他们发挥作用 的方式以旁分泌(paracrine)和自分泌 (autocrine)为主,前者指其对临近细胞
细胞免疫的概念 凡是由免疫细胞发挥效应以清除异物的作用即称为细胞免疫。参予的细胞称为免疫效应细胞。目前认为具有天然杀伤作用的天然杀伤细胞(NK)和抗体依赖的细胞介导的细胞毒性细胞(antibody dependent cell-mediatedcytotoxicity,ADCC)如巨噬细胞(Mφ)和杀伤细胞(K)以及由T细胞介导的细胞免疫均属细胞免疫的范畴。前二类免疫细胞在其细胞表面不具有抗原识别受体,因此它们的活化无需经抗原激发即能发挥效应细胞的作用,故可视之为非特异性细胞免疫。而效应T细胞则具有抗原识别受体,因此它们必需经抗原激发才能活化发挥其效应细胞的作用,故可视之为特异性细胞免疫。 由T细胞介导的细胞的免疫有二种基本形式,它们分别由二类不同的T细胞亚类参与。一种是迟发型超敏性的T细胞(TDH,CD4+),该细胞和抗原起反应后可分泌细胞因子。这些细胞因子再吸引和活化巨噬细胞和其它类型的细胞在反应部位聚集,成为组织慢性炎症的非特异效应细胞。另一种是细胞毒性T细胞(TC,CD8+),对靶细胞有特异杀伤作用。 上述二种类型的效应T细胞的存在虽然均可经体外实验分别证实。但通常在体内反应过程中,二种类型的效应细胞均有不同程度的表现。 引起细胞免疫的抗原多为T细胞依赖抗原(TD抗原),与体液免疫相同,参与特异细胞免疫的细胞也是由多细胞系完成的。即由抗原呈递细胞(巨噬细胞或树突状细胞)、免疫调节细胞(TH和TS)以及效应T细胞(TDTH和TC)等。 在无抗原激发的情况下,效应T细胞是以不活化的静息型细胞形式存在。当抗原进入机体后,在抗原呈递细胞或靶细胞的作用下使静息型T细胞活化增殖并分化为效应T细胞。即由T细胞介导的细胞免疫应答也需经过抗原识别(诱导期)、活化与分化(增殖期)和效应期才能发挥细胞免疫作用。 由T细胞介导的主要细胞免疫现象有:①迟发型超敏性反应;②以胞内寄生物的抗感染作用;③抗肿瘤免疫;④同种移植排斥反应;⑤移植物抗宿主反应;⑥某些药物过敏症; ⑦某些自身免疫病。
龙源期刊网 https://www.doczj.com/doc/041408252.html, CaMKIV在免疫细胞中的作用 作者:彭雪峰游捷 来源:《中国医学创新》2011年第14期 基金项目:福建省自然科学基金(C0710017) 作者单位:350001 福建医科大学附属内分泌研究所 通讯作者:游捷 【摘要】钙调蛋白激酶(CaMK)IV是Ca2+信号转导过程中的一个关键激酶,主要表达在神经组织和免疫系统。研究表明,在经过一系列级联反应激活后,CaMKIV转位至细胞核,通过调节转录因子CREB、MEF2及AP-1等活性,参与调节T细胞发育和激活,树突状细胞 分化和存活,以及骨髓造血干细胞的维护。新近关于骨免疫学方面的研究显示,CaMKIV参与调节免疫应答,本文针对部分表达该蛋白的免疫细胞,探讨CaMKIV在免疫炎症中的作用。 【关键词】钙调蛋白激酶IV;炎症反应; T淋巴细胞;树突状细胞 Ca2+是一个通用而普遍存在的第二信使,广泛参与各种基础细胞进程,钙调蛋白(CaM)是Ca2+的一个主要受体,在所有真核细胞中表达。Ca2+与CaM结合形成复合体,使得CaM内部构象改变,进而可与许多不同靶酶相互作用,这些靶酶中较重要的是钙调蛋白激酶(CaMKs)家族,包括磷酸化酶激酶、肌球蛋白轻链激酶(MLCK)、CaMKⅠ、Ⅱ、Ⅲ和Ⅳ[1]。CaMKs家族目前研究较多的是CaMK Ⅱ和Ⅳ,主要在神经组织和免疫系统。 1 CaMKIV概述 1.1 基因和蛋白 CaMKIV主要表达于脑组织和胸腺,脾脏、卵巢和睾丸也有少量表达。在免疫系统中表达于T细胞、树突状细胞、造血干细胞,在B细胞及单核细胞中未见报道。编 码CaMKIV的基因由42 kb DNA组成,包括12个外显子和11个内含子,由于剪接差别和转 录起始位点的不同,能够产生多种mRNA。CaMKIV的分子量约为60 KDa,基本结构包括一个N-末端激酶区域,一个自动调整区域和一个重叠的CaM结合区域。CaMKIV蛋白包括α、β两种亚型,后者包含一个由28个氨基酸残基组成的N-末端扩展,其余结构基本相同[2]。 1.2 激活过程在细胞质中CaMKIV是一个由钙调蛋白激酶激酶(CaMKK)和蛋白磷酸酶2A(PP2A)组成的复合体,是无活性的。当胞内Ca2+浓度增加时,部分Ca2+结合CaM,然后Ca2+/CaM复合物结合CaMKIV,由于Ca2+/CaM的结合位点与PP2A相同,故而取代PP2A, 并且使得CaMKIV构象改变,进而使CaMKIV具备最基础的激酶活性,暴露出可被CaMKK 磷酸化的活性环。CaMKK磷酸化Thr200(在鼠类为Thr196)位点,使CaMKIV完全激活,之后Ser12-Ser13位点自发磷酸化,称为“自主激活”[3]。只有自主激活的CaMKIV才能转位至核内,参与基因转录的调控。此后,PP2A在细胞核内重新结合CaMKIV,并使活性环上的苏氨
NK细胞(Natural Killer Cell)又称自然杀伤细胞。属于大颗粒淋巴细胞,来源于骨髓,占外周血淋巴细胞总数的5%-10%,是机体重要的免疫细胞,具有广谱抗肿瘤细胞作用,其不依赖于抗原刺激作用,就可以非特异直接杀伤肿瘤细胞和病毒感染的靶细胞,对肺癌、肝癌、卵巢癌、食道癌、结肠癌、胃癌、宫颈癌、骨癌等均有效果,以NK细胞为中心的巨噬细胞,24小时加以监视,一旦发现癌细胞,就陆续加以清除。特别是对造血细胞来源的肿瘤细胞更为敏感。特别是对淋巴瘤和白血病细胞作用更为明显,因此,在机体免疫监视和早期抗感染免疫过程中起重要作用,是抗瘤免疫的第一线细胞,能迅速溶解某些肿瘤细胞。 人体的健康是由免疫系统来保证的,因此绝大多数的保健品都是为了提高机体免疫力的。NK细胞作为免疫系统中最重要的效应杀伤细胞,就像免疫系统中的巡警,时刻游弋在人体的血液中,一旦遇到入侵体内的细菌、病毒和体内产生的癌变、病变、衰老细胞,便启动免疫攻击和免疫稳定功能,当自己无法独立完成攻击和清除任务,就会发出信号,调集其他类型的免疫细胞来共同完成清除任务。 ·人体的健康是由免疫系统来保证的。免疫系统被医学专家誉为世界上最好的医生,就像一支不知疲倦的部队,24小时保护着我们的健康。 ·NK细胞作为先天免疫系统中最重要的效应细胞,是免疫系统在进化过程中所分化出的广谱性防御机制,对外清除病毒、细菌及其他有害物质,对内清除衰老、病变及癌变细胞,维护着我们机体的相对健康状态,被医学界誉为“人体第一道防线”。 ·NK细胞平时像巡警一样游弋在人体的血液中,行使着免疫监视功能,当遇到癌变,疾病及衰老的细胞时,便启动免疫攻击和免疫稳定功能。 ·NK细胞与我们的生活息息相关,它可以抑制病毒和细菌的入侵,清除体内癌变、病变及衰老细胞,具有延缓机体衰老的功能。 NK细胞功能在人生不同阶段呈现不同趋势和特征。科学研究发现,在人的一生中,NK细胞功能变化大致可分为五个阶段:
. 免疫系统的组成及作用 免疫系统具有以下功能: 抵抗各种细菌、病毒、污染物及疾病对人体造成的攻击。 清除新代谢的废物及免疫细胞与敌人打仗时遗留下来的病毒死伤尸体。 修补受损的组织器官,使其恢复原来的功能。 免疫系统的组成及作用
. . 免疫系统是一个由免疫细胞和有机器官构成的网状系统,它遍布整个人体,能自动对抗外来的有害物质,清除坏死细胞,并毁灭可能致癌的突变细胞。免疫系统的结构是繁多而复杂的,其主要的免疫器官有骨髓、扁桃体、胸腺、脾脏、盲肠、骨髓、淋巴结、淋巴管。这些关卡都是用来防堵入侵的毒素及微生物。 扁桃体位于咽部,是制造淋巴球与产生抗体的地方,人的淋巴球会对由口腔(食物及空气)进入的细菌产生反应。 胸腺属于中枢淋巴器官,位于胸腔顶部,是系统发展功能的中心,它负责训练免疫细胞让它们知道自己的责任。能供应具有免疫力的细胞到所有周边淋巴组织,也是淋巴干细胞增生并分化成T淋巴球之处。 脾脏位于腹腔内,近似卵圆形或指形是人体内最大的淋巴器官, 是血液的过滤器。脾脏常会因疾病而肿大,没有脾脏者,较易受到病菌的感染。 骨髓为白血球、红血球衍生与形成的主要器官,能产生定型与成熟的淋巴球,并将其释放进入其它淋巴器官及血液循环系统,进
行特定免疫功能。 盲肠最明显的特征是有大量的淋巴小结,它们会在此互相融合并伸入粘膜下层。 淋巴结为体内重要的防御关口。沿着淋巴管的途径分布,具有过. . 滤免疫反应、再循环的功能,还具有清除淋巴异物的功能。细菌进入淋巴结后,约有99%会陷在其中,并受摧毁。 淋巴管为淋巴液在体内特定部位循环的管道,负责将淋巴液由组织带入血液中。 B细胞和T细胞都来自于骨髓,但T细胞形成于胸腺,它的主要功能是消灭外来侵袭物。 成熟且经过启发的T细胞将演变为以下各种细胞: 辅助细胞:确认入侵者,发送讯号,召集B细胞及巨噬细胞进入备战状态;
II型细胞因子及其受体研究进展 目前已经发现的细胞因子有200多种,随着基因测序技术的快速发展,相信会有更多的因子被发现,并且随着细胞工程技术和蛋白重组技术的发展,一定会有更多的细胞因子重组蛋白被纯化制备。细胞因子功能多样,不同因子间可以相互作用,同一因子可以有不同的功能,因此,细胞因子构成了一个复杂的网络功能图。而细胞因子想要发挥作用,必须与相应的受体结合行。细胞因子与其受体结合后,会对细胞产生作用,可以刺激细胞生长增殖分化,调控机体免疫应答,为在细胞及分子水平研究某些自身免疫性疾病、肿瘤、免疫缺陷疾病的发病机理提供数据,为临床治疗和诊断提供指导依据。 细胞因子受体一般分成四个类型:Ⅰ型细胞因子受体(Type ⅠCytokine Receptor)、Ⅱ型细胞因子受体家族(Type ⅡCytokine Receptor)、TNF超家族受体以及趋化因子受体。在本文,将主要介绍Ⅱ型细胞因子及其受体的研究进展及其应用。 Ⅱ型细胞因子受体家族(Type ⅡCytokine Receptor ),也称干扰素受体家族(Interferon receptors family)。主要包含Ⅱ型白介素(IL-10,IL-19,IL-20,IL-22等)受体,Ⅰ型干扰素(IFNA,IFNB)受体和Ⅱ型干扰素(IFNG)受体。此类受体的结构特点治是在膜外区近氨基端含有四个保守半胱氨酸残基细无Trp-Ser-X-Trp-Ser序列,一般为具有高亲和力的异二聚体或多聚体。II型细胞因子受体的细胞外结构域由串联Ig样结构域组成,细胞内结构域通常与属于Janus激酶(JAK)家族的酪氨酸激酶相关。
趋化因子受体CCR研究概述 趋化因子要发挥生物学作用,必须与相应的受体结合才行。趋化因子受体(Chemokine Receptor)属于G蛋白偶联受体,具有7个富含疏水氨基酸的α螺旋穿膜区结构,主要表达于骨髓来源的各白细胞亚群,同时也表达于上皮细胞、血管内皮细胞、神经细胞等类型的细胞。趋化因子受体根据其结合的配体不同也分为4个亚家族:CCR、CXCR、XCR和CX3CR。其中CCR亚族已克隆11种(CCR1-CCR11),CXCR亚族6种(CXCR1-CXCR6),另俩个亚族分别各有1种:XCR1和CX3CR1。本文主要论述CCR的研究进展。 CCR1对多种人类CC趋化因子有反应,包括钙动员、腺苷酸环化酶抑制、细胞外酸化和趋化性增加。CCR1已经从多个种属获得克隆,如恒河猴、兔、小鼠和大鼠,并且这些序列之间存在高度的序列同源性,人和恒河猴的相似性为87%。人CCR1序列的大部分显著特征是保守的,其存在的变化主要限于N末端和细胞外环,可能参与配体结合的区域。人和小鼠CCR1蛋白以高亲和力结合人和小鼠CCL3和CCL5。通过靶向基因破坏研究和通过有效的CCR1拮抗剂的研究,提供了对CCR1的生理和病理生理作用的了解。 CCR2的cDNA可以编码两个蛋白质CCR2A和CCR2B。CCR2B是主要表达形式,并且在慢性炎症中起作用,特别是动脉粥样硬化和多发性硬化疾病。CCR2的mRNA可以在单核细胞、血源性树突状细胞、天然杀伤细胞和T淋巴细胞中检测到,但不能在嗜中性粒细胞或嗜酸性
粒细胞中检测到。抗体研究显示CCR2B在单核细胞
、活化记忆T细胞、B细胞和嗜碱性粒细胞中表达。CCR2通过与配体结合,产生许多生物学信号,包括腺苷酸环化酶的抑制、细胞内钙动员和细胞趋化性的增加。CCR2已从许多物种克隆,包括小鼠、大鼠和恒河猴。序列高度同源并且显示与人CCR2的78-95%氨基酸一致。小鼠CCR2特异性结合了具有高亲和力的与MCP-1和MCP-3。在诱发的腹膜巨噬细胞以及几只小鼠器官中检测到CCR2 mRNA表达。Spiropiperidine家族的成员是CCR2的拮抗剂之一,可以特异性的阻断CCL2与CCR2的结合,而不会抑制CXCR1、CCR1或CCR3与相应配体的结合。小鼠敲除CCR2的结果表明,CCR2在动脉粥样硬化形成中起重要作用。 CCR3主要在嗜酸性粒细胞发现,在调节这些细胞的迁移中起重要作用。近期研究结果显示CCR3中和单克隆抗体7B11,阻断嗜酸细胞活化趋化因子与CCR3转染子或嗜酸性粒细胞的结合。CCR3可能更多参与TH2反应,并在哮喘和特应性皮炎在内的过敏反应中发挥重要作用。CCR3由几组显示为HIV-1共同受体,并且在脑的小胶质细胞上表达,其可能潜在地促进HIV-1对AIDS的感染,从而导致艾滋病、痴呆等疾病。此外,CCR3也被证明在树突细胞上表达,并且可能在HIV-1感染中发挥作用。 CCR4最初是从人类嗜碱性白血病细胞系文库克隆出来的。许多研究表明CCR4是TH2淋巴细胞的选择性标记,并被T细胞受体激活上调。CCR4可在血液中的记忆T细胞检测到,参与全身性的淋巴细胞免疫反应。CCR4可能在肝损伤的病理生理学中起作用。 CCR5除了作为趋化因子受体外,还被证明在HIV-1的关键细胞进入共感受器的病理学上起作用。最近的三篇研究论文表明,人类CCR5基因(CCR5-32)中的32个碱基对缺失导致了氨基酸的移码并产生严重截短。CCR5也可以通过将修饰的CC趋化因子(intrakine)靶向内质网来阻断新合成的CCR5的表面表达而失活。CCR5配体还包括来自M-Tropic HIV-1菌株的gp120包膜糖蛋白,其需要CD4结合。CCR5拮抗剂包括Met-RANTES和AOP RANTES,它们都是N 末端修饰的RANTES蛋白,它们是有效的CCR5拮抗剂,并抑制巨噬细胞和淋巴细胞中M-tropic HIV-1毒株的感染。虽然CCR5在TH1和TH2系上均表达,但在几个TH2克隆中没有表达,其表达受到白介素IL-2的显著影响。这些结果表明,趋化因子受体基因表达的灵活程序可以控制效应T细胞的组织特异性迁移并发挥作用。 CCR6主要表达于脾脏、淋巴结、阑尾和胎肝。在各种白细胞亚群中,在淋巴细胞(CD4(+)和CD8(+)T细胞和B细胞)中检测到CCR6 mRNA,而在自然杀伤细胞、单核细胞或粒细胞中未检测到。CD4(+)和CD8(+)T细胞中CCR6 mRNA的表达被IL-2强烈上调。由活化的巨噬细胞、树突状细胞和内皮细胞产生的CCL20(LARC)是CCR6唯一的高亲和力配体和有效的激动剂。
免疫系统的组成及作用 免疫系统具有以下功能: 抵抗各种细菌、病毒、污染物及疾病对人体造成的攻击。 清除新代谢的废物及免疫细胞与敌人打仗时遗留下来的病毒死伤尸体。 修补受损的组织器官,使其恢复原来的功能。 免疫系统的组成及作用
免疫系统是一个由免疫细胞和有机器官构成的网状系统,它遍布整个人体,能自动对抗外来的有害物质,清除坏死细胞,并毁灭可能致癌的突变细胞。免疫系统的结构是繁多而复杂的,其主要的免疫器官有骨髓、扁桃体、胸腺、脾脏、盲肠、骨髓、淋巴结、淋巴管。这些关卡都是用来防堵入侵的毒素及微生物。 扁桃体位于咽部,是制造淋巴球与产生抗体的地方,人的淋巴球会对由口腔(食物及空气)进入的细菌产生反应。 胸腺属于中枢淋巴器官,位于胸腔顶部,是系统发展功能的中心,它负责训练免疫细胞让它们知道自己的责任。能供应具有免疫力的细胞到所有周边淋巴组织,也是淋巴干细胞增生并分化成T淋巴球之处。 脾脏位于腹腔内,近似卵圆形或指形是人体内最大的淋巴器官,是血液的过滤器。脾脏常会因疾病而肿大,没有脾脏者,较易受到病菌的感染。 骨髓为白血球、红血球衍生与形成的主要器官,能产生定型与成熟的淋巴球,并将其释放进入其它淋巴器官及血液循环系统,进行特定免疫功能。 盲肠最明显的特征是有大量的淋巴小结,它们会在此互相融合并伸入粘膜下层。 淋巴结为体内重要的防御关口。沿着淋巴管的途径分布,具有过
滤免疫反应、再循环的功能,还具有清除淋巴异物的功能。细菌进入淋巴结后,约有99%会陷在其中,并受摧毁。 淋巴管为淋巴液在体内特定部位循环的管道,负责将淋巴液由组织带入血液中。 B细胞和T细胞都来自于骨髓,但T细胞形成于胸腺,它的主要 功能是消灭外来侵袭物。 成熟且经过启发的T细胞将演变为以下各种细胞: 辅助细胞:确认入侵者,发送讯号,召集B细胞及巨噬细胞进入备战状态; 抑制细胞:随时观察战况,发送停战信号,避免免疫系统因工作过度而杀死自身成员; 自然杀手细胞:是免疫系统中的另一重要成员。是人体对抗癌症及肿瘤最强的防御武器。虽然自然杀手细胞较之其所对抗的癌细胞小很多,但它却能够粘附在癌细胞上,将癌细胞连根拔起。 昭妃博士说:“我虽然研究了许许多多的化学药品对付癌症,可是 到如今,我只能说唯一只有靠我们自身的免疫细胞才能把癌细胞毁灭掉。我发现免疫细胞具有这样的功能,我们称它为自然杀手,它不会毁灭我们身体里面任何一个好的细胞,它单单只会毁灭掉癌细胞。当自然杀手