间充质干细胞抗肝纤维化注射液的制作方法
- 格式:pdf
- 大小:148.41 KB
- 文档页数:10

临床医学研究与实践2021年2月第6卷第6期综述DOI :10.19347/ki.2096-1413.202106064基金项目:国家自然科学基金委员会资助项目(No.81903949);浙江省基础公益研究计划项目(No.LQ19H290004)。
作者简介:戚亚钦(1999-),女,汉族,浙江绍兴人。
研究方向:临床医学。
*通讯作者:方燕,E -mail :fangyan@.间充质干细胞(mesenchymal stem cells,MSCs )是具有自我更新能力并表现出多向分化潜能的成体非造血干细胞,广泛存在于骨髓、脂肪、外周血、脐带、胎儿组织、肌肉等中。
MSCs 具有来源丰富、获取方便、增殖率高等特点,已成为组织工程和临床研究的理想种子细胞[1]。
近年来,随着国内外对MSCS 的研究越来越深入,以MSCs 为基础的细胞移植替代治疗显现出良好的效果,MSCs 在临床试验中的安全性和有效性也已得到了更好的证明[2]。
1MSCs 的临床应用1.1MSCs 在神经系统疾病中的临床研究与应用目前,许多神经系统疾病如缺血、缺氧性脑病、恶性脑胶质瘤、神经系统退行性病变等仍无有效治疗方法,预后较差。
脑缺血后神经元的坏死将导致永久性神经功能缺陷,现有治疗手段尚不能逆转神经元和神经胶质细胞变性引起的神经功能障碍[3]。
MSCs 通过旁分泌作用,增加神经生长因子和脑源性神经营养因子的释放,促进神经障碍中丢失或损坏的神经元的恢复,减少神经元细胞的凋亡[4]。
MSCs 还可通过增加血管生成因子的分泌,促进病灶区新生血管生成;通过抑制血管内皮的凋亡和氧化应激,减少血管炎性损伤,增加脑血管的完整性[5]。
Xu 等[6]通过建立缺血缺氧性脑病的大鼠模型,证实MSCs 的脑内移植可减小脑梗塞体积,有效改善神经损伤,进而改善大鼠运动功能,为临床进一步研究提供实验依据。
但研究发现,缺血区局部不利的微环境使得能够迁移并存活在损伤区的MSCs 数量很少,严重限制了MSCs 的应用前景[7]。



·综述·间充质干细胞的免疫学特性与系统性红斑狼疮的治疗丘美兰陈建DOI :10.3877/cma.j.issn.1674-0785.2012.22.065作者单位:350025福州,福建医科大学福总临床医学院(丘美兰);南京军区福州总医院肾内科(陈建)通讯作者:陈建,Email :doctorj1@163.com 系统性红斑狼疮(SLE )是一种以多器官或多系统病变和血清中出现多种自身抗体为特征的自身免疫性疾病。
SLE 传统的治疗方案,如糖皮质激素联合免疫抑制剂治疗,虽能有效提高SLE 患者的长期存活率,但部分患者仍然复发,部分患者治疗无效,这类SLE 被称为难治性SLE ,而糖皮质激素及免疫抑制药物不良反应大,骨髓抑制和感染的发生率高。
SLE 目前尚无特效的治疗方法,近10年来大量实验与临床证据显示干细胞包括间充质干细胞(MSC )、[脐带血MSC (UC-MSC )或其他来源的MSC ]具有显著的组织与细胞修复、抗纤维化、免疫抑制与免疫调节功能。
MSC 在治疗SLE 上取得了一定的疗效,而理论上MSC 的生物学作用可用于治疗SLE 。
一、SLE 的发病机制SLE 有明显的免疫紊乱,其基本病理改变是免疫复合物介导的血管炎,具体机制尚未完全清楚,目前认为其发病是在多种因素作用下,引起机体免疫调节功能紊乱,出现造血干细胞、B 淋巴细胞、T 淋巴细胞、巨噬细胞和NK 细胞功能异常,细胞因子分泌异常,机体失去正常的免疫耐受性,发生自身免疫反应,产生自身抗体。
1.SLE 存在MSC 异常:研究发现,SLE 患者MSC 存在异常,表现为MSC 生长较正常缓慢,易衰老,传代过程中活力会逐渐丧失[1],因此有些学者认为,SLE 是一种MSC 异常性疾病[2]。
Papadaki 等[3]研究表明SLE 患者骨髓MSC 不能正常支持造血。
2.SLE 的发病与免疫紊乱:SLE 是一种免疫复合物病[4]。



!L"!骨髓间充质干细胞及其外泌体治疗终末期肝病的研究进展梁 悦1,2,胡永红1,2,刘 伟1,2,慕永平1,2,陈佳美1,2,刘 平1,2,31上海中医药大学附属曙光医院,上海市中医药研究院肝病研究所,上海201203;2肝肾疾病病证教育部重点实验室,上海市中医临床重点实验室,上海201203;3上海中医药大学交叉科学研究院,上海市中医药化学生物学前沿基地,上海201203摘要:终末期肝病是各种急慢性肝病的晚期阶段,病死率高,严重危害人民健康。
目前有效的治疗方法是肝移植,但囿于供体短缺、费用高昂等因素极大地限制了其临床应用。
近年来临床与基础研究表明,骨髓间充质干细胞及其外泌体在治疗终末期肝病上具有良好的临床应用前景。
本文就骨髓间充质干细胞及其外泌体在终末期肝病治疗中的作用机制与临床应用研究概况作一综述,期冀为进一步研究提供参考。
关键词:终末期肝病;间充质干细胞;外泌体;治疗学基金项目:国家自然科学基金重点项目(82130120);国家自然科学基金面上项目(81973613);中国博士后基金面上项目(2021M702218)Researchadvancesinbonemarrowmesenchymalstemcellsanditsexosomesintreatmentofend-stageliverdiseaseLIANGYue1,2,HUYonghong1,2,LIUWei1,2,MUYongping1,2,CHENJiamei1,2,LIUPing1,2,3.(1.InstituteofLiverDiseases,ShanghaiInstituteofTraditionalChineseMedicine,ShuguangHospitalAffiliatedtoShanghaiUniversityofTraditionalChineseMedicine,Shanghai201203,China;2.KeyLaboratoryofLiverandKidneyDiseases,MinistryofEducation,ShanghaiKeyLaboratoryofTraditionalChineseMedicine,Shanghai201203,China;3.ShanghaiAdvancedBaseofChemistryandBiologyofTraditionalChineseMedicine,InstituteofInter disciplinaryIntegrativeMedicineResearch,ShanghaiUniversityofTraditionalChineseMedicine,Shanghai201203,China)Correspondingauthors:CHENJiamei,cjm0102@126.com(ORCID:0000-0001-9808-9610);LIUPing,liuliver@vip.sina.com(ORCID:0000-0002-6152-4508)Abstract:End-stageliverdiseaseisthelatestageofvariousacuteandchronicliverdiseaseswithhighmortalityandseriouslythreatenspeople’shealth.Livertransplantationiscurrentlyaneffectivetreatmentmethodforthisdisease,butitsclinicalapplicationisgreatlylimitedbythefactorssuchasshortageofdonorsandhighcosts.Inrecentyears,clinicalandbasicstudieshaveshownthatbonemarrowmesenchy malstemcellanditsexosomeshavegoodclinicalapplicationprospectsinthetreatmentofend-stageliverdisease.Thisarticlereviewsthemechanismofactionandclinicalapplicationofbonemarrowmesenchymalstemcellanditsexosomesinthetreatmentofend-stageliverdis ease,soastoprovideareferenceforfurtherresearch.Keywords:End-StageLiverDisease;MesenchymalStemCells;Exosomes;TherapeuticsResearchfunding:KeyProjectofNationalNaturalScienceFoundationofChina(82130120);GeneralProjectofNationalNaturalScienceFoundationofChina(81973613);ChinaPostdoctoralScienceFoundation(2021M702218)DOI:10.3969/j.issn.1001-5256.2022.11.041收稿日期:2022-04-15;录用日期:2022-07-14通信作者:陈佳美,cjm0102@126.com;刘平,liuliver@vip.sina.com 终末期肝病(end-stageliverdisease,ESLD)以肝功能不能满足人体的正常生理需求为特征,是各种急、慢性肝损伤所致的晚期阶段,主要包括病毒性肝炎、酒精性肝病、自身免疫性肝炎等疾病引起的失代偿期肝硬化及肝衰竭。

本技术公开了骨髓间充质干细胞膜片的制备方法及其在治疗心肌缺血再灌注损伤上的应用。
利用密度梯度离心、细胞贴壁和细胞冻存的方法提取扩增细胞,可以获得足够量的未分化的较为单一的MSCs,增殖能力较强,纯度高,可以作为组织工程的种子细胞,为组织工程血管的构建提供依据。
而且较Reyes方法去除了免疫磁珠选择的步骤,在实际应用中减少了昂贵的费用,操作中减少了污染的机会。
权利要求书1.骨髓间充质干细胞膜片的制备方法,其特征在于,包括以下步骤:S1:用20ml注射器吸取10ml骨髓液,将细胞悬液贴壁缓慢注入到预置有等体积密度为1.077kg/L的人淋巴细胞分离液的试管内,使两者间形成清晰的界面;S2:以2500r/min离心20min,吸取中间的乳白色云雾状单核细胞层,PBS漂洗,1500r/min离心10min,弃上清,加入含15%FBSDMEM-LG培养液10ml,制成单细胞悬液;S3:以3×105/cm2密度接种于50ml培养皿内,置入37℃、5%CO2饱和湿度条件下培养,4d后首次半量换液,将未贴壁的细胞全部弃掉,以后每2~3d全量换液一次;S4:待细胞汇合成单层后,以0.25%胰蛋白酶(含0.02%EDTA)消化,即得到原代MSCs悬液,再以1×104/cm2的密度以1:2传代培养以形成细胞膜片;S5:倒置显微镜观察细胞生长;S6:绘制细胞生长曲线;S7:测定贴壁率并绘制贴壁率曲线。
2.根据权利要求1所述的骨髓间充质干细胞膜片的制备方法,其特征在于,在所述的S1中,注射器内含稀释的肝素钠2500U/ml约0.5ml。
3.根据权利要求1所述的骨髓间充质干细胞膜片的制备方法,其特征在于,在所述的S1中,骨髓液的吸取方法为选髂后上棘穿刺点,无菌条件下局部麻醉后骨髓穿刺针穿刺成功后拔出针芯,接含有5ml生理盐水和肝素(100U/ml)的10ml注射器穿刺抽取骨髓10ml。
4.根据权利要求1所述的骨髓间充质干细胞膜片的制备方法,其特征在于,在所述的S2中,用于离心的离心机为台式高速离心机。
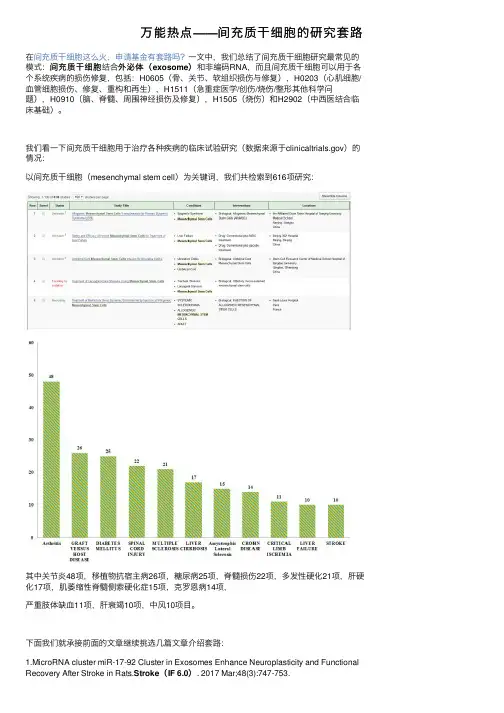
万能热点——间充质⼲细胞的研究套路在间充质⼲细胞这么⽕,申请基⾦有套路吗?⼀⽂中,我们总结了间充质⼲细胞研究最常见的间充质⼲细胞结合外泌体(外泌体(exosome)和⾮编码RNA,⽽且间充质⼲细胞可以⽤于各模式:间充质⼲细胞个系统疾病的损伤修复,包括:H0605(⾻、关节、软组织损伤与修复),H0203(⼼肌细胞/⾎管细胞损伤、修复、重构和再⽣),H1511(急重症医学/创伤/烧伤/整形其他科学问题),H0910(脑、脊髓、周围神经损伤及修复),H1505(烧伤)和H2902(中西医结合临床基础)。
我们看⼀下间充质⼲细胞⽤于治疗各种疾病的临床试验研究(数据来源于)的情况:以间充质⼲细胞(mesenchymal stem cell)为关键词,我们共检索到616项研究:其中关节炎48项,移植物抗宿主病26项,糖尿病25项,脊髓损伤22项,多发性硬化21项,肝硬化17项,肌萎缩性脊髓侧索硬化症15项,克罗恩病14项,严重肢体缺⾎11项,肝衰竭10项,中风10项⽬。
下⾯我们就承接前⾯的⽂章继续挑选⼏篇⽂章介绍套路:1.MicroRNA cluster miR-17-92 Cluster in Exosomes Enhance Neuroplasticity and Functional Recovery After Stroke in Rats.Stroke(IF 6.0). 2017 Mar;48(3):747-753.间充质⼲细胞治疗中风的功能和机制研究:间充质⼲细胞通过外泌体中miR-17-92调控PTEN 间充质⼲细胞治疗中风的功能和机制研究表达从⽽激活PI3K/Akt/mTOR 通路调控神经元可塑性,并促进中风后功能恢复。
2. Exosomes derived from miR-122-modified adipose tissue-derived MSCs increase chemosensitivity of hepatocellular carcinoma.J Hematol Oncol(IF 6.3). 2015 Oct 29;8:122.肝癌化疗敏感性的功能和机制研miR-122修饰的脂肪组织来源的间充质⼲细胞(AMSC)增加肝癌化疗敏感性究:AMSC通过外泌体将miR-122传递给肝癌细胞,通过调控肝癌细胞靶基因IGF1R,ADAM10和CCNG1表达增加肝癌细胞对化疗药5-FU的敏感性,同样的肿瘤注射miR-122也可增加肝癌细胞的5-FU化疗敏感性。

两种肝组织匀浆上清液诱导人脐带间充质干细胞向肝细胞分化的比较闫成;薛改;吴丽颖;刘建芳;侯艳宁【摘要】BACKGROUND:Previous studies have demonstrated that normal rat liver homogenate supernatant can induce human umbilical cord mesenchymal stem cels to differentiate into hepatocyte-like cels with partial hepatocyte functions. However, whether fibrotic liver homogenate supernatant can work or how the inducing effect is remains unclear. OBJECTIVE:To investigate the differentiation potential of human umbilical cord mesenchymal stem cels into hepatocytes under the normal liver and fibrotic liver microenvironment in vitro. METHODS:Liver fibrosis was induced in the SD rats by repeated intraperitoneal injections of 3% thioacetamide at a dose of 200 mg/kg body mass, twice a week for 4 weeks, and then fibrotic liver tissues and normal liver tissues were used to prepare liver homogenate supernatants. Passage 3 human umbilical cord mesenchymal stem cels were used and divided into standard control group (cels were cultured in DMEM/F12 with 10% fetal bovine serum), fibrotic liver homogenate supernatants group (cels were cultured in DMEM/F12 with 10% fetal bovine serum and 50 g/L fibrotic liver homogenate supernatants), normal liver homogenate supernatants group (cels were cultured in DMEM/F12 with 10% fetal bovine serum and 100 g/L normal liver homogenate supernatants). The morphological changes of the cels in each group were recorded under inverted microscope; the proteinlevels of CK18, AFP, CYP3A4, CYP2E1, CYP2D6 and TPH2 were evaluated using western blot assay. Furthermore, the concentration of albumin in the cels was measured. RESULTS AND CONCLUSION:After a 7-day inducement, the stem cels in liver homogenate supernatants groups lost their fusiform shape and changed into hepatocyte-like cels with the morphous of round shape. Compared with the standard control group, the hepatocyte-like cels in the two liver homogenate supernatants groups exhibited human hepatocyte biomarkers, CK18 and AFP. The standard control group cels could express a little amount of CYP2E1, while cels in the two liver homogenate supernatants groups could express CYP3A4, CYP2E1, CYP2D6, TPH2. Compared with the standard control group, the expression level of CYP2E1 in the two liver homogenate supernatants groups increased significantly (P < 0.01), and however, the relative levels of CYP3A4, CYP2E1, CYP2D6, TPH2 in the two liver homogenate supernatants groups showed no statistical significance (P > 0.05). At the same time, compared with the standard control group, the concentration of albumin in the two liver homogenate supernatants groups markedly increased (P < 0.01), but there was no difference between the two liver homogenate supernatants groups (P > 0.05). Experimental findings demonstrated that both of normal liver tissue and fibrotic liver tissue microenvironments could induce human umbilical cord mesenchymal stem cels to differentiate into hepatocyte-like cels. To achieve the same effect, compared with normal liver tissue, fibrotic liver tissue required lower concentrations, suggesting that fibrotic liver tissue microenvironment may be more conducive to differentiation ofumbilical cord mesenchymal stem cels into hepatocytes.%背景:前期研究证明正常大鼠肝组织匀浆上清液可诱导人脐带间充质干细胞定向分化为具有部分肝细胞功能的肝样细胞,而肝纤维化大鼠肝组织匀浆上清液的诱导可行性及与前者诱导效果的比较尚不明确.目的:比较正常肝组织及纤维化肝组织微环境诱导人脐带间充质干细胞向肝细胞分化的能力.方法:采用腹腔注射3%硫代乙酰胺生理盐水溶液(200 mg/kg,2次/周,共4周)的方法制备SD大鼠肝纤维化模型,取肝纤维化大鼠及正常大鼠肝脏制备肝组织匀浆上清.将第 3 代人脐带间充质干细胞进行分组诱导培养:①标准对照组:加入含体积分数为 10%胎牛血清的 DMEM/F12 培养基.②纤维化肝组织匀浆组:加入含体积分数为10%胎牛血清及50 g/L纤维化肝组织匀浆的DMEM/F12培养基.③正常肝组织匀浆组:加入含体积分数为10%胎牛血清及100 g/L正常肝组织匀浆的DMEM/F12培养基.诱导开始后于倒置显微镜下观察各组细胞形态学变化;取标准对照组及诱导7 d的匀浆组细胞采用Western Blot法检测CK18、AFP、CYP3A4、CYP2E1、CYP2D6、TPH2的表达情况,采用ELISA法测定各组细胞培养液中白蛋白水平.结果与结论:与标准对照组长梭形成纤维样细胞相比,诱导7 d时,肝纤维化匀浆组及正常匀浆组细胞形态变化明显,呈类圆形,胞体丰满.与标准对照组相比,两匀浆组细胞均可表达肝细胞标志物CK18和AFP.标准对照组细胞可表达少量CYP2E1,两匀浆组细胞表达CYP3A4、CYP2E1、CYP2D6、TPH2等肝细胞功能蛋白,且CYP2E1的表达量较标准对照组明显增加(P < 0.01),而两匀浆组间上述蛋白的相对表达量差异无显著性意义(P > 0.05).同时,两匀浆组细胞分泌白蛋白的能力较标准对照组亦明显增强(P < 0.01),两匀浆组相比差异无显著性意义(P > 0.05).实验结果显示正常肝组织和纤维化肝组织微环境均可诱导人脐带间充质干细胞向肝细胞分化,在达到相同诱导效果时,纤维化肝组织所需组织液浓度更低,提示纤维化肝组织微环境可能更有利于人脐带间充质干细胞向肝细胞分化.【期刊名称】《中国组织工程研究》【年(卷),期】2015(019)019【总页数】6页(P2993-2998)【关键词】干细胞;脐带脐血干细胞;肝纤维化;肝组织匀浆上清液;微环境;人脐带间充质干细胞;诱导分化;肝细胞;细胞色素P450酶;白蛋白【作者】闫成;薛改;吴丽颖;刘建芳;侯艳宁【作者单位】解放军医学院,北京市 100853;解放军白求恩国际和平医院药剂科,河北省石家庄市 050082;解放军白求恩国际和平医院药剂科,河北省石家庄市050082;解放军白求恩国际和平医院药剂科,河北省石家庄市 050082;解放军白求恩国际和平医院药剂科,河北省石家庄市 050082;解放军白求恩国际和平医院药剂科,河北省石家庄市 050082【正文语种】中文【中图分类】R394.2文章亮点:1间充质干细胞治疗肝纤维化的机制之一是其移植入血后可归巢至受损肝组织并向肝细胞分化,促进肝脏修复。

间充质干细胞产品及其外泌体在炎症性肠病治疗中的研究进展杨婧雯1,陈 芊1,单云龙1,刘嘉莉1,尉 宁1,2,王 婧2,王广基1*,周 芳1**(1中国药科大学药物代谢动力学重点实验室, 南京 210009;2江苏睿源生物技术有限公司, 南京211103)摘 要 炎症性肠病(inflammatory bowel disease, IBD )发病机制不明,特征为进行性和终身复发性消化道炎症反应。
尽管现阶段新的治疗药物和策略不断涌现,但治疗作用局限于单一的抗炎功能,在复杂黏膜免疫环境下易出现耐药导致治疗失败。
间充质干细胞(mesenchymal stem cells, MSCs )能定向归巢到结肠炎症部位,具有强大的免疫调节能力,可重塑肠道免疫环境和修复上皮屏障,为药物难治性患者的治疗提供了极具潜力的替代方案。
本文对MSCs 产品及其衍生的外泌体在临床上的应用、作用机制和工程化进行综述,以期为MSCs 及其外泌体产品用于IBD 的治疗提供参考。
关键词 炎症性肠病;间充质干细胞;外泌体;工程化中图分类号 R574 文献标志码 A文章编号 1000−5048(2024)01−0103−12doi :10.11665/j.issn.1000−5048.2023113001引用本文 杨婧雯,陈芊,单云龙,等. 间充质干细胞产品及其外泌体在炎症性肠病治疗中的研究进展[J]. 中国药科大学学报,2024,55(1):103 − 114.Cite this article as: YANG Jingwen, CHEN Qian, SHAN Yunlong, et al . Research progress on mesenchymal stem cell products and their exosomes in the treatment of inflammatory bowel disease[J]. J China Pharm Univ , 2024, 55(1): 103 − 114.Research progress on mesenchymal stem cell products and their exosomes in the treatment of inflammatory bowel diseaseYANG Jingwen 1, CHEN Qian 1, SHAN Yunlong 1, LIU Jiali 1, WEI Ning 1,2, WANG Jing 2, WANG Guangji 1*,ZHOU Fang 1**1Key Laboratory of Drug Metabolism and Pharmacokinetics, China Pharmaceutical University, Nanjing 210009;2Renocell Biotechnology Co., Ltd., Nanjing 211103, ChinaAbstract Inflammatory bowel disease (IBD), whose pathogenesis remains elusive, is a group of autoimmune diseases characterized by chronic, progressive, and lifelong inflammation of the digestive tract. The pathogenesis of IBD remains elusive. Although a number of drugs have been developed to treat IBD, their effects are merely anti-inflammatory. In addition, current treatments for IBD are easily susceptible to resistance in clinical practice.Mesenchymal stem cells (MSCs) have been reported to have the ability to migrate to the site of inflammation,with potent immunoregulatory effects, and to rebalance the immune microenvironment and restore the integrity of the epithelial barrier with significant value of application, particularly for patients who are refractory to classic medicines. In this paper, we reviewed the clinical applications, mechanisms and engineerable properties of MSC products and their exosomes to provide some reference for the use of MSCs and their exosomes in the treatment of IBD.Key words inflammatory bowel disease; mesenchymal stem cells; exosomes; engineering收稿日期 2023-11-30 通信作者 *Tel :************ E-mail :*************************Tel :************ E-mail :**************基金项目 国家自然科学基金项目(No. 82073928);南京市生命健康科技专项(No.202110006);细胞生态海河实验室创新基金项目(22HHXBSS00005);江苏省南京市联合资助项目(SBK2023070039)学报 2024, 55(1): 103 − 114103This study was supported by the National Natural Science Foundation of China (No. 82073928); the Nanjing Life and Health Science and Technology Program (No.202110006); the Haihe Laboratory of Cell Ecosystem Innovation Fund (22HHXBSS00005); and the Co-funded Programs in Nanjing, Jiangsu Province (SBK2023070039)炎症性肠病(inflammatory bowel disease, IBD)包括溃疡性结肠炎(ulcerative colitis, UC)和克罗恩病(Crohn's disease, CD),是由环境、免疫系统、肠道微生物组和个体遗传等因素的复杂互作引起的一类自身免疫性疾病,其一线治疗药物包括糖皮质激素、免疫抑制剂、抗生素和抗肿瘤坏死因子-α(tumor necrosis factor, TNF-α)疗法。