聚苯胺在一些有机溶剂中溶解性
- 格式:pdf
- 大小:272.90 KB
- 文档页数:5

聚苯胺综述1、引言导电高分子材料也称导电聚合物,其分子是由许多小的、重复出现的结构单元组成,即具有明显聚合物特征;若在材料两端加上一定电压,在材料中有电流通过,即具有导电的性质。
同时具备上述两条性质的材料,称为导电聚合物。
虽然都是导电体,但导电聚合物和常规金属导电体不同。
前者属于分子导电物质,后者是金属晶体导电物质。
因此,其结构和导电方式都不同。
高分子导电材料包括结构型高分子导电材料和复合型高分子导电材料两大类。
结构型导电高分子材料又称本征导电高分子,是指聚合物获得导电性能不是通过加入导电性物质,而是由其本身结构带来的。
如掺杂后的导电高分子聚合物:聚乙炔(PAc)、聚吡咯(PPy)、聚噻吩(PTh)、聚苯胺(PAn)、聚苯乙烯撑(PPV)等,这类聚合物大多是具有共轭π键结构的结晶聚合物,共轭双键可以通过电子转移的氧化还原反应变成高分子离子。
复合型导电高分子材料是将各种导电性物质(高效导电粒子或导电纤维)通过分散、层合、涂敷等工艺填充到聚合物基体中。
2、聚苯胺由于导电聚合物具有良好的电学、光学以及氧化还原特性在近20年里一直备受关注,在能源、电磁屏蔽和电致变色等领域有着广阔的前景。
自从1984年MacDiarmid在酸性条件下由苯胺单体获得具有导电性聚合物,聚苯胺已成为现在研究进展最快的导电聚合物之一。
原因在于聚苯胺具有以下诱人的独特优势:a)原料易得,合成简单;b)具有优良的电磁微波吸收性能、电化学性能、化学稳定性及光学性能;c)独特的掺杂现象;d)高的电导率;e)拥有良好的环境稳定性[1,2]。
聚苯胺被认为是最有希望在实际中得到应用的导电高分子材料。
以导电聚苯胺为基础材料,目前正在开发许多新技术,例如电磁屏蔽技术、抗静电技术、船舶防污技术、隐身技术、全塑金属防腐技术、太阳能电池、电致变色、传感器元件、二次电池材料、催化材料和防腐材料[3~11]。
3、聚苯胺的结构聚苯胺有多种结构,这是由反应条件决定的,它们之间的转化关系如下[12,13]:其中,聚苯胺最重要的存在形式是翠绿苯胺(EM,emeraldine),它具有导电性,通常可以在酸性条件下(如盐酸)通过化学氧化法制得,如果氧化剂过量,翠绿苯胺就被氧化成全氧化态聚苯胺(PNB,blue protonated pernigraniline),这种形态的聚苯胺可能具有导电性。

聚苯胺浅析作者:张艳来源:《科学与财富》2017年第30期一、概述一百多年聚苯胺就已经被发现,但只用作颜料,被称为“苯胺黑”。
1987年,人们广泛接受AG.MacDiarmid提出的苯式和醌式结构共存的模型。
依据氧化程度的不同,聚苯胺可以分为还原态、氧化态及本征态,且不同状态下的聚苯胺可以相互转化。
其中还原态和氧化态聚苯胺均为绝缘体,本征态聚苯胺在适当的掺杂方式下还具有导电性。
依据电导率的大小不同可将物质分为绝缘体、半导体、导体和超导体。
在20世纪70年代前还没有“导电高分子”的概念,人们一直将有机聚合物当作是绝缘体来使用。
直到1984年,人们首次发现对聚乙炔进行P型掺杂获得类似金属的导电性,这一传统观念才逐渐打破,随后人们继续研究开发了一系列的导电聚合物。
作为一种典型高分子材料,聚苯胺具有良好的导电性,且合成工艺简单,它的发现打破了高分子是绝缘体的传统观念,推动了导电高聚物领域的研究和发展。
聚苯胺以其良好的热稳定性、化学稳定性和电化学可逆性,优良的电磁微波吸收性能,潜在的溶液和熔融加工性能,原料易得,合成方法简便,还有独特的掺杂现象等特性,成为现在研究进展最快的导电高分子材料之一。
以其为基础材料,目前正在开发许多新技术,对聚苯胺的结构、物理化学性能、合成、掺杂、独特的光电磁性能、改性、用途等方面的研究已经取得了长足的进展。
二、聚苯胺的基本性质1.可溶性因为聚苯胺具有刚性链且链间存在很强的作用力,故溶解性能很差,其应用也被极大的限制。
目前,科学家,主要通过化学复合、结构修饰、乳液聚合等方法获得水溶性或可溶性的导电聚苯胺。
2.导电性导电性是聚苯胺重要的特性之一。
本征态的聚苯胺具有很低的电导率,但通过质子酸掺杂或氧化可以实现绝缘体与导体之间的相互转化,提高导电性。
聚苯胺的导电性受很多条件的干扰,如分子链结构、温度、湿度等。
3.光电性质及非线性光学性质聚苯胺还具有较显著的光电转换性。
作为一种P型半导体,其分子主链上含有许多共轭π电子,比较容易极化,不仅呈现快速响应的性质还具有较高的三阶非线性系数]。

聚苯胺的合成及表征(省市师学院550018)摘要:本实验采用氧化聚合法,以苯胺为单体,过硫酸铵为氧化剂,探究投料比、酸种类、温度对合成聚苯胺的影响,及本征态聚苯胺的溶解性影响因素。
用傅里叶红外光谱仪对聚苯胺参杂前后的结构变化进行了测试,讨论了不同条件对聚合物的影响。
同时探究不同条件下合成的聚苯胺的溶解性。
关键词:聚苯胺合成表征溶解性前言:聚苯胺( PANI) 具有多样结构,独特的掺杂机,良好的稳定性和原料价廉易得等优点,一直是高分子领域的研究热点,在诸多领域都有良好的应用前景目前应用最为广泛的合成聚苯胺的方法是MacDiarm id 等提出的水溶液化学氧化聚合法。
该法简便易行, 适合大批量工业生产, 但通过该法制备所得聚苯胺的分子链含有大量缺陷,产物电导率较低,因此对苯胺化学氧化法合成条件对产率的影响进行了探究。
1. 实验部分1.1 实验试剂及仪器苯胺(An)(分析纯,AR天津博迪化工股份)、过硫酸铵(APS)(分析纯,AR 天津市科密欧化学试剂)、盐酸(HCl,优级纯)、硫酸(H2SO4)、高氯酸(HClO4)、磷酸(H3PO4)、氨水(NH3·H2O)、四氢呋喃(分析纯AR,天津博迪化工股份)、N,N-二甲基甲酰胺(分析纯AR,光华科技股份)、二甲基亚砜(分析纯AR,光华科技股份)、恒温玻璃搅拌器、85-2恒温磁力搅拌器(金坛市城东新瑞仪器厂)、傅里叶TENSOR-27型红外光谱仪(KBr压片)1.2 聚苯胺的合成1.2.1 聚苯胺的性质溶解性——聚苯胺由于其链刚性和链间强相互作用,使它的可溶性极差,在大部分常用的有机溶剂中几乎不溶,仅部分溶于N,N-二甲基甲酰胺和N-甲基吡咯烷酮,这就给表征带来一定的困难,并且极限制了聚苯胺的应用。
通过结构修饰(衍生物、接枝、共聚)、掺杂诱导、聚合、复合和制备胶体颗粒等方法获得可溶性或水溶性的导电聚苯胺。
如在聚苯胺分子链上引入磺酸基团可得到水溶性导电高分子。

聚苯胺的主链上含有交替的苯环和氮原子,是一种特殊的导电聚合物。
可溶于N -甲基吡咯烷酮中。
聚苯胺随氧化程度的不同呈现出不同的颜色。
完全还原的聚苯胺(Leucoe meraldine碱)不导电,为白色,主链中个重复单元间不共轭;经氧化掺杂,得到Emeraldine碱,蓝色,不导电;再经酸掺杂,得到Emeraldine盐,绿色,导电;如果Emeraldine碱完全氧化,则得到Pernigraniline碱,不能导电。
聚苯胺具有优良的环境稳定性。
可用于制备传感器、电池、电容器等。
聚苯胺由苯胺单体在酸性水溶液中中经化学氧化或电化学氧化得到,常用的氧化剂为过硫酸铵(APS)。
中性条件下聚合的聚苯胺常常含有枝化结构。
苯胺的毒性较大,是致癌物质.由于聚苯胺的性能不稳定,贮存中会发生变化,所以,一般是在酸洗现场现用现配。
这种缓蚀剂的主要优点是合成工艺简单,水溶性较好,缓蚀效果也好。
缺点是所使用的原料(甲醛和苯胺)都具有一定的毒性,对人体有危害。
评论|2013-03-30 17:54热心网友聚苯胺(Polyaniline)一种重要的导电聚合物。
聚苯胺的主链上含有交替的苯环和氮原子,是一种特殊的导电聚合物。
可溶于N-甲基吡咯烷酮中。
聚苯胺随氧化程度的不同呈现出不同的颜色。
完全还原的聚苯胺(Leucoe meraldine碱)不导电,为白色,主链中个重复单元间不共轭;经氧化掺杂,得到Emeraldine碱,蓝色,不导电;再经酸掺杂,得到Emeraldine盐,绿色,导电;如果Emeraldine碱完全氧化,则得到Pernigraniline碱,不能导电。
聚苯胺具有优良的环境稳定性。
可用于制备传感器、电池、电容器等。
聚苯胺由苯胺单体在酸性水溶液中中经化学氧化或电化学氧化得到,常用的氧化剂为过硫酸铵(APS)。
中性条件下聚合的聚苯胺常常含有枝化结构。
聚苯胺是一种具有金属光泽的粉末,因分子内具有大的线型共轭π电子体系,其自由电子可随意迁移和传递,而成为最具代表性的有机半导体材料。
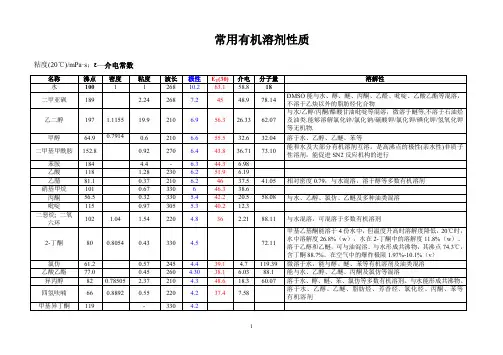
常用有机溶剂性质粘度(20℃)/mPa·s; —介电常数名称沸点密度粘度波长极性E T(30) 介电分子量溶解性水100 1 1 268 10.2 63.1 58.8 18二甲亚砜189 2.24 268 7.2 45 48.9 78.14 DMSO能与水、醇、醚、丙酮、乙醛、吡啶、乙酸乙酯等混溶,不溶于乙炔以外的脂肪烃化合物乙二醇197 1.1155 19.9 210 6.9 56.3 26.33 62.07 与水/乙醇/丙酮/醋酸甘油吡啶等混溶,微溶于醚等,不溶于石油烃及油类.能够溶解氯化锌/氯化钠/碳酸钾/氯化钾/碘化钾/氢氧化钾等无机物.甲醇64.9 0.7914 0.6 210 6.6 55.5 32.6 32.04 溶于水、乙醇、乙醚、苯等二甲基甲酰胺152.8 0.92 270 6.4 43.8 36.71 73.10 能和水及大部分有机溶剂互溶,是高沸点的极性(亲水性)非质子性溶剂,能促进SN2反应机构的进行苯胺184 4.4 - 6.3 44.3 6.98乙酸118 1.28 230 6.2 51.9 6.19乙腈81.1 0.37 210 6.2 46 37.5 41.05 相对密度0.79,与水混溶,溶于醇等多数有机溶剂硝基甲烷101 0.67 330 6 46.3 38.6丙酮56.5 0.32 330 5.4 42.2 20.5 58.08 与水、乙醇、氯仿、乙醚及多种油类混溶吡啶115 0.97 305 5.3 40.2 12.3二恶烷; 二氧六环102 1.04 1.54 220 4.8 36 2.21 88.11 与水混溶,可混溶于多数有机溶剂2-丁酮80 0.8054 0.43 330 4.5 72.11 甲基乙基酮能溶于4份水中,但温度升高时溶解度降低,20℃时,水中溶解度26.8%(w),水在2-丁酮中的溶解度11.8%(w)。
溶于乙醇和乙醚,可与油混溶。

101 概述自从1977年最早报道聚乙炔具有导电性以来,改变了科研界对聚合物的传统认识,激起了对本征导电聚合物研究探索热情,有关导电聚合物的制备、性能研究与应用受到了科学界的关注与重视。
但研究发现,大多数本征型导电聚合物的加工性能和机械性能不高,使其实际应用受到限制[1]。
到目前为止,研究最多的本征型导电聚合物有:聚对苯乙炔(PPV)、聚苯胺(PANI)、聚吡咯(PPY)、聚噻吩(PTH)、聚3,4-次乙二氧基噻吩(PEDOT)等。
而聚苯胺因原料易得,可加工性好,制备工艺相对简单,环境稳定性较好,最有可能获得大规模实际应用。
聚苯胺的导电性是由其结构决定的,与其他导电聚合物相比,聚苯胺分子结构最为特殊,其分子结构随着氧化程度的不同而不同。
目前,聚苯胺的分子结构被认为是由苯式-醌式结构单元共存的"首-尾"相接结构()。
分子链上存在苯二胺和醌二亚胺两种结构单元,它们主要取决于氧化剂的种类和浓度、苯胺单体的浓度、聚合反应的温度、反应时间等。
主链上y 值表示聚苯胺的分子的氧化-还原程度,不同的y 值对应不同的结构、组分、颜色及电导率。
由于导电聚苯胺具有特殊的结构,加之不同的掺杂机制,得到一系列可以互相转换的不同电子结构态,尤其独特的氧化-还原、质子交换性、催化性和光电转换性,使得聚苯胺在锂离子电池、超级电容器、燃料电池、金属防腐、电致变色等领域表现出来重要的应用价值。
本文重点对聚苯胺的制备方法进行研究。
2 导电聚苯胺的制备2.1 乳液聚合(emulsion polymerization )乳液聚合制备聚苯胺是将苯胺单体、表面活性剂、非极性或弱极性有机溶剂、水和质子酸混合,加入氧化剂引发聚合反应而得到。
表面活性剂(如十二烷基苯磺酸等质子酸)的加入是为了稳定乳化体系,形成均一稳定乳液。
研究发现,一般乳液聚合反应完成后,所得到的产物不能直接分离,因为聚苯胺和副产物同时存在于乳液体系中。
产物通过加入破乳剂(如丙酮)来破乳分离,然后收集、清洗[2]。

高聚物与有机溶剂溶度参数及有机溶剂溶解性对照表高聚物与有机溶剂溶度参数及有机溶剂溶解性对照表溶剂δ/103(J/m3)1/2 聚合物δ/103(J/m3)1/2 溶剂δ/103(J/m3)1/2戊烷14.4(13.8) 聚乙烯15.8~17.0 水47.9 正已烷14.9 聚丙烯16.6~16.8 氨水25环已烷16.8 聚氧化丙烯15.3~20.3 乙二醇32.1(29.0)正庚烷15.2 聚苯乙烯17.4~19.0 丙三醇33.8正辛烷15.4 聚甲基丙烯酸甲酯18.6(26.2) 环已醇23.3异辛烷14 聚氯乙烯19.2~19.8 甲醇29.7正壬烷15.7 聚丙烯酸甲酯19.8~21.3 乙醇26正癸烷15.9 聚偏二氯乙烯20.3~25.0 正丁醇23.3正十四烷16.3 氯磺化聚乙烯16.4~20.5 正戊醇 22.3~21.6丁二烯13.9 环氧树脂19.8~22.5 异戊醇19.6异戊二烯14.8 聚甲醛20.3~22.5 环已酮19苯18.7 尼龙-66 27.8 四氢呋喃19甲苯18.2 聚丙烯腈25.6~31.5 醋酸25.6(18.9)二甲苯17.9~18.4 酚醛树脂23.5 甲酸27.6乙苯18 聚三氟氯乙烯14.7~16.2 甲酸甲酯21.9氯苯19.4(19.8) 聚四氟乙烯12.7 乙酸乙酯18.6硝基苯20.5(19.6) 聚丁二烯16.6~17.6 甲基丙烯17.8乙醚15.7 天然橡胶16.2(16.7) 三乙胺14.9正已醇21.9 氯丁橡胶16.8~18.8 苯甲醛22.1正辛醇21.1 丁苯橡胶16.6~17.6 乙醛20.1正庚醇20.5 聚硫橡胶18.4~19.2 甲酰胺36.4苯胺16.1(24.3) 聚碳酸酯19.4~20.1 乙酰胺34.2丙烯腈21.4 丁基橡胶15.8 二乙酮18 DMF 24.8 聚醋酸乙酯19.2(22.5) 氰乙烯17.8 DMAC 22.7 丁腈橡胶19.4(18.9) 偏二氯乙烯17.6丙酮20.1(20.5) 聚硅氧烷19.2 氯丁二烯19丁酮19 二硝基纤维素21.5(23.5) 二硫化碳20.5苯乙烯17.7(18.8)醋酸纤维素22.3~23.3 二甲砜29.9二氯甲烷19.8(20.5) 聚氨基甲酸酯20.5 二甲亚砜27.4氯仿19 聚乙烯醇47.9(25.8) 萘20.3 四氯化碳17.6 乙丙橡胶16.2 溶纤剂19三氯乙烯18.8 聚二甲基硅氧烷14.9~15.5四氯乙烯19.1 聚对苯二甲酸乙二醇酯21.9(19.8)四氯乙烷21.3(19.4) 聚二甲基硅氧烷14.9~15.5溶剂名称沸点(101.3kPa)溶解性毒性甲胺-6.3 是多数有机物和无机物的优良溶剂,液态甲胺与水、醚、苯、丙酮、低级醇混溶,其盐酸盐易溶于水,不溶于醇、醚、酮、氯仿、乙酸乙酯中等毒性,易燃二甲胺7.4 是有机物和无机物的优良溶剂,溶于水、低级醇、醚、低极性溶剂强烈刺激性乙醚34.6 微溶于水,易溶与盐酸.与醇、醚、石油醚、苯、氯仿等多数有机溶剂混溶"麻醉性"戊烷36.1 与乙醇、乙醚等多数有机溶剂混溶低毒性二氯甲烷39.75 与醇、醚、氯仿、苯、二硫化碳等有机溶剂混溶"低毒,麻醉性强"溶剂石油脑与乙醇、丙酮、戊醇混溶较其他石油系溶剂大丙酮56.12 与水、醇、醚、烃混溶低毒,类乙醇1,1-二氯乙烷57.28 与醇、醚等大多数有机溶剂混溶低毒、局部刺激性氯仿61.15 与乙醇、乙醚、石油醚、卤代烃、四氯化碳、二硫化碳等混溶"中等毒性,强麻醉性"甲醇64.5 与水、乙醚、醇、酯、卤代烃、苯、酮混溶中等毒性,麻醉性四氢呋喃66 优良溶剂,与水混溶,很好的溶解乙醇、乙醚、脂肪烃、芳香烃、氯化烃"吸入微毒,经口低毒"己烷68.7 甲醇部分溶解,比乙醇高的醇、醚丙酮、氯仿混溶低毒"麻醉性,刺激性"1,1,1-三氯乙烷74 与丙酮、、甲醇、乙醚、苯、四氯化碳等有机溶剂混溶"低毒类"四氯化碳76.75 与醇、醚、石油醚、石油脑、冰醋酸、二硫化碳、氯代烃混溶氯代甲烷中"毒性最强"乙酸乙酯77.112 与醇、醚、氯仿、丙酮、苯等大多数有机溶剂溶解,能溶解某些金属盐"低毒,麻醉性"乙醇78.3 与水、乙醚、氯仿、酯、烃类衍生物等有机溶剂混溶"微毒类,麻醉性"丁酮79.64 与丙酮相似,与醇、醚、苯等大多数有机溶剂混溶"低毒,毒性强于丙酮"苯80.1 难溶于水,与甘油、乙二醇、乙醇、氯仿、乙醚、、四氯化碳、二硫化碳、丙酮、甲苯、二甲苯、冰醋酸、脂肪烃等大多有机物混溶"强烈毒性"环己烷80.72 与乙醇、高级醇、醚、丙酮、烃、氯代烃、高级脂肪酸、胺类混溶"低毒,中枢抑制作用"乙睛81.6 与水、甲醇、乙酸甲酯、乙酸乙酯、丙酮、醚、氯仿、四氯化碳、氯乙烯及各种不饱和烃混溶,但是不与饱和烃混溶"中等毒性,大量吸入蒸气,引起急性中毒"异丙醇82.4 与乙醇、乙醚、氯仿、水混溶微毒,类似乙醇1,2-二氯乙烷83.48 与乙醇、乙醚、氯仿、四氯化碳等多种有机溶剂混溶"高毒性、致癌涂"乙二醇二甲醚85.2 溶于水,与醇、醚、酮、酯、烃、氯代烃等多种有机溶剂混溶。

1 .二甲胺:有机物和无机物的优秀溶剂,溶于水、初级醇、醚、低极性溶剂,激烈刺激性。
2 .石油醚:不溶于水,与丙酮、乙醚、乙酸乙酯、苯、氯仿及甲醇以上高级醇混溶,与初级烷相像。
3 .乙醚:微溶于水,易溶与盐酸,与醇、醚、石油醚、苯、氯仿等多半有机溶剂混溶。
麻醉性4 .戊烷:与乙醇、乙醚等多半有机溶剂混溶,低毒性。
5 .二氯甲烷:与醇、醚、氯仿、苯、二硫化碳等有机溶剂混溶。
低毒性,麻醉性强7 .二硫化碳:微溶与水,与多种有机溶剂混溶。
麻醉性,强刺激性8 . 丙酮:与水、醇、醚、烃混溶。
低毒,类乙醇,但较大9 .1,1- 二氯乙烷:与醇、醚等大部分有机溶剂混溶。
低毒、局部刺激性10 .氯仿:与乙醇、乙醚、石油醚、卤代烃、四氯化碳、二硫化碳等混溶。
中等毒性,强麻醉性11.12. 甲醇:与水、乙醚、醇、酯、卤代烃、苯、酮混溶。
中等毒性,麻醉性四氢呋喃:优秀溶剂,与水混溶,很好的溶解乙醇、乙醚、脂肪烃、芳香烃、氯化烃。
吸入微毒,经口低毒。
13 .己烷:与甲醇部分溶解,与比乙醇高的醇、醚、丙酮、氯仿混溶。
低毒,麻醉性,刺激性14 .三氟代乙酸:与水、乙醇、乙醚、丙酮、苯、四氯化碳、己烷混溶,溶解多种脂肪族、芬芳族化合物。
15 .1, 1,1- 三氯乙烷:与丙酮、、甲醇、乙醚、苯、四氯化碳等有机溶剂混溶。
低毒类溶剂16 .四氯化碳:与醇、醚、石油醚、冰醋酸、二硫化碳、氯代烃混溶。
氯代甲烷中毒性最强。
17 .乙酸乙酯:与醇、醚、氯仿、丙酮、苯等大部分有机溶剂互溶,能溶解某些金属盐。
低毒,麻醉性18 .乙醇:与水、乙醚、氯仿、酯、烃类衍生物等有机溶剂混溶。
微毒类,麻醉性19 .丁酮:与丙酮相像,与醇、醚、苯等大部分有机溶剂混溶。
低毒,毒性强于丙酮20 .苯:难溶于水,与甘油、乙二醇、乙醇、氯仿、乙醚、四氯化碳、二硫化碳、丙酮、甲苯、二甲苯、冰醋酸、脂肪烃等大多有机物混溶。
激烈毒性21 .乙睛:与水、甲醇、乙酸甲酯、乙酸乙酯、丙酮、醚、氯仿、四氯化碳、氯乙烯及各样不饱和烃混溶,可是不与饱和烃混溶。

聚苯胺的合成及表征作者:杨政权学号:1108040540056同组人:卢香王梅周春林贵州师范学院2011级化本一班摘要本实验主要采用溶液制备聚苯胺;以苯胺为单体,过硫酸铵为氧化剂,在不同的投料比、不同的酸种类、酸浓度以及不同的温度下合成聚苯胺,用傅里叶红外光谱对聚苯胺参杂前后的结构进行了测试,讨论了酸参杂对聚合产物的影响。
探究不同有机溶剂对聚苯胺的溶解率。
关键词聚苯胺溶解性红外光谱绪论1826年,德国化学家Otto Unverdorben通过热解蒸馏靛蓝首次制得苯胺(aniline),产物当时被称为“Krystallin”,意即结晶,因其可与硫酸、磷酸形成盐的结晶。
1840年,Fdtzsche从靛蓝中得到无色的油状不同氧化态聚苯胺之间的可逆反应(3张)物苯胺,将其命名为aniline,该词源于西班牙语的anti(靛蓝)并在1856年用于染料工业。
而且他可能制得了少量苯胺的低聚物,1862年HLhetbey也证实苯胺可以在氧化下形成某些固体颗粒。
但由于对高分子本质缺乏足够的认知,聚苯胺的实际研究拖延了几乎一个世纪,直到1984年,MacDiarmid提出了被广泛接受的苯式(还原单元)-醌式(氧化单元)结构共存的模型。
随着两种结构单元的含量不同,聚苯胺处于不同程度的氧化还原状态,并可以相互转化。
不同氧化还原状态的聚苯胺可通过适当的掺杂方式获得导电聚苯胺。
聚苯胺有许多性能,如导实验内容电性、氧化还原性、催化性能、电致变色行为、质子交换性质及光电性质,最重要的是导电性及电化学性能。
由于导电高分子特殊的结构和的物化性能,使其在电子工业、信息工程、国防工程及其新技术的开发和发展方面都具有重大的意义。
其中因聚苯胺具有原料易得、合成工艺简单、化学及环境稳定性好等特点而得到了广泛的研究和应用。
1.1仪器与试剂仪器:85-2恒温磁力搅拌器(金坛市城东新瑞仪器厂)、HC210006低温恒温器(中国.重庆银河实验仪器有限公司)、红外光谱仪试剂:苯胺、过硫酸铵(分析纯)、盐酸(优级纯)、甲醇(分析纯)1.2聚苯胺的合成探究投料比对合成产率的影响(氧化剂1:1、1:1.5、1:2、1:3)在反应支口烧瓶中,加入蒸馏水50mL、0.1mL/L苯胺9.342g 、150mL 浓盐酸,剧烈搅拌下,滴加0 .5 mo l /L过硫酸铵的水溶液,反应温度为25 ℃, 反应立即发生,溶液呈黄绿色,滴加完毕后,在搅拌下反应24h,产物为墨绿色乳胶液。

各种聚合物的溶解度参数聚合物的溶解度参数是指聚合物在溶液中溶解的能力,即聚合物与溶剂之间相互作用的强弱程度。
不同种类的聚合物具有不同的化学结构和溶解特性,因此其溶解度参数也有所不同。
下面将介绍几种常见的聚合物的溶解度参数。
1.聚乙烯(polyethylene,PE):聚乙烯是一种由乙烯单体(C2H4)聚合而成的聚合物,可分为低密度聚乙烯(LDPE)和高密度聚乙烯(HDPE)。
LDPE在常见溶剂中溶解性较好,如乙酸乙酯、四氢呋喃等。
而HDPE溶解度较低,只能在强极性溶剂如氯仿、二氯甲烷中有限度的溶解。
2.聚丙烯(polypropylene,PP):聚丙烯是一种由丙烯单体(C3H6)聚合而成的聚合物。
聚丙烯溶解度较低,只能在一些溶剂中溶解,如四氢呋喃、二甲基甲酰胺等。
但在大多数非极性溶剂中,聚丙烯几乎不溶解。
3.聚苯乙烯(polystyrene,PS):聚苯乙烯是一种由苯乙烯单体(C8H8)聚合而成的聚合物。
聚苯乙烯在非极性溶剂中的溶解度较低,如甲苯、二氯甲烷等。
而在强极性溶剂如醇类、酮类等中,聚苯乙烯溶解度较好。
4.聚氨酯(polyurethane,PU):聚氨酯是一种由异氰酸酯和多元醇通过缩聚反应形成的聚合物。
聚氨酯具有较好的可溶性,可在多种溶剂中溶解,如酮类、醇类、芳香烃等。
但在极性溶剂如水中溶解度较低。
5.聚乙烯醇(polyvinyl alcohol,PVA):聚乙烯醇是由乙烯醇(C2H4O)单体聚合而成的聚合物。
聚乙烯醇在水中可完全溶解,具有良好的溶解度。
而在有机溶剂中的溶解度则较低,只能在一些溶剂中溶解,如甲醇、乙醇等。
6.聚丙烯酸(polyacrylic acid,PAA):聚丙烯酸是一种由丙烯酸(C3H4O2)单体聚合而成的聚合物。
聚丙烯酸具有较好的水溶性,在水中可溶解生成含酸性的溶液。
而在非极性溶剂中的溶解度较低。
以上是几种常见聚合物的溶解度参数的简介,不同聚合物的溶解度受到多种因素的影响,如溶剂的极性、聚合物的分子量、结构等。

聚苯胺的化学氧化聚合法,是在酸性水溶液中用氧化剂使苯胺单体氧化聚合。
化学氧化法能够制备大批量的聚苯胺,也是最常用的一种制备聚苯胺的方法。
化学氧化法合成聚苯胺主要受反应介质酸的种类及浓度、氧化剂的种类及浓度、单体浓度和反应温度、反应时间等因素的影响。
质子酸是影响苯胺氧化聚合的重要因素,它主要起两方面的作用:提供反应介质所需要的pH值和以掺杂剂的形式进入聚苯胺骨架赋予其一定的导电性。
苯胺化学氧化聚合常用的氧化剂有:过氧化氢、重铬酸盐、过硫酸盐、氯化铁等,所得聚苯胺性质基本相同。
也有用过硫酸铵和碳酸酯类过氧化物组成复合氧化剂制备聚苯胺的相关报道[4]。
以Fe2+为催化剂和H2O2为氧化剂可合成高溶解性的聚苯胺[5]。
过硫酸铵不含金属离子,后处理简便,氧化能力强,是最常用的氧化剂。
苯胺聚合是放热反应,且聚合过程有一个自加速过程。
如果单体浓度过高,则会发生暴聚,一般单体浓度在0.25~0.5mol/L为宜。
在一定的酸浓度范围内,聚合温度与聚苯胺的电导率无关,但与聚苯胺的分子质量有关。
随着聚合温度的降低,聚苯胺的分子质量升高,并且结晶度增加[6]。
聚合反应在装有搅拌器的三口瓶中进行,首先在经氮气置换且保护的三口瓶中,依次加入水、盐酸、苯胺,然后在搅拌下滴加过硫酸铵的盐酸水溶液。
在一定温度下聚合,将得到的产物过滤,用1mol/L的盐酸反复洗涤,然后水洗至滤液基本无色为止。
产物在60℃下,真空干燥48h,得到墨绿色掺杂态聚苯胺。
2.2 电化学聚合法电化学法制备聚苯胺是在含苯胺的电解质溶液中,选择适当的电化学条件,使苯胺在阳极上发生氧化聚合反应,生成粘附于电极表面的聚苯胺薄膜或是沉积在电极表面的聚苯胺粉末。
操作过程如下:氨与氢氟酸反应制得电解质溶液,以铂丝为对电极,铂微盘电极为工作电极,Cu/CuF2为参比电极,在含电解质和苯胺的电解池中,以动电位扫描法进行电化学聚合,反应一段时间后,聚苯胺便牢固地吸附在电极上,形成坚硬的聚苯胺薄膜。
简述不同酸掺杂聚苯胺的性能1.研究背景超级电容器是一种介于传统静电电容器和电池之间的绿色新型储能元件。
兼有传统电容器和二次电池的特性。
根据储存静电能量机理的不同,可以分为双电层电容器和赝电容电容器两大类。
超级电容器以其原理和结构上的特点,使其具有众多优点:长循环寿命大于105次;良好的功率密度;简单的原理和制备方式;可焊接,不存在像电池接触不牢固等问题;能够与二次电池结合做混合应用;充电速度快;瞬时电流大;低温性能优越等,目前在很多领域都受到广泛关注。
目前应用于超级电容器的电极材料主要有三类:碳材料[1]、过渡金属氧化物[2-3]和导电聚合物材料[4]。
其中导电聚合物材料由于制备方便,价格便宜,具有快速的掺杂和去掺杂能力,因此受到了广泛关注。
导电聚合物是由具有共轭π键的聚合物经过化学和电化学的掺杂而形成的,通过掺杂将部分电子从分子链中迁移出来从而使得电导率由绝缘体级别跃迁至导体级别。
导电聚合物除了具有高分子聚合物的一般的结构特点外还含有一价的对阴离子(P型掺杂)或对阳离子(N型掺杂)。
导电聚合物最引人注目的一个特点是其电导率可以在绝缘体—半导体—金属态(10-9到105S/cm)较宽的范围里变化。
这是目前其他材料所无法比拟的。
目前应用于超级电容器的导电聚合物主要由聚吡咯、聚苯胺和聚噻吩。
自上个世纪八十年代Macdiarmid在酸性条件发现了聚苯胺的导电性以来,在众多导电高分子的研究中,掺杂聚苯胺具有较高的室温导电率、可逆的氧化还原机质子掺杂特性、掺杂时伴随颜色变化及快速响应、较高的三阶非线性光学系数、良好的电学和磁学特性等[5-6];再加上良好的环境稳定性、较低的价格和简单的合成方法,是聚苯胺在商业中得到了广泛应用。
在二次电池、光电子器件、发光二极管、传感器、新型电磁屏蔽及吸波材料等诸多领域有很好的应用前景[7-8],因此聚苯胺是目前公认的最有应用潜力的导电高分子材料。
PAN掺杂一般通过化学掺杂、电化学掺杂、质子酸掺杂和物理掺杂等手段来实现。
文章编号:1000-582X(2002)02-0124-04导电高分子材料聚苯胺的研究进展马 利,汤 琪(重庆大学化学化工学院,重庆 400044)摘 要:结合导电高分子材料聚苯胺目前研究的现状,综述了聚苯胺的结构、特性,聚苯胺的电化学合成法及化学合成法的影响因数及最佳条件,聚苯胺的掺杂机制、无机酸掺杂和有机酸掺杂、二次掺杂,提高聚苯胺的溶解性和可加工性的方法以及聚苯胺的广泛用途。
指出了聚苯胺的发展方向和发展前景。
关键词:聚苯胺;掺杂;改性中图分类号:O63 文献标识码:A 聚合物一直被认为是绝缘体,但是自从1976年,美国宾夕法尼亚大学的化学家MacDiarmid领导的研究小组首次发现掺杂后的聚乙炔具有类似金属的导电性以后,人们对共轭聚合物的结构和认识不断深入和提高,逐渐产生了导电高分子这门新兴学科。
在随后的研究中逐步发现了聚吡咯、聚对苯撑、聚苯硫醚、聚噻吩、聚对苯撑乙烯撑、聚苯胺等导电高分子,由于导电高分子材料作为新兴不可替代的基础有机材料之一,几乎可以用于现代所有新兴产业及高科技领域之中,因此对导电高分子研究不仅具有重大的理论价值,而且具有巨大的应用价值。
在众多的导电高分子材料中,人们对聚乙炔的研究较早,也最为深入,但由于它的制备条件比较苛刻,且它的抗氧化能力和环境稳定性差,给它的实用化带来了极大困难。
而聚苯胺原料便宜,合成简便,耐高温及抗氧化性能良好,有较高的电导和潜在的溶液、熔融加工可能性,易成膜且膜柔软、坚韧等优点和具有优良的电致变色性,在日用商品及高科技等方面有着广泛的应用前景。
因此虽然聚苯胺于1984年才被Mac Diar mid等重新开发,却一跃成为当今导电高分子研究的热点和推动力之一,倍受人们的广泛关注。
在这十多年期间,国内外相关研究者们已对聚苯胺的结构、特性、合成、掺杂、改性等方面进行了较为深入的研究。
1 聚苯胺的结构与特性1.1 聚苯胺的结构MacDiarmid重新开发聚苯胺后,在固体13C-NMR 及IR研究的基础上提出聚苯胺是一种头-尾连接的线性聚合物,由苯环-醌环交替结构所组成,但这种结构和后来出现的大量实验数据相矛盾。