联碱法各工段流程图
- 格式:doc
- 大小:390.50 KB
- 文档页数:4



精锐教育学科教师辅导讲义学员编号:年级:高三课时数:3学员:辅导科目:化学学科教师:授课主题侯式制碱法原理和简单流程教学目的侯氏制碱法在高考中占有比较特殊的地位,出现的几率较大;常考的知识点是侯氏制碱法的原理、温度的选择、母液的成分、处理及与氨碱法的优劣比较,学生在温度的控制和母液的处理上出现的错误几率较大。
教学容1.【2013年高考6】与索尔维制碱法相比,侯德榜制碱法最突出的优点是()A.原料利用率高 B.设备少C.循环利用的物质多 D.原料易得2.【2012年高考八】碳酸氢铵是一种重要的铵盐。
实验室中,将二氧化碳通入氨水可制得碳酸氢铵,用碳酸氢铵和氯化钠可制得纯碱。
完成下列填空:41.二氧化碳通入氨水的过程中,先有________晶体(填写化学式)析出,然后晶体溶解,最后析出NH4HCO3晶体。
3.【2010年高考27】工业生产纯碱的工艺流程示意图如下:完成下列填空:1)粗盐水加入沉淀剂A、B除杂质(沉淀剂A来源于石灰窑厂),写出A、B的化学式。
A B2)实验室提纯粗盐的实验操作依次为:取样、、沉淀、、、冷却结晶、、烘干。
3)工业生产纯碱工艺流程中,碳酸化时产生的现象是。
碳酸化时没有析出碳酸钠晶体,其原因是。
内容回顾4)碳酸化后过滤,滤液D 最主要的成分是(填写化学式),检验这一成分的阴离子的具体方法是:。
5)氨碱法流程中氨是循环使用的,为此,滤液D 加入石灰水产生氨。
加石灰水后所发生的反应的离子方程式为: 滤液D 加石灰水前先要加热,原因是。
6)产品纯碱中含有碳酸氢钠。
如果用加热分解的方法测定纯碱中碳酸氢钠的质量分数,纯碱中碳酸氢钠的质量分数可表示为:(注明你的表达式中所用的有关符号的含义)4.【2005年高考五26(A )】我国化学侯德榜(右图)改革国外的纯碱生产工艺,生产流程可简要表示如下:(1) 上述生产纯碱的方法称,副产品的一种用途为。
(2) 沉淀池中发生的化学反应方程式是。
(3) 写出上述流程中X 物质的分子式。




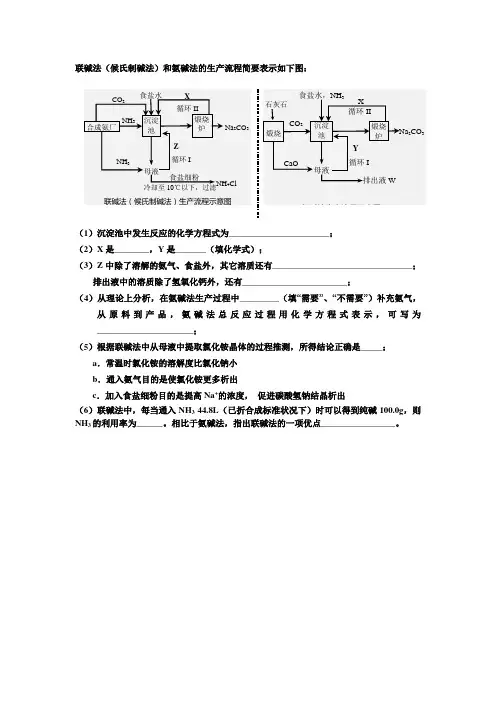
联碱法(候氏制碱法)和氨碱法的生产流程简要表示如下图:
(1)沉淀池中发生反应的化学方程式为_______________________;
(2)X是________,Y是_______(填化学式);
(3)Z中除了溶解的氨气、食盐外,其它溶质还有________________________________;
排出液中的溶质除了氢氧化钙外,还有________________________;
(4)从理论上分析,在氨碱法生产过程中_________(填“需要”、“不需要”)补充氨气,从原料到产品,氨碱法总反应过程用化学方程式表示,可写为______________________;
(5)根据联碱法中从母液中提取氯化铵晶体的过程推测,所得结论正确是_____;
a.常温时氯化铵的溶解度比氯化钠小
b.通入氨气目的是使氯化铵更多析出
c.加入食盐细粉目的是提高Na+的浓度,促进碳酸氢钠结晶析出
(6)联碱法中,每当通入NH3 44.8L(已折合成标准状况下)时可以得到纯碱100.0g,则NH3的利用率为______。
相比于氨碱法,指出联碱法的一项优点_________________。

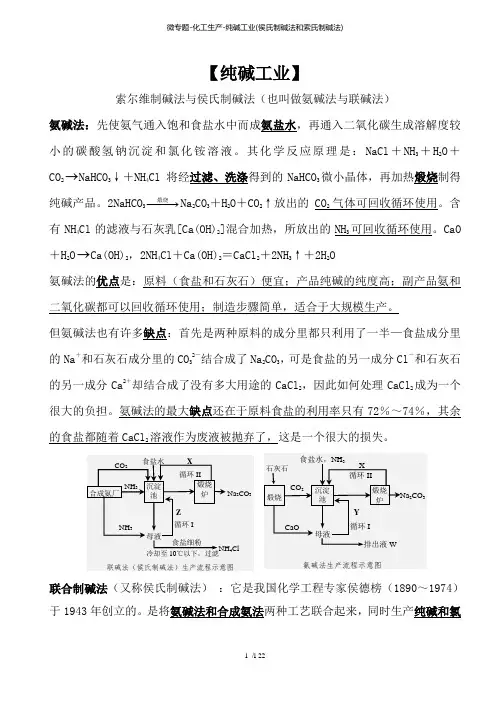
【纯碱工业】索尔维制碱法与侯氏制碱法(也叫做氨碱法与联碱法)氨碱法:先使氨气通入饱和食盐水中而成氨盐水,再通入二氧化碳生成溶解度较小的碳酸氢钠沉淀和氯化铵溶液。
其化学反应原理是:NaCl +NH 3+H 2O +CO 2→NaHCO 3↓+NH 4Cl 将经过滤、洗涤得到的NaHCO 3微小晶体,再加热煅烧制得纯碱产品。
2NaHCO 3−−−→煅烧Na 2CO 3+H 2O +CO 2↑放出的CO 2气体可回收循环使用。
含有NH 4Cl 的滤液与石灰乳[Ca(OH)2]混合加热,所放出的NH 3可回收循环使用。
CaO +H 2O →Ca(OH)2,2NH 4Cl +Ca(OH)2=CaCl 2+2NH 3↑+2H 2O氨碱法的优点是:原料(食盐和石灰石)便宜;产品纯碱的纯度高;副产品氨和二氧化碳都可以回收循环使用;制造步骤简单,适合于大规模生产。
但氨碱法也有许多缺点:首先是两种原料的成分里都只利用了一半—食盐成分里的Na +和石灰石成分里的CO 32-结合成了Na 2CO 3,可是食盐的另一成分Cl -和石灰石的另一成分Ca 2+却结合成了没有多大用途的CaCl 2,因此如何处理CaCl 2成为一个很大的负担。
氨碱法的最大缺点还在于原料食盐的利用率只有72%~74%,其余的食盐都随着CaCl 2溶液作为废液被抛弃了,这是一个很大的损失。
联合制碱法(又称侯氏制碱法) :它是我国化学工程专家侯德榜(1890~1974)于1943年创立的。
是将氨碱法和合成氨法两种工艺联合起来,同时生产纯碱和氯化铵两种产品的方法。
原料是食盐、氨和二氧化碳(合成氨厂用水煤气制取氢气时的废气,其化学反应原理是:C+H2O→CO+H2 CO+H2O→CO2+H2)联合制碱法包括两个过程:第一个过程与氨碱法相同,将氨通入饱和食盐水而成氨盐水,再通入二氧化碳生成碳酸氢钠沉淀,经过滤、洗涤得NaHCO3微小晶体,再煅烧制得纯碱产品,其滤液是含有氯化铵和氯化钠的溶液。

联碱工艺流程简介联碱生产按工序可分为碳滤、压缩、煅烧、重灰、重灰包装、结晶、制冷、干铵、干铵包装9个工序。
一:碳滤工序碳滤工序包括碳化、过滤、综合回收几个过程。
碳化过程碳化过程是利用氨母液II在碳化塔中吸收CO2生成NaHCO3结晶同时生成NH4Cl的过程。
碳化塔里的反应可用方程式NaCl+NH3+CO2+H2O NaHCO3 +NH4Cl来表示。
液相流程用方框图表示为:碳化尾气中含有大量的气氨,需经过综合回收后才能排放;其气相流程可用以下方框图表示:碳化过程是一个放热反应过程,反应过程中有大量的反应热需要移走;本工艺选用循环水冷却,下进上出间接换热闭路循环,在此不做介绍。
碳化取出液经取出槽至过滤机,气相里同样含有大量的气氨需经引风机引至净氨塔净氨后放空;过滤机上方以及MI桶放空气体同时净氨后放空。
过滤过程过滤过程是利用真空过滤原理将碳化取出液里的NaHCO3结晶分离出来,同时利用洗水降低NaHCO3里的NaCl含量;滤液去MI桶,NaHCO3结晶去煅烧;过滤尾气经净氨后去压缩工序。
用方框图可表示为:综合回收过程综合回收主要是回收碳化、过滤尾气及煅烧冷凝液里的氨;同时实现用水的回收利用。
煅烧冷凝液回收可用以下方框图表示。
碳化尾气经综合回收后放空、过滤尾气经综合回收后去压缩工序;其回收流程可用以下方框图表示:二、压缩工序压缩工序包括压缩和真空两个环节;压缩是利用压缩机将合成送过来的含98.5%和68.77%的CO2以及回收的煅烧炉气压缩、冷却后分中、下段送入碳化塔。
可用以下方框图表示。
真空环节是利用真空机抽吸过滤尾气放空,起到使过滤机连续稳定运行的作用。
三、煅烧工序煅烧工序使用蒸汽在煅烧炉内加热碳化工序送过来的NaHCO3结晶使之分解生成Na2CO3成品同时对炉气进行回收洗涤的过程。
在煅烧炉内发生以下化学反应: 2 NaHCO3 Na2CO3 + H2O +CO2 其流程可用以下方框图表示:因煅烧炉气中含有大量的CO2气、氨气及碱尘,CO2气和氨气是联碱生产的原料气;碱尘回收及是产品;而这些气体如不加以回收不光对环境造成污染,还增加生产成本。
简述联合制碱法的工艺流程联合制碱法可是个超有趣的化学工艺呢!联合制碱法啊,它有自己独特的一套流程。
它的原料主要是食盐、氨和二氧化碳。
那这些原料怎么开始它们的奇妙之旅呢?咱们先说说氨。
氨在这个过程中可起着很重要的作用呢。
氨先被通入饱和的食盐水里面。
这个时候啊,溶液就发生了很神奇的变化。
会形成一种氨化的饱和食盐水。
这就像是给溶液施了魔法一样,让它具备了特殊的性质。
接下来就轮到二氧化碳出场啦。
二氧化碳被通入到刚才形成的氨化饱和食盐水中。
这一进去呀,就会发生化学反应。
这个反应可不得了,会生成碳酸氢钠沉淀。
你能想象到吗?溶液里突然就出现了小颗粒一样的碳酸氢钠沉淀,就像变魔术似的。
碳酸氢钠沉淀在这个过程里就像是个调皮的小客人,突然冒出来了。
然后呢,要把碳酸氢钠沉淀过滤出来。
这就好比把调皮的小客人从一群小伙伴里挑出来一样。
把碳酸氢钠沉淀过滤出来之后,就可以对它进行加热了。
加热后的碳酸氢钠会分解呢,就像小客人变身了一样,变成了碳酸钠。
碳酸钠可是个很有用的东西哦,我们平常用的很多东西里都有它的身影。
那溶液里剩下的东西也没被浪费哦。
溶液里还含有氯化铵呢。
氯化铵也有它自己的用途。
可以通过一些后续的处理,把氯化铵分离出来。
这样整个联合制碱法的流程就差不多完成啦。
你看,联合制碱法的这个流程就像是一场精心编排的舞台剧。
每个原料都像舞台上的演员,在不同的环节发挥着自己的作用。
氨就像个开场的小引子,把整个故事拉开序幕。
二氧化碳一进来,就和氨以及食盐水共同演绎出碳酸氢钠沉淀这个小高潮。
然后把碳酸氢钠沉淀挑出来加热,这就像是给这个小高潮来了个后续的精彩延续。
最后剩下的氯化铵也能找到自己的归宿。
整个流程充满了化学的奇妙和智慧,是不是很有趣呢?而且啊,联合制碱法还有很多优点呢。
它不像一些老的制碱方法会有很多浪费或者产生很多污染。
它是一种比较环保和高效的制碱方法。
这就像是一个聪明的工匠,用最少的材料做出最好的东西,还不把周围环境弄得乱七八糟的。