n2的电子式和结构式
- 格式:docx
- 大小:11.77 KB
- 文档页数:1

化学用语作者:张炳腾来源:《广东教育·高中》2011年第12期化学用语是富有特色的化学语言,它贯穿于化学的始终,是化学试题的重要组成部分。
正确理解和规范使用化学用语是《考纲》的要求。
原子结构示意图、电子式、结构简式的书写及正误判断,化学方程式的书写,质量守恒定律的应用等都是历年高考的热点。
以新知识介绍为载体,考查对化学用语的理解和规范使用将是高考的命题模式。
一、表示物质组成的化学用语1.元素符号、离子符号。
(1)元素符号:元素是原子核里质子数(即核电荷数)相同的一类原子的总称。
每一种元素都有一个国际上统一的符号,它既可以表示一种元素,又可以表示这种元素的一个原子。
如Cl既可以表示氯元素,又可以表示一个氯原子。
(2)离子符号:带电的原子或原子团称为离子。
用以表示各种离子的符号称为离子符号。
如Fe2+(二价铁离子)、Fe3+(三价铁离子)、NH4+(铵根离子)、O2-(氧离子)、O22-(过氧根离子)、HCO3-(碳酸氢根离子)、MnO4-(高锰酸根离子)、AlO2-(偏铝酸根离子)等。
2. 原子结构示意图。
3. 元素的化合价。
化合价是指一种元素一定数目的原子与其他元素一定数目的原子化合的性质。
同种元素因其存在形式不同,其化合价有所不同。
①单质中元素的化合价为零。
②化合物中,元素正、负化合价的代数和为零,且金属元素为正价。
对于离子化合物,元素化合价的数值就等于该元素的一个原子得失电子的数目。
化合价的正负与离子所带电荷一致。
对于共价化合物,元素化合价的数值就等于该元素的一个原子跟其他元素的原子形成共用电子对的数目。
化合价的正负由共用电子对的偏移来决定的。
共用电子对偏向哪一种原子哪一种元素就显负价,共用电子对偏离哪一种原子哪一种元素就显正价。
③一般来说,非金属元素与氢元素化合时,非金属元素显负价;非金属元素与氧元素化合时,非金属元素显正价。
【例1】国际上已禁止民用产品使用石棉制品,避免人体吸入石棉纤维而诱发肺病。

课时作业5氮的固定1.下列反应属于氮的固定的是()①N2和H2在一定条件下合成NH3②NO2和H2O反应生成HNO3和NO③Mg在N2中燃烧生成Mg3N2④NO被空气氧化为NO2 A.①②B.②③C.①③D.①④2.Murad等三位教授最早提出NO在人体内有独特的功能,近年来此项研究有很大进展,因此这三位教授荣获了1998年诺贝尔生理学及医学奖。
关于NO的下列叙述,不正确的是()A.NO可以是某些含低价N物质氧化的产物B.已知亚硝酸钠的化学式是NaNO2,则NO不是亚硝酸的酸酐C.NO可以是某些含高价N物质还原的产物D.NO是红棕色气体3.自然界的氮循环如图所示,下列说法不正确的是()A.①中N2与O2反应生成NOB.②中合成氨属于人工固氮C.③中氮元素被氧化D.氧元素参与了氮循环4.下列叙述中正确的是()A.N2既可以和O2反应,又可以和H2反应,因此N2的化学性质很活泼B.在NO2和H2O的反应中,NO2是还原剂,H2O是氧化剂C.雷雨时,发生氮的固定变化可增加土壤中硝酸盐类氮肥的含量D.NO可用向上排空气法收集5.下列关于实验室收集NO和NO2气体的方法中,正确的是() A.都是排水法B.都用向上排空气法C.NO用向上排空气法,NO2用排水法D.NO用排水法,NO2用向上排空气法6.上世纪80年代后期人们逐渐认识到,NO 在人体内起着多方面的重要生理作用。
下列关于NO 说法错误的是( )A .NO 是具有刺激性的红棕色气体B .NO 是汽车尾气的有害成分之一C .NO 在人体的血管系统内具有传送信号的功能D .NO 能够与人体血红蛋白结合,造成人体缺氧中毒7.在常温下,向盛满水并倒置于水槽中的试管里先后通入4 mL NO 2、4 mL NO 、5 mL O 2,经过一段时间后,试管里剩余的气体有( )A .NOB .O 2C .NO 2和O 2D .NO 和O 28.(双选)如图所示,试管中盛装的是红棕色气体,当倒扣在盛有水的水槽中时,试管内水面上升,但不能充满试管,当向试管内鼓入氧气后,可以观察到试管中水柱继续上升,经过多次重复后,试管内完全被水充满,原来试管中盛装的可能是什么气体( )A .可能是N 2与NO 2的混合气体B .可能是O 2与NO 2的混合气体C .可能是NO 与NO 2的混合气体D .只可能是NO 2一种气体9选项 原因结果 A植树造林 温室效应 B SO 2和NO 2的大量排放酸雨 C汽车尾气的排放 光化学烟雾 D 含氮、磷等元素的生活废水的大量排放赤潮 2使之转化为无污染的物质。

第四讲氮及氮的化合物(一)氮1. 氮元素的存在既有游离态又有化合态。
它以双原子分子( N2)存在于大气中,约占空气总体积的78%或总质量的75%氮是生命物质中的重要组成元素,是构成蛋白质和核酸不可缺少的元素。
是农作物生长所必需的元素.充足的氮肥使植物枝叶茂盛.叶片增大,从而提高农作物的产量和质量。
2. 氮气的结构和性质(1)物理性质纯净的氮气是一种无色、无味、密度比空气稍小的气体,熔点为—209.86 'C。
沸点为—195.8 'C,难溶于水。
(思考N2的收集方法?)(2)______________________________ 结构:电子式为:____ 结构式为,氮氮叁键的键能高达946kJ • mol—1,键能大,分子结构稳定,化学性质不活泼。
(3)化学性质常温下,Nb的化学性质很不活泼,可代替稀有气体做保护气,但在高温、放电、点燃等条件下,Nb能与HL、O2等发生化学反应。
①NL+3H 謁益隈2NH (可逆反应)是工业上合成氨的反应原理。
②与C2反应:.「3. 氮气的用途与工业制法(1 )氮气的用途:合成氨;制硝酸;用作保护气;保护农副产品;液氮可作冷冻剂。
(2)氮气的工业制法:工业上从液态空气中,利用液态氮的沸点比液态氧的沸点低加以分离而制得氮气。
4. 氮的固定将空气中游离的氮气转变为氮的化合物的方法,统称为氮的固定。
氮的固定有三种途径:(1 )生物固氮:豆科作物根瘤菌将(2)自然固氮:天空中打雷闪电时,N2转化为化合态氮。
N2转化为NQ M+02放电2NQ(3)工业固氮:在一定的条件下,(二)氮的氧化物N2和H2人工合成氨。
N+3H 穿扯冃人2NH (可逆反应)1 2 3 4 5各种价态氮氧化物:N(N2O)、N(NO、N(MC)、N( NO、NbC)、N(N2C),其中N2Q和NLC5分别是HNC 和HNC的酸酐。
气态的氮氧化物几乎都是剧毒性物质,在太阳辐射下还会与碳氢化物反应形成光化学烟雾。
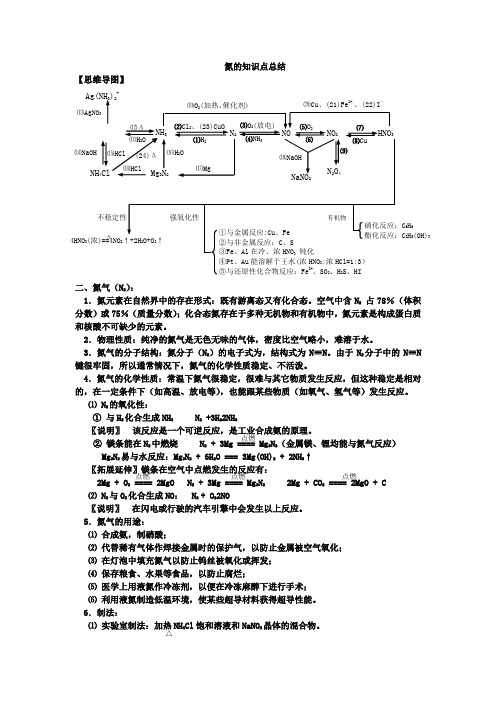
氮的知识点总结【思维导图】二、氮气(N 2):1.氮元素在自然界中的存在形式:既有游离态又有化合态。
空气中含N 2 占78%(体积分数)或75%(质量分数);化合态氮存在于多种无机物和有机物中,氮元素是构成蛋白质和核酸不可缺少的元素。
2.物理性质:纯净的氮气是无色无味的气体,密度比空气略小,难溶于水。
3.氮气的分子结构:氮分子(N 2)的电子式为,结构式为N ≡N 。
由于N 2分子中的N ≡N 键很牢固,所以通常情况下,氮气的化学性质稳定、不活泼。
4.氮气的化学性质:常温下氮气很稳定,很难与其它物质发生反应,但这种稳定是相对的,在一定条件下(如高温、放电等),也能跟某些物质(如氧气、氢气等)发生反应。
⑴ N 2的氧化性:① 与H 2化合生成NH 3 N 2 +3H 22NH 3〖说明〗 该反应是一个可逆反应,是工业合成氨的原理。
② 镁条能在N 2中燃烧 N 2 + 3Mg ==== Mg 3N 2(金属镁、锂均能与氮气反应)Mg 3N 2易与水反应:Mg 3N 2 + 6H 2O === 3Mg(OH)2 + 2NH 3↑〖拓展延伸〗镁条在空气中点燃发生的反应有: 2Mg + O 2 ==== 2MgO N 2 + 3Mg ==== Mg 3N 2 2Mg + CO 2 ==== 2MgO + C⑵ N 2与O 2化合生成NO : N 2 + O 22NO〖说明〗 在闪电或行驶的汽车引擎中会发生以上反应。
5.氮气的用途:⑴ 合成氨,制硝酸;⑵ 代替稀有气体作焊接金属时的保护气,以防止金属被空气氧化;⑶ 在灯泡中填充氮气以防止钨丝被氧化或挥发;⑷ 保存粮食、水果等食品,以防止腐烂;⑸ 医学上用液氮作冷冻剂,以便在冷冻麻醉下进行手术;⑹ 利用液氮制造低温环境,使某些超导材料获得超导性能。
6.制法:⑴ 实验室制法:加热NH 4Cl 饱和溶液和NaNO 2晶体的混合物。
⒆O 2(加热、催化剂) 4HNO 3(浓 Ag(NH 3)2+NH 4Cl ⒀AgNO 3 ⒁NaOH ⒂⒇Cu 、(21)Fe 2+、、(22)I — C 6H 6 C 3H 5(OH)3 点燃 点燃 点燃 点燃 △NaNO 2 + NH 4Cl === NaCl + N 2↑+ 2H 2O⑵ 工业制法:液氮(沸点℃) N 2 空气 ────→ ───→液氧(沸点-183℃) O 27.氮的固定:游离态氮转变为化合态氮的方法。

一、选择题1.Se 是人体必需的微量元素。
下列关于78803434Se Se 和的说法错误的是( ) A .78803434Se Se 和互为同素异形体 B .78803434Se Se 和都含有34个电子 C .78803434Se Se 和分别含有44和46个中子D .78803434Se Se 和的质量数不同2.X 、Y 、Z 、W 四种短周期主族元素在周期表中的相对位置如图,下列说法不正确的是( ) X Y ZWA .Y 的气态氢化物的稳定性一定比W 的强B .W 的原子序数可能是Y 的原子序数的3倍C .Y 原子形成的简单离子半径比X 原子形成的简单离子半径小D .若Z 元素最高价氧化物的水化物是强酸,则W 元素的单质具有强氧化性 3.下列性质比较正确的是 A .离子半径: K +>Cl ->Na +>F - B .还原性: Cl ->Br ->I ->S 2- C .酸性: HClO 4>H 3PO 4>H 2S >H 3AlO 3D .沸点: 甲醛>甲醇>甲烷4.由位于元素周期表前三周期的W 、X 、Y 、Z 四种元素“组合”成的一种超分子结构如图。
Z 、X 、Y 的族序数依次增大,X 、Y 位于同一周期,Z 与W 同主族。
下列说法正确的是( )A .Y 的单质的氧化性在同主族中最弱B .简单离子半径:Y >ZC .W 与Y 可组成多种离子化合物D .氢化物的热稳定性:X >Y5.已知短周期元素的离子:a A 2+、b B +、c C 3-、d D -都具有相同的电子层结构,则下列叙述正确的是( )A .原子半径A >B >D >C B .原子序数d >c >b >aC.离子半径C3->D->B+>A2+D.单质的还原性A>B>D>C6.短周期主族元素X、Y、Z、W、Q的原子序数依次增大,X的气态氢化物极易溶于Y 的氢化物中,常温下,Z的单质能溶于W的最高价氧化物的水化物的稀溶液,却不溶于其浓溶液。

离子键:构成离子化合物极性键:构成共价化合物 非极键:构成非金属单质 配位键:构成特殊的原子 团,如鞍根,水合氢离子等金属键:存在于单质或合金中重点掌握:定义,形成条件,判断方法。
共价化学键哪些物质可以形成离子晶体?大部分盐类、强碱、活泼金属的氧化物及过氧化物等。
哪些物质可以形成分子晶体?卤素、氧气、氢气等大多数非金属单质(稀有体),犬多数非金属氧化物、非金属氢化物、含氧酸和多数有机物等。
(有单个分子存在;化学式就是分子式。
熔沸点较低,硬度较小,易升华)常见的原子晶体:金刚石、单晶硅、碳化硅SiC、二氧化硅、氮化硅(Si3N4)等。
练习二U用电子式表示下列物质中键的* 形成过程:Na2O> KBr、A1F3>N2、HC1、H2ONa-_-Mg-•p- -s-• ••Al- -Si-:Cl -•()•+ 2 Na xNa[:o:]• •K- + -Br:• •3:F,+ir • • —3+• •(•F:1A1[:F:• •(:E:1、以下两种式子有何区别和联系:•Na + :Cl—Na[:Cl:• • • •物质的电子式及结构式£氮气的电子式、结构式:N:: N:N=N三*气分子的电子式、结构式结构式H: O :HM硫化氢的分子式H: S :H /S\- H H氨分子的电子式、结构式H: N :H H—N—H出二氧化碳的电子式• •• •o:: c::o• •• •o=c=o二硫化碳的电子式s::c::s • •• •s=c=s烷的电子式、HH:C*H• •H结构式四氯化碳的电子式:Cl ::C1 : C :C1 :•• •• ••:C1:£四氯化碳的结构式ci- c -ci一氯甲烷的电子式、结构:C1 :• •Cl iH: C :H H• •C H iH H 普的电子式、结构式H H••• • I H:C:O:H H-C-O-H••• • IH H三氯化磷的电子式、:C1 : P 2 C1 : Cl—p —次氯酸的电子式、H-O:C1:O/ \ H C1聲酸的电子式、结构式H: C :: N:H—C = N化硼的电子式三氟化硼的结构式电子式+r・・Na :O :H■草氧化顿的电子式H:O:••2+r ••Ba :O:H师化钾的电子式化钠的电子式”过氧化钠的电子式+•• ••: NaNa :O:O£氧化镁的电子式•• 、2・ Mg :O : 24-:Br :1 ~Mg2+e« )Br :lJ氯化鞍的电子式H+rH:N:H :Cl:£氮化钠的电子式N护I ••、3■Na :N: Nf次氯酸钠的电子式Na :O : Cl:X氢化钠的电子式”氮化镁的电子式Mg'fiN N j3_Mg+• •• •Al Al ■Cl芽氯化铝的结构式Cl C1 4\ / \ /Al A1二硫化亚铁的电子式碳化钙(电石)的电子式。
第四单元物质结构和元素周期律第3课化学键(一)一、基础巩固1.意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的气态N4分子,其分子结构如图所示。
N4转变为N2并释放出大量能量。
判断下列说法正确的是()A.N4属于一种新型的化合物B.N4分子中存在非极性键C.N4和N2互为同位素D.N4比N2更稳定【答案】B【解析】A、N4是单质,而不是化合物,故A错误;B、相同原子形成的共价键为非极性共价键,所以N4分子中存在非极性键,故B正确;C、同位素是原子之间,而N4和N2是氮元素的两种不同的单质,两者互为同素异形体,故C错误;D、N4转变为N2并释放出大量能量,则N4的能量高于N2,则N2比N4更稳定,故D错误;故选:B。
2.利用固体表面催化工艺进行NO分解的过程如图所示(●N〇O)。
下列说法不正确的是()A.NO属于极性分子B.O2含有非极性共价键C.过程②释放能量,过程③吸收能量D.标准状况下,NO分解生成5.6LN2转移电子数为6.02×1023【答案】C【解析】A.NO为极性键结合,属于极性分子,故A正确;B.氧气中两个氧原子共用1对电子,且电子对不发生偏移,属于非极性共价键,故B正确;C.过程②是断裂化学键的过程,吸收能量;过程③是形成化学键的过程,释放能量,故C错误;D.依据方程式:2NO N2+O2,生成1mol氮气转移4mol电子,则生成5.6LN2转移电子数为×4×6.02×1023mol﹣1=6.02×1023,故D正确;故选:C。
3.清洁的水对人类的生存非常重要,关于H2O的描述正确的是()A.含有非极性键和极性键B.纯水几乎不导电,属于非电解质C.带静电的玻璃棒接近,水流会发生偏转D.水分子间作用力大,所以加热很难分解【答案】C【解析】A.H2O含有极性键,不含非极性键,故A错误;B.纯水几乎不导电,属于弱电解质,故B错误;C.水是极性分子正电中心和负电中心不重合,分子一端带正电,一端带负电,当用带有静电的玻璃棒接近水流时,带相反电荷的一端会产生静电吸引,使水流发生偏转,故C正确;D.水分子中的氢氧键的键能比较大,所以加热很难分解,故D错误;故选:C。
氮与其化合物:一、氮气1、基础知识:“三无气体”;密度近似于空气;非极性分子;难溶于水;体积分数约为78%;2、结构:N2与CO互为等电子体电子式:结构式:键能:946 KJ/mol3、用途:保护气;合成氨;4、化学性质:常温稳定,高温反应(1)氮气流:三口瓶制取NO实验中应用氮气流排尽空气;开始前通入:排尽装置中气体,防止氧化,防止爆炸;结束后通入:用氮气流推流至后续装置,保证气体被充分吸收;(2)高温反应:a 活泼金属镁在集气瓶中燃烧,打开止水夹后,水倒吸入集气瓶几乎充满;Mg+(O2,N2,CO2,H2O)===(MgO,Mg3H2,MgO+C,Mg(OH)2+H2)N2+Na===NaN3(叠氮化钠)NaN3===NaN+N2(快速反应放出氮气,安全气囊)N2+Mg===Mg3N2(氮化镁)Mg3N2+H2O===Mg(OH)2+NH3(两种碱)N2+2Al===2AlN (具有空间网状结构、原子晶体、高温结构陶瓷)b 与非金属反应固氮反应:天然固氮(雷雨(N2→NO→HNO3)、根瘤菌)氮的氧化过程人工固氮(合成氨:N2+3H2===2NH3)氮的还原过程5、N2的制备a 工业法:分离液态空气法(物理变化)N2:-197℃O2:-183℃(工业先把空气液化到-200℃,然后上升温度,故先得到N2)b 实验室制法:(1)空气制N2(化学变化)反应流程:空气→铜网(除去氧气)→NaOH(aq,除去CO2)→浓硫酸(除水)空气→铜网(除去氧气)→碱石灰(CaO,NaOH)(2)归中法制氮气:NH4Cl+NaNO2=(加热)=N2+NaCl+2H2O (归中反应)莱姆赛在制取氮气的时候,发现通过两种不同的方法,在氮气密度方面出现了小数点后4位的误差,发现了稀有气体。
二、氨气1、基础知识:无色、有刺激性气味的气体;密度(17)小于空气(29);氨分子间可成氢键,极易溶于水、易液化(-34℃)2、结构:电子式:结构式:sp3杂化,三角锥形3、化学性质:氨分子和水中的氢离子形成配位物,留下氢氧根,显碱性;氨分子可和A n+空轨道形成配合物,如Ag(NH3)2OH;氨分子可和A(氧化性)反应,显还原性;(1)自偶电离2H2O===H3O++OH-K w=10-142NH3===NH4++NH2-K NH3<<K w(铵根)(氨基负离子)NH4++OH-===NH3+H2O(2)碱性:碱性气体(唯一)原理解释:NH3+H2O===NH3·H2O====NH4++OH-类比CO2:CO2+H2O===H2CO3===H++HCO3-(2)还原性:NH3a 与Cl2反应2NH3+3Cl2===N2+6HCl (氨气过量)6NH4Cl(白烟) 可用于检验氯气管道是否漏气b 与O2反应4NH3+5O2=(高温,催化剂)=4NO+6H2O (特殊条件) 可用于制硝酸4NH3+3O2=(加热)=2N2+6H2O (常规)练习:2NH3+3CuO=(加热)=N2+3Cu+3H2O(3)络合:向AgNO3中加入NH3·H2O(氨水) 现象:产生白烟,白色沉淀消失1AgNO3+NH3·H2O===AgOH+NH4NO32AgOH+NH3·H2O===Ag(NH3)2OH(银氨溶液)+2H2OCu2+--(NH3·H2O)-->Cu(OH)2--(NH3·H2O)-->Cu(NH3)4(OH)2(铜氨,绛蓝色溶液)4、氨气的制备a 工业:合成氨N2(g)+3H2(g)===2NH3(g) H<+0KJ/molb 实验室制备(1)铵碱法(固固加热-大试管+酒精灯)2NH4Cl+Ca(OH)2=(加热)=CaCl2+2NH3+2H2O药品变化:(NH4)2SO4可用于代替NH4Cl (粉末不会被覆盖)NH4NO3不可用于NH4Cl (硝酸根爆炸)CaO可用于代替Ca(OH)2 (最好用这个代替,生成水可以变少)NaOH不可用于代替(可能会腐蚀玻璃)单一药品:NH4Cl=(加热)=NH3+HCl (加热分解,冷却化合)不可用于制取氨气NH4HCO3=(加热)=NH3+H2O+CO2加除杂装置(碱石灰)后可以制取氨气(2)氨碱法(固液不需加热-快速得到氨气)锥形瓶+分液漏斗用平衡原理去解释加入NaOH的作用?NH3·H2O=(NaOH)=NH3+H2O解释:NH3+H2O=(可逆)=NH3·H2O=(水解)=NH4++OH-NaOH作用:[OH-]上升上述平衡向左移动,生成NH3(3)补充:金氮水解:固液不需加热Mg3N2+6H2O===3Mg(OH)2+2NH3干燥:必须碱石灰(御用干燥) 和浓硫酸反应,和CaCl2生成络合物收集:向下排空气法验满:湿润的红色石蕊试纸(变蓝);蘸有浓盐酸的玻璃棒看是否生成白烟尾处:水/硫酸(防止倒吸)三、其他负价氮1、N2H4 (联氨,肼) 可用于做火箭燃料电子式:结构式:化学性质:(1)2N2H4(g)+2NO2(g)===3N2+4H2O H=-1135kJ/mol(2)还原性:绿色还原剂N2H4+2H2O2===N2+4H2O(3)制备2NH3+NaClO===N2H4+NaCl+H2O2、CN-和SCN-(氰根和硫氰根)CN- 14e-和N2、CO为等电子体系电子式:结构式:迁移:氰气(CN)2 (拟卤素,和卤素有相似性质)(CN)2+H 2O===HCN+HCNO (❌)(CN)2+H 2O===HCN+HOCN (✔)去除CN -和SCN -的危害(2016年化学全国卷:两段法去除危害)NaCN+NaClO===NaOCN+NaCl2NaOCN+3NaClO+H 2O===2NaHCO 3+3NaCl+N 210SCN -+22ClO 2===10SO 4+22Cl -+5N 2+10CO 2+16H + (标零法,将负电子给其中任意一种元素)四、氮氧化物2、 NO 2性质详解 (1)标况下,1mol NO 2体积为22.4L (❌) NO 2沸点21℃ NO 沸点-152℃ 用于分离NO 和NO 2的混合物 不可做制冷剂,NO 2为剧毒/腐蚀性*冷却分离法五、硝酸 化学性质:不稳定性; 强氧化性; 强酸1、 不稳定性 [棕色瓶(见光易分解)]*见光易分解的物质有:AgNO 3; KMnO 4; H 2O 2; (氯溴碘)水; 硝酸; 次氯酸; 卤化银; (过超臭)氧化物4HNO 3(浓)==(光)==4NO 2+O 2+2H 2O 浓硝酸显黄色的原因: 吸收了自身分解的NO 2所致2、强氧化性 H N O 3A+HNO 3===AO x +NO x +H 2O(1) A 具有还原性:a 金属(除Pt 、Au 外)b 非金属(C 、S 、P) 浓硝酸加热为标配条件c 低价元素 Fe 2+、I -、SO 32-、S 2-(2) HNO 3勿论硝酸浓或稀,均不产生氢气体硝酸浓度浓到稀,氮被还原价更低HNO 3→NO HNO 3(浓)→NO 2*探究:硝酸浓度越来越稀,可能会出现越来越低的氮产物(N 2、NH3NO4)(3) AO x /A +:稳定物质/最高价(产物存在形式)练习:(1) Fe+6HNO 3(浓)===Fe(NO 3)3+3NO 2+3H 2O (❌) 钝化反应,不反应(2) 3FeO+10HNO 3===3Fe(NO 3)3+NO+5H 2O(3) Fe 2O 3+6HNO 3===2Fe(NO 3)3+3H 2O(4) 3Fe 3O 4+28HNO 3===9Fe(NO 3)3+NO+14H 2O2、硝酸的制备工业(三步制法):NH3----Pt,O2,高温---->NO+H2O+Q(放热)----氧气---->NO2---H2O--->HNO3第一步第二步第三步实验室制法(难挥发性酸制挥发性酸)H2SO4(浓)+2NaNO3==(加热)==Na2SO4+2HNO3(g)类比:H2SO4(浓)+2NaCl==(加热)==Na2SO4+2HCl(g)六、NO x综合处理1、氧水化法得HNO3NO x-----(H2O+O2)---->HNO3例如:2mol NO和1mol NO2通入______mol O2耗_______mol H2O 转化为_______mol HNO3三大守恒:氮守恒:nNO x===nHNO3氢守恒:nHNO3===n/2 H2O电子守恒:设NO a mol,NO2 b mol,(3a+b)/4=nO2练习(1)2mol NO2和3mol NO 通入_2.75_mol O2 转化_5_mol HNO3(2)2mol NO和1 mol N2O4通入2mol O2后转化为_4_mol HNO32、碱液吸收法NO2能不能被NaOH所充分吸收?不能,因为NO2会和H2O反应生成NO(❌)2NO2+H2O===HNO3+HNO2HNO2+NaOH===NaNO2+H2O (NaNO2稳定不分解)3HNO2===HNO3+2NO+H2O在NaOH中不反应故总反应方程(歧化反应):2NO2+2NaOH===NaNO3+NaNO2+H2O故能!(✔)NO能不能被NaOH所充分吸收?不能,NO为不成盐氧化物(✔)但是,NO与NO2一起能与NaOH反应!归中反应:NO2+NO+2NaOH===2NaNO2+H2O结论:混合气体中V(NO)/V(NO2)≤1 就可以被NaOH(aq)吸收3、氧还互相伤害法:A(毒,还原)+NO x(毒,氧)===AO x+N2(无毒)A:CO、H2S、NH3、CH4-2e-+2e--3e--8e-产物CO2、S 、N2、CO2e.g. 2CO+2NO=(催化剂)=2CO2+N2(尾气)练习:有3.0 L NO和NO2混合气体在一定条件下与3.5 L NH3恰好完全反应,求V(NO)/V(NO2)=十字交叉法:A×a%+B×b%=(A+B)×c%(理想放两边,现实摆中间,交叉求比例,答案就出现)(1)硼有2种同位素,10B和11B,已知B原子量为10.2,求10B和11B的丰度比:4:1(2)FeCl2和FeCl3混合物测得nCl:nFe=2.1:1求FeCl3 摩尔百分含量:10%4、电解法:。