高考化学一轮综合复习第十一章物质结构与性质本章重要有机物之间的转化关系练习
- 格式:doc
- 大小:206.50 KB
- 文档页数:4

大题冲关滚动练十——有机合成及推断1.以乙烯为原料合成化合物C 的流程如图所示:(1)B 和C 中含有的官能团名称分别为________,_________________________。
(2)写出A 的结构简式:_______________________________________________。
(3)①③的反应类型分别为________反应和________反应。
(4)写出乙醇的同分异构体的结构简式:___________________________________。
(5)写出反应②和④的化学方程式:②_____________________________________________________________________; ④_____________________________________________________________________。
(6)写出B 与新制Cu(OH)2悬浊液反应的化学方程式:_______________________________________________________________________。
答案 (1)醛基 酯基 (2)ClCH 2CH 2Cl (3)加成 取代 (4)CH 3OCH 3 (5)2CH 3CH 2OH+O 2――→Cu △2CH 3CHO +2H 2O 2CH 3COOH +HOCH 2—CH 2OH 浓H 2SO 4△CH 3COOCH 2—CH 2OOCCH 3+2H 2O(6)CH 3CHO +2Cu(OH)2+NaOH ――→△CH 3COONa +Cu 2O↓+3H 2O解析 根据题给的合成路线,可知A 为ClCH 2CH 2Cl ,B 为CH 3CHO ,C 为CH 3COOCH 2CH 2OOCCH 3。
(1)B 的官能团名称为醛基,C 的官能团名称为酯基。

章末总结提升一、根据有机物的性质推断官能团的结构1.能发生加成反应的物质中含有C===C或C≡C(—CHO及—C6H5一般只能与H2发生加成反应)。
2.能发生银镜反应或与新制的Cu(OH)2悬浊液共热产生砖红色沉淀的物质必含有—CHO。
既能氧化成羧酸又能还原成醇的是醛;常温下能溶解Cu(OH)2的是羧酸;遇石蕊试液显红色的是羧酸。
3.能与Na、Mg等活泼金属反应生成H2的物质中含有—OH 或—COOH.4.能与Na2CO3、NaHCO3溶液作用生成CO2的物质中含有—COOH。
5.与NaOH溶液反应的有酚、羧酸、酯或卤代烃。
6.能氧化成羧酸的醇必含“-CH2OH”的结构(能氧化的醇,羟基相“连”的碳原子上含有氢原子;能发生消去反应的醇,羟基相“邻”的碳原子上含有氢原子)。
7.能水解的有机物有酯、卤代烃、二糖和多糖、肽键和蛋白质.8.能水解生成醇和羧酸的物质中含有酯基—COO-。
9.与FeCl3溶液反应显紫色的物质是酚.10.能发生消去反应的物质中含有或(X 表示如卤原子)。
茶是我国的传统饮品,茶叶中含有的茶多酚可以替代食品添加剂中对人体有害的合成抗氧化剂,用于多种食品保鲜等,如图所示是茶多酚中含量最高的一种儿茶素A的结构简式,关于这种儿茶素A的有关叙述正确的是()①分子式为C15H14O7②1 mol儿茶素A在一定条件下最多能与7 mol H2加成③等质量的儿茶素A分别与足量的金属钠和氢氧化钠反应消耗金属钠和氢氧化钠的物质的量之比为1∶1④1 mol儿茶素A与足量的浓溴水反应,最多消耗Br2 4 molA.①②B.②③C.③④D.①④解析:儿茶素A分子中含有两个苯环,所以1 mol儿茶素A 最多可与6 mol H2加成;分子中的—OH有5个酚羟基、1个醇羟基,只有酚羟基与NaOH反应,1 mol儿茶素A最多消耗5 mol NaOH,而醇羟基和酚羟基均能与Na反应,1 mol儿茶素A最多消耗6 mol Na。

2019版高考化学一轮复习第十一章物质结构与性质章末检测编辑整理:尊敬的读者朋友们:这里是精品文档编辑中心,本文档内容是由我和我的同事精心编辑整理后发布的,发布之前我们对文中内容进行仔细校对,但是难免会有疏漏的地方,但是任然希望(2019版高考化学一轮复习第十一章物质结构与性质章末检测)的内容能够给您的工作和学习带来便利。
同时也真诚的希望收到您的建议和反馈,这将是我们进步的源泉,前进的动力。
本文可编辑可修改,如果觉得对您有帮助请收藏以便随时查阅,最后祝您生活愉快业绩进步,以下为2019版高考化学一轮复习第十一章物质结构与性质章末检测的全部内容。
第十一章物质结构与性质章末检测1.(2017·全国卷Ⅰ)钾和碘的相关化合物在化工、医药、材料等领域有着广泛的应用。
回答下列问题:(1)元素K的焰色反应呈紫红色,其中紫色对应的辐射波长为______nm (填标号)。
A.404。
4 B.553.5C.589.2 D.670。
8E.766。
5(2)基态K原子中,核外电子占据的最高能层的符号是________,占据该能层电子的电子云轮廓图形状为________。
K和Cr属于同一周期,且核外最外层电子构型相同,但金属K的熔点、沸点等都比金属Cr低,原因是________________________________________________________________________________________________________________________________________________________。
(3)X射线衍射测定等发现,I3AsF6中存在I错误!离子。
I错误!离子的几何构型为________,中心原子的杂化形式为________________。
(4)KIO3晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立体结构,边长为a=0。
446 nm,晶胞中K、I、O分别处于顶角、体心、面心位置,如图所示.K与O间的最短距离为________nm,与K紧邻的O个数为________.(5)在KIO3晶胞结构的另一种表示中,I处于各顶角位置,则K处于________位置,O处于________位置。

2019年高考化学一轮综合复习第十一章物质结构与性质专题讲座六有机综合推断题突破策略练习编辑整理:尊敬的读者朋友们:这里是精品文档编辑中心,本文档内容是由我和我的同事精心编辑整理后发布的,发布之前我们对文中内容进行仔细校对,但是难免会有疏漏的地方,但是任然希望(2019年高考化学一轮综合复习第十一章物质结构与性质专题讲座六有机综合推断题突破策略练习)的内容能够给您的工作和学习带来便利。
同时也真诚的希望收到您的建议和反馈,这将是我们进步的源泉,前进的动力。
本文可编辑可修改,如果觉得对您有帮助请收藏以便随时查阅,最后祝您生活愉快业绩进步,以下为2019年高考化学一轮综合复习第十一章物质结构与性质专题讲座六有机综合推断题突破策略练习的全部内容。
专题讲座六有机综合推断题突破策略题型示例(2017·全国卷Ⅲ,36)题型解读氟他胺G是一种可用于治疗肿瘤的药物。
实验室由芳香烃A制备G的合成路线如下:题干:简介原料及产品合成路线:①箭头:上面一般标注反应条件或试剂。
可推测官能团的转化及反应类型。
②化学式:确定不饱和度,可能的官能团及转化.③结构简式:用正推、逆推、中间推等方法确定未知物的结构及转化过程。
回答下列问题:(1)A的结构简式为________________。
C的化学名称是________________。
考查有机物的结构及名称。
根据C的结构简式及B的化学式Y,运用逆推法是确定A的结构的关键(2)③的反应试剂和反应条件分别是______________,该反应的类型是____________。
要求能根据官能团的变化(苯环上引入硝基)确定反应条件,根据反应前后有机物的组成或结构的变化确定反应类型。
(3)⑤的反应方程式为_________________.吡啶是一种有机碱,其作用是_____________。
(4)G的分子式为____________。
要求能根据G倒推F的结构,再根据取代反应的基本规律,写反应方程式;能根据吡啶的碱性,结合平衡移动判断有机碱的作用;能根据键线式书写分子式。

2019年高考化学一轮综合复习第十一章物质结构与性质第33讲认识有机化合物练习编辑整理:尊敬的读者朋友们:这里是精品文档编辑中心,本文档内容是由我和我的同事精心编辑整理后发布的,发布之前我们对文中内容进行仔细校对,但是难免会有疏漏的地方,但是任然希望(2019年高考化学一轮综合复习第十一章物质结构与性质第33讲认识有机化合物练习)的内容能够给您的工作和学习带来便利。
同时也真诚的希望收到您的建议和反馈,这将是我们进步的源泉,前进的动力。
本文可编辑可修改,如果觉得对您有帮助请收藏以便随时查阅,最后祝您生活愉快业绩进步,以下为2019年高考化学一轮综合复习第十一章物质结构与性质第33讲认识有机化合物练习的全部内容。
第33讲认识有机化合物考纲要求 1.能根据有机化合物的元素含量、相对分子质量确定有机化合物的分子式.2.了解常见有机化合物的结构;了解有机物分子中的官能团,能正确地表示它们的结构。
3。
了解确定有机化合物结构的化学方法和物理方法(如质谱、红外光谱、核磁共振氢谱等).4。
能正确书写有机化合物的同分异构体(不包括手性异构体)。
5。
能够正确命名简单的有机化合物.考点一有机物的官能团、分类和命名1.按碳的骨架分类(1)有机化合物错误!(2)烃错误!2.按官能团分类(1)官能团:决定化合物特殊性质的原子或原子团。
(2)有机物的主要类别、官能团和典型代表物类别官能团代表物名称、结构简式烷烃甲烷CH4乙烯H2C==CH2烯烃(碳碳双键)炔烃-C≡C—(碳碳三键)乙炔HC≡CH芳香烃苯卤代烃—X(卤素原子)溴乙烷C2H5Br醇—OH(羟基)乙醇C2H5OH酚苯酚乙醚CH3CH2OCH2CH3醚(醚键)乙醛CH3CHO醛(醛基)酮丙酮CH3COCH3(羰基)乙酸CH3COOH羧酸(羧基)酯乙酸乙酯CH3COOCH2CH3(酯基)3.有机化合物的命名(1)烷烃的习惯命名法(2)烷烃的系统命名法(3)烯烃和炔烃的命名(4)苯的同系物的命名苯作为母体,其他基团作为取代基。

2019年高考化学一轮课时达标习题第11章选修3 物质结构与性质(2)(含解析)编辑整理:尊敬的读者朋友们:这里是精品文档编辑中心,本文档内容是由我和我的同事精心编辑整理后发布的,发布之前我们对文中内容进行仔细校对,但是难免会有疏漏的地方,但是任然希望(2019年高考化学一轮课时达标习题第11章选修3 物质结构与性质(2)(含解析))的内容能够给您的工作和学习带来便利。
同时也真诚的希望收到您的建议和反馈,这将是我们进步的源泉,前进的动力。
本文可编辑可修改,如果觉得对您有帮助请收藏以便随时查阅,最后祝您生活愉快业绩进步,以下为2019年高考化学一轮课时达标习题第11章选修3 物质结构与性质(2)(含解析)的全部内容。
第11章选修3:物质结构与性质(2)1.(2018·石家庄调研)铜及其化合物在生产生活中有着广泛的用途.(1)基态铜原子的核外电子排布式为__1s22s22p63s23p63d104s1__,其晶体的堆积方式为__面心立方最密堆积__,其中铜原子的配位数为__12__.(2)向硫酸铜溶液中滴加氨水,首先形成蓝色沉淀;继续滴加氨水,沉淀溶解,得到深蓝色的透明溶液;继续向溶液中加入乙醇,会析出深蓝色晶体[Cu(NH3)4SO4·H2O].①氨水中各元素原子的电负性由大到小的顺序为__O>N>H__(用元素符号表示)。
②NH3中N原子的杂化轨道类型为__sp3__,与其互为等电子体的阳离子为__H3O+__。
③向蓝色沉淀中继续滴加氨水,沉淀溶解是因为生成了四氨合铜配离子,四氨合铜配离子的结构式为__ 降低溶剂极性,使Cu(NH3)SO4·H2O析出(答案合理即可)__。
4(3)CuCl2和CuCl是铜的两种常见的氯化物。
①如图表示的是__CuCl__(填“CuCl2"或“CuCl")的晶胞。
②原子坐标参数表示晶胞内部各原子的相对位置,图中各原子坐标参数:A为(0,0,0),B为(0,1,1),C为(1,1,0),则D原子的坐标参数为__错误! __.③晶胞中C、D两原子核间距为298 pm,阿伏加德罗常数为N A,则该晶体密度为错误!g·cm-3(列出计算式即可)。

2019年高考化学一轮综合复习第十一章物质结构与性质第34讲烃和卤代烃练习编辑整理:尊敬的读者朋友们:这里是精品文档编辑中心,本文档内容是由我和我的同事精心编辑整理后发布的,发布之前我们对文中内容进行仔细校对,但是难免会有疏漏的地方,但是任然希望(2019年高考化学一轮综合复习第十一章物质结构与性质第34讲烃和卤代烃练习)的内容能够给您的工作和学习带来便利。
同时也真诚的希望收到您的建议和反馈,这将是我们进步的源泉,前进的动力。
本文可编辑可修改,如果觉得对您有帮助请收藏以便随时查阅,最后祝您生活愉快业绩进步,以下为2019年高考化学一轮综合复习第十一章物质结构与性质第34讲烃和卤代烃练习的全部内容。
第34讲烃和卤代烃考纲要求 1.掌握烷、烯、炔和芳香烃的结构和性质。
2。
掌握卤代烃的结构和性质.3.了解烃类物质的重要应用。
考点一烷烃、烯烃、炔烃的结构与性质1.烷烃、烯烃、炔烃的组成、结构特点和通式2.脂肪烃的物理性质性质变化规律状态常温下含有1~4个碳原子的烃都是气态,随着碳原子数的增多,逐渐过渡到液态、固态沸点随着碳原子数的增多,沸点逐渐升高;同分异构体之间,支链越多,沸点越低相对密度随着碳原子数的增多,相对密度逐渐增大,密度均比水小水溶性均难溶于水3。
脂肪烃的化学性质(1)烷烃的取代反应①取代反应:有机物分子中某些原子或原子团被其他原子或原子团所替代的反应.②烷烃的卤代反应a.反应条件:气态烷烃与气态卤素单质在光照下反应。
b.产物成分:多种卤代烃混合物(非纯净物)+HX。
c.定量关系:~Cl2~HCl即取代1mol氢原子,消耗1_mol卤素单质生成1molHCl。
(2)烯烃、炔烃的加成反应①加成反应:有机物分子中的不饱和碳原子与其他原子或原子团直接结合生成新的化合物的反应。
②烯烃、炔烃的加成反应(写出有关反应方程式)(3)加聚反应①丙烯加聚反应方程式为n CH==CH—CH3错误!.2②乙炔加聚反应方程式为n CH≡CH错误!?CH==CH?。
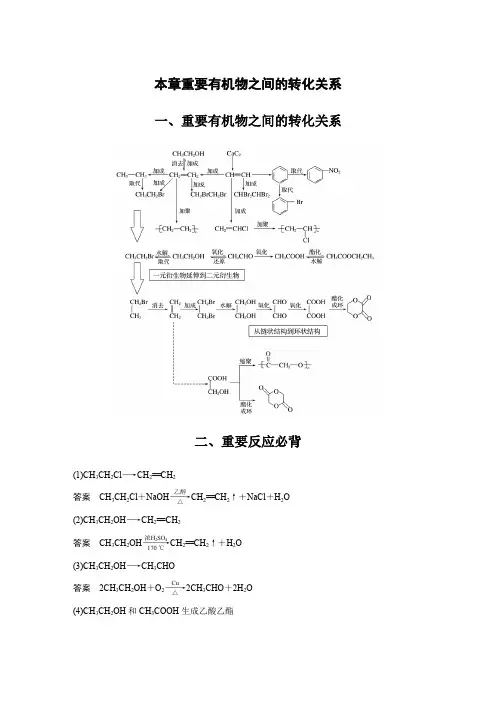
本章重要有机物之间的转化关系一、重要有机物之间的转化关系二、重要反应必背(1)CH 3CH 2Cl ―→CH 2==CH 2答案 CH 3CH 2Cl +NaOH ――→乙醇△CH 2==CH 2↑+NaCl +H 2O (2)CH 3CH 2OH ―→CH 2==CH 2答案 CH 3CH 2OH ―――→浓H 2SO 4170 ℃CH 2==CH 2↑+H 2O (3)CH 3CH 2OH ―→CH 3CHO答案 2CH 3CH 2OH +O 2――→Cu △2CH 3CHO +2H 2O (4)CH 3CH 2OH 和CH 3COOH 生成乙酸乙酯答案 CH 3COOH +CH 3CH 2OH浓H 2SO 4△CH 3COOC 2H 5+H 2O (5)OHC —CHO ―→HOOC —COOH答案 OHC —CHO +O 2――→催化剂△HOOC —COOH (6)乙二醇和乙二酸生成聚酯答案 n HOCH 2—CH 2OH +n HOOC —COOH 一定条件+2n H 2O(7)乙醛和银氨溶液的反应答案 CH 3CHO +2Ag(NH 3)2OH ―→△CH 3COONH 4+2Ag ↓+3NH 3+H 2O(8)乙醛和新制Cu(OH)2悬浊液的反应答案 CH 3CHO +2Cu(OH)2―→△CH 3COOH +Cu 2O ↓+2H 2O (9)答案 +2NaOH ――→醇△+2NaCl +2H 2O (10)答案 +Br 2――→FeBr 3+HBr (11)和饱和溴水的反应答案 +3Br 2―→↓+3HBr(12)和溴蒸气(光照)的反应答案 +Br 2―→光+HBr(13) 和HCHO 的反应答案 n +n HCHO ―→H ++n H 2O(14)酯在碱性条件的水解(以乙酸乙酯在NaOH 溶液中为例)答案 CH 3COOC 2H 5+NaOH ――→△CH 3COONa +C 2H 5OH (15)和NaOH 的反应答案 +2NaOH ――→△CH 3COONa ++H 2O三、有机物的检验辨析1.卤代烃中卤素的检验取样,滴入NaOH 溶液,加热至分层现象消失,冷却后加入稀硝酸酸化,再滴入AgNO 3溶液,观察沉淀的颜色,确定是何种卤素。

2022年高考化学一轮综合复习第十一章物质结构与性质本章重要从小丘西行百二十步,隔篁竹,闻水声,如鸣珮环,心乐之。
伐竹取道,下见小潭,水尤清冽。
全石以为底,近岸,卷石底以出,为坻,为屿,为嵁,为岩。
青树翠蔓,蒙络摇缀,参差披拂。
珮通:佩2022年高考化学一轮综合复习第十一章物质结构与性质本章重要有机物之间的转化关系练习一、重要有机物之间的转化关系二、重要反应必背(1)CH3CH2Cl―→CH2==CH2答案CH3CH2Cl+NaOHCH2==CH2↑+NaCl+H2O(2)CH3CH2OH―→CH2==CH2答案CH3CH2OHCH2==CH2↑+H2O(3)CH3CH2OH―→CH3CHO答案2CH3CH2OH+O22CH3CHO+2H2O(4)CH3CH2OH和CH3COOH生成乙酸乙酯答案CH3COOH+CH3CH2OHCH3COOC2H5+H2O(5)OHC—CHO―→HOOC—COOH答案OHC—CHO+O2HOOC—COOH(6)乙二醇和乙二酸生成聚酯答案nHOCH2—CH2OH+nHOOC—COOH(7)乙醛和银氨溶液的反应答案CH3CHO+2Ag(NH3)2OHCH3COONH4+2Ag↓+3NH3+H2O(8)乙醛和新制Cu(OH)2悬浊液的反应欧阳修,字永叔,庐陵人。
四岁而孤,母郑,守节自誓,亲诲之学。
家贫,至以荻画地学书。
幼敏悟过人,读书辄成诵。
及冠,嶷然有声。
修始在滁州,号醉翁,晚更号六一居士。
天资刚劲,见义勇为,虽机阱在前,触发之不顾。
放逐流离,至于再三,志气自若也。
-1-/5从小丘西行百二十步,隔篁竹,闻水声,如鸣珮环,心乐之。
伐竹取道,下见小潭,水尤清冽。
全石以为底,近岸,卷石底以出,为坻,为屿,为嵁,为岩。
青树翠蔓,蒙络摇缀,参差披拂。
珮通:佩答案CH3CHO+2Cu(OH)2+NaOHCH3COONa+Cu2O↓+3H2O(9)答案+2NaCl+2H2O(10)答案(11)和饱和溴水的反应答案(12)和溴蒸气(光照)的反应答案(13)和HCHO的反应欧阳修,字永叔,庐陵人。
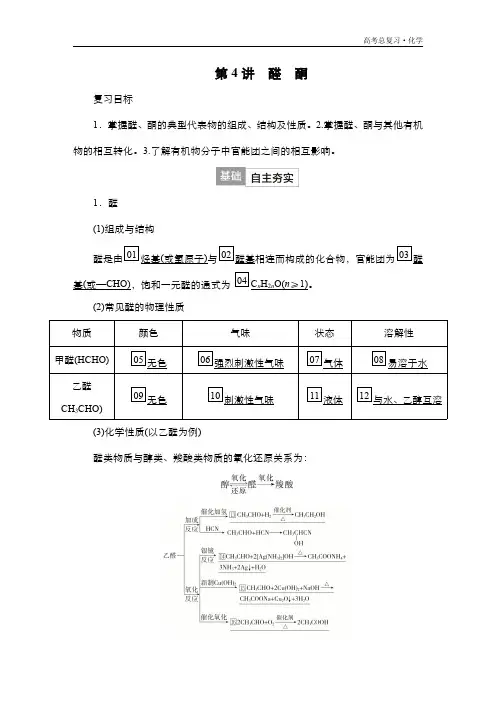
第4讲醛酮复习目标1.掌握醛、酮的典型代表物的组成、结构及性质。
2.掌握醛、酮与其他有机物的相互转化。
3.了解有机物分子中官能团之间的相互影响。
1.醛(1)组成与结构醛是由01烃基(或氢原子)与02醛基相连而构成的化合物,官能团为03醛基(或—CHO),饱和一元醛的通式为04C n H2n O(n≥1)。
(2)常见醛的物理性质物质颜色气味状态溶解性甲醛(HCHO)05无色06强烈刺激性气味07气体08易溶于水乙醛09无色10刺激性气味11液体12与水、乙醇互溶CH3CHO)(3)化学性质(以乙醛为例)醛类物质与醇类、羧酸类物质的氧化还原关系为:(4)在生产、生活中的作用和影响①35%~40%的甲醛水溶液称为17福尔马林,具有杀菌消毒作用和防腐性能,常用作防腐剂和消毒剂,用于种子消毒和浸制生物标本。
但甲醛有毒,不可用于食品保鲜。
②劣质的装饰材料中挥发出的18甲醛,对环境和人体健康影响很大,是室内主要污染物之一。
2.酮(1)组成与结构酮是01羰基与02两个烃基相连的化合物,其结构可表示为03。
04丙酮是最简单的酮。
(2)化学性质(以丙酮为例)①不能被银氨溶液、新制Cu(OH)2等弱氧化剂氧化。
②催化加氢05。
③与HCN加成06。
请指出下列各说法的错因(1)醛基的结构简式可以写成—CHO,也可以写成—COH。
错因:醛基不能写成—COH。
(2)甲醛、乙醛、丙醛均无同分异构体。
错因:丙醛与丙酮互为同分异构体。
(3)欲检验CH2===CH—CHO分子中的官能团,应先检验“”后检验“—CHO”。
错因:检验“”一般用溴水或KMnO4(H+)溶液,而两试剂均可氧化“—CHO”,故应先检验“—CHO”,后检验“”。
(4)凡是能发生银镜反应的有机物都是醛。
错因:甲酸、甲酸盐、甲酸酯都可发生银镜反应。
(5)1mol HCHO与足量银氨溶液充分反应,可生成2mol Ag。
错因:甲醛分子中相当于有2个—CHO,故1__mol__HCHO与足量银氨溶液充分反应,可生成4__mol__Ag。

2019年高考化学一轮综合复习第十一章物质结构与性质第35讲烃的含氧衍生物练习编辑整理:尊敬的读者朋友们:这里是精品文档编辑中心,本文档内容是由我和我的同事精心编辑整理后发布的,发布之前我们对文中内容进行仔细校对,但是难免会有疏漏的地方,但是任然希望(2019年高考化学一轮综合复习第十一章物质结构与性质第35讲烃的含氧衍生物练习)的内容能够给您的工作和学习带来便利。
同时也真诚的希望收到您的建议和反馈,这将是我们进步的源泉,前进的动力。
本文可编辑可修改,如果觉得对您有帮助请收藏以便随时查阅,最后祝您生活愉快业绩进步,以下为2019年高考化学一轮综合复习第十一章物质结构与性质第35讲烃的含氧衍生物练习的全部内容。
第35讲烃的含氧衍生物考纲要求 1.掌握醇、酚、醛、羧酸、酯的结构与性质,以及它们之间的相互转化。
2.了解烃的衍生物合成方法.3。
了解有机分子中官能团之间的相互影响。
4。
根据信息能设计有机化合物的合成路线。
考点一醇、酚1.醇、酚的概念(1)醇是羟基与烃基或苯环侧链上的碳原子相连的化合物,饱和一元醇的分子通式为C n H2n+1OH(n≥1).(2)酚是羟基与苯环直接相连而形成的化合物,最简单的酚为苯酚()。
(3)醇的分类2.醇类物理性质的变化规律(1)溶解性低级脂肪醇易溶于水。
(2)密度一元脂肪醇的密度一般小于1g·cm-3.(3)沸点①直链饱和一元醇的沸点随着分子中碳原子数的递增而逐渐升高。
②醇分子间存在氢键,所以相对分子质量相近的醇和烷烃相比,醇的沸点远远高于烷烃。
3.苯酚的物理性质(1)纯净的苯酚是无色晶体,有特殊气味,易被空气氧化呈粉红色.(2)苯酚常温下在水中的溶解度不大,当温度高于65_℃时,能与水混溶,苯酚易溶于酒精.(3)苯酚有毒,对皮肤有强烈的腐蚀作用,如果不慎沾到皮肤上应立即用酒精洗涤。
4.由断键方式理解醇的化学性质如果将醇分子中的化学键进行标号如图所示,那么醇发生化学反应时化学键的断裂情况如下所示:以1-丙醇为例,完成下列条件下的化学方程式,并指明断键部位。
(通用版)2019版高考化学一轮复习第十一章物质结构与性质学案编辑整理:尊敬的读者朋友们:这里是精品文档编辑中心,本文档内容是由我和我的同事精心编辑整理后发布的,发布之前我们对文中内容进行仔细校对,但是难免会有疏漏的地方,但是任然希望((通用版)2019版高考化学一轮复习第十一章物质结构与性质学案)的内容能够给您的工作和学习带来便利。
同时也真诚的希望收到您的建议和反馈,这将是我们进步的源泉,前进的动力。
本文可编辑可修改,如果觉得对您有帮助请收藏以便随时查阅,最后祝您生活愉快业绩进步,以下为(通用版)2019版高考化学一轮复习第十一章物质结构与性质学案的全部内容。
第十一章物质结构与性质第一板块教材复习课原子结构与性质原子核外电子排布1能层一二三四五能层符号K L M N O能级符号错误!2s错误!错误!3p错误!错误!错误!错误!4f5s 5p……轨道数1131351357……最多电子数2错误!6错误!错误!错误!2错误!错误!14……2错误!错误!错误!50原子轨道错误!3.基态原子核外电子排布的三个原理(1)能量最低原理电子总是先占有能量低的轨道,然后依次进入能量较高的轨道,使整个原子的能量处于最低状态。
即原子的电子排布遵循构造原理能使整个原子的能量处于最低状态。
如图为构造原理示意图:(2)泡利原理在一个原子轨道中,最多只能容纳2个电子,并且这两个电子的自旋状态相反。
如2s轨道上的电子排布为,不能表示为。
(3)洪特规则当电子排布在同一能级的不同轨道时,基态原子中的电子总是优先单独占据一个轨道,并且自旋状态相同。
如2p3的电子排布为,不能表示为或。
洪特规则特例:当能量相同的原子轨道在全满(p6、d10、f14)、半满(p3、d5、f7)和全空(p0、d0、f0)状态时,体系的能量最低,如:24Cr的电子排布式为1s22s22p63s23p63d54s1。
4.基态原子核外电子排布的表示方法表示方法以硫原子为例电子排布式1s22s22p63s23p4简化电子排布式[Ne]3s23p4电子排布图(轨道表达式)外围(价)电子排布式3s23p45.原子状态与原子光谱(1)原子的状态①基态原子:处于最低能量的原子。
本章重要有机物之间的转化关系一、重要有机物之间的转化关系二、重要反应必背(1)CH 3CH 2Cl ―→CH 2==CH 2答案 CH 3CH 2Cl +NaOH ――→乙醇△CH 2==CH 2↑+NaCl +H 2O (2)CH 3CH 2OH ―→CH 2==CH 2答案 CH 3CH 2OH ――→浓H 2SO 4170℃CH 2==CH 2↑+H 2O(3)CH 3CH 2OH ―→CH 3CHO答案 2CH 3CH 2OH +O 2――→Cu △2CH 3CHO +2H 2O (4)CH 3CH 2OH 和CH 3COOH 生成乙酸乙酯答案 CH 3COOH +CH 3CH 2OH ????浓H 2SO 4△CH 3COOC 2H 5+H 2O(5)OHC —CHO ―→HOOC —COOH答案 OHC —CHO +O 2――→催化剂△HOOC —COOH (6)乙二醇和乙二酸生成聚酯答案 n HOCH 2—CH 2OH +n HOOC —COOH(7)乙醛和银氨溶液的反应答案 CH 3CHO +2Ag(NH 3)2OH ――→△CH 3COONH 4+2Ag ↓+3NH 3+H 2O(8)乙醛和新制Cu(OH)2悬浊液的反应答案 CH 3CHO +2Cu(OH)2+NaOH ――→△CH 3COONa +Cu 2O ↓+3H 2O (9)答案 ――→醇△+2NaCl +2H 2O (10)答案 (11)和饱和溴水的反应答案 (12)和溴蒸气(光照)的反应答案 (13)和HCHO 的反应答案 +(n -1)H 2O(14)酯在碱性条件的水解(以乙酸乙酯在NaOH 溶液中为例)答案 CH 3COOC 2H 5+NaOH ――→△CH 3COONa +C 2H 5OH (15)答案三、有机物的检验辨析1.卤代烃中卤素的检验取样,滴入NaOH 溶液,加热至分层现象消失,冷却后加入稀硝酸酸化,再滴入AgNO 3溶液,观察沉淀的颜色,确定是何种卤素。
【2019最新】精选高考化学一轮综合复习第十一章物质结构与性质本章
重要有机物之间的转化关系练习
一、重要有机物之间的转化关系
二、重要反应必背
(1)CH3CH2Cl―→CH2==CH2
答案CH3CH2Cl+NaOHCH2==CH2↑+NaCl+H2O
(2)CH3CH2OH―→CH2==CH2
答案CH3CH2OHCH2==CH2↑+H2O
(3)CH3CH2OH―→CH3CHO
答案2CH3CH2OH+O22CH3CHO+2H2O
(4)CH3CH2OH和CH3COOH生成乙酸乙酯
答案CH3COOH+CH3CH2OHCH3COOC2H5+H2O
(5)OHC—CHO―→HOOC—COOH
答案OHC—CHO+O2HOOC—COOH
(6)乙二醇和乙二酸生成聚酯
答案nHOCH2—CH2OH+nHOOC—COOH
(7)乙醛和银氨溶液的反应
答案CH3CHO+2Ag(NH3)2OHCH3COONH4+2Ag↓+3NH3+H2O
(8)乙醛和新制Cu(OH)2悬浊液的反应
答案CH3CHO+2Cu(OH)2+NaOHCH3COONa+Cu2O↓+3H2O
(9)
答案+2NaCl+2H2O (10)
答案
(11)和饱和溴水的反应
答案
(12)和溴蒸气(光照)的反应
答案
(13)和HCHO的反应
答案+(n-1)H2O
(14)酯在碱性条件的水解(以乙酸乙酯在NaOH溶液中为例)
答案CH3COOC2H5+NaOHCH3COONa+C2H5OH
(15)
答案
三、有机物的检验辨析
1.卤代烃中卤素的检验
取样,滴入NaOH溶液,加热至分层现象消失,冷却后加入稀硝酸酸化,再滴入AgNO3溶液,观察沉淀的颜色,确定是何种卤素。
2.烯醛中碳碳双键的检验
(1)若是纯净的液态样品,则可向所取试样中加入溴的四氯化碳溶液,若褪色,则证明含有碳碳双键。
(2)若样品为水溶液,则先向样品中加入足量的新制Cu(OH)2悬浊液,加热煮沸,充分反应后冷却过滤,向滤液中加入稀硝酸酸化,再加入溴水,若褪色,则证明含有碳碳双键。
提醒:若直接向样品水溶液中滴加溴水,则会有反应:—CHO+Br2+H2O―→—COOH +2HBr而使溴水褪色。
3.二糖或多糖水解产物的检验
若二糖或多糖是在稀硫酸作用下水解的,则先向冷却后的水解液中加入足量的NaOH 溶液,中和稀硫酸,然后再加入银氨溶液或新制的氢氧化铜悬浊液,(水浴)加热,观察现象,作出判断。
4.如何检验溶解在苯中的苯酚?
取样,向试样中加入NaOH溶液,振荡后静置、分液,向水溶液中加入盐酸酸化,再滴入几滴FeCl3溶液(或过量饱和溴水),若溶液呈紫色(或有白色沉淀生成),则说
明有苯酚。
提醒:(1)若向样品中直接滴入FeCl3溶液,则由于苯酚仍溶解在苯中,不能进入水溶液中与Fe3+进行离子反应;若向样品中直接加入饱和溴水,则生成的三溴苯酚会溶解在苯中而看不到白色沉淀。
(2)若所用溴水太稀,则一方面可能由于生成溶解度相对较大的一溴苯酚或二溴苯酚,另一方面可能生成的三溴苯酚溶解在过量的苯酚之中而看不到沉淀。
5.检验实验室制得的乙烯气体中含有CH2==CH2、SO2、CO2、H2O,可将气体依次通过
无水硫酸铜→品红溶液→饱和Fe2(SO4)3溶液→品红溶液
(检验水) (检验SO2)(除去SO2) 确认SO2已除尽
→澄清石灰水→溴水或溴的四氯化碳溶液或酸性高锰酸
钾溶液
(检验CO2) (检验CH2==CH2)
四、有机反应条件的重要性
1.有机化学反应一般需要在适当的条件下才能发生,且常伴有副反应,通常只写出主反应的化学方程式。
在书写化学方程式时,应注意标明正确的反应条件。
2.反应条件不同,反应类型和反应产物可能不同。
(1)温度不同,反应产物不同。
例如:
(2)溶剂不同,反应产物不同。
例如:
(3)催化剂不同,反应产物不同。
例如:。