铁矿石的测定方法
- 格式:doc
- 大小:55.00 KB
- 文档页数:4

铁矿石中全铁含量的测定(重铬酸钾容量法)基本原理:在酸性溶液中,用氯化亚锡将三价铁还原为二价铁,加入氯化汞以除去过量的氯化亚锡,以二苯胺磺酸钠为指示剂,用重铬酸钾标准溶液滴定至紫色。
反应方程式:2Fe 3+ + Sn 2+ + 6Cl ―—→ 2Fe 2+ + SnCl 62―Sn 2+ + 4Cl ― + 2HgCl 2 —→ SnCl 62―+ Hg 2Cl 2↓6Fe 2+ + Cr 2O 72- + 14H + —→ 6Fe 3+ + 2Cr 3+ + 2Cr 3+ + 7H 2O 计算结果:()m V m V Fe 2.01000020.0%=⨯⨯=此法的优点是:过量的氯化亚锡容易除去,重铬酸钾溶液比较稳定,滴定终点的变化明显,受温度的影响(30℃以下)较小,测定的结果比较准确。
一、硫—磷混酸溶样1、药品及试剂①(2+3)硫磷混合酸② 重铬酸钾标准溶液:1.00 mL 此溶液相当于0.0020g 铁。
称取1.7559g 预先在150℃烘干1h 的重铬酸钾(基准试剂)于250 mL 烧杯中,以少量水溶解后移入1L 容量瓶中,用水定容。
③ 氯化亚锡溶液:10%称取10g 氯化亚锡溶于20 mL 盐酸中,用水稀释至100 mL 。
④ 氯化高汞饱和溶液:5%⑤ 二苯胺磺酸钠指示剂:0.5%⑥ 氟化钠2、分析步骤:准确称取0.2g 试样于250mL 锥形瓶中,用少许水润湿,摇匀。
加入10mL (2+3)硫磷混合酸及0.5g 氟化钠,摇匀。
在高温电炉上加热溶解完全,取下冷却,加入15mL 盐酸,低温加热至近沸并维持3~5min ,溶液变澄清,取下趁热滴加氯化亚锡溶液至铁(Ⅲ)离子的黄色消失,并过量2滴,用水冲洗杯壁。
在水槽中冷却,加入10mL 氯化高汞饱和溶液,摇动后放置2~3 min ,加水至120mL 左右,冷却后加入5滴0.5%二苯胺磺酸钠指示剂,用重铬酸钾标准溶液滴定至紫色。
与试样分析的同时进行空白试验。

重铬酸钾法测定铁矿石中铁的含量(无汞法)一、实验目的1. 掌握重铬酸钾法测定亚铁盐中铁含量的原理和方法;2. 了解氧化还原指示剂的作用原理和使用方法。
二.原理:经典的重铬酸钾法测定铁时,每一份试液需加入饱和氯化汞溶液10mL,这样约有480mg 的汞排入下水道,而国家环境部门规定汞的允许排放量是0.05mg·L-1,因此,实验中的排放量是大大超过允许排放量的。
实际上,汞盐沉积在底泥和水质中,造成严重的环境污染,有害于人的健康。
近年来研究了无汞测铁的许多新方法,如新重铬酸钾法,硫酸铈法和EDTA 法等。
本法是新重铬酸钾法。
新重铬酸钾法是在经典的有汞重铬酸钾法的基础上,去掉氯化汞试剂,采用钨酸钠作为指示剂指示Fe3+还原Fe2+的方法。
试样用硫-磷混酸溶剂后,先用氯化亚锡还原大部分Fe3+,继而用三氯化钛定量还原剩余部分的Fe3+,当Fe3+定量还原成Fe2+之后,过量一滴三氯化钛溶液,即可使溶液中作为指示剂的六价钨(无色的磷钨酸)还原为蓝色的五价钨化合物,俗称“钨蓝”,故使溶液呈现蓝色。
滴入重铬酸钾溶液,使钨蓝刚好褪色,以消除少量还原剂的影响。
“钨蓝”的结构式较为复杂定量还原Fe3+时,不能单用氯化亚锡,因为在此酸度下,氯化亚锡不能很好的还原W(Ⅵ)为W(V),故溶液无明显颜色变化。
采用SnCl2-TiCl3联合还原Fe3+为Fe2+,过量一滴TiCl3与Na2WO4作用即显示“钨蓝”而指示。
如果单用TiCl3为还原剂也不好,尤其是试样中铁含量高时,则使溶液中引入较多的钛盐,当加水稀释试液时,易出现大量的四价钛沉淀,影响测定。
在无汞测定铁实验中常用SnCl2-TiCl3联合还原,反应式如下:2Fe3++SnCl42-+2Cl-=2Fe2++SnCl62-Fe3++Ti3++H2O=Fe2++TiO2++2H+试液中Fe3+已经被还原为Fe2+,加入二苯胺磺酸钠指示剂,用K2Cr2O7标准溶液滴定溶液呈现稳定的紫色即为终点。


铁矿石化学分析方法:容量法测定磷量
磷量是铁矿石中重要化学成分,以含量高低可以预测铁矿石品位。
容量法是测定铁矿石磷量的常用方法,此方法简便有效。
容量法测定铁矿石磷量的基本原理是将铁矿石样品置于产气容器中,在指定条件下加热,使铁矿石中的硫形成硫酸,将其吸收在玻璃针中,再用浓硫酸滴定得到硫酸铁,正确测量所得数值即为样品中磷量。
测定步骤主要是:将铁矿石样品称量放入分析皿,用锡板封住样品的表面,放入真空保护性烧瓶中,加热到在高温条件下迅速分解,并将硫逸出并形成铁硫酸,再加入浓硫酸滴定出硫酸铁,以硫酸铁含量数值即为铁矿石样品中磷量。
容量法测定铁矿石磷量的优点是:快速、简便、准确;缺点是:需要较多仪器辅助,如真空保护性烧瓶,酶漆漆,锡板等,耗费时间大。
综上所述,容量法是测定铁矿石磷量的有效方法,能够快速准确的得出结果,但仪器辅助较多,耗时多。
经过正确的操作流程,以及控制好温度和时间等条件,能够准确有效的得出测定结果。
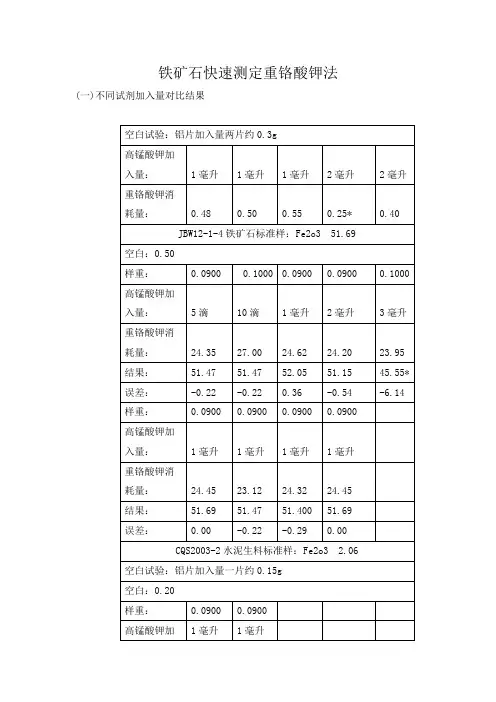
铁矿石快速测定重铬酸钾法(一)不同试剂加入量对比结果(二)铁矿石快速测定重铬酸钾法1.试剂1)重铬酸钾0.0300ml/l:准确称取已在150℃烘干2小时重铬酸钾基准试剂1.4709g,溶于150-200ml水中,然后移入1000ml容量瓶中,加水稀释至标线,摇匀。
2)二苯胺磺酸钠指示剂溶液10g/l:将1g二苯胺磺酸钠溶于100ml水中加5-6滴硫酸(1+1),此溶液较易失效有效使用期限为一个月。
3)高锰酸钾溶液10g/l:将1g高锰酸钾溶于100ml水中,此溶液较易失效有效使用期限为一个月。
4)硫磷酸混合溶液(1+1+2):将一份硫酸缓慢注入两分水中摇匀后在与一份磷酸混合。
2.测定步骤准确称取约0.1g(G)试样,置于250毫升锥形瓶中。
用少量水冲洗瓶壁,加入1毫升高锰酸钾及5毫升磷酸,摇荡锥形瓶,使与试样混合均匀。
将锥形瓶放在小电炉上于250-300℃的温度下加热,使试样充分溶解。
至开始冒白烟时,取下锥形瓶,稍冷(约1分钟),然后加入20毫升盐酸(1+1),摇荡片刻,加入两片铝片,于60-70℃下还原。
待铝片全部溶解后(此时溶液由黄色变为无色),迅速用橡皮塞塞住瓶口,立即将锥形瓶放在冷水槽内急冷(大约30秒中间摇动两三测次)。
然后用水稀释约100ml,加入20ml硫磷混合酸及2-3滴10g/l二苯胺磺酸钠指示剂溶液,用重铬酸钾0.0300ml/l标准滴定溶液滴定至呈现蓝紫色(V)。
3. 重铬酸钾对Fe2O3滴定度计算:T Fe2O3= Fe2O3*G/VFe2O3:标准样中Fe2O3含量百分数G:标样试料质量gV:滴定时消耗重铬酸钾标准滴定溶液的体积ml重铬酸钾秤样量计算(g):C(1/6K2CR2O7)=0.0300*49.03*1重铬酸钾浓度度计算(mol/l):C(1/6K2CR2O7)= T Fe2O3/79.85C(1/6K2CR2O7)= m*1000/V*M4.注意事项:1)高锰酸钾及铝片的加入量要固定,并扣除空白2)铝片要一次加入,不可分几次加入,否则结果偏低3)加入硫磷酸混合溶液,使滴定终点明显4)还原完毕后迅速用橡皮赛将锥形瓶瓶口塞住,避免溶液接触更多的空气,溶液必须急冷。
![[精品]铁矿石中总铁量的测定](https://uimg.taocdn.com/2f15be9cdc3383c4bb4cf7ec4afe04a1b071b0fb.webp)
[精品]铁矿石中总铁量的测定铁矿石是重要的钢铁原料,在钢铁工业中有着重要的地位。
为了生产高质量的钢铁产品,需要对铁矿石中总铁量进行准确的测定。
本文将介绍两种测定方法,分别是重量法和滴定法。
一、重量法重量法是一种简单、准确的测定总铁量的方法,主要利用化学反应中的质量守恒原理进行测定。
1. 实验原理铁矿石样品与盐酸反应,生成氢气和铁离子,然后通过滴加硫酸亚铁标准溶液,使得铁离子还原成为二价铁离子,接着再滴加二氧化锰标准溶液,使其氧化成为三价铁离子。
通过质量差计算出铁离子的含量,从而计算出总铁量。
2. 实验仪器和试剂仪器:电子天平、滴定管、容量瓶。
试剂:浓盐酸、硫酸亚铁标准溶液、氢氧化钠溶液、二氧化锰标准溶液。
3. 实验步骤①取重约为 1g 的干燥铁矿石样品,粉碎并过筛,放入干净的锥形瓶中,加入 50 mL 浓盐酸溶液,加热溶解。
②当样品完全溶解,加入 5 mL 硫酸亚铁标准溶液,使铁离子还原成二价的铁离子。
③加入氢氧化钠溶液至中性或碱性,使二氧化锰标准溶液能够氧化铁离子为三价的铁离子。
④将二氧化锰标准溶液滴加到瓶中,直到液体变为淡红色,并经过搅拌反应数分钟。
⑤根据方程计算出铁离子的含量,从而计算出总铁量。
4. 实验结果分析通过重量法测定,可以得出铁矿石中总铁量的含量,但是在实验过程中需要注意样品的干燥程度、溶解程度、滴加标准溶液的数量等因素,对误差进行修正和消除,从而保证实验结果的准确性和可靠性。
二、滴定法滴定法是另一种测定铁矿石中总铁量的常用方法,主要是利用硫酸亚铁和二氧化锰溶液进行滴定,以测定铁离子的含量。
②加入 10 mL 浓盐酸,加热溶解样品,直至溶液变为透明。
④用二氧化锰标准溶液滴加,至溶液呈粉红色。
总之,以上两种测定方法都可以用于铁矿石中总铁量的测定,选用何种方法取决于实验者的需求和实验条件。
无论哪种方法,都需要进行严格的操作和控制,以确保实验结果的准确性和可靠性。


铁矿石中全铁含量测定方法分析在钢铁工业中,铁矿石是至关重要的原材料,而准确测定铁矿石中全铁的含量对于评估矿石质量、优化冶炼工艺以及控制生产成本都具有极其重要的意义。
本文将对常见的铁矿石中全铁含量测定方法进行详细分析。
一、重铬酸钾滴定法重铬酸钾滴定法是测定铁矿石中全铁含量的经典方法之一。
其基本原理是将铁矿石样品用酸溶解,使其中的铁全部转化为二价铁离子。
然后,在酸性条件下,用过量的重铬酸钾标准溶液将二价铁氧化为三价铁,最后以二苯胺磺酸钠为指示剂,用硫酸亚铁铵标准溶液滴定过量的重铬酸钾,从而计算出全铁的含量。
该方法的优点是准确度高、重现性好,适用于各种类型铁矿石中全铁含量的测定。
但也存在一些不足之处,比如操作过程较为繁琐,需要进行多次加热和滴定,耗时较长;同时,使用的重铬酸钾具有一定的毒性,对环境和操作人员的健康有一定影响。
二、氯化亚锡氯化汞重铬酸钾滴定法这种方法是在重铬酸钾滴定法的基础上进行改进的。
首先用盐酸和氟化钠溶解样品,然后加入氯化亚锡将大部分三价铁还原为二价铁。
接着,加入氯化汞氧化过量的氯化亚锡,最后用重铬酸钾标准溶液滴定二价铁,计算全铁含量。
此方法相较于传统的重铬酸钾滴定法,简化了操作步骤,缩短了分析时间。
然而,氯化汞是一种剧毒物质,对环境和人体危害极大,需要在操作过程中特别小心,严格控制其使用和排放。
三、EDTA 配位滴定法EDTA 配位滴定法也是常用的测定铁矿石中全铁含量的方法之一。
在酸性条件下,将铁矿石样品溶解,用还原剂将铁全部还原为二价铁。
然后,加入过量的 EDTA 标准溶液与二价铁配位,再以二甲酚橙为指示剂,用锌标准溶液滴定剩余的 EDTA,从而计算出全铁的含量。
EDTA 配位滴定法的优点是操作相对简便,分析速度较快,且试剂毒性较小。
但该方法的选择性相对较差,容易受到其他金属离子的干扰,因此在测定前需要对样品进行预处理,以消除干扰。
四、原子吸收光谱法原子吸收光谱法是一种基于物质对特定波长光的吸收特性来测定元素含量的方法。


铁矿石中全铁量的测定
一、原理
试样以盐酸氟化钠溶解,氯化亚锡还原大部分铁后,三氯化钛还原剩余铁为低价,过量三氯化钛用重铬酸钾回滴,以二苯胺磺酸钠作指示剂,用标准重铬酸钾溶液滴定铁,求得试样铁含量。
二、试剂
1、浓盐酸
2、氟化钠(固体)
3、6%氯化亚锡:6g氯化亚锡溶于20 mL盐酸中,用水稀释至100 mL
4、硫磷混酸:硫酸:磷酸:水 = 2:3:5
5、25%钨酸钠:1:20磷酸溶液
6、1:19三氯化钛:取15 ~ 20%三氯化钛用1:9盐酸稀释后加一层液体石蜡保护(或现用现配)
7、重铬酸钾标准溶液:(1/6) 0.05 mol/L
三、分析步骤
称取试样0.2 g两份于300 mL三角瓶中,加少许水使其散开,加氟化钠0.3 g,盐酸20 mL,低温加热溶解,滴加二氯化锡至溶液呈现浅黄色,继续加热10 ~ 20 min(体积约10 mL)取下,加水150 ~ 200 mL,加钨酸钠15 d,用三氯化钛还原兰色出现,用重铬酸钾标准溶液滴至兰色消失(不计读数),立即加硫磷混液10 mL,二苯胺磺酸钠5 d,用重铬酸钾标准溶液滴定至紫色为终点,记下消耗重铬酸钾溶液的毫升数V,则;
Fe% =
式中:M—重铬酸钾溶液浓度
V-滴定消耗重铬酸钾溶液毫升数。

实验报告:铁矿石中全铁含量的测定1. 背景铁矿石是一种重要的矿产资源,广泛应用于钢铁工业和建筑业等领域。
准确测定铁矿石中的全铁含量对于评估其品质和价值具有重要意义。
本实验旨在通过一种简单而有效的方法来测定铁矿石中全铁含量。
2. 分析2.1 实验原理本实验采用酸溶法测定铁矿石中的全铁含量。
主要步骤如下:1.取适量细粉末样品,加入足量稀盐酸。
2.将混合物加热至沸腾,持续加热一段时间以完全溶解样品。
3.将溶液冷却至室温,并转移至容量为100 mL的容器中。
4.加入足够的去离子水使总体积达到100 mL。
5.用适当浓度的标准高锰酸钾溶液滴定样品溶液,直到出现粉红色终点。
6.记录滴定所需的高锰酸钾溶液体积,并根据反应方程计算出样品中全铁的含量。
2.2 实验步骤1.准备所需试剂和仪器:稀盐酸、去离子水、标准高锰酸钾溶液、容量瓶、滴定管等。
2.称取适量铁矿石样品,将其细粉末化。
3.将细粉末样品加入容量瓶中,并加入足够的稀盐酸。
4.将容量瓶放置在加热板上,加热至沸腾,持续加热15分钟以完全溶解样品。
5.将溶液冷却至室温,并转移至容量为100 mL的容器中。
6.加入足够的去离子水使总体积达到100 mL,充分混合溶液。
7.取一定体积的样品溶液(如10 mL),倒入滴定管中。
8.用标准高锰酸钾溶液滴定样品溶液,直到出现粉红色终点。
记录滴定所需的高锰酸钾溶液体积(V)。
9.重复3次滴定,计算平均滴定体积(V_ave)。
10.根据反应方程和滴定结果计算出样品中全铁的含量。
3. 结果3.1 数据记录•实验样品质量:10 g•平均滴定体积(V_ave):20.5 mL3.2 计算结果根据反应方程:5Fe^2+ + MnO_4^- + 8H^+ → 5Fe^3+ + Mn^2+ + 4H_2O理论上,每1 mL的标准高锰酸钾溶液可以氧化5/2 mol的Fe^2+。
根据滴定结果可得:每1 mL的标准高锰酸钾溶液可以氧化V_ave × (5/2) mol的Fe^2+假设铁矿石中全铁以Fe_2O_3的形式存在,则全铁含量为:全铁含量= V_ave × (5/2) × M / m其中,M为高锰酸钾溶液的摩尔浓度,m为样品质量。
铁矿石中全铁含量的测定(重铬酸钾容量法)铁矿石一般能被盐酸在低温电炉上加热分解,如残渣为白色,表明试样分解完全,若残渣有黑色或其它颜色,是因为铁的硅酸盐难溶于盐酸,可加入氢氟酸或氟化钠再加热使试样分解完全,SiO 2+4HF==SiF 4↑+2H 2OMSiO 3+4HF+2HCl==MCl 2+SiF 4↑+2H 2O还可以加入少量磷酸,以消除溶液中铁的黄色对终点的干扰同时降低Fe 3+/Fe 2+电位,增大终点突跃范围,使反应更完全。
磁铁矿的分解速度很慢,可用硫-磷混合酸(1+2)在高温电炉上加热分解,但应注意加热时间不能太长,以防止生成焦磷酸盐。
部分铁矿石试样的酸分解较困难,宜采用碱熔法分解试样,常用的熔剂有碳酸钠、过氧化钠、氢氧化钠和过氧化钠-碳酸钠(1+2)混合熔剂等,在银坩埚、镍坩埚、高铝坩埚或石墨坩埚中进行。
碱熔分解后,再用盐酸溶液浸取。
基本原理:在酸性溶液中,用氯化亚锡将三价铁还原为二价铁,加入氯化汞以除去过量的氯化亚锡,以二苯胺磺酸钠为指示剂,用重铬酸钾标准溶液滴定至紫色。
反应方程式:2Fe 3+ + Sn 2+ + 6Cl -—→ 2Fe 2+ + SnCl 62―Sn 2+ + 4Cl - + 2HgCl 2 —→ SnCl 62― + Hg 2Cl 2↓6Fe 2+ + Cr 2O 72- + 14H + —→ 6Fe 3+ + 2Cr 3+ + 2Cr 3+ + 7H 2O计算结果:()m V m V Fe 2.01000020.0%=⨯⨯=此法的优点是:过量的氯化亚锡容易除去,重铬酸钾溶液比较稳定,滴定终点的变化明显,受温度的影响(30℃以下)较小,测定的结果比较准确。
一、硫—磷混酸溶样1、药品及试剂①(2+3)硫磷混合酸②重铬酸钾标准溶液: mL此溶液相当于铁。
称取预先在150℃烘干1h的重铬酸钾(基准试剂)于250 mL烧杯中,以少量水溶解后移入1L容量瓶中,用水定容。
铁矿石中全铁(tfe)含量的测定国标下载温馨提示:该文档是我店铺精心编制而成,希望大家下载以后,能够帮助大家解决实际的问题。
文档下载后可定制随意修改,请根据实际需要进行相应的调整和使用,谢谢!并且,本店铺为大家提供各种各样类型的实用资料,如教育随笔、日记赏析、句子摘抄、古诗大全、经典美文、话题作文、工作总结、词语解析、文案摘录、其他资料等等,如想了解不同资料格式和写法,敬请关注!Download tips: This document is carefully compiled by the editor. I hope that after you download them, they can help you solve practical problems. The document can be customized and modified after downloading, please adjust and use it according to actual needs, thank you!In addition, our shop provides you with various types of practical materials, such as educational essays, diary appreciation, sentence excerpts, ancient poems, classic articles, topic composition, work summary, word parsing, copy excerpts, other materials and so on, want to know different data formats and writing methods, please pay attention!铁矿石中全铁(tFe)含量的测定国标1. 引言铁矿石是钢铁生产的主要原料之一,其含铁量的准确测定对于钢铁行业至关重要。
铁矿石全铁含量的测定三氯化钛还原重铬酸钾滴定法一、方法原理:式样以硫磷混酸和盐酸分解后,用氯化亚锡还原大部分的三价铁,再以钨酸钠为指示剂,三氯化钛将剩余的三价铁全部还原为二价铁至生成钨蓝,以稀重铬酸钾溶液氧化过剩的还原剂。
以二苯胺磺酸钠作指示剂,用重铬酸钾标准溶液滴定二价铁,计算全铁含量。
二、试剂:1、硫磷混酸:1:12、氟化钾:25%3、盐酸:1:14、高锰酸钾:4g/L5、氯化亚锡:60g/L6、钨酸钠:250g/L(称取25g钨酸钠溶于适量水中,加磷酸5ml,用水稀释至100ml)7、三氯化钛:1+9(取10ml三氯化钛溶液,用1:1盐酸稀释至100ml,当班用当班配制)8、稀重铬酸钾:0.5g/L9、二苯胺磺酸钠:2.5g/L三、分析方法称取预先干燥的式样0.2g精确到0.0001g,置于300ml锥形瓶中,用少量水吹洗杯壁,加入硫磷混酸(1:1)20ml、氢氟酸5ml,加热溶解试样,轻轻晃动瓶子1-2次,继续加热至冒硫酸烟到200刻度时取下锥形瓶。
冷却至不烫手时,用少量水吹洗杯壁,加入20ml盐酸(1:1),加热溶解至冒大泡,取下用氯化亚锡还原至微黄色,若还原时过量可滴加少量的高锰酸钾氧化至微黄色,冷却至室温,加水50ml,10滴钨酸钠,滴加三氯化钛溶液至试液呈蓝色。
滴加稀重铬酸钾至蓝色消失,加二苯胺磺酸钠5滴作指示剂,用重铬酸钾标准溶液滴定至由绿色至蓝色到最后一滴变紫红色时为终点。
四、注意事项1、分析时同时代两个以上标样。
2、三氯化钛溶液当班使用当班配制。
3、用氯化亚锡还原三价铁时,一定保证还原至微黄色,过量会导致结果偏高,黄色过深时用三氯化钛还原剩余的三价铁时难以还原至蓝色。
4、用稀重铬酸钾溶液氧化过剩的还原剂时,试液由蓝色变为无色过量至1-2滴即可。
不可滴加过多,会导致结果偏低。
5、滴定过程中,始终保持滴定速度一致。
5、终点颜色要掌握好,一定要到终点,但不能过量。