有机化学基础知识点立体化学的基本概念
- 格式:docx
- 大小:37.23 KB
- 文档页数:3


有机化学基础知识点整理立体化学和空间构型有机化学基础知识点整理——立体化学和空间构型立体化学是有机化学中的重要分支,研究有机化合物的空间构型和手性性质。
在有机化学反应中,立体因素对反应机理、速率和产物的构成有着影响。
本文将对有机化学中的立体化学和空间构型进行整理。
一、手性和立体异构在有机化学中,手性是指分子无法与其镜像重合的性质,分为左旋(L)和右旋(D)两种。
与此相对应的是非手性分子,其镜像可以重合。
手性分子与非手性分子之间的异构体现在空间构型上,可以分为构象异构和对映异构。
构象异构是指分子在空间中的不同排列方式,由于键的旋转或原子的旋转而导致分子结构的变化。
常见的构象异构包括旋转异构和推移异构。
旋转异构是指由于单键或双键的旋转而形成的异构体,如顺式异构和反式异构。
推移异构是指由于取代基的推移而形成的异构体,如轴向异构和轴向交替异构。
对映异构是指分子与其镜像之间不能通过旋转或推移相互重合的异构体,也称为手性异构。
对映异构体的特点是具有光学活性,能够旋光。
分子的对映异构体通过手性中心来区分,手性中心是一个碳原子,其四个取代基中有三个不同。
二、立体化学符号和表示方法为了描述和表示分子的立体化学特性,人们提出了一些特定的符号和表示方法。
1. Fischer投影式:是一种在平面上表示立体结构的简洁方法。
分子的主轴垂直于纸面,水平的线代表键,垂直的线代表在纸面上向后延伸,朝向观察者。
常用于描述手性中心和立体异构。
2. 齐墩果式:是一种用球体表示分子的三维结构。
通常用于解决研究立体异构产物的问题。
齐墩果式中,不同的原子用不同颜色的球表示,通过连线表示原子之间的键。
三、分子的空间构型了解分子的空间构型对于理解和预测化学反应是至关重要的。
1. 立体异构立体异构是指化学物质在三维空间中的不同排列方式,包括同分异构和构象异构。
同分异构是指化学物质的分子式相同但结构不同,常见的同分异构有链式异构、环式异构和官能团异构等。

有机化学第二讲 立体化学【竞赛要求】有机立体化学基本概念。
构型与构象。
顺反异构(trans -、cis -和Z -、E -构型)。
手性异构。
endo -和exo -。
D,L 构型。
【知识梳理】从三维空间结构研究分子的立体结构,及其立体结构对其物理性质和化学性质的影响的科学叫立体化学。
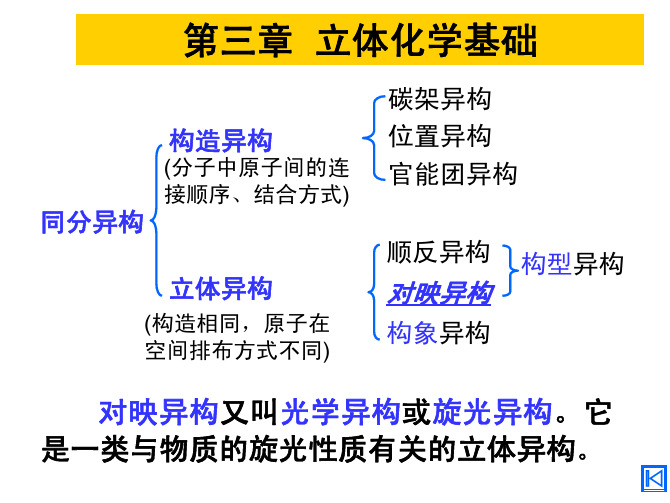
一、异构体的分类按结构不同,同分异构现象分为两大类。
一类是由于分子中原子或原子团的连接次序不同而产生的异构,称为构造异构。
构造异构包括碳链异构、官能团异构、位置异构及互变异构等。
另一类是由于分子中原子或原子团在空间的排列位置不同而引起的异构,称为立体异构。
立体异构包括顺反异构、对映异构和构象异构。
二、立体异构(一)顺反异构但顺反异构体的两个双键碳原子上没有两个相同的取代基用这种命名法就无能为力。
如:系统命名法规定将双键碳链上连接的取代基按次序规则的顺序比较,高序位基在双键同侧的称Z 型,反之称E 型。
如上化合物按此规定应为E 型。
命名为E – 4 – 甲基 – 3 – 已基 – 2 – 戊烯。
(5)当取代基的结构完全相同,只是构型不同时,则R >S ,Z >E 。
按次序规则可以对下列化合物进行标记:对于环状化合物,由于环的存在阻止了碳碳单键的自由旋转,所以也有顺反异构体。
(2Z ,4E) – 庚二烯(二)对映异构1、分子的对称性、手性与旋光性(1)分子的对称因素:对称因素可以是一个点、一个轴或一个面。
H 3C CH 2CH 3 C = H CH(CH 3)2C H H C = CH 3 C 2 1 H C = H CH 2CH 3 C 425 73 顺 –1,4 – 二甲基环乙烷 3 3反 –1,4 – 二甲基环乙对称面:把分子分成互为实物和镜像关系两半的假想平面,称为对称面。
对称中心:分子中任意原子或原子团与P点连线的延长线上等距离处,仍是相同的原子或原子团时,P点就称为对称中心。
凡具有对称面或对称中心任何一种对称因素的分子,称为对称分子,凡不具有任何对称因素的分子,称为不对称分子。


有机化合物的立体化学和构象分析有机化合物是由碳和氢等元素组成的化合物,其中碳原子的立体化学和构象分析是有机化学中非常重要的一部分。
立体化学研究的是分子中原子的空间排列方式,而构象分析则是研究分子在空间中的不同构象。
这两个方面的研究对于理解有机化合物的性质和反应机理具有重要意义。
一、立体化学的概念及基本原理立体化学研究的是分子中原子的空间排列方式,包括立体异构体和手性。
立体异构体是指分子结构相同但空间排列不同的化合物,如顺式异构体和反式异构体。
而手性则是指分子不对称性,即分子无法与其镜像重合。
手性分子具有两种互为镜像的结构,分别称为左旋体和右旋体。
立体化学的基本原理包括空间取向性、立体障碍和立体效应。
空间取向性是指分子中原子或基团相对于其他原子或基团的空间取向。
立体障碍是指分子中不同原子或基团之间的空间阻碍,导致分子只能采取特定的构象。
立体效应是指分子中原子或基团的空间排列对于化学性质和反应速率的影响。
二、构象分析的方法和应用构象分析是研究分子在空间中的不同构象,即分子的不同空间排列方式。
构象分析的方法包括分子模型、分子轨道理论和核磁共振等技术。
分子模型是一种直观的方法,通过建立分子的三维模型来研究构象。
分子轨道理论则是一种量子化学的方法,通过计算分子的电子结构来预测构象。
核磁共振是一种实验技术,通过测量分子中原子核的共振信号来确定构象。
构象分析在有机化学中有广泛的应用。
例如,研究分子的构象可以帮助理解分子的性质和反应机理。
构象分析还可以用于设计和合成具有特定性质的有机化合物,如药物和材料。
三、有机化合物的立体化学和构象分析的案例1. 手性药物的立体化学分析手性药物是指具有手性的药物分子。
由于手性药物的两个手性体在生物体内的相互作用不同,因此其药效和毒性也会有差异。
立体化学分析可以帮助确定手性药物的结构和手性体的含量,从而指导药物的合成和应用。
2. 立体异构体的构象分析立体异构体是指分子结构相同但空间排列不同的化合物。
有机合成中的立体化学问题探讨有机合成是化学领域的重要分支,它涉及到合成有机化合物的方法和技术。
在有机合成中,立体化学是一个关键问题,它涉及到分子的三维结构和空间构型。
本文将探讨有机合成中的立体化学问题,并讨论其在合成化学中的重要性和应用。
一、立体化学的基本概念立体化学研究的是分子的三维结构和空间构型。
在有机化合物中,分子的立体构型决定了其物理性质和化学性质。
立体化学主要涉及手性和立体异构体的概念。
手性是指分子不重合的镜像形式,即左右手的概念。
而立体异构体则是指分子结构相同但空间构型不同的化合物。
二、手性分子的合成手性分子的合成是有机合成中的重要问题。
手性分子的合成通常涉及到对称分子的不对称转化。
常见的手性合成方法包括催化不对称合成、手性试剂的使用和手性助剂的应用等。
催化不对称合成是通过使用手性催化剂来实现对称分子的不对称转化,从而得到手性产物。
手性试剂的使用是指在反应中引入手性试剂,使得反应产生手性产物。
手性助剂的应用则是指在反应中添加手性助剂,通过与反应物形成复合物来实现对称分子的不对称转化。
三、立体异构体的合成立体异构体的合成是有机合成中的另一个重要问题。
立体异构体的合成通常涉及到分子的构象变化。
构象是指分子在空间中的不同排列方式。
常见的立体异构体包括顺式异构体和反式异构体。
顺式异构体是指分子中两个取代基位于同一侧,而反式异构体则是指分子中两个取代基位于相对侧。
立体异构体的合成通常涉及到键合的旋转和取代基的移位。
键合的旋转是指通过旋转化学键来改变分子的构象。
取代基的移位是指通过改变取代基的位置来改变分子的构象。
立体异构体的合成方法包括化学反应、物理方法和生物方法等。
化学反应中常用的方法包括环化反应、消旋反应和取代反应等。
物理方法包括光学活性和核磁共振等。
生物方法则是指利用生物体系合成立体异构体。
四、立体化学在药物合成中的应用立体化学在药物合成中起着重要的作用。
药物分子的立体构型决定了其与生物体的相互作用方式。
有机化学的相对构型判定
相对构型判定是有机化学中一种重要的方法,用于确定有机分子中各个原子的空间排列方式。
常见的相对构型判定方法包括以下几种:
1. 立体化学的基本概念:立体中心、手性运动、手性分子等。
通过分析分子中的立体中心和手性运动,可以判断其相对构型。
2. 单键轴变构:若化合物中存在单键轴变构,则可以根据化学键的相对位置确定其相对构型。
3. 立体异构关系:通过立体异构体之间的相互转化关系,如环化、开环等反应,可以推测各个异构体的相对构型。
4. 空间构象:通过分析分子中的键角、键长、电荷平面等特征,可以确定空间构象,从而判断相对构型。
5. 共价键平面关系:通过分析共价键平面的相对位置关系,可以判定相对构型。
需要注意的是,相对构型判定是一种无法直接观察的手段,主要依赖于理论、实验和推理等方法进行推断和判断。
因此,在进行相对构型判定时,需要综合考虑多种因素,同时结合实验数据和理论知识进行分析。
有机化学基础知识点整理立体化学中的光学活性有机化学基础知识点整理立体化学中的光学活性在有机化学领域中,立体化学是一个非常重要的分支,而光学活性是其中的一个关键概念。
本文将对有机化学基础知识点进行整理,并详细介绍立体化学中的光学活性。
一、立体化学基础知识点1. 手性和对映体在有机化学中,分子的手性是指其不可重合的镜像结构。
这种手性导致了分子的对映体存在,对映体即为一个分子与其手性镜像分子。
对映体具有相同的物理化学性质,但其对于其他手性物质(如光)却表现出截然不同的相互作用。
2. 手性中心手性中心是指一个分子中由于它的四个取代基的不同而产生的非对称碳、硫、磷等原子,也可以是一种光学活性的金属离子。
手性中心的存在决定了分子是否具有光学活性。
3. 非对称碳原子的命名方法非对称碳原子通常用R和S表示。
通过将优先级较高的取代基指向观察者,然后按照顺时针或逆时针的方向依次连接剩余的取代基,最终确定非对称碳原子的命名。
4. 共轭和异极效应共轭是指分子中存在相邻的双键或烯烃基团。
共轭体系可以调整成分子的π电子分布,从而影响分子的电子性质。
异极效应则是由于不同基团中的键极性而引起的整体极性。
共轭和异极效应对于调整分子结构和稳定性具有重要作用。
二、光学活性的概念和原理1. 光学活性的定义光学活性是指物质能够使平面偏振光的振动面发生旋转的性质。
具有光学活性的化合物被称为旋光体,可以分为两类:左旋体和右旋体。
2. 极性分子和非极性分子极性分子具有正负电荷的区分,例如带正电荷和带负电荷的官能团。
非极性分子则没有电荷的区分。
光学活性主要是由于分子的立体构型而产生,而与极性与否无直接关系。
3. 过圆性和比旋光度过圆性是指旋光体的旋光角随光的波长的变化。
过圆性可分为正过圆性和负过圆性。
比旋光度是指单位浓度下旋光体的旋光角与光经过的物质的长度的比值。
三、光学活性的应用1. 手性药物的制备与分离光学活性的物质在医药领域有广泛的应用。
有机化学基础知识点立体化学的基本概念立体化学是有机化学中非常重要的一个概念,它涉及到分子的空间结构和构象。
在有机化学反应中,分子的立体构型对反应的速率和产物的选择性有着重要的影响。
本文将介绍立体化学的基本概念,包括立体异构、手性分子、构象等知识点。
1. 立体异构
立体异构是指化学物质的分子在空间中的排列方式不同,从而导致其化学性质与物理性质的差异。
立体异构可以分为构造异构和空间异构两种类型。
1.1 构造异构
构造异构是指分子结构的连接方式不同,分为链式异构、官能团异构和位置异构三种类型。
链式异构:同分子式下,碳骨架的排列方式不同,如正丁烷和异丁烷就是一对链式异构体。
官能团异构:同分子式下,分子中的官能团位置不同,如乙醇和甲醚就是一对官能团异构体。
位置异构:同分子式下,官能团位置相对于主链排列的位置不同,如2-丁醇和3-丁醇就是一对位置异构体。
1.2 空间异构
空间异构是指分子在空间中的三维排列方式不同,分为立体异构和对映异构两种类型。
立体异构:分子中存在非自由旋转的键,由于旋转受限,使得分子结构不同,如顺式-反式异构。
对映异构:对称分子具有镜像关系,不能通过旋转重叠,如手性分子。
2. 手性分子
手性分子是指与其镜像物不可重叠的化合物,也称为不对称分子。
手性分子通常包含一个或多个手性中心,手性中心是一个碳原子,与四个不同的基团连接。
手性分子的最重要特征是其对映异构体的存在。
对映异构体具有相同的分子式、相同的化学键,但是无法通过旋转或平移重叠。
这种现象称为手性体。
手性分子有很多实际应用,如生物活性物质、药物、拆分光等。
同时,手性分子还涉及到光学活性、旋光度等概念。
3. 构象
构象是指分子在空间中的不同取向,由于化学键的旋转、振动等运动而引起的。
构象是立体化学中的重要概念之一,它与立体异构密切相关。
分子的构象由于化学键的自由旋转而产生,通常与键长、键角、键的取代基团等因素有关。
构象的改变可能会导致分子性能的变化。
构象的研究对于了解分子的空间结构、相互作用以及反应机理都具有重要的意义。
分子器件、分子机器等研究领域都基于分子结构的构象变化。
总结:
立体化学是有机化学中重要的基础知识点,涉及到分子的空间结构和构象。
立体异构包括构造异构和空间异构,手性分子是一类不对称分子,具有镜像异构体。
构象是分子在空间中的不同取向,由化学键的旋转和振动所引起。
在有机化学中,理解和应用立体化学的基本概念对于研究物质的性质和反应机理至关重要。