制药工艺流程图
- 格式:ppt
- 大小:14.84 MB
- 文档页数:38
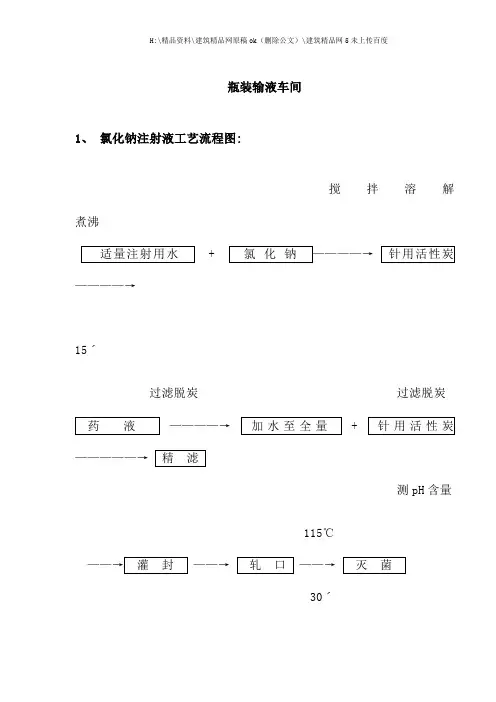
瓶装输液车间1、氯化钠注射液工艺流程图:搅拌溶解煮沸————→15ˊ过滤脱炭过滤脱炭————→ +测pH含量115℃30ˊ氯化钠注射液生产过程质量控制要点:2、 葡萄糖注射液工艺流程图:煮沸 搅拌溶解煮沸过滤脱炭15ˊ过滤脱炭测pH值含量115℃30ˊ葡萄糖注射液生产过程质量控制要点:3、 葡萄糖氯化钠注射液工艺流程图:煮沸 搅拌溶解煮沸 过滤脱炭15ˊ过滤脱炭测pH值含量115℃30ˊ葡萄糖氯化钠注射液生产过程质量控制要点:灭菌后半成品外壁清洁度、标志、存放区每柜灯检灯检品可见异物每个工号/班每瓶标志随时/班包装贴签内容、外观随时/班装箱数量、装箱单、内容每箱4、复方氨基酸注射液( 15AA) 工艺流程图:复方氨基酸注射液( 15AA) 生产过程质量控制要点:灭菌灭菌柜标志、装量、压力、温度、时间、记录每柜灭菌前半成品标志、存放区每柜灭菌后半成品外壁清洁度、标志、存放区每柜灯检灯检品可见异物每个工号/班每瓶标志随时/班包装贴签内容、外观随时/班装箱数量、装箱单、内容每箱5、复方氨基酸注射液( 18AA) 工艺流程图:复方氨基酸注射液( 18AA) 生产过程质量控制要点:可见异物1次/批轧口铝盖铝盖紧密度随时/班灭菌灭菌柜标志、装量、压力、温度、时间、记录每柜灭菌前半成品标志、存放区每柜灭菌后半成品外壁清洁度、标志、存放区每柜灯检灯检品可见异物每个工号/班每瓶标志随时/班包装贴签内容、外观随时/班装箱数量、装箱单、内容每箱6、复方氨基酸注射液( 18AA) 30g工艺流程图:复方氨基酸注射液( 18AA) 30g生产过程质量控制要点:7、 甘露醇注射液工艺流程图:煮沸 搅拌溶解煮沸30 ˊ 过滤脱炭过滤脱炭—————→泵至稀配锅测PH含量120℃40ˊ甘露醇注射液生产过程质量控制要点:8、甲硝唑氯化钠注射液工艺流程图:搅拌溶解过滤脱炭+测PH含量115℃30ˊ甲硝唑氯化钠注射液生产过程质量控制要点:9、氧氟沙星葡萄糖注射液工艺流程图:搅拌溶解煮沸15ˊ冷却至30℃ 搅拌倒入饱和NaOH溶液乳酸过滤———————→调节PH4.0-5.0116℃30ˊ氧氟沙星葡萄糖注射液生产过程质量控制要点:灌封胶塞洗涤水可见异物1次/每锅灌装后半成品药液装量1次/每小时可见异物1次/批轧口铝盖铝盖紧密度随时/班灭菌灭菌柜标志、装量、压力、温度、时间、记录每柜灭菌前半成品标志、存放区每柜灭菌后半成品外壁清洁度、标志、存放区每柜灯检灯检品可见异物每个工号/班每瓶标志随时/班包装贴签内容、外观随时/班装箱数量、装箱单、内容每箱10、硫酸依替米星氯化钠注射液工艺流程图:硫酸依替米星氯化钠注射液生产过程质量控制要点:软包装输液车间1、 氯化钠注射液工艺流程图:搅拌溶解煮沸————→15ˊ过滤脱炭过滤脱炭测pH含量115℃30ˊ氯化钠注射液生产过程质量控制要点:2、葡萄糖注射液工艺流程图:煮沸搅拌溶解煮沸过滤脱炭15ˊ过滤脱炭115℃测pH值含量 30ˊ葡萄糖注射液生产过程质量控制要点:3、葡萄糖氯化钠注射液工艺流程图:煮沸搅拌溶解煮沸过滤脱炭15分钟过滤脱炭115℃测pH值含量 30ˊ葡萄糖氯化钠注射液生产过程质量控制要点:4、 甲硝唑氯化钠注射液工艺流程图:搅拌溶解过滤脱炭 115℃测PH含量 30ˊ甲硝唑氯化钠注射液生产过程质量控制要点:小容量注射液车间1、苯甲醇注射液工艺流程图:搅拌至溶解测PH值( 必要时加热)测含量100℃30ˊ苯甲醇注射液生产过程质量控制要点:2、酚磺乙胺注射液工艺流程图:溶解后搅拌均匀测PH值搅拌+活性炭放置10ˊ100℃30ˊ酚磺乙胺注射液生产过程质量控制要点:3、肌苷注射液工艺流程图:加热微沸边加边搅拌搅拌调PH值85℃保温30分钟测定含量通N2100℃30ˊ肌苷注射液生产过程质量控制要点:4、氟罗沙星注射液工艺流程图:搅拌溶解加热至85-90℃搅拌80℃保温30ˊ——→溶解冷却至45℃澄明100℃———→30ˊ氟罗沙星注射液生产过程质量控制要点:5、甲钴胺注射液工艺流程图:溶解煮沸20ˊ冷却至45℃ 至澄明100℃30ˊ甲钴胺注射液生产过程质量控制要点:6、 利巴韦林注射液工艺流程图:搅拌后 搅拌溶解过滤测PH 至澄明100℃含量 30ˊ。
目录1.大容量注射剂生产区概况2.需要验证的关键工序及工艺验证3.工艺流程的实施4.操作过程及工艺条件5.技术安全、工艺卫生及劳动保护6.物料平衡及技经指标7.设备一览表8.岗位定员9.附件(含设备操作、清洁规程)10.变更记录1.大容量注射剂生产区概况本生产区面积904㎡,其中1万级净化区域167㎡,10万级净化区域174㎡。
大容量注射剂车间采用10万级和1万级(局部百级)空气净化洁净级别,10万级区域设置缓冲、更衣、洗涤、洁具、称量、配碳、浓配、洗瓶等,1万级区域设置缓冲、更衣更鞋、稀配、化验、灌装、加塞、轧盖、洗涤、存放、洁具等功能间,所有隔断采用无粉尘产生的静电喷涂彩钢板,结合处采用圆角处理,不易产生积灰;人员经过三次更衣和二次更鞋后进入洁净区操作,物料进入洁净区均采用传递窗或气闸进行传递,人流、物流的进入相对分开,保证了洁净区空气洁净度要求;生产设备均采用优质不锈钢材料制造,采用洗瓶、灌装、压塞、轧盖联动线生产,其中洗瓶出口、灌装、加塞采用百级层流保护,灭菌器采用水浴式灭菌器。
1.1 大容量注射剂生产工艺流程图(见后页)1.2 大容量注射剂生产区工艺布局布置图(见后页)1.3 大容量注射剂生产区工艺设备布置图(见后页)1.4 大容量注射剂生产区送回风口平面布置图(见后页)以上项目按验证文件规定,均已在规定周期内进行相关的验证,验证方案及报告见相应文件。
大容量注射剂生产工艺流程图3.工艺流程的实施3.1 批生产指令的签发3.1.1 批生产指令由车间技术负责人根据生产计划表起草,并依据产品工艺规程于生产前一个工作日制定。
3.1.2 批生产指令应经QA质监员审核并签字,由车间主任签字批准后生效。
3.2 生产批记录的发放3.2.1 除配制工序和包装工序外,工序相应的生产批记录于生产当日由车间工艺质监员发放给各工序负责人,并于工序结束当日填写完整返回车间工艺质监员处汇总。
3.2.2 配制工序和包装工序的生产批记录于生产前一天由车间工艺质监员随同批生产指令或批包装指令一同发放,并于工序结束当日填写完整返回车间工艺质监员处汇总。

造粒车间工艺流程图一、引言造粒车间是制药工厂中的关键环节之一,主要用于将药物原料转化为固体颗粒状,以便后续的包装和贮存。
本文将详细描述造粒车间的工艺流程图,以便于操作人员和相关人员了解和执行。
二、工艺流程图以下是造粒车间的工艺流程图,包括了主要的步骤和操作要点:1. 原料准备- 原料称量:根据配方要求,将所需原料按照一定比例称量。
- 原料检查:对原料进行外观、颜色、气味等方面的检查,确保原料的质量符合要求。
2. 制粒过程- 混合:将称量好的原料进行混合,以确保药物成份均匀分布。
- 研磨:将混合好的原料进行研磨,使其达到所需的颗粒大小。
- 湿法造粒:将研磨好的原料与粘结剂一起加入造粒机中,通过湿法造粒的方法将原料转化为颗粒状。
- 干燥:将湿法造粒后的颗粒进行干燥,以去除多余的水分。
3. 筛分和包装- 筛分:将干燥后的颗粒进行筛分,以去除不合格的颗粒。
- 包装:将筛分好的颗粒根据包装要求进行分装,通常采用自动包装机进行操作。
4. 清洁和消毒- 清洁:定期对造粒车间进行清洁,包括地面、设备、工作台等的清洁。
- 消毒:定期对造粒车间进行消毒,以确保无菌环境。
5. 记录和报告- 记录:对每一个步骤进行记录,包括原料的批次号、操作人员、时间等信息。
- 报告:根据记录的数据生成相应的报告,以便于管理人员进行分析和决策。
三、数据示例以下是一个示例数据,用于说明造粒车间的工艺流程中的一些关键数据:- 原料称量:A药物100g,B药物200g,C药物50g。
- 原料检查:外观正常,颜色无异物,气味符合要求。
- 混合:将A、B、C药物按比例混合,混合时间10分钟。
- 研磨:将混合好的药物研磨至颗粒大小在100-200微米之间。
- 湿法造粒:将研磨好的药物与粘结剂按比例加入造粒机中,造粒时间30分钟。
- 干燥:将湿法造粒后的颗粒进行干燥,干燥温度80摄氏度,干燥时间2小时。
- 筛分:通过筛网筛分,颗粒大小符合要求的通过,不合格的剔除。



造粒车间工艺流程图标题:造粒车间工艺流程图引言概述:造粒车间是制药行业中重要的生产环节之一,其工艺流程图对于保证产品质量和提高生产效率具有重要意义。
本文将详细介绍造粒车间工艺流程图的内容和作用。
一、原料准备1.1 原料检验:对进入车间的原料进行检验,包括外观、成份、含杂质等指标的检测。
1.2 原料研磨:将原料进行研磨,使其达到所需的颗粒大小和均匀度。
1.3 原料混合:将不同的原料按照一定的配比进行混合,确保最终产品的成份均匀。
二、造粒过程2.1 湿法造粒:将混合好的原料与溶剂进行混合,形成湿糊状物,然后通过造粒机进行造粒,使其成为所需的颗粒状物料。
2.2 干法造粒:将混合好的原料通过干燥机进行烘干,然后通过造粒机进行造粒,形成所需的颗粒状物料。
2.3 烘干:将湿法或者干法造粒得到的颗粒状物料进行烘干,去除多余的水分,提高颗粒的稳定性和质量。
三、造粒后处理3.1 筛分:将造粒后的颗粒进行筛分,去除不符合要求的颗粒,保证产品的均匀度。
3.2 包装:将符合要求的颗粒进行包装,以确保产品的安全性和卫生性。
3.3 清洁和维护:对造粒车间的设备进行定期清洁和维护,保证设备的正常运行和生产的连续性。
四、质量控制4.1 在线监测:通过在工艺流程中设置传感器和监测仪器,对关键指标进行在线监测,及时发现和处理异常情况。
4.2 抽样检验:对生产过程中的样品进行抽样检验,检测产品的质量指标是否符合标准要求。
4.3 数据分析:对监测和检验得到的数据进行分析,评估产品的质量水平和生产过程的稳定性,为工艺改进提供依据。
结论:造粒车间工艺流程图是指导生产操作和质量控制的重要工具,通过准确的流程图可以保证原料的准备、造粒过程、后处理和质量控制的有序进行,提高产品的质量和生产效率。
在实际操作中,应根据具体情况进行调整和改进,以适应不同产品的生产需求。


造粒车间工艺流程图标题:造粒车间工艺流程图引言概述:造粒车间是制药工业中非常重要的一个环节,通过工艺流程图可以清晰地展示每一个步骤的操作顺序和关联,有助于提高生产效率和质量。
本文将详细介绍造粒车间工艺流程图的内容和重要性。
一、原料准备阶段1.1 确定原料种类和数量:根据产品配方确定所需原料的种类和数量,确保生产过程中原料供应充足。
1.2 原料清洁处理:对原料进行清洁处理,去除杂质和异物,确保产品质量。
1.3 原料称量:按照配方要求对原料进行称量,确保每一个批次的原料使用量准确。
二、混合造粒阶段2.1 混合:将各种原料按照配方比例加入混合机中进行混合,确保原料均匀混合。
2.2 加水造粒:在混合过程中逐渐加入适量的水或者溶剂,形成颗粒状的混合物。
2.3 混合物检验:对混合物进行质量检验,确保颗粒大小和形状符合要求。
三、造粒干燥阶段3.1 干燥:将混合造粒物料送入干燥机中,通过加热和通风使其脱水干燥,减少水分含量。
3.2 干燥温度控制:根据不同产品的要求,控制干燥机的温度和时间,确保产品干燥均匀。
3.3 干燥后检验:对干燥后的颗粒进行外观和质量检验,确保产品符合标准。
四、筛分包装阶段4.1 筛分:将干燥后的颗粒进行筛分,去除过大或者过小的颗粒,保证产品粒度均匀。
4.2 包装:将符合要求的颗粒进行包装,根据产品规格选择合适的包装材料和方式。
4.3 包装检验:对包装好的产品进行外观和分量检验,确保包装完好无损。
五、清洁消毒阶段5.1 清洁:对造粒车间的设备和环境进行定期清洁,防止交叉污染。
5.2 消毒:使用适当的消毒剂对车间进行消毒,确保生产环境卫生。
5.3 清洁消毒记录:记录清洁消毒的时间和方法,建立健全的清洁消毒管理制度。
结论:通过工艺流程图可以清晰地展示造粒车间的生产流程,匡助生产人员了解每一个步骤的操作要点和关联,提高生产效率和产品质量。
因此,制定和遵循科学的工艺流程图对于造粒车间的生产至关重要。
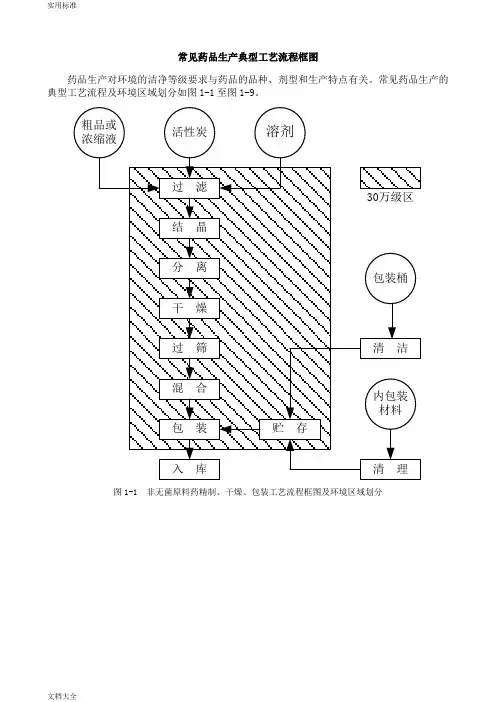
常见药品生产典型工艺流程框图
药品生产对环境的洁净等级要求与药品的品种、剂型和生产特点有关。
常见药品生产的典型工艺流程及环境区域划分如图1-1至图1-9。
图1-1 非无菌原料药精制、干燥、包装工艺流程框图及环境区域划分
图1-2 无菌原料药精制、干燥、包装工艺流程框图及环境区域划分
图1-3 片剂生产工艺流程框图及环境区域划分
图1-4 硬胶囊剂生产工艺流程框图及环境区域划分
图1-5 压制法软胶囊剂生产工艺流程框图及环境区域划分
图1-6 可灭菌小容量注射剂生产工艺流程框图及环境区域划分
图1-7 可灭菌大容量注射剂生产工艺流程框图及环境区域划分
图1-8 注射用无菌分装产品生产工艺流程框图及环境区域划分
图1-9 注射用冷冻干燥制品生产工艺流程框图及环境区域划分。

流程图-仿制药一、概述本文档将介绍关于仿制药的制造流程图。
仿制药是指在原研药品专利期满后,其他制药企业通过开发新的工艺、新的配方,生产与原研药品相同或相似的药品。
通过流程图展示,可以清晰地了解仿制药的制造过程。
二、流程图在下面的流程图中,将展示仿制药的制造流程,包括原料采购、药品研发、生产、质检和包装等环节。
graph LRA[原料采购] --> B[药品研发]B --> C[生产]C --> D[质检]D --> E[包装]三、详细说明1. 原料采购原料采购是仿制药制造的第一步。
制药企业需要根据药品的配方和工艺要求,采购符合标准的原料。
采购人员需要与供应商进行沟通,确认原料的质量和数量,并进行采购订单的签订。
2. 药品研发药品研发是仿制药制造的核心环节。
研发团队需要根据原研药品的配方和工艺,以及自身的技术实力,进行药品的研发工作。
这包括对原料的配比、药品制造工艺的改进等方面的工作。
研发人员需要进行大量的试验和实验室测试,最终确定出符合要求的制药工艺和配方。
3. 生产生产是仿制药制造的主要环节。
根据药品研发阶段确定的工艺和配方,制药企业需要按照严格的操作规程进行药品的生产。
生产人员需要准确地按照工艺流程进行操作,以确保药品的质量和安全性。
4. 质检质检环节是对生产出来的仿制药进行质量检验的过程。
制药企业需要建立完善的质检体系,对药品进行各种指标的检测。
质检人员需要使用各种仪器设备,对药品的外观、成分、纯度等方面进行检测,以确保药品符合国家相关的质量标准。
5. 包装包装环节是对仿制药进行包装和标识的过程。
制药企业需要使用适当的包装材料,将生产出来的仿制药进行包装,并在包装上标识药品的信息,如药品名称、用法、剂量等。
包装人员需要按照相关规定,进行包装和标识的操作。
四、总结通过以上流程图,我们可以清晰地了解仿制药的制造流程。
原料采购、药品研发、生产、质检和包装等环节都是制造一款仿制药所必须的步骤。

造粒车间工艺流程图一、引言造粒车间是制药工厂中非常重要的一个环节,主要用于将药物原料制成颗粒状,以便于后续的包装和使用。
本文将详细介绍造粒车间的工艺流程图,包括原料准备、混合、造粒、干燥和包装等环节。
二、工艺流程图以下是造粒车间的工艺流程图:1. 原料准备- 原料入库:原料从仓库中取出,并进行验收,确保质量符合要求。
- 称量:按照配方要求,将各种原料进行称量,确保准确的配比。
2. 混合- 将称量好的原料放入混合机中,启动混合机进行搅拌,使各种原料充分混合均匀。
3. 造粒- 将混合好的原料送入造粒机中,通过挤压和切割的作用,将原料制成颗粒状。
- 造粒机的参数设置:包括挤压力、切割速度、刀具形状等,根据不同的原料和产品要求进行调整。
4. 干燥- 将造粒好的颗粒送入干燥机中,通过热风的作用,将颗粒中的水分蒸发掉,使颗粒变得干燥。
- 干燥机的参数设置:包括温度、湿度、风速等,根据不同的原料和产品要求进行调整。
5. 包装- 干燥好的颗粒通过输送带送入包装机中,进行自动包装。
- 包装机的参数设置:包括包装速度、包装材料、包装形式等,根据产品要求进行调整。
三、工艺流程图解析1. 原料准备:确保原料质量符合要求,避免对产品质量产生不良影响。
2. 混合:保证各种原料充分混合均匀,避免浮现局部成份不均匀的情况。
3. 造粒:通过挤压和切割的作用,将原料制成颗粒状,确保颗粒的形状和大小符合要求。
4. 干燥:将颗粒中的水分蒸发掉,使颗粒变得干燥,以便于后续的包装和使用。
5. 包装:对干燥好的颗粒进行自动包装,确保包装质量和效率。
四、工艺流程图的优势1. 易于理解:通过图形化的形式,直观地展示了整个工艺流程,使人们更容易理解和掌握。
2. 信息全面:工艺流程图中包含了每一个环节的具体步骤和参数设置,使人们能够全面了解整个工艺过程。
3. 便于优化:通过观察工艺流程图,可以发现其中的问题和瓶颈,从而进行优化和改进,提高生产效率和产品质量。
造粒车间工艺流程图一、引言造粒车间是制药工厂中的重要环节之一,主要用于将原料药粉末转化为颗粒状,以便后续的制剂工艺使用。
本文将详细介绍造粒车间的工艺流程图及各个步骤的操作要点。
二、工艺流程图以下是造粒车间的工艺流程图,包括了主要的工艺步骤和设备。
1. 原料准备- 原料药粉的称量:根据配方要求,将所需的原料药粉进行准确的称量。
- 原料药粉的筛选:通过筛网将原料药粉进行筛选,以去除杂质和团聚的颗粒。
2. 湿法造粒- 溶液制备:将一定比例的溶剂和辅料加入搅拌槽中,充分搅拌均匀。
- 混合:将称量好的原料药粉逐步加入搅拌槽中,与溶液进行充分混合。
- 湿法造粒:将混合好的药物溶液通过喷雾装置喷洒到旋转的造粒盘上,形成颗粒状的湿团。
- 干燥:将湿团放入烘干设备中,通过热风将水分蒸发,使颗粒逐渐变干。
3. 干法造粒- 原料药粉的筛选:同样需要对原料药粉进行筛选,以去除杂质和团聚的颗粒。
- 干法造粒:将筛选好的原料药粉通过造粒机进行干法造粒,通过机械力的作用使粉末会萃成颗粒。
- 筛分:将干法造粒得到的颗粒进行筛分,以控制颗粒的大小范围。
4. 成品处理- 冷却:将造粒后的颗粒通过冷却设备进行降温,以防止颗粒在后续的包装过程中变软或者粘连。
- 包装:将冷却好的颗粒通过自动包装机进行包装,通常使用密封袋或者瓶装。
5. 清洁和消毒- 设备清洁:定期对造粒车间的设备进行清洁,以确保生产环境的卫生和产品质量的稳定。
- 环境消毒:定期对车间进行消毒处理,以杀灭细菌和微生物,防止交叉污染。
三、操作要点1. 原料准备阶段:- 确保原料药粉的准确称量,避免误差对产品质量造成影响。
- 注意原料药粉的筛选工作,确保颗粒的均匀性和纯净度。
2. 湿法造粒阶段:- 溶液制备时要充分搅拌均匀,确保药物和溶剂的充分混合。
- 控制喷雾装置的喷雾量和角度,以获得均匀的湿团。
- 干燥过程中要控制热风的温度和流量,避免颗粒过度干燥或者过度结块。
3. 干法造粒阶段:- 控制干法造粒机的转速和压力,以获得理想的颗粒形态和大小。
常见药品生产典型工艺流程框图
药品生产对环境的洁净等级要求与药品的品种、剂型和生产特点有关;常见药品生产的典型工艺流程及环境区域划分如图1-1至图1-9;
图1-1 非无菌原料药精制、干燥、包装工艺流程框图及环境区域划分
图1-2 无菌原料药精制、干燥、包装工艺流程框图及环境区域划分
图1-3 片剂生产工艺流程框图及环境区域划分
图1-4 硬胶囊剂生产工艺流程框图及环境区域划分
图1-5 压制法软胶囊剂生产工艺流程框图及环境区域划分
图1-6 可灭菌小容量注射剂生产工艺流程框图及环境区域划分
图1-7 可灭菌大容量注射剂生产工艺流程框图及环境区域划分
图1-8 注射用无菌分装产品生产工艺流程框图及环境区域划分
图1-9 注射用冷冻干燥制品生产工艺流程框图及环境区域划分。
造粒车间工艺流程图一、引言造粒车间是制药工厂中的重要环节,主要用于将原料粉末转化为颗粒状的制剂。
本文将详细介绍造粒车间的工艺流程图,并对每一个步骤进行详细解释。
二、工艺流程图以下是造粒车间的工艺流程图:1. 原料准备- 原料称量:根据配方要求,将所需原料按照一定比例进行称量。
- 原料筛选:将称量好的原料进行筛选,去除杂质和颗粒不均匀的原料。
2. 混合- 原料混合:将筛选好的原料放入混合机中,进行均匀混合,确保每一个颗粒中含有相同的成份。
3. 湿法造粒- 混合物溶解:将混合好的原料溶解在适量的溶剂中,形成浆状物。
- 搅拌:通过搅拌机对浆状物进行搅拌,使其均匀混合。
- 喷雾造粒:将搅拌好的浆状物通过喷雾器喷雾到烘干室中,形成颗粒状的制剂。
- 干燥:将喷雾后的颗粒状制剂在烘干室中进行干燥,除去溶剂,使其固化。
4. 干法造粒- 混合物压缩:将混合好的原料放入造粒机中,通过压力将其压缩成颗粒状的制剂。
- 筛分:将压缩后的颗粒进行筛分,去除不符合要求的颗粒。
- 干燥:将筛分后的颗粒状制剂在烘干室中进行干燥,除去水分,使其固化。
5. 筛分和包装- 筛分:将干燥后的颗粒进行筛分,去除不符合要求的颗粒。
- 包装:将筛分好的颗粒状制剂进行包装,通常使用密封包装袋或者瓶子。
6. 清洁和消毒- 清洁:定期对造粒车间的设备进行清洁,确保无尘和杂质。
- 消毒:定期对造粒车间进行消毒,以确保制剂的质量和卫生安全。
三、工艺流程解释1. 原料准备:原料的准备是创造高质量制剂的关键步骤。
通过精确的称量和筛选,可以确保原料的质量和成份的准确性。
2. 混合:混合过程中,原料的均匀性对最终产品的质量起着重要作用。
混合机的选择和操作技术对混合效果有直接影响。
3. 湿法造粒:湿法造粒适合于一些难以通过干法造粒实现的制剂。
溶解和搅拌过程确保原料均匀分散,喷雾造粒和干燥过程将浆状物转化为颗粒状制剂。
4. 干法造粒:干法造粒适合于一些不适合湿法造粒的制剂。
1 目的规范阿莫西林车间生产工艺规程,使本产品生产操作过程具有一致性和保证产品质量的均一性,为该产品的生产提供技术标准。
2 范围适用于阿莫西林原料药生产的全过程。
3 责任生产部组织制订,生产车间按要求严格执行,质管部、生产部监督实施。
4 内容4.1 产品概述4.1.1 产品名称:4.1.1.1 法定名称:阿莫西林4.1.1.2 别名:羟氨苄青霉素4.1.1.3 汉语拼音:Amoxilin4.1.1.4 英文名:Amoxicillin4.1.2 产品概述:4.1.2.1 化学名称:(2S,5R,6R)-3,3-二甲基-6-[(R)-(-)-2-氨基-2-(4-羟基苯基)乙酰氨基]-7-氧代-4-硫杂-1-氮杂双环[3.2.0]庚烷-2-甲酸三水合物。
4.1.2.2 分子式:C16H19N3O5S·3H2O4.1.2.3 分子量:419.464.1.2.4 结构式:4.1.2.5 理化性质本品为白色或类白色结晶性粉末;味微苦;在水中微溶,在乙醇中几乎不溶。
比旋度+290~+305℃。
4.1.2.6 用途:阿莫西林为青霉素类抗生素,具有抗菌谱广、疗效高、疗程短、安全可靠,毒副作用少、使用方便、使用成本低等特点。
对肺炎链球菌、溶血性链球菌等链球菌属、不产青霉素酶葡萄球菌、粪肠球菌等需氧革兰阳性球菌,大肠埃希菌、奇异变形杆菌、沙门菌属、流感嗜血杆菌、淋病奈瑟菌等需氧革兰阴性菌的不产β内酰胺酶菌株及幽门螺杆菌具有良好的抗菌活性。
阿莫西林通过抑制细菌细胞壁合成而发挥杀菌作用,可使细菌迅速成为球状体而溶解、破裂。
4.1.2.7 包装规格:25Kg/桶。
4.1.2.8 贮藏:遮光,密封保存。
4.2 主要原辅料、包装材料质量标准4.2.1 原辅料酰基转移酶干物质,%14.0~16.0 酶活力,u/g≥800水质符合饮用水标准,其中结晶所用水符合纯化水标准。
4.2.2 包装材料 4.2.2.1 塑料袋无色聚乙烯塑料袋为药用规格,其质量标准符合国家标准GB/T 10005—1998。