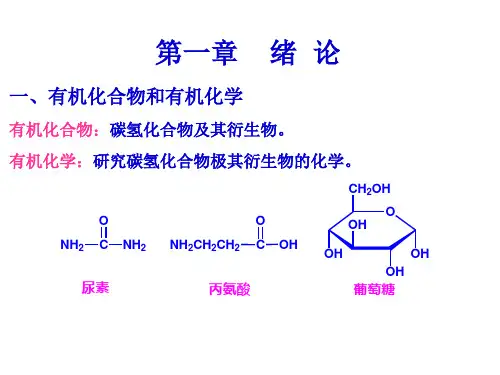
优选有机化学绪论
- 格式:ppt
- 大小:1.95 MB
- 文档页数:71

有机化学之绪论知识点1.有机反应类型均裂反应1.均裂反应:共价键断裂时,成键的一对电子平均分给两个成键的原子或基团,这种断裂方式成为均裂。
2.均裂产生的具有未成对电子的原子或基团称为自由基。
3.共价键均裂产生自由基而引发的反应称为自由基反应。
异裂反应1.共价键断裂时,成键一对电子完全由一个原子或基团独得成负离子,另一个原子或基团则缺一个电子而成正离子,这种断裂方式为异裂。
2.由共价键异裂产生离子而进行的反应称为离子型反应。
3.自由基,碳正离子和碳负离子都是反应过程中暂时生成的,瞬间存在的活性中间体。
协同反应在反应中没有明显分布的共价键的均裂和异裂,即没有自由基或带电荷的离子生成,反应是通过一个环状的过渡态,化学键的断裂和形成同时完成而得到产物。
2.有机化合物构造式的表示方法分子式,电子式、结构式、结构简式、键线式3.便于理解有机物分子的结构—分子模型球棍模型、比例模型4.异构现象1.异构体一般分为构造异构体和构型异构体。
2.构造异构体指分子中原子的连接方式和顺序不同。
3.构型异构体指分子的构造相同而原子或基团在空间的排布方式不同。
5.有机化合物的分类1.按碳链分类:开链化合物、碳环化合物、杂环化合物2.按官能团分类:烯、炔、卤代烃、醇或酚、醚等。
6.质子理论1.凡是能给出质子的物质为酸,能接受质子的物质为碱2.一个酸给出质子后生成的物质,即为该酸的共轭碱,一个碱接受质子后形成的物质,即为该碱的共轭酸。
3.酸越强,它的共轭碱的碱性就越弱。
4.优缺点:酸碱的质子理论扩大了酸碱的范围,应用十分方便。
它的缺点是那些不交换H+而具有酸性的物质不能包含在内。
7.电子理论1.由路易斯提出2.能够接受电子对的物质为酸,能够给出电子对的物质为碱。
3.酸碱电子理论中的酸碱反应实际上是形成配位键的过程。
8.分子间力1.即分子间存在的引力,一般称为范德华力2.范德华力包括:取向力、诱导力、色散力。
3.氢键是一种特殊的永久偶极间作用力。


有机化学课件绪论一、引言有机化学是研究碳原子与氢原子以及其他元素原子之间化学键形成、断裂和转化的科学。
作为一门重要的自然科学学科,有机化学在生命科学、材料科学、环境科学等领域具有广泛的应用。
本课件旨在系统介绍有机化学的基本概念、基本理论和基本技能,使读者能够掌握有机化学的基本原理,为后续学习和研究打下坚实基础。
二、有机化学的研究对象与任务1.研究对象(1)脂肪烃:由碳原子和氢原子组成的链状或环状化合物,如烷烃、烯烃、炔烃等。
(2)芳香烃:含有苯环或稠苯体系的化合物,如苯、甲苯、萘等。
(3)卤代烃:含有卤素(氟、氯、溴、碘)原子的有机化合物,如氟利昂、四氯化碳等。
(4)醇、酚、醚:含有羟基(-OH)或氧桥(-O-)的有机化合物,如甲醇、苯酚、乙醚等。
(5)醛、酮:含有羰基(>C=O)的有机化合物,如甲醛、丙酮等。
(6)羧酸、酯:含有羧基(-COOH)或酯基(-COO-)的有机化合物,如乙酸、乙酸乙酯等。
(7)胺、酰胺:含有氨基(-NH2)或酰胺基(-CONH2)的有机化合物,如甲胺、乙酰胺等。
(8)糖类、脂类、蛋白质、核酸等生物大分子:构成生命体的基本物质,具有复杂的结构和多样的功能。
2.研究任务(1)研究有机化合物的结构:通过现代化学实验技术和理论计算方法,揭示有机化合物的分子结构、立体结构和电子结构。
(2)研究有机化合物的性质:探讨有机化合物的物理性质、化学性质和生物学性质,为实际应用提供理论基础。
(3)研究有机化合物的合成方法:发展高效、绿色、可控的有机合成方法,为新材料、新药物的研发提供技术支持。
(4)研究有机化合物的反应机理:深入了解有机化学反应的历程,为有机合成提供理论指导。
(5)研究有机化学在交叉领域的应用:将有机化学与生命科学、材料科学、环境科学等领域相结合,解决实际问题。
三、有机化学的基本理论1.共价键理论:共价键是有机化合物中碳原子与氢原子以及其他元素原子之间形成的化学键。


《有机化学》第一章绪论一、教学内容本节课的教学内容来自于《有机化学》第一章绪论。
这部分内容主要包括有机化学的基本概念、有机化合物的分类、有机化学反应类型以及有机化合物的结构和性质。
具体内容包括:1. 有机化合物的定义和特点:介绍有机化合物的概念,解释有机化合物的特点,如碳氢化合物的存在、有机化合物的命名规则等。
2. 有机化合物的分类:介绍烷烃、烯烃、炔烃、芳香烃等有机化合物的分类和特点,解释它们的结构差异和性质特点。
3. 有机化学反应类型:介绍加成反应、消除反应、取代反应等有机化学反应类型,解释反应机理和反应条件。
4. 有机化合物的结构和性质:介绍有机化合物的结构特点,如碳原子的四价键、有机化合物的同分异构现象等,解释有机化合物的物理性质和化学性质。
二、教学目标1. 学生能够理解有机化学的基本概念和特点,掌握有机化合物的分类和命名规则。
2. 学生能够了解有机化学反应的类型和机理,理解反应条件和反应产物的关系。
3. 学生能够分析有机化合物的结构和性质,运用有机化学的基本原理解决实际问题。
三、教学难点与重点重点:有机化合物的分类和特点、有机化学反应类型和机理、有机化合物的结构和性质。
难点:有机化合物的结构和性质的理解和应用、有机化学反应机理的掌握。
四、教具与学具准备教具:黑板、粉笔、多媒体教具、有机化合物的模型或图示。
学具:笔记本、笔、有机化合物的结构模型或图示、有机化学反应机理的图示。
五、教学过程1. 引入:通过展示有机化合物的实际例子,如糖类、脂肪、蛋白质等,引起学生对有机化学的兴趣,引出本节课的主题。
2. 讲解:在黑板上用粉笔写出有机化合物的定义和特点,引导学生理解有机化合物的概念和特点。
然后,通过图示和模型,讲解有机化合物的分类和结构特点,如烷烃、烯烃、炔烃、芳香烃等。
3. 示例:通过具体的有机化学反应实例,讲解加成反应、消除反应、取代反应等有机化学反应类型,解释反应机理和反应条件。
4. 练习:给出一些有机化合物的结构和性质的题目,让学生通过观察和分析,回答题目,巩固对有机化合物的结构和性质的理解。


大一有机化学绪论知识点1.有机化合物的分类:有机化合物是含有碳元素的化合物,按照功能基团可以分为醇、醚、醛、酮、羧酸、酯等。
2.有机化学键:有机化合物中的化学键可以分为共价键和极性键。
共价键是由共用电子对形成的,常见的有单键、双键和三键。
极性键则是由于电负性差异而产生的偏向性。
3.共轭体系:共轭体系是指一个或多个单键和一个或多个共轭双键相互交替排列而形成的一组π键的结构。
共轭体系具有较小的能量差异,因此比较稳定。
4.异构体:异构体是指分子式相同但结构不同的化合物。
包括构造异构体、空间异构体和立体异构体。
构造异构体是指化合物的分子结构不同,如链异构体和环异构体。
空间异构体是指化合物的空间取向不同,如顺反异构体。
立体异构体是指化合物分子中具有手性中心,存在手性异构体。
5.有机反应的基本原理:有机反应是有机化合物发生变化的过程。
常见的有机反应包括加成反应、消除反应、取代反应和重排反应。
加成反应是指两个分子结合而形成一个新的分子,消除反应是指一个分子分解为两个分子,取代反应是指一个原子或基团被另一个原子或基团取代,重排反应是指分子内原子或基团的位置发生变化。
6.极性和溶解性:极性是指分子中正负电荷分布的不均匀性。
极性分子通常具有较强的溶解性,而非极性分子溶解性较差。
极性溶剂通常可以溶解极性物质,非极性溶剂可以溶解非极性物质。
7.共沉淀和分配:共沉淀是指两种或更多种物质在溶液中发生反应而形成沉淀。
分配是指两个相互不相溶的液体中的物质在两相之间分配的过程。
分配系数是用来描述分配过程的指标。
8.杂环化合物:杂环化合物是指含有不同原子的环状化合物。
常见的杂环化合物包括含氧杂环、含氮杂环、含硫杂环等。
杂环化合物具有较强的化学活性和生物活性。
9.光学活性和手性:光学活性是指一些化合物对旋光的作用。
手性是指分子不具有镜面对称性,分为左旋体和右旋体。
手性分子与手性反应物之间发生反应时会产生对映异构体。
10.环加成反应和开链加成反应:环加成反应是指在环状化合物中发生加成反应,如环状醇的开环加成反应。