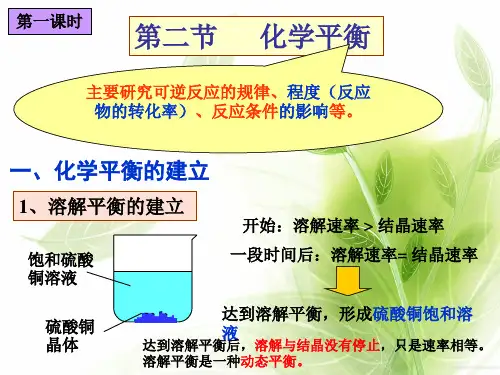
率增大,A错误,C正确;加压平衡正向移动,说明a>c+d,物质D的浓度增大,B、
D错误。
学以致用•随堂检测全达标
1.反应X(g)+Y(g)
(
2Z(g)
ΔH<0,达到平衡状态时,下列说法正确的是
)
A.减小容器容积,平衡向右移动
B.加入催化剂,Z的产率增大
C.增大X的浓度,X的转化率增大
D.降低温度,Y的转化率增大
答案D
解析因为该反应为反应前后气态物质物质的量不变的反应,故减小容器容
积,化学平衡不发生移动,A项错误;加入催化剂可同等程度地改变正、逆反
应速率,故化学平衡不会发生移动,B项错误;增大X的浓度,化学平衡向右移
动,但X的转化率减小,C项错误;该反应的正反应放热,降低温度,化学平衡
向移动;体系冷却颜色变浅,说明c(NO2)减小,即平衡向放
热反应方向移动
2.温度对化学平衡影响的解释
从化学平衡的影响因素和Q与K的关系角度分析,填写下表:
反应类型 温度变化
升温
放热反应
降温
升温
吸热反应
降温
K值变化 Q与K的关系
Q>K
减小
Q<K
增大
Q<K
增大
Q>K
减小
平衡移动方向
逆向移动
正向移动
正向移动
为常数,移走后平衡不移动;D项,通入NH3,c平(NH3)增大,平衡左移。
易错警示 化学平衡移动中浓度的“决定性”作用
(1)恒温、恒容条件:原平衡体系体系
各组分的浓度不变→平衡不移动。
(2)恒温、恒压条件:
总压强增大→体系中
变式训练2在新制的氯水中存在平衡:Cl2+H2O