初中化学溶解度曲线及其应用
- 格式:ppt
- 大小:2.23 MB
- 文档页数:16

【班主任⽀招】中考化学核⼼考点:溶解度曲线及其应⽤⼀、近年中考溶解度曲线考查⽅式:(固体物质)溶解度曲线属于中考的必考内容。
考查⽅式:⼀线型、⼆线型、三线型、四线型、实验与曲线融合型等。
要明确:①各物质溶解度曲线的由来:⽤纵坐标表⽰溶解度,横坐标表⽰温度,许多点组成的⼀条光滑曲线,反过来讲:纵坐标表⽰溶解度,横坐标表⽰相应的温度;②会看图中各类曲线的⾛势,明确其中的含义;③知道各类曲线的交点的含义:在该温度下两类物质的溶解度相同;④会通过⽐对坐标图中纵截距的长短,来判断温度变化引起各饱和溶液析出的晶体多少;⑤根据曲线的⾛势,会采取⼀定⽅法(改变温度、溶剂量等)实现该溶质的溶液饱和溶液变与不饱和溶液相互转化;⑥会⽐较某⼀温度下,不同溶质的溶解度的⼤⼩等;⑦知道氢氧化钙的溶解度曲线以其溶解度 “反常” 的特性;⑧会判断“线外点”所对应的溶液的状态。
⼆、知识梳理与答题指导★★★点的意义1.溶解度曲线上的点表⽰物质在该点所⽰温度下的溶解度,溶液所处的状态是饱和溶液。
2.溶解度曲线下⾯的⾯积上的点,表⽰溶液所处的状态是不饱和状态,依其数据配制的溶液为对应湿度时的不饱和溶液。
3.溶解度曲线上⾯的⾯积上的点,依其数据配制的溶液为对应温度时的饱和溶液,且该溶质有剩余。
4.两条溶解度曲线的交点,表⽰在该点所⽰的温度下,两种物质的溶解度相等。
★★★变化规律1.⼤多数固体物质的溶解度随湿度升⾼⽽增⼤,曲线为"陡升型,如硝酸钾。
2.少数固体物质的溶解度受湿度的影响很⼩,曲线为"缓升型,如氯化钠。
3.极少数固体物质的溶解度随湿度的升⾼⽽减⼩,曲线为"下降型,如氢氧化钙。
4.⽓体物质的溶解度均随湿度的升⾼⽽减⼩(纵坐标表⽰体积),曲线也为"下降型,如氧⽓。
★★★应⽤1.查找指定温度时物质的溶解度,并根据溶解度判断溶解性。
2.⽐较相同湿度时(或⼀定湿度范围内)不同物质溶解度的⼤⼩。
3.⽐较和确定物质的溶解度受温度影响的程度,并据此确定物质结晶或混合物分离提纯的⽅法。



溶解度曲线的意义及应用一、溶解度曲线的概念在直角坐标系中,用横坐标表示温度(t),纵坐标表示溶解度(S),由t—S的坐标画出固体物质的溶解度随温度变化的曲线,称之为溶解度曲线。
二、溶解度曲线的意义1、点曲线上的点叫饱和点,①曲线上任一点表示对应温度下(横坐标)该物质的溶解度(纵坐标);②两曲线的交点表示两物质在交点的温度下溶解度相等。
2、线溶解度曲线表示物质的溶解度随温度变化的趋势。
其变化趋势分为三种:①陡升型大多数固体物质的溶解度随温度升高而增大,如KNO3;②缓升型少数物质的溶解度随温度升高而增幅小,如NaCl;③下降型极小数物质的溶解度随温度升高而减小,如Ca(OH)2。
3、面⑴溶解度曲线下方的面表示不同温度下该物质的不饱和溶液。
⑵溶解度曲线上方的面表示相应温度下的过饱和溶液(不作要求)。
三、溶解度曲线的应用1.判断或比较某一物质在不同温度下溶解度的大小。
例1:(2010•南昌)右图为氯化钠、碳酸钠(俗称纯碱)在水中的溶解度曲线。
(1)当温度为10℃时,碳酸钠的溶解度为;(2)当温度时,氯化钠的溶解度大于碳酸钠的溶解度;(3)生活在盐湖附近的人们习惯“夏天晒盐,冬天捞碱”。
请你解释原因:“夏天晒盐”。
例2、(2009•泰州)右图是A、B两种物质的溶解度曲线,根据图示回答下列问题:℃时,向两只盛有100g水的烧杯中,分别加(1)t入A、B两种物质至不能溶解为止,所得溶液的溶质质量分数较大的是___________溶液(填“A”或“B””)。
(2)t2℃时,欲配制等质量的A、B两种物质的饱和溶液,所需水的质量关系是A________B。
(填写“>”、“<”或“=”,下同)(3)将t2℃的A、B两种物质的饱和溶液各200g,降温至t1℃,析出晶体的质量关系是A______B。
(4)将t2℃的A、B两种物质的饱和溶液各200g,升温至t3℃,欲使它们仍为饱和溶液,若不改变溶剂质量,所需加入固体溶质的质量关系是A_______B。



初三化学溶解度曲线知识点天高鸟飞,海阔鱼跃;考试这舞台,秀出你特殊的杰出;一宿好的睡眠,精神能百倍;一颗淡定的平常心,冷静应对,努力备考,考入理想院校!下面是作者给大家带来的初三化学溶解度曲线知识点,欢迎大家浏览参考,我们一起来看看吧!初三化学溶解度曲线知识点一、溶解度曲线图上的点1、溶解度曲线上的点:表示在该点所示温度下某物质的溶解度。
如A点表示当温度为t2时,物质R的溶解度为ag。
2、两条曲线的交点:表示在该点所示温度下,两种物质的溶解度相同。
如B点表示当温度为t1时,物质R和N的溶解度相等,都为bg。
二、溶解度曲线图上的线每一条曲线都表示这种物质的溶解度随温度变化而变化的总趋势,主要有:1、陡升型:绝大多数固体物质的溶解度随温度的升高而增大,曲线峻峭。
如曲线R,代表物质有KNO3、NH4NO3等。
2、缓升型:少数固体物质的溶解度受温度的影响较小。
如曲线M,代表物质有NaCl。
3、降落型:极少数固体物质的溶解度随温度的升高而减小。
如曲线N,代表物质有Ca(OH)2。
三、溶解度曲线图上的面1、在溶解度曲线上方平面上的任何点:表示在该点所示温度下形成了含有部分固体溶质的饱和溶液,即依照该点所示温度和溶质质量,在100g溶剂中配制得到的溶液是饱和溶液,且还有未溶解完的溶质存在。
如C点。
2、在溶解度曲线下方平面上的任何点:表示在该点所示温度下形成了不饱和溶液,即依照该点所示温度和溶质质量,在100g溶剂中配制得到的溶液是不饱和溶液。
如D点。
四、溶解度曲线图的综合运用1、溶解度曲线上的每一点都代表着对应温度下该物质的溶解度,所以利用溶解度曲线可以查找出某种物质在不同温度时的溶解度。
2、根据溶解度曲线的走向,可以判定或比较各物质的溶解度随温度变化的趋势。
3、可以比较在同一温度下不同物质的溶解度大小。
如在t3时,R、M、N三种物质的溶解度由小到大的顺序为N M R。
初三化学,溶解度曲线解题技能溶解度曲线题型可从点、线、面和交点四个方面进行解答:1.溶解度曲线上的点:溶解度曲线上的每一个点都是表示的是某温度下某种物质的溶解度。


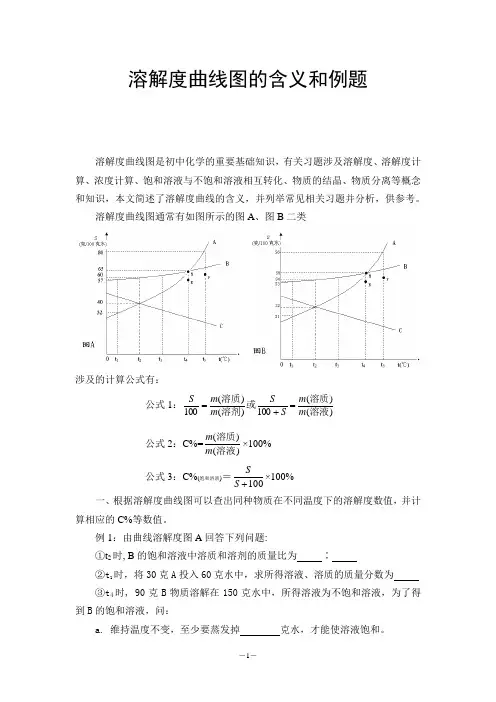
溶解度曲线图的含义和例题溶解度曲线图是初中化学的重要基础知识,有关习题涉及溶解度、溶解度计算、浓度计算、饱和溶液与不饱和溶液相互转化、物质的结晶、物质分离等概念和知识,本文简述了溶解度曲线的含义,并列举常见相关习题并分析,供参考。
溶解度曲线图通常有如图所示的图A、图B二类涉及的计算公式有:公式1:)()(100)()(100溶液溶质或溶剂溶质mmSSmmS=+=公式2:C%=)()(溶液溶质mm×100%公式3:C%(饱和溶液)=100+SS×100%一、根据溶解度曲线图可以查出同种物质在不同温度下的溶解度数值,并计算相应的C%等数值。
例1:由曲线溶解度图A回答下列问题:①t2时, B的饱和溶液中溶质和溶剂的质量比为∶②t1时,将30克A投入60克水中,求所得溶液、溶质的质量分数为③t4时, 90克B物质溶解在150克水中,所得溶液为不饱和溶液,为了得到B的饱和溶液,问:a. 维持温度不变,至少要蒸发掉克水,才能使溶液饱和。
b. 维持温度不变,原溶液中至少再加入B 克,才能使溶液饱和。
c.不改变溶液组成,只要把温度降低到 ℃,也能使溶液恰好达到 饱和。
④要配制C%为28.6%的C 物质溶液,配制时的温度应控制在 ℃。
解:①由图A 知t 2时,S B =60克∕100克水,由公式1,则溶质和溶剂的质量比为60∶100②由图A 知t 1时,S A =32克∕100克水,根据公式可知在60克水中最多溶解19.2克A 物质,则C%=602.192.19+×100%=24.2% ③a :已知t 4时,S B =65克∕100克水,根据公式1,x 9010065= x =138克, 则150-138=12克,即蒸发12克水可使溶液饱和。
b :同理15010065y = y =97.5 97.5-90=7.5,即加入7.5克B 物质可使溶液饱和。
c :同理,根据公式1,15090100=S S =60克∕100克水,即把温度降低 到t 2时,溶液恰好饱和。

溶解度曲线及其应用1.溶解度曲线上每一点表示该物质在不同温度下的不同的溶解度。
2.溶解度曲线上的任意一点表示在该温度下某物质的溶解度是多少克。
3.不同物质溶解度曲线的交点处,表示不同物质在相对应的同一温度下的溶解度相同。
4.溶解度曲线上方的一点,表示在指定温度下,溶液中的溶质质量已超过该物质的溶解度,溶液是过饱和的;溶解度曲线下方的一点,表示在指定温度下,溶液中溶质质量还没有达到溶解度的量,溶液是不饱和的。
5.溶解度曲线的特征是:(1)大部分固体物质的溶解度曲线左低右高,溶解度随温度的升高而增加;(2)少数固体物质的溶解度曲线较平缓,溶解度受温度的影响小,如食盐;(3)极少数固体物质的溶解度曲线是左高右低,溶解度随温度的升高而降低,如熟石灰。
6.溶解度曲线的应用:(l)由已知温度查某物质对应的溶解度;(2)由物质的溶解度查该物质所处的温度;(3)比较同一温度下不同物质的溶解度;(4)设计混合物分离或提纯的方法,例如提纯NaCl可用蒸发溶剂法,分离NaCl和NaNO3可用降温结晶法。
下面举一例来说明溶解度曲线的应用。
图中曲线a、b、c分别表示a、b、c三种物质的溶解度曲线,试回答:(1)t1℃时,a、b、c溶解度大小的顺序是______。
(2)m点表示在t3℃下,a溶液是______溶液,b溶液是______溶液,c溶液是______溶液。
(3)n点表示在t2℃时,______和______物质的______相同。
(4)在t3℃时,a、b、c分别在50g水里达到饱和,冷却到t1℃,析出晶体最多的是______。
(5)从a的热饱和溶液中提取a最好的方法是______;要从c溶液中提取c最好采用的方法是______。
(6)为了从混有少量的c物质的a物质的溶液中提取纯净的a可采用的方法是______。
溶解度练习题一、溶液的形成1、溶液(1)溶液的概念:(2)溶液的基本特征:均一性、稳定性注意:a、溶液不一定无色,如CuSO4溶液为蓝色FeSO4溶液为浅绿色Fe2(SO4)3溶液为黄色b、溶质可以是固体、液体或气体;水是最常用的溶剂c、溶液的质量= 溶质的质量+ 溶剂的质量溶液的体积<溶质的体积+ 溶剂的体积d、溶液的名称:溶质的溶剂溶液(如:碘酒——碘的酒精溶液)2、溶质和溶剂的判断(1)固体、气体溶于液体时,固体、气体是溶剂;(2)两种液体相溶时,量多的是溶剂,量少的是溶质。
(一)溶解度曲线及其应用类型一一条曲线获取的信息1,太空“冰雪”实验中,过饱和醋酸钠溶液形成的“液球”在接触绳子的一端后瞬间变成温热的“冰球”。
醋酸钠的溶解度曲线如图所示,下列说法不正确的是()A.常温下,醋酸钠易溶于水B.40 ℃时,饱和醋酸钠溶液的溶质质量分数是65.6%C.加水能使醋酸钠溶液从饱和变成不饱和D.过饱和醋酸钠溶液结晶过程释放热量初三化学第1部分(一)溶解度曲线及其应用(二)金属活动性顺序的探究及应用(三)物质的检验、鉴别、除杂、分离(四)物质的转化与推断类型二 两条曲线获取的信息2.KNO 3和NaCl 的溶解度曲线如图所示。
下列说法正确的是( )A.KNO 3的溶解度比NaCl 大B.将室温下KNO 3的饱和溶液升高温度,溶液仍饱和C.KNO 3和NaCl 均属于难溶物质D.除去KNO 3中少量NaCl 可用冷却热饱和溶液结晶的方法 类型三 三条曲线获取的信息3.(2023安徽中考)煤化工废水中含有NaCl 、Na 2SO 4、NaNO 3,这三种盐的溶解度曲线如图所示。
下列有关说法正确的是( )A.与NaNO 3相比,NaCl 更适合通过饱和溶液降温结晶得到B.a 1 ℃时,NaNO 3的饱和溶液溶质的质量分数为80%C.a 2 ℃时,NaCl 和Na 2SO 4的饱和溶液溶质质量分数相等D.40 ℃时,Na 2SO 4的饱和溶液升温到60 ℃变为不饱和溶液 类型四 图、表、线综合分析4.【学科素养·科学思维】(2023江苏扬州江都二模)MgSO 4和Na 2CO 3的溶解度表及溶解度曲线如下,下列说法正确的是 ( ) 温度/℃ 20304050607080溶解度 S /gMgSO 4 25.1 28.2 30.8 32.9 34.3 35.0 34.9 Na 2CO 321.5 39.7 49.0 48.5 46.0 45.2 43.9A.甲为MgSO4B.b、c点乙的饱和溶液溶质质量分数相等C.甲的饱和溶液从t1℃升温到t3℃,溶质质量分数增大D.等质量甲、乙饱和溶液从t3℃降温到t1℃,析出晶体的质量(不带结晶水):乙>甲5.(2023山西长治期末)在学习了“溶解度”的相关知识后,小晋用盛有150 g水的烧杯进行如图1所示的实验,图2是相关的溶解度曲线。
九年级化学溶解度曲线专题
化学溶解度曲线专题主要涉及以下内容:
1. 溶解度的定义:溶解度是指在一定温度下,单位溶剂中能
溶解的最大溶质量。
溶解度的大小与溶质和溶剂的性质、温度、压力等因素有关。
2. 饱和溶解度曲线:饱和溶解度是指在某一温度下,溶液中
溶质的浓度达到最大值时的溶质质量。
饱和溶解度曲线是指在不同温度下测定饱和溶解度后绘制的曲线,可以用来研究溶解度与温度的关系。
3. 温度对溶解度的影响:一般情况下,溶解度随温度的升高
而增加,即温度越高,溶解度越大。
但也存在一些特殊情况,如饱和溶解度随温度的升高而减小的物质,称为逆温度溶解度曲线。
4. 溶解度曲线的应用:溶解度曲线可以用来预测溶解度值、
判断溶液的饱和度、计算溶解度相关的热力学参数等。
在实际应用中,可以通过溶解度曲线来优化晶体生长、提高药物溶解度、控制溶解速率等。
5. 溶解度曲线的实验方法:常用的测定溶解度的方法包括连
续加热法、连续冷却法、恒温法等。
实验中需要准确测量溶质质量和溶液的浓度,控制温度和压力等条件,以获得可靠的数据。
总之,九年级化学溶解度曲线专题主要包括溶解度的定义、饱和溶解度曲线、温度对溶解度的影响、溶解度曲线的应用以及实验方法等内容。
初中化学溶解度曲线知识点讲解初中化学溶解度曲线知识点讲解溶解度曲线溶解度曲线,是同种物质在不同温度下的溶解度绘制出来的曲线。
下面是店铺整理的初中化学溶解度曲线知识点讲解,欢迎阅览。
溶解度曲线的意义①溶解度曲线表示某物质在不同温度下的溶解度或溶解度随温度的变化情况。
②溶解度曲线上的每一个点表示溶质在某一温度下的溶解度。
此时,溶液必定是饱和溶液。
③两条曲线的交叉点表示两种物质在该温度下具有相同的溶解度。
在该温度下,这两种物质的饱和溶液中溶质的质量分数相等。
④在溶解度曲线的下方的点,表示该温度下的溶液是该物质的不饱和溶液。
⑤在溶解度曲线上方的点,表示该温度下的溶液是该物质的过饱和溶液,也就是说,在溶液中存在未溶解的溶质。
相信上面对化学中溶解度曲线的意义知识点的讲学习,同学们都能很好的掌握了吧,希望同学在考试中取得优异成绩。
初中化学溶解度曲线表示知识点讲解关于化学中溶解度曲线表示知识点的内容学习,希望同学们很好的掌握下面的内容。
溶解度曲线表示1点溶解度曲线上的每个点表示的是某温度下某种物质的溶解度。
2线溶解度曲线表示某物质在不同温度下的溶解度或溶解度随温度的变化情况。
根据溶解度曲线,选择分离某些可溶性混合物的方法。
3交点两条溶解度曲线的交点表示该点所示的温度下两物质的溶解度相同,此时两种物质饱和溶液的溶质质量分数也相同。
大部分固体随温度升高溶解度增大,如硝酸钾;少部分固体溶解度受温度影响不大,如食盐;极少数物质溶解度随温度升高反而减小,如氢氧化钙。
希望上对化学中溶解度曲线表示知识点的讲解学习,同学们都能很好的掌握上面的知识,相信同学们会从中学习的更好的。
初中化学金属与酸的置换反应知识讲解下面是对化学中金属与酸的置换反应知识的内容讲解,希望同学们认真学习下面的知识。
金属与酸的置换反应(1)金属的活动顺序。
只有排在氢前面的金属才能置换出酸里的氢(不是氢气);这里的酸常用稀盐酸和稀硫酸,不能用浓硫酸和硝酸(氧化性太强,得不到氢气而是水,不属于置换反应)。
溶解度/gt/℃21m m m m 溶解度曲线❖ 教学目标1.正确理解溶解度曲线2.掌握溶解度曲线的相关应用❖ 知识梳理一、溶解度曲线的涵义 1.涵义:物质的溶解度受温度影响,温度变化溶解度也变化。
如果在直角坐标系中,用横坐标表示温度,纵坐标表示溶解度,根据物质在不同温度下的溶解度,我们可以得到一系的点,将这些点以光滑的曲线连贯起来就得到了溶解度曲线。
溶解度曲线就是在直角坐标系中,用来描述物质的溶解度随温度变化而变化的曲线。
根据溶解度曲线可进行溶液的配制,混合物的分离与提纯,以及进行物质结晶或溶解的计算。
2.说明 (1)点① 曲线上的点:表示对应温度下该物质的溶解度。
如:下图中a 表示 A 物质在t 1℃时溶解度为m 1g 。
曲线上方的点:表示在对应温度下该物质的饱和溶液中存在 不能继续溶解的溶质。
如:图中b 表示在t 1℃时,A 的饱和溶液中有 (m 2-m 1)g 未溶解的溶质。
曲线下方的点:表示在对应温度下该物质的不饱和溶液。
如:图中C 表示在t 1℃时,A 的不饱和溶液中,还需要加入(m 1-m 3)gA 物质才达到饱和。
②曲线交点:表示在对应温度下不同物质的溶解度相同。
如图中d 表示在t 2℃,A 、B 两物质的溶解度都为m 4g 。
(2)线○1如图中A 物质的溶解度随温度升高而明显增大,A 曲线为“陡升型”。
如KNO 3等大多数固体物质:○2图中B 物质的溶解度随温度变化不大,B 曲线为“缓升型”,溶解度/g如NaCl等少数固体物质。
○3图中C物质的溶解度随温度升高而减小,C曲线为“下降型”,如气体及Ca(OH)2等极少数固体物质。
二、溶解度曲线的应用1.溶解度曲线上的每一点,代表着某温度下某物质的溶解度,因此利用溶解度曲线可以查出某物质在不同温度下的溶解度,并根据物质的溶解度判断其溶解性。
2.可以比较在同一温度下不同物质溶解度的相对大小。
3.根据溶解度曲线的形状走向,可以看出某物质的溶解度随温度的变化情况。
初中化学溶解度曲线图的解读与分析方法溶解度是指在一定温度下溶质在溶剂中溶解成溶液的最大量。
溶解度曲线图是描述溶解度随温度变化的图表。
通过解读和分析溶解度曲线图,我们可以了解不同物质溶解度的规律性,并对溶解过程进行深入理解。
解读溶解度曲线图的第一步是观察曲线的趋势。
溶解度曲线通常呈现出不同的形态,如正常溶解度曲线、倒U型曲线、S型曲线等。
根据曲线的形态,我们可以初步判断物质的溶解过程特点。
例如,正常溶解度曲线代表溶解度随温度的升高而增加,这表明溶解过程是吸热的;倒U型曲线则表示溶解度随温度的升高先增加后减少,这表明在一定温度范围内溶解度最大,超过该温度后溶解度降低;S型曲线则表示溶解度随温度的升高先减少后增加,这可能是由于溶质在低温下产生了某种结晶,而在高温下重新溶解所导致。
在进一步分析时,我们需要关注曲线上的特殊点或特征。
首先,峰值点通常表示溶解度达到最大值的温度。
通过观察峰值点的位置,我们可以比较不同物质的溶解度大小。
其次,曲线上的水平线段表示溶解度在该温度范围内保持不变。
这些水平线段可能与某种相变过程相关,如晶体水合物的结晶水的脱失。
最后,曲线上的斜率表示溶解度随温度变化的速率。
斜率的变化率可以反映溶解过程的速度,例如,斜率越大,表示溶解过程越快。
为进一步深入分析溶解度曲线图,我们可以考虑以下几个方面:1. 温度变化对溶解度的影响:通过比较不同物质的溶解度曲线,我们可以观察不同物质在不同温度下的溶解度变化规律。
这有助于我们理解物质的溶解特性以及温度对溶解过程的影响。
2. 物质的溶解热:根据溶解度曲线的形态,我们可以初步判断溶解过程是吸热还是放热的。
进一步分析可以计算出物质的溶解热,并比较不同物质的溶解热大小。
3. 溶液中溶质的浓度变化:通过分析溶解度曲线,我们可以了解溶质浓度随温度变化的趋势。
这可以帮助我们理解溶解过程中溶质在溶液中的分布规律。
4. 物质的晶体结构:溶解度曲线的特殊点和特征可以与物质的晶体结构相关联。