姜黄色素稳定性研究
- 格式:pdf
- 大小:305.69 KB
- 文档页数:4

姜黄素类化合物的光稳定性研究王雪梅;陈利华;施文婷【摘要】The photo-stability of curcuminoid was studied, and its solutions were analyzed pre and post light by HPLC. The results showed that curcuminoid in ethanol solution was unstable exposured to sunlight and stable under the conditions of indoor lighting, UV irradiation and dark; Citric acid, BHT and β-CD were less helpful for the stability of curcuminoid; curcuminoid powder was relatively stable. The analysis of HPLC showed that the degradation rates of curcumin, demethoxycurcumin and bisdemethoxycurcumin were 68. 9% , 51.5% and 21.5% , respectively, after exposure to sunlight for 5 days. And the major degradation products were ferulic acid and vanillin.%研究姜黄素类化合物的光稳定性,并采用高效液相色谱法对光照前后的姜黄素类化合物溶液进行分析.结果表明:室外光照下,姜黄素的乙醇溶液极不稳定,加入柠檬酸、BHT和β-CD不能显著增强其稳定性,姜黄素固体粉末则较为稳定;室内光照、紫外光照和避光条件下姜黄素溶液均较为稳定.高效液相色谱分析显示:室外光照5d后,姜黄素、单脱甲氧基姜黄素、双脱甲氧基姜黄素的降解率分别为68.9%、51.5%和21.5%;姜黄素类化合物的主要分解产物为阿魏酸和香草醛.【期刊名称】《安徽大学学报(自然科学版)》【年(卷),期】2012(036)003【总页数】6页(P73-78)【关键词】姜黄素类化合物;稳定性;光照;降解率;阿魏酸;香草醛【作者】王雪梅;陈利华;施文婷【作者单位】安徽大学化学化工学院,安徽合肥230039;安徽大学化学化工学院,安徽合肥230039;安徽大学化学化工学院,安徽合肥230039【正文语种】中文【中图分类】R284.1姜黄素类化合物为姜黄属植物姜黄、郁金、莪术等干燥根茎的主要活性物质,包括姜黄素(curcumin)、单脱甲氧基姜黄素(demethoxycurcumin)、双脱甲氧基姜黄素(bisdemethoxycurcumin)等,统称姜黄色素或姜黄素[1].其安全性高,长期以来作为一种常用的天然色素被广泛应用于食品工业[2].近年来的研究表明姜黄素具有抗炎、抗氧化、抗肿瘤、抗突变、提高免疫力等多种药理作用和保健功能[3-6],因而使其成为国内外研究的热点.但姜黄素类化合物不稳定,易受温度、光线、湿度、pH等影响[7-8].作者将对不同状态下的姜黄素类化合物的光稳定性进行系统研究,并采用高效液相色谱法对光照前后的姜黄素类化合物溶液进行分析,进而推断其光降解产物及过程.1.1 仪器及试剂TU-1901紫外-可见分光光度计,北京普析通用仪器有限公司;AB104-N电子天平,梅特勒-托利多仪器上海有限公司;VARIAN Prostar 210高效液相色谱仪,美国瓦里安公司;40 W紫外灯,北京三源华辉电光源制造有限公司.姜黄素,纯度大于95%,美国 Alta公司;柠檬酸、2,6-叔丁基对甲酚(BHT)、β-环糊精(β-CD)、香草醛、阿魏酸、冰醋酸、无水乙醇,均为分析纯;乙腈,色谱纯;姜黄素(CurⅠ)、单脱甲氧基姜黄素(CurⅡ)、双脱甲氧基姜黄素(CurⅢ)对照品、重蒸水,作者实验室自制.1.2 实验方法1.2.1 姜黄素溶液的光稳定性实验1.2.1.1 姜黄素溶液的配制以无水乙醇为溶剂,配制成浓度为1.92×10-3mo l·L-1的姜黄素溶液,并分装于20个10 mL容量瓶中,为样品溶液1;另取适量上述溶液稀释100倍后分装于20个10 mL容量瓶中,为样品溶液2,该组溶液中姜黄素的浓度为1.92×10-5mol·L-1.1.2.1.2 姜黄素溶液的光照实验将配制好的样品溶液1和样品溶液2平均分为4组,分别采用室外阳光照射、室内光照、紫外灯距离20 cm照射、避光保存进行实验.选择连续晴好天气,所有实验均于每日上午10:00将样品放于指定的实验条件下,下午6:00取回避光保存,保留其中一份样品,其余样品次日10:00仍置于指定实验条件下,依此类推,实验为期5 d.1.2.1.3 光照实验测试光照实验结束后,用无水乙醇将所有的样品溶液重新定容至刻度,再将样品溶液1稀释100倍.以1 cm石英比色皿为吸收池、无水乙醇为参比,测定其在425 nm 处的吸光度.1.2.2 姜黄素在不同介质中的光稳定性实验1.2.2.1 姜黄素在不同介质中溶液的配制以无水乙醇为溶剂,配制样品溶液3(姜黄素的浓度为1.92×10-3mol·L-1,柠檬酸的浓度为5.20×10-3mol·L-1)和样品溶液 4(姜黄素的浓度为1.92×10-3mol·L-1,BHT 的浓度为4.50×10-3mol·L-1);以 60%乙醇(V∶V)水溶液为溶剂,配制样品溶液 5(姜黄素的浓度为1.92×10-3mol·L-1,β-CD 的浓度为1.00×10-2mol·L-1).各样品溶液均分装于5个10 mL容量瓶中.1.2.2.2 姜黄素固体粉末的准备分别取等量的姜黄素固体粉末于5个透明塑料袋内,密封后平摊于白磁盘中待用.1.2.2.3 光照实验分别取上述各样品溶液及姜黄素固体粉末进行室外阳光照射实验,实验方法与1.2.1.2中相同.1.2.2.4 光照实验测试光照实验结束后,用无水乙醇将各样品溶液重新定容至刻度,再分别稀释100倍后,测定其在425 nm处的吸光度.精确称取光照后的姜黄素粉末0.073 6 g,无水乙醇溶解后定容于100 mL容量瓶中,稀释100倍后测定其在425 nm处的吸光度.1.2.3 姜黄素溶液光照前后的高效液相色谱分析1.2.3.1 色谱条件色谱柱:Gemini 5u C18 110A(250 mm×4.6 mm,5 μm);流动相:V(乙腈)∶V(水(0.5%冰醋酸))=50 ∶50;柱温:35 ℃;流速:1.0 mL· min-1;检测波长:310 nm;进样量:20 μL.1.2.3.2 实验方法精密称取CurⅠ、CurⅡ、CurⅢ、阿魏酸和香草醛各10 mg,用无水乙醇溶解后定容于100 mL容量瓶中,配制成对照品混合溶液.分别取该混合溶液5.0、2.5、1.5、1.0、0.5 mL 于10 mL 容量瓶中定容,高效液相色谱测定,以峰面积为纵坐标,绘制标准曲线.选择样品溶液1中未经光照及室外光照5 d后的样品,稀释10倍后,在上述色谱条件下测定,计算各物质含量.2.1 姜黄素的光稳定性2.1.1 姜黄素溶液在不同光照下的稳定性姜黄素的紫外光谱中出现两个取代苯的吸收带,由于苯环上的取代基与苯环分别存在p-π共轭和π-π共轭,使吸收带发生红移,最大吸收波长为425 nm,已经进入了可见光区[9].通常选择其最大吸收波长425 nm处吸光度作为定量依据.图1为两种不同浓度姜黄素溶液在不同光照下吸光度随时间变化的曲线图.由图1可见,样品溶液1在室外光照下随光照时间延长其吸光度明显下降,光照5 d后,吸光度由光照前的1.15降至0.38,表明溶液中约67%的姜黄素分解;姜黄素样品溶液2经1 d阳光照射后就已完全分解.而室内光照、避光保存及紫外光照,都未能使两种溶液的吸光度发生明显变化,由此可见紫外光不是导致姜黄素发生降解的因素.2.1.2 姜黄素在不同介质中的光稳定性图2为姜黄素在不同介质中室外光照下吸光度随时间变化的曲线图.柠檬酸、BHT和β-CD为食品中常用的添加剂,分别具有酸度调节、抗氧化和包埋作用[10-12],由图2a~c可见,室外光照下,分别添加3种物质的姜黄素溶液的吸光度均随照射时间延长而明显下降,光照5 d后,吸光度降至0.5左右,仍有约57%的姜黄素分解,说明加入柠檬酸、BHT和β-CD只能稍微减缓姜黄素的降解,对其稳定保存并无明显作用.而图2d中经过连续5 d的阳光照射,吸光度仅略微下降,说明姜黄素以固体粉末状态放置时光稳定性较好.2.2 姜黄素及其光降解产物的高效液相色谱分析图3为样品溶液1未经光照(图3a)以及经5 d室外光照后(图3b)的高效液相色谱图.图4为对照品的高效液相色谱图.图3中标号1、2、3的峰分别为姜黄素、单脱甲氧基姜黄素及双脱甲氧基姜黄素(保留时间tR分别为12.7、11.5、10.4 min),光照后各峰强度均下降,尤以姜黄素最为明显;此外,图 3b中在保留时间为2.5~7.5 min处出现若干色谱峰,应为姜黄素类化合物的光降解产物,其中4号峰和5号峰相对较强.与对照品的色谱图(图4)进行比对可知4号峰为香草醛(tR=4.24 min)、5号峰为阿魏酸(tR=3.59 min).以峰面积y(v×t)为纵坐标、浓度x(mg·L-1)为横坐标,分别作5种对照品的标准工作曲线,线性方程见表1.由表 1 可知,5 种对照品分别在 5.5 ~55 mg·L-1(CurⅠ)、5.0 ~50 mg·L-1(CurⅡ)、4.6 ~46 mg·L-1(Cur Ⅲ)、5.5 ~55 mg·L-1(阿魏酸)和 5.5 ~ 55 mg·L-1(香草醛)范围内线性关系良好,相关系数均大于0.999 6.样品溶液1中姜黄素类化合物光照前后的质量浓度及降解率见表2.由表2可知,CurⅠ、CurⅡ及CurⅢ的降解率分别为68.9%、51.5%和21.5%.姜黄素类苯环上的—OH和— OCH3都是给电子能力较强的基团,使苯环电子密度增加,碳链上发生亲电反应的反应活性增加;而失去—OCH3后,给电子能力减弱,亲电反应活性减弱[8],因此姜黄素类化合物中姜黄素最不稳定,双脱甲氧基姜黄素最为稳定.由表2还可看出,样品溶液1经5 d照射后生成阿魏酸和香草醛的质量浓度分别为127 mg·L-1和59.9 mg·L-1,相当于每1.00 mol姜黄素类化合物经 5 d 照射后生成了 0 .342 mol的阿魏酸和 0 .205 mol的香草醛.2.3 姜黄素类化合物光降解机理根据HPLC的分析结果,可大致推断姜黄素类化合物溶液在室外光照条件下的分解情况,如图5所示.姜黄素类化合物分子经室外阳光照射后获取一定能量,会从紧邻羰基的α-碳处发生断裂,生成阿魏醛,进而氧化成阿魏酸;若脱除—CO,断裂产物进一步被氧化,可生成香草醛及香草酸.室外光照会导致乙醇溶液中的姜黄素降解,浓度越低,降解越明显;加入柠檬酸、BHT和β-CD不能显著增强其稳定性;姜黄素溶液在室内光照、紫外光照和避光条件下均能稳定存在;姜黄素以固体粉末状保存较为稳定.高效液相色谱分析显示:室外光照5 d后,姜黄素、单脱甲氧基姜黄素、双脱甲氧基姜黄素的降解率分别为68.9%、51.5%和21.5%,说明姜黄素类化合物中姜黄素最不稳定,双脱甲氧基姜黄素最为稳定;姜黄素的主要分解产物为阿魏酸和香草醛.需要指出的是,因缺乏标准样品,文中对姜黄素光降解过程的分析尚不够全面,除确定了2种主要降解产物外,未能对其他降解产物进行分析.【相关文献】[1]陆鹏,童强松,姜凤超,等.姜黄素前体药物的合成及其体外抗肿瘤活性研究[J].中国药理学通报,2006,22(3):321-324.[2]卢新军,蒋和体.姜黄素生理功能及其在食品工业中的应用前景[J].中国食物与营养,2006,4:31-32.[3]胡静,李立.姜黄素药理作用研究现状[J].检验医学与临床,2007,4(12):1186-1187. [4]李湘洲,张炎强,旷春桃,等.姜黄色素的生物和提取分离研究进展[J].中南林业科技大学学报,2009,29(3):190-193.[5]Tuba A K,Gülɕin Í G.Antioxidant and radical scavenging properties of curcumin [J].Chemico-Biological Interactions,2008,174(1):27-37.[6]Shishu,Kaur I P.Antimutagenicity of curcumin and related compounds against genotoxic heterocyclic amines from cooked food:the structural requirement[J].Food Chemistry,2008,111(3):573-579.[7]齐莉莉,王进波.单体姜黄素稳定性的研究[J].食品工业科技,2007,28(1):181-182. [8]韩刚,崔静静,毕瑞,等.姜黄素、去甲氧基姜黄素和双去甲氧基姜黄素稳定性研究[J].中国中药杂志,2008,33(22):2611-2614.[9]索全伶,黄延春,翁林红,等.天然姜黄素的纯化和分子与晶体结构研究[J].食品科学,2006,27(3):27-30.[10]张素娟.食品中柠檬酸的检测方法研究进展[J].食品工业科技,2011,32(1):352-354. [11]曾丹丹,罗林,吴移山,等.气相色谱法测定食用植物油中抗氧化剂 BHA、BHT[J].中国食品,2009,9:62-63.[12]周雅文,熊敏,韩富,等.特种表面活性剂和功能性表面活性剂(Ⅻ)-环糊精及其衍生物的制备与性能[J].日用化学工业,2011,41(1):61-67.。

一、实验目的1. 了解新鲜姜黄的基本成分及其性质。
2. 学习使用化学方法对新鲜姜黄进行定性分析。
3. 掌握实验操作的技能和注意事项。
二、实验原理新鲜姜黄是一种具有浓郁香味的黄色根茎类植物,其主要成分为姜黄素(Curcumin)。
姜黄素是一种多酚类化合物,具有多种生物活性,如抗氧化、抗炎、抗肿瘤等。
本实验通过化学方法对新鲜姜黄进行定性分析,主要检测其中的姜黄素含量。
三、实验材料与仪器1. 实验材料:新鲜姜黄、无水乙醇、氢氧化钠、盐酸、铁氰化钾、硫酸、苯酚、碳酸钠等。
2. 实验仪器:电子天平、研钵、烧杯、试管、移液管、滴定管、试管架、酒精灯、磁力搅拌器、紫外-可见分光光度计等。
四、实验步骤1. 新鲜姜黄的制备(1)将新鲜姜黄洗净,去皮,切成小块。
(2)将姜黄块放入研钵中,加入适量无水乙醇,研磨成匀浆。
(3)将匀浆过滤,收集滤液,备用。
2. 姜黄素的提取(1)取一定量的滤液,加入适量的氢氧化钠溶液,调节pH值为8.5。
(2)加入适量的铁氰化钾溶液,搅拌均匀,室温下放置30分钟。
(3)加入适量的盐酸溶液,调节pH值为4.5。
(4)加入适量的硫酸,搅拌均匀,室温下放置30分钟。
(5)加入适量的碳酸钠溶液,调节pH值为8.5。
(6)将混合液过滤,收集滤液,备用。
3. 姜黄素的定量分析(1)取适量的滤液,用移液管移入比色皿中。
(2)用紫外-可见分光光度计测定滤液在最大吸收波长(约425nm)处的吸光度。
(3)根据标准曲线计算姜黄素的含量。
4. 标准曲线的绘制(1)取不同浓度的姜黄素标准溶液,用移液管移入比色皿中。
(2)用紫外-可见分光光度计测定标准溶液在最大吸收波长(约425nm)处的吸光度。
(3)以吸光度为纵坐标,浓度(mg/mL)为横坐标,绘制标准曲线。
五、实验结果与分析1. 新鲜姜黄的制备实验过程中,新鲜姜黄经过研磨、过滤等步骤,得到较纯净的滤液,为后续实验提供了良好的实验材料。
2. 姜黄素的提取实验中,通过调节pH值、加入铁氰化钾、盐酸、硫酸和碳酸钠等试剂,成功提取了姜黄素。

姜黄色素的稳定化研究及应用前景近年来天然色素日益受到人们重视,而开发具有一定营养价值或药理作用的功能性天然色素,是色素工业发展的一个重要方向。
姜黄色素,又称为"郁金黄色素",是姜科植物姜黄的提取物。
姜黄素具有利胆、行气、抗炎、抗氧化、抗菌、抗动脉粥样硬化、镇痛、降血脂、抗癌等诸多药理作用。
同时作为一种天然色素,姜黄色素着色力强,且安全无毒,是我国食品卫生法允许使用的食用天然色素,同时也是联合国粮农组织(FAO)和世界卫生组织(WHO)所规定的使用安全性很高的天然色素之一。
可广泛用于饮料、糕点、糖果、冰激淋等多种食品,是当前最具开发价值的食用天然色素之一。
1姜黄色素的理化性质姜黄色素是一种植物多酚,主要成分包括姜黄素(C21H20O6)、脱甲氧基姜黄素(C20H18O5)、脱双甲氧基姜黄素(C19H16O4),是自然界中极为稀少的二酮类有色物质。
姜黄色素呈橙黄色粉末结晶状态,具有类似胡椒芳香,稍有苦味。
熔点为179~182℃。
姜黄色素为亲脂性物质,不溶于水、苯和乙醚等,溶于甲醇、乙醇、冰醋酸、丙二醇、乙酸乙酯和碱性溶液。
在不同pH条件下呈现的颜色不同。
对光、热稳定性差。
有很好的着色性,特别是对蛋白的着色力强。
姜黄色素的最大允许日摄入量(ADI)为0.1mg/kgbw。
2姜黄色素的稳定性影响因素姜黄分子中含有多个双键以及酚羟基、羰基等基团,因此很容易发生化学反应。
其稳定性易受光照、温度、酸度等多种因素的影响。
酸碱度是影响姜黄色素稳定性的一个重要因素。
偏酸性环境中姜黄色素呈浅黄色,在中性环境中则呈现玫瑰红色,而在碱性环境下姜黄色素呈红褐色或棕色。
因此可作为化学反应指示剂测定硼离子。
此外有研究表明在姜黄色素在pH≤4.5的酸性溶液中易出现沉淀,而在碱性条件下色素则呈可溶状态。
有学者还研究了姜黄色素在不同pH的缓冲液中的稳定性,试验结果表明,在pH为中性的缓冲液中姜黄色素分解最快。
温度越高,姜黄色素显色能力越差。

食品中色素的稳定性与抗氧化性能研究在食品加工中,色素是赋予食物丰富色彩和吸引力的重要成分。
然而,色素的稳定性和抗氧化性能对于保持食品的色泽和品质至关重要。
本文将探讨食品中色素的稳定性与抗氧化性能的研究,并探讨其对食品行业的意义。
1. 色素的稳定性色素的稳定性是指色素在食品加工和存储过程中是否容易受到光、热、氧化等因素的影响而导致变色或降解。
研究表明,不同种类的色素具有不同的稳定性。
一些天然色素如胡萝卜素和叶绿素在加工过程中相对稳定,而人工合成的色素如染料黄4和染料红40则较为不稳定。
色素的稳定性与其结构有很大关系。
例如,苯酚类和醛类结构的色素较为稳定,而酮类和羰基结构的色素容易发生自氧化反应。
此外,色素的水溶性和脂溶性也对其稳定性有影响。
一般来说,水溶性色素在食品中的稳定性相对较差,而脂溶性色素则相对较好。
为了提高色素的稳定性,研究人员着重研究了各种方法。
一种常见的方法是利用稳定剂来保护色素不受光、热、氧化等因素的影响。
例如,添加抗氧化剂可以有效延缓色素的氧化反应。
此外,改变食品的加工条件,如温度、pH值等,也可以对色素的稳定性产生一定影响。
2. 色素的抗氧化性能色素的抗氧化性能指的是色素在食品中具有的抗氧化能力。
氧化反应是食品在加工和保存过程中不可避免的反应,会导致食品的变质和营养价值的损失。
因此,寻找具有良好抗氧化性能的色素对于提高食品的品质和延长保质期具有重要意义。
研究发现,某些天然色素具有显著的抗氧化性能。
例如,花青素和类胡萝卜素被广泛应用于食品工业中,不仅能赋予食物艳丽的颜色,还可以作为抗氧化剂延缓食品的氧化反应。
此外,一些常用的香料和调味料如姜黄素和丁香酚也具有一定的抗氧化活性。
研究人员还发现,色素的抗氧化性能与其在食品中的存在形式有关。
例如,色素以纳米颗粒的形式存在时,其抗氧化性能较好,可以有效防止食物中的自由基产生。
此外,色素的抗氧化性能还受到其他因素如温度、pH值和金属离子等的影响。

姜黄素的稳定性研究韩刚;霍文;李秋影;孙广利;段离潼【期刊名称】《中成药》【年(卷),期】2007(029)002【摘要】姜黄素是姜科姜黄属(Curcuma longa L.)植物姜黄、莪术、郁金等根茎中的一种有效成分,具有抗肿瘤、抗炎、抗氧化、抗菌、保肝等多种药理活性近年来对姜黄素的药理作用报道较多,但有关姜黄素制剂的报道较少。
其主要原因是姜黄素几乎不溶于水,体内吸收差,姜黄素不稳定易降解。
本文采用动力学方法,对姜黄素在不同pH的缓冲溶液中降解速率常数进行了测定,并考察了不同类型的表面活性剂对姜黄素稳定性的影响。
结果发现十二烷基硫酸钠(SDS)可使姜黄素的稳定性增大一倍。
【总页数】3页(P291-293)【作者】韩刚;霍文;李秋影;孙广利;段离潼【作者单位】华北煤炭医学院药学系,唐山市新药基础研究重点实验室,河北,唐山,063000;华北煤炭医学院药学系,唐山市新药基础研究重点实验室,河北,唐山,063000;华北煤炭医学院药学系,唐山市新药基础研究重点实验室,河北,唐山,063000;华北煤炭医学院药学系,唐山市新药基础研究重点实验室,河北,唐山,063000;华北煤炭医学院药学系,唐山市新药基础研究重点实验室,河北,唐山,063000【正文语种】中文【中图分类】R284.1【相关文献】1.姜黄素的增溶及稳定性研究 [J], 陶慧;余楚钦;黄劲恒;张伦;解仲伯;林华庆2.姜黄素-胡椒碱复方自微乳结肠稳定性研究 [J], 李秋萍;蒋俏丽;翟文文;戴俊东3.姜黄素在PEG-400中的溶解度及稳定性研究 [J], 仝永涛;高勇;高保安;岳力群;陈建明4.姜黄素立方液晶制备工艺过程中的光稳定性研究 [J], 李瑾;李楠;李晓琴;邓盛齐;尹罡5.姜黄素、去甲氧基姜黄素和双去甲氧基姜黄素稳定性研究 [J], 韩刚;崔静静;毕瑞;赵琳琳;张卫国因版权原因,仅展示原文概要,查看原文内容请购买。

姜黄黄色素的化学成分研究目的:研究姜黄黄色素的化学成分。
方法:利用各种色谱方法分离纯化姜黄乙醇提取物,并通过理化性质和波谱数据分析鉴定化合物的结构。
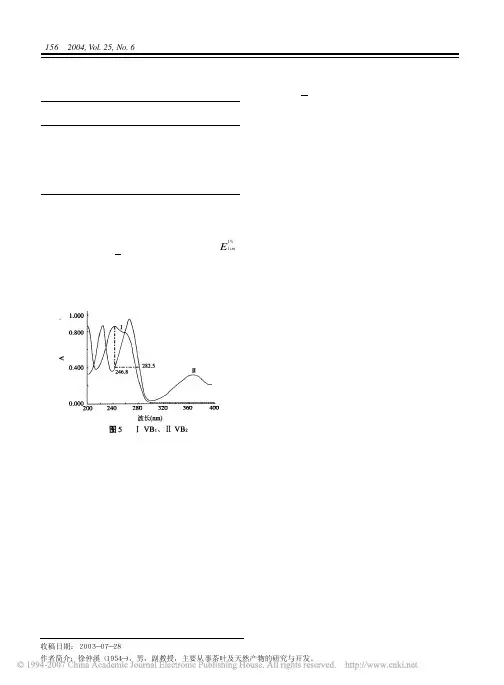
结果:分离得到2个化合物,鉴定为姜黄素(Ⅰ)和1,5-二(4-羟基苯基)-戊-(1E,4E)-1,4-二烯-3-酮(Ⅱ)。
结论:化合物Ⅰ以酮-烯醇互变异构体的形式存在,化合物Ⅱ为首次从药材姜黄中分离得到,这为姜黄黄色素的组成、定量分析、药理及应用研究提供了实验依据。
[Abstract] Objective: To study the constituents of yellow pigment from the rhizome of curcuma longa. Methods: The chemical constituents were purified from ethanol extraction by all kinds of column chromatographies. Their structures were identified by physicochemical properties and spectral methods. Results: Two compounds were isolated and identified as curcumin (Ⅰ), 1,5-bis(4-hydroxyphenyl)-penta-(1E,4E)-1,4-dien-3-one(Ⅱ), respectively. Conclusion: Compound Ⅰexists predominantly as a keto-enol tautomer, Compound Ⅱwas isolated from the rhizome of Curcuma longa L. for the first time, which provided the experimental data of constituents, quantitative assay, pharmacological and use studies for the yellow pigments of the rhizome of curcuma longa.[Key words] Curcuma longa; Yellow pigments; Curcumin; 1,5-bis(4-hydroxyphenyl)-penta-(1E,4E) -1,4-dien-3-one姜黄为姜科植物姜黄的干燥根茎[1],除用于医药外,姜黄黄色素还是一种天然染料,在我国用于萝卜干、咖喱粉的着色也已有很久的历史。

姜黄素的增溶及稳定性研究陶慧;余楚钦;黄劲恒;张伦;解仲伯;林华庆【摘要】姜黄素为难溶性且不稳定的一类天然食用色素,在食品、医药行业等领域中的应用受到极大限制.研究通过添加表面活性剂与助表面活性剂,以增加姜黄素在水性溶液中的溶解度.采用添加抗氧化剂、金属螯合剂以及调节pH值等手段,以色价损失率为评价指标,考察其对增溶后姜黄素溶液的稳定性影响.溶解度结果表明,当助表面活性剂与表面活性剂的用量质量比为1∶2时,可提高姜黄素溶解度至40 mg/g,且增溶后的姜黄素溶液为全水系,用水可稀释成澄清透明的水溶液.稳定性研究表明:抗氧剂的种类以及用量对姜黄素溶液的稳定性影响较大,以0.30%没食子酸丙酯的效果最佳;金属螯合剂对提高姜黄素稳定性的效果不及抗氧化剂;姜黄素溶液在强酸和碱性环境中的稳定性较差,当调节姜黄素溶液pH值为4.56时,其稳定性与加入0.30%没食子酸丙酯(propyl gallate,PG)的相当.【期刊名称】《食品与发酵工业》【年(卷),期】2016(042)008【总页数】6页(P160-165)【关键词】姜黄素;增溶;稳定性;色价损失率【作者】陶慧;余楚钦;黄劲恒;张伦;解仲伯;林华庆【作者单位】广东药学院,广东省药物新剂型重点实验室,广东广州,510006;广东药学院,广东省药物新剂型重点实验室,广东广州,510006;广东药学院,广东省药物新剂型重点实验室,广东广州,510006;广东药学院,广东省药物新剂型重点实验室,广东广州,510006;广东药学院,广东省药物新剂型重点实验室,广东广州,510006;广东药学院,广东省药物新剂型重点实验室,广东广州,510006【正文语种】中文姜黄色素(curcumine)是从姜科姜黄属(Curcuma longa L)植物姜黄、莪术、郁金等根茎中提取而得的一类天然食用色素,是由姜黄素(curcumin)、去甲氧基姜黄素(demethoxycurcumin)和双去甲氧基姜黄素(bisdemethoxycurcumin)组成的混合体[1]。


影响姜黄中姜黄素因素的研究摘要以总姜黄素含量为考察指标,采用正交优化乙醇法提取姜黄中姜黄素,用分光光度法对姜黄素提取液总姜黄素含量进行检测。
考察了料液比、浸提时间、温度、乙醇浓度等因素对提取量的影响。
关键词姜黄素姜黄提取1.前言姜黄为姜科姜黄属植物姜黄的根茎。
姜黄素是从姜科植物姜黄中提取的一种色素,也存在其它姜科植物中。
姜黄素不仅是一种优良的天然食用色素,而且还具有十分广泛的药用价值,现发现姜黄素具有利胆、降血脂、抗病毒、抗炎、抗氧化、抗肿瘤、防止衰老和延年益寿的作用。
因此,研究姜黄中有效成分提取技术具有重要的现实意义。
提取工艺的方法有很多,但存在着操作过程复杂、pH 值对有效成份的影响大、不易控制和不宜工业化大生产等缺点。
2.实验目的研究以固液比、浸提时间、温度、乙醇浓度等因素对提取姜黄中总姜黄素的影响,确定正交试验考查范围,筛选出了优化工艺条件。
3.实验原理姜黄素为橙黄色结晶粉末,味稍苦。
不溶于水,溶于乙醇、丙二醇,易溶于冰醋酸和碱溶液,对光、热、铁离子敏感,耐光性、耐热性、耐铁离子性较差。
通过改变固液比、浸提时间、温度、乙醇浓度等因素,探究姜黄中总姜黄素主要由什么影响。
4.实验器材紫外可见分光光度计、1ml移液管、热恒温水浴锅、分析天平、离心机,50ml的容量瓶6个,250ml容量瓶一个,玻璃棒。
5、实验材料及试剂5. 1实验试剂及其配制30%的乙醇溶液:准确量取95%的无水乙醇15.8ml,加水定容至50ml.40%的乙醇溶液:准确量取95%的无水乙醇21.1ml,加水定容至50ml.50%的乙醇溶液:准确量取95%的无水乙醇26.3ml,加水定容至50ml.60%的乙醇溶液:准确量取95%的无水乙醇31.6ml,加水定容至50ml.70%的乙醇溶液:准确量取95%的无水乙醇184.21ml,加水定容至250ml75%的乙醇溶液:准确量取95%的无水乙醇39.5ml,加水定容至50ml80%的乙醇溶液:准确量取95%的无水乙醇42.1ml,加水定容至50ml5. 2实验材料及其处理把新鲜的姜黄洗净,烘干,粉碎,过40目筛,备用。

姜黄素的研究进展魏瑞芝,刘广志,王乐涛,韩 昆(东阿县检验检测中心,山东聊城 252000)摘 要:姜黄素是姜黄中提取的多酚类物质,常作为天然色素应用于各个领域。
本文从姜黄素的提取方法、生物活性以及在食品工业中的应用等方面进行综述,为姜黄素的开发利用提供参考。
关键词:姜黄素;提取;生物活性;天然色素;应用The Research of CurcuminWEI Ruizhi, LIU Guangzhi, WANG Letao, HAN Kun(Dong’e County Inspection and Testing Center, Liaocheng 252000, China) Abstract: Curcumin is polyphenols which is extracted from turmeric. Curcumin is applied to all fields as natural pigment. This article summarized from methods of extract curcumin, biological activity and application in food industry, and give a reference for application and development of Curcumin.Keywords: curcumin; extract; biological activity; natural pigment; application姜黄素目前是世界上销量最大的一种天然食用色素之一,染色能力强,具有较好的热稳定性和着色性[1]。
姜黄素主要来源于姜科姜黄属植物姜黄的根茎,在我国用于咖喱粉的着色已有很久的历史。
由于它安全无毒、无副作用,被认为是最具开发价值的天然活性成分,被世界卫生组织/食品药品管理局批准为天然食品添加剂[2]。
• 72 •山东化工SHANDONG CHEMICAL INDUSTRY2017年第46卷天然可食用姜黄色素的研究进展张娜〃,翁伟锋1(1.中山火炬职业技术学院,广东中山528436;2.国家中药现代化工程技术研究中心中山健康产品分中心,广东中山528436)摘要:本文对天然可食用姜黄色素的研究现状进行综述.并对姜黄色素的应用前景进行展望.以期对天然可食用姜黄色素的开发和利用奠定基础。
关键词:天然可食用姜黄色素;研究现状;应用前景中图分类号:TS 202.3 文献标识码:A文章编号:1008 -021X (2017)21 -0072-02The Research Progress of Natural Edible CurcuminZhang N a 1,2 ,Weng Weifeng 1(1. Zhongshan Torch Polytechnic,Zhongshan 528436, China ;2. Zhongshan Health Products Center,NationalEngineering Research Center for Modernization of Traditional Chinese Medicine, Zhongshan 528436, China)Abstract ; In this paper,it summarized the research status of natural edible curcumin,with a broad application prospect,in order to lay the foundation for further development of natural edible curcumin.Key words : natural edible curcumin ; research status application prospect 色素与食品的关系密切,色素赋予食品特殊的色泽,消费 者选购食品时,最吸引人的眼球,给消费者带来良好的感官刺 激和强烈购买欲。
0引言姜黄(Curcuma longa L.)为多年生草本植物,其性味辛、苦、温,入心、肝、脾经,可行气破瘀,通经止痛,并可用作调味品、天然色素和天然染料[1]。
姜黄色素是存在于姜科植物姜黄根茎中的一种活性物质,含量为3%~6%,其主要成分为姜黄素、脱甲氧基姜黄素、双脱甲氧基姜黄素,是大自然中极为稀少的二酮类有色物质。
它是由中药材姜黄经乙醇等有机溶剂抽提、精制所得。
姜黄色素是橙黄色结晶状粉末,不溶于冷水,微溶于乙醚和苯,加热时溶于乙醇、乙二醇,易溶于冰醋酸和碱溶液。
在酸性和中性溶液中显黄色,在碱性溶液中呈红褐色。
研究表明,姜黄色素可药用,具有抗病毒、抗炎、抗氧化、抗肿瘤、防止衰老和延年益寿等诸多功效,成为近年来天然药物行业的研究热点,已有人将姜黄用于AIDS 患者及HIV 感染者的治疗[2-5]姜黄色素是最有开发价值的天然色素之一,同时被认为是一种良好的天然防腐剂。
姜黄色素作为着色剂已广泛应用于食品中,随着人们对食品安全的日益关注,集着色、防腐与保健为一体的无毒副作用的姜黄色素必将具有更广阔的开发应用前景[6-8]。
本文通过研究姜黄色素在不同条件下的稳定性,为更好地开发利用姜黄色素提供参考。
1材料与方法1.1材料姜黄根,购自药店;氯化钙,氯化铝,硫酸铜,硫酸亚铁硫酸钠,硫酸钾,亚硫酸钠,柠檬酸,双氧水,抗坏血酸等均为分析纯,蔗糖、食盐等均为食品级。
1.2仪器设备101-A-2型电热鼓风干燥箱:上海试验仪器有限公司;TU —1901型紫外可见分光光度计:北京普析通用仪器有限责任公司;FW —200型粉碎机:北京中兴伟业仪器有限公司。
1.3试验方法1.3.1色素提取将姜黄以80%乙醇,1∶8的料液比,50℃下浸提2.5h 提取姜黄色素,过滤,定容到50mL 后,稀释90倍得姜黄色素提取液,备用。
工艺流程如下:姜黄→粉碎→过40目筛→浸提→真空抽滤→滤液减压浓缩→姜黄色素提取液1.3.2光谱性质用60%乙醇浸提姜黄,得黄色提取液,采用紫外分光光度计在400~600nm 范围内扫描。
文献综述生物工程天然色素的稳定性研究摘要:合成色素品种对人体有较为严重的毒性和致畸、致癌性,不少合成色素在各国允许使用的程度被大大限制,尤其在食品、医药、和化妆品行业。
天然色素的利用成为新的趋势,而天然色素的稳定性制约着其在各个领域的应用,所以研究天然色素的稳定性有着重要的意思。
本文对14种常见天然色素的稳定性做了归纳。
为预测、提高和改善其他天然色素的稳定具有一定的指导意义。
关键词:天然色素;稳定性;应用前景色素分为人工合成色素和天然色素两大类,在实际生活中应用广泛。
合成色素由于具有着色力强、色泽鲜艳、稳定性好、无臭无味、品质均一,易于溶解和拼色,以及成本低廉等一系列优点,曾一度被广泛应用。
随着毒理学和分析化学的不断发展,人类逐渐认识到多数合成色素品种对人体有较为严重的毒性和致畸、致癌性。
不少合成色素在各国允许使用的程度被大大限制,尤其在食品、医药、和化妆品行业。
[1]而天然色素却不断体现出它自身对人类健康有益的许多独特的优点:(1)大多数天然色素来自可食用的动植物组织安全性高无毒副作用;(2)很多天然色素中含有人体必需的营养物质或其本身就是维生素或具有维生素性质的物质;(3)有些天然色素具有药理作用对某些疾病具有防治作用;[2] (4)天然色素色调自然易为消费者接受有的品种甚至具有特殊的芳香气味添加到食品中会带来愉快的感觉。
因而,现在利用无毒无害的天然物质提取食用和化妆品用色素,成为一种新的发展趋势。
虽然天然色素越来越受到人们的青睐,然而天然色素却存在稳定性较差价格较贵等缺点严重制约着它的开发应用。
本文对14 种不同类型的天然色素的稳定性进行了研究。
1 一些常见天然色素的稳定性1.1 子囊菌SD29701 产天然红色素的稳定性研究子囊菌SD29701 所产生的红色素在丙酮和乙酸乙酯中溶解性很好,可溶解于水、甲醇和乙醇,不溶于石油醚;其丙酮色素提取液在可见光区的最大吸收峰在520 nm 处。
[3]通过实验发现该色素的耐光耐热性较好;在碱性条件下稳定;对氧化剂和还原剂皆较敏感,在使用与保存时应尽量避免与之触;Vc 、糖和苯甲酸钠对色素稳定性无不良影响,可作为添加剂与色素共同使用;金属离子Fe3 + ,Cu2 +,Sn2 +和Pb2 +对该色素稳定性有不良影响,Fe2 +有一定的影响,而Na +,Mg2 +,K+ ,Ca2 +,Zn2 +和Al3 +对色素的稳定性皆无不良影响。