2-甲硫基-4,6-二氟嘧啶的合成研究(双氯磺草胺)
- 格式:pdf
- 大小:140.20 KB
- 文档页数:3
![4,6-二氯嘧啶的合成方法[发明专利]](https://uimg.taocdn.com/d1ca6834e97101f69e3143323968011ca300f792.webp)
(19)中华人民共和国国家知识产权局(12)发明专利申请(10)申请公布号 (43)申请公布日 (21)申请号 201610151172.8(22)申请日 2016.03.16(71)申请人 重庆紫光国际化工有限责任公司地址 401221 重庆市长寿区重庆市(长寿)化工园区化北路北区(72)发明人 丁永良 张飞 刘佳 何咏梅 唐大家 陈依柔 刘文枚 郑道敏 (74)专利代理机构 上海光华专利事务所 31219代理人 尹丽云(51)Int.Cl.C07D 239/30(2006.01)(54)发明名称4,6-二氯嘧啶的合成方法(57)摘要本发明提供一种4,6-二氯嘧啶的合成方法,包括如下步骤:1)将4,6-二羟基嘧啶与三氯氧磷混合,并加入光气、双光气、三光气中的一种或几种组合进行反应;2)对步骤1)所得的反应液分离提纯制得三氯氧磷和4,6-二氯嘧啶,回收的三氯氧磷作为步骤1)的原料用于4,6-二氯嘧啶合成反应。
本发明避免了有机碱回收和再利用的繁琐过程,也不使用昂贵的催化剂,避免了资源的浪费和产品损失,环境友好,不会产生额外的固废,也不会产生大量的含磷废液和废渣,并且产品收率高,纯度好,不需二次纯化即能达到市售要求,可用于大规模工业化生产。
权利要求书1页 说明书4页CN 105732514 A 2016.07.06C N 105732514A1.一种4,6-二氯嘧啶的合成方法,其特征在于,包括如下步骤:1)将4,6-二羟基嘧啶与三氯氧磷混合,并加入光气、双光气、三光气中的一种或几种组合进行反应;2)对步骤1)所得的反应液分离提纯制得三氯氧磷和4,6-二氯嘧啶,回收的三氯氧磷作为步骤1)的原料用于4,6-二氯嘧啶合成反应。
2.根据权利要求1所述的4,6-二氯嘧啶的合成方法,其特征在于:步骤1)中所述三氯氧磷与4,6-二羟基嘧啶的重量比为1-50:1。
3.根据权利要求1所述的4,6-二氯嘧啶的合成方法,其特征在于:步骤1)中加入光气反应时,光气与4,6-二羟基嘧啶的摩尔比为2-4:1。
![制备4,6-二氯嘧啶的方法[发明专利]](https://uimg.taocdn.com/acdfbc0d0812a21614791711cc7931b765ce7bbf.webp)
[19]中华人民共和国国家知识产权局[12]发明专利申请公开说明书[11]公开号CN 1687036A [43]公开日2005年10月26日[21]申请号200510077242.1[22]申请日2005.06.20[21]申请号200510077242.1[71]申请人江苏省激素研究所有限公司地址213022江苏省常州市常州新区岷江路98号[72]发明人孔繁蕾 吴国平 [74]专利代理机构北京金富邦专利事务所有限责任公司代理人孙伯庆 崔玉珍[51]Int.CI 7C07D 239/30权利要求书 1 页 说明书 3 页[54]发明名称制备4,6-二氯嘧啶的方法[57]摘要一种在合适的碱和一定溶剂或混合溶剂存在下,用双光气或三光气氯化4,6-二羟基嘧啶生成4,6-二氯嘧啶的方法。
本发明的目的在于提供一种操作简便、适于工业化的4,6-二氯嘧啶的制备方法。
200510077242.1权 利 要 求 书第1/1页 1.一种制备4,6-二氯嘧啶的方法,其特征在于在合适的碱存在下,用双光气或三光气处理4,6-二羟基嘧啶。
三光气的使用量为:三光气∶4,6-二羟基嘧啶=2/3∶1至2∶1(摩尔比),双光气的使用量为:双光气∶4,6-二羟基嘧啶=1∶1至3∶1(摩尔比);碱的使用量为:碱∶三光气=1∶1至7∶1(摩尔比),或碱∶双光气=0.5∶1至5∶1(摩尔比);反应在溶剂或混合溶剂中进行;反应在-20℃~120℃温度范围内进行,反应物在加热前应置于冰浴中。
2.根据权利要求1的方法,其特征在于,三光气的使用量为:三光气∶4,6-二羟基嘧啶=2/3∶1至1∶1。
双光气的使用量为:双光气∶4,6-二羟基嘧啶=1∶1至2∶1。
3.根据权利要求1的方法,其特征在于上述的合适的碱为叔胺和杂环胺。
碱的使用量为:碱∶三光气=1∶1至3∶1;或碱∶双光气=0.5∶1至2∶1。
4.根据权利要求1的方法,其特征在于将双光气或三光气加到4,6-二羟基嘧啶和碱的混合物中,也包括将碱加到4,6-二羟基嘧啶和双光气或三光气的混合物中。

新型除草剂双氟磺草胺的研究双氟磺草胺(florasulam)是由美国陶氏农业科学(Dow Agroscience)公司开发的三唑并嘧啶磺酰胺类除草剂。
20世纪80 年代美国陶氏农业科学公司首次报道了嘧啶酰胺类除草剂,其后成功开发了多个以三唑并嘧啶磺酰胺为母体化合物的高效除草剂新品种。
双氟磺草胺是继磺草唑胺、唑嘧磺草胺、氯酯磺草胺与双氯磺草胺之后于20 世纪90 年代中期开发成功的第五个三唑嘧啶磺酰胺类除草剂新品种。
1 理化性质纯品熔点193.5 -230.5℃,相对密度1.77(21℃)。
蒸气压:1×10-2mPa(25℃),水中溶解度(20℃,pH7.0)为6.36g/L。
土壤半衰期DT50 为1-4.5d,田间DT50 为2-18d。
离解常数pKa=4.54(23℃)。
化学名称:2’,6’-二氟-5-甲氧基-8-氟[1,2,4]三唑并[1,5-c]嘧啶-2-磺酰苯胺。
2’,6’-difluoro-5-methoxy-8-fluoro[1,2,4]triazolo[1,5-c]Pyrimidine-2-Sulfonanilide 分子式:C12H8F3N5O3S分子量:359.3CAS 登录号:[145701-23-1]结构式:2 毒性及环境生物安全评价大鼠急性经口LD50>6000mg/kg,兔急性经皮LD50>2000mg/kg。
对兔眼睛有刺激性,对兔皮肤无刺激性。
无致畸、致癌、致突变作用,对遗传无不良影响。
NOEL 数据:大、小鼠(90d)100mg/kg·d。
无致畸、致癌、致突变作用,对遗传亦无不良影响。
鹌鹑急性经口LD50>6000mg/kg。
鹌鹑和野鸭饲喂LD50(5d)>5000mg/kg 饲料。
鱼毒LC50(96h,mg/L):虹鳟鱼>86,大翻车鱼>98。
密蜂LD50(48h)>100μg/只(经口和接触)。
蚯蚓LD50(14d)>1320mg/kg 土壤。

2-氯嘧啶的合成工艺研究
张进;肖国民;杨为华
【期刊名称】《化工时刊》
【年(卷),期】2004(18)10
【摘要】介绍了2-氯嘧啶的合成工艺路线,研究了多种因素对每步反应收率的影响,得到较佳的工艺条件.实验结果表明丙二酸二乙酯和盐酸胍反应以4 h为佳,合成的4,6-二羟基-2-氨基嘧啶以二氯甲烷为溶剂反应得4,6-二氯-2-氨基嘧啶,脱氯反应的较佳配比为n(Na)∶n(Zn)∶n(4,6-二氯-2-氨基嘧啶)=2.6∶3∶1,合成2-氯嘧啶的较佳原料配比为n(2-氨基嘧啶)∶n(ZnCl2)∶n(NaNO2)=1∶3∶1.7,反应总收率为43.7%.
【总页数】3页(P22-24)
【作者】张进;肖国民;杨为华
【作者单位】东南大学化学化工系,江苏,南京,210096;东南大学化学化工系,江苏,南京,210096;东南大学化学化工系,江苏,南京,210096
【正文语种】中文
【中图分类】TQ45
【相关文献】
1.2-氨基-4,6-二氯-5-甲酰胺基嘧啶的合成工艺研究 [J], 李国俊;王辉;程杰;柏俊
2.(E)-2-[2-(6-氯嘧啶-4-基氧)苯基]-3-甲氧基丙烯酸甲酯的合成工艺研究 [J], 许标
3.4,6-二氯-2-甲基嘧啶的合成工艺研究 [J], 陈磊祥;邓胜松;管秋香;顾雷鸣
4.(E)-2-{2-[6-(2-氰基苯氧基)嘧啶-4-基氧]苯基)-3-甲氧基丙烯酸甲酯合成工艺研究 [J], 奕民
5.4-(3-氯-4-甲氧基苄基氨基)-5-乙氧基羰基-2-甲硫基嘧啶的合成工艺研究 [J], 胥稳智;徐志栋;刘维岩;刘亚彬;杨瑜涛;李玮
因版权原因,仅展示原文概要,查看原文内容请购买。

2-氨基-4,6-二甲氧基嘧啶合成工艺
2-氨基-4,6-二甲氧基嘧啶的合成工艺可以分为以下几个步骤:
1. 首先,需要准备2-氨基-4,6-二甲氧基嘧啶的原材料。
原材料可以是2-氨基-4,6-二甲氧基嘧啶的前体化合物,例如2-氨基-4,6-二甲氧基嘧啶醇。
2. 将2-氨基-4,6-二甲氧基嘧啶的原材料与适当的有机溶剂(例如二甲基亚砜)混合,并加入适量的碱(例如三乙胺)进行反应。
该反应通常在低温下进行,以控制反应速率。
3. 在反应过程中,可以进一步添加适当的酸性催化剂(例如盐酸)来促进反应的进行。
酸性催化剂可以帮助生成目标产物。
4. 反应完成后,通过减压蒸馏或其他分离技术将有机溶剂和副产物从反应混合物中去除。
5. 最后,得到的2-氨基-4,6-二甲氧基嘧啶可以通过结晶、洗涤和干燥等步骤进行纯化和提纯。
需要注意的是,该合成工艺只是一种可能的方法,具体的合成工艺可能会因实际情况而有所不同,例如反应条件、催化剂选择等。
在实际操作中,应根据具体情况进行优化和调整。
![一种2-甲氧基-4-氯-5-氟嘧啶的制备方法[发明专利]](https://uimg.taocdn.com/c5f019f64431b90d6d85c7d7.webp)
专利名称:一种2-甲氧基-4-氯-5-氟嘧啶的制备方法专利类型:发明专利
发明人:白著双,胡博文,徐治敏,张青前,陈为强
申请号:CN201710372486.5
申请日:20170524
公开号:CN108929277A
公开日:
20181204
专利内容由知识产权出版社提供
摘要:本发明公开了一种2‑甲氧基‑4‑氯‑5‑氟嘧啶的制备方法,属于有机化学中间体化工工艺技术领域。
其工艺过程概括为:向反应容器中加入碱性物质、溶剂并搅拌,然后加入光气、双光气或三光气,作为氯化试剂。
最后加入2‑甲氧基‑4‑羟基‑5‑氟嘧啶,检测反应完成后经简单的后处理工艺,得到高收率、高纯度的目标产物。
本发明工艺反应条件温和、后处理简单、成本低,收率高,达到
97‑98.5%。
申请人:徐治敏
地址:528400 广东省中山市西区富华道42号荣隆大厦7楼704
国籍:CN
更多信息请下载全文后查看。
![[doc]4,6-二氯嘧啶的合成工艺研究](https://uimg.taocdn.com/de7a14f0227916888586d788.webp)
[doc] 4,6-二氯嘧啶的合成工艺研究4,6-二氯嘧啶的合成工艺研究第23卷第2期20o9.O6沈阳化工学院JOURNALOFSHENYANGUNIVERSrrYOFCHEMIcALTECHNOLOGYV0I.23No.2Jun.2O09文章编号:1004—4639(2009)02—0118—034,6一二氯嘧啶的合成工艺研究杨桂秋.,彭立刚,田晋’,韩燕(1.沈阳化工学院化学工程学院,辽宁沈阳l10142;2.东北育才学校,辽宁沈阳110179)摘要:以甲酰胺,丙二酸二甲酯为原料首先合成4,6-二羟基嘧啶,收率为59.73%,然后与POCI,反应合成目标化合物.以反应温度,反应时间及POCI的用量作为考察因素进行正交实验,用这3个指标评定工艺的优劣.由正交实验得到最佳合成工艺条件为:反应温度75?,反应时间3h,r/(4,6一二羟基嘧啶):t/(POCI3)=l:6,收率为72.52%.2步反应总收率为43.3l%,产物经红外光谱鉴定.结构正确.关键词:4,6-二氯嘧啶;合成工艺;正交实验中图分类号:TQ252.4文献标识码:A4,6一二氯嘧啶是合成嘧啶类化合物的重要中间体,广泛应用于医药,农药嘧啶类产品的合成.在农药的发展史中,嘧啶类化合物一直显示很高的生物活性,此类化合物的开发一直受到医药和农药界的重视?J.关于4,6一二氯嘧啶的合成方法,选用不同的氯化试剂,则有不同的工艺路线.经总结大致有2种,即POCI氯化法和固体光气氯化法J.但是,根据现有文献,在这2 种合成方法中催化剂的用量占了很大的比例,这无疑对工业生产造成了成本的增加.本文采用的4,6-二氯嘧啶合成路线如下:nocNI-I:+MeOOCCH2COOM~佣伽}OH!Q-N,N一二甲基苯胺该合成路线在氯化试剂POCI的条件下,加入很少量的催化剂N,N一二甲基苯胺进行合成反应,并采用正交实验对该合成工艺条件进行优选,拟选择一条催化剂用量少,产品收率高的工艺路线.1实验部分1.1试剂甲酰胺,丙二酸二甲酯,三氯氧磷,N,N一二甲基苯胺,二氯乙烷,均为分析纯试剂.1.2实验仪器三口瓶(连接搅拌装置),分液漏斗,减压蒸馏整套装置,冷凝器,温度计,油浴锅,X-4数字显微熔点测定仪,TermoNicoletNEXUX470FT—IR型红外光谱仪.1.3实验方法1.3.14,6一二羟基嘧啶的合成将丙二酸二甲酯(2.47g,0.019mo1)和甲酰胺(2.96g,0.066mo1)加入到甲醇一甲醇钠(自制)溶液中.室温搅拌15min后,用大约lh左右的时间升温至5O?,在此温度下反应4h.反应结束后,冷却至30—35?,减压蒸馏出过量的甲醇.然后,向剩余的反应物中加入蒸馏水,用质量分数为l8%的盐酸溶液控制pH=2—3,有大收稿日期:2008—07—15作者简介:杨桂秋(1970一),女,辽宁盘锦人,副教授,博士,主要从事有机合成和药物中间体的研究第2期杨桂秋,等:4,6?二氯嘧啶的合成工艺研究ll9量淡黄色固体生成.抽滤干燥后,得淡黄色4,6一二羟基嘧啶,收率59.73%.1.3.24,6一二氯嘧啶的合成将4,6一二羟基嘧啶(5.6lg,0.05mol,质量分数98%)加入到三氯氧磷(38.34g,0.25mo1)中,再向其中滴加2—3滴N,N一二甲基苯胺,室温搅拌15min后,用大约1h左右的时间升温至75?,在此温度下反应3h.反应结束后, 冷却至55—65?,减压蒸馏出过量的三氯氧磷. 将剩余的反应物加入到冰水中,温度控制在0—5?,析出淡黄色固体,控制pH=5—7,立即用冰水洗涤2次,再用100mL二氯乙烷萃取2 次.然后,将滤饼用100mL二氯乙烷溶解,合并萃取液和溶解液,再用10mL饱和氯化钠溶液洗涤1次,用无水硫酸镁干燥,抽滤后,滤液减压蒸于溶剂并干燥,得淡黄色4,6一二氯嘧啶,收率72.52%.2结果与讨论2.1正交实验在4,6一二氯嘧啶的合成中影响因素很多,在催化剂及其用量固定的条件下,反应温度,反应时间和反应原料配比是影响反应的主要因素. 根据文献和现有实验数据,选择三因素三水平的正交实验考察方案,选用L.(3)正交表,实验因素水平设置见表1.表1实验的因素水平表Table1Experimentalfactorsandlevels注:原料配比为4,6一二羟基嘧啶和POCl3的摩尔比. 按照正交实验表的实验序号顺序,并经随机化处理,根据上述4,6一二氯嘧啶的合成方法进行实验,制得产品,并称重计算收率,正交实验结果见表2.从表2可以看出所考察的各因素对4,6一二氯嘧啶收率的影响程度,可以得出以下结论:(1)3个因素对实验结果影响的显着性依次为:因素A>因素B>因素C;(2)对于因素A,3个水平对实验收率的影响顺序为:7Ooc>90oC>105?;对于因素B,3个水平对实验收率的影响顺序为:3h>5h>7h;对于因素c,3个水平对实验收率的影响顺序为:1:6>1:5>1:7;(3) 根据正交试验所得收率和表2结果:3个因素的尺值的大小依次为A(32.91),B(13.15),c(1.34).综合数据得出结论:各因素对收率影响的大小为:温度>时间>P()Cl用量.本次正交实验得到的最优工艺条件为:A.Bc:,即在75?,6倍于4,6一二氯嘧啶的物质的量的POC1的用量下,反应3h,能够得到最优收率.表2正交实验结果Table2Resultsoforthogonalexperiment以正交设计得出的最优条件A,Bc进行重复实验,结果见表3.表3重复实验Table3Repeatedexperiments2.2产物结构表征分别对所合成的产物4,6-二羟基嘧啶和4,6一二氯嘧啶进行红外光谱分析,结果如下: (1)4,6一二羟基嘧啶的红外光谱分析根据嘧啶类主要官能团的红外特征吸收频率和实验得到的4,6一二羟基嘧啶的红外图谱分析得出:在波数3071cm和3039cm一处是C—H弱的伸缩振动吸收峰;在1679cm,,120沈阳化工学院2009年1541cm和1431cm处是嘧啶环的骨架振动吸收峰;指纹区在1000—960cm和825,775cm的范围内,也呈现出嘧啶环上的C—H中等强度的弯曲振动吸收峰.与4,6一二羟基嘧啶的红外标准图谱对照基本吻合.(2)4,6一二氯嘧啶的红外光谱分析同样根据嘧啶类主要官能团的红外特征吸收频率和实验得到的4,6一二氯嘧啶的红外图谱分析得出:在波数3080cm和3040cm处是C—H弱的伸缩振动吸收峰;在1646cm,,1606cm和1362cm处是嘧啶环的骨架振动吸收峰;指纹区在1000—960cm和825,775cm的范围内也呈现出嘧啶环上的C—H中等强度的弯曲振动吸收峰.与4,6一二氯嘧啶的红外标准图谱对照基本吻合.3结论(1)在实验中,反应温度对目标产物收率的影响较大.反应时间和POC1用量2个因素对产物收率的影响较小.在催化剂及其用量方面,由于使用的催化剂价格低廉,用量较小,对节约生产成本有利.(2)由于实验条件的限制,实验采用最原始的实验方法,经过2步反应总收率为43.31%.与目前先进的生产工艺2步总收率(>75%)相比,存在很大差距,究其原因可能存在以下几个方面:在后处理过程中损失较大;未使用回收溶剂进行实验;生产工艺较原始等.(3)实验未对反应原料成本,反应三废等方面作更深入的研究,只在催化剂及其用量方面有所改进,今后工作将会对以上方面做出更加细致深入的研究,以期有新的突破.参考文献:[1]马亚团,周文明.2一乙氧基4,6?二氯嘧啶的合成[J].西北农业,2007,16(5):195—198.[2]刘长令.农药的生产与合成[M].北京:化学工业出版社,2000:120—124.[3]苏少泉.新的乙酰乳酸合成抑制剂?磺酰胺类除草剂[J].农药译丛,1997,19(5):18—23.[4]周垂龙,唐玉平,龙晓钦,等.4,6-二氯嘧啶的制备方法:中国,CNI830907A[P].2006—03—3O.[5]DoyleT.SynthesisofChlorinatedPyrimidine:A?merica,WO02/04428[P].2002一O1一l7.[6]DoyleT.SynthesisofChlorinatedPyrimidine:A—merica,WO02/00628[P].2002—01—03.Synthesisof4.6一DichloropyrimidineYANGGui—qiu,PENGLi—gang,TIANJin,HANYAN(1.ShenyangUniversityofChemicalTechnology,Shenyang110142,China;2.NortheasternYucaiSchool,Shenyang110179,China)Abstract:ThetitlecompoundwassynthesizedfromPOC13and4,6-dihydroxypyrimidinewhichwassynthesizedfromamideandethylmalonatein59.73%ingtemperatureof thereaction.timeofthereactionandtheamountofPOCI3asaffectingfactors,theorthogonaltestwa sconductedtoassessthepreparationprocessinthethreeindexes.Theresultsofoptimizedpreparation processwereshownasfol—lows:thetemperatureofthereactionwas75oc,thetimeofthereactionwas3hour sandtheamountofPOC13was6timesofthatof4,6一dihydroxypyrimidinein72.52%yield.Thetotalyieldwas43.31%.TheproductwascharacterizedbyIRandcorrect.Keywords:4,6-dichloropyrimidine;synthesistechnology;orthogonaldesignmethods。

2―氨基―4,6―二甲氧基嘧啶的合成磺酰脲类除草剂主要是在上世纪80 年代发展起来的,是一类广谱高效的水稻、玉米、大豆田地除草剂,具有活性高、用量少以及毒性低等特点,在世界上被公认为高效、环保的绿色型农药。
在磺酰脲类除草剂的生产中,2-氨基-4,6-二甲氧基嘧啶是其合成的重要中间体,以其为原料制备的磺酰脲类除草剂品种有很多,如烟嘧磺隆、苄嘧磺隆、吡嘧磺隆、嘧啶磺隆、砜嘧磺隆、乙氧嘧磺隆、酰嘧磺隆、啶嘧磺隆、环丙嘧磺隆、玉嘧磺隆、四唑嘧磺隆、氯吡嘧磺隆、氟啶嘧磺隆、甲磺胺磺隆等。
因此,2-氨基-4,6-二甲氧基嘧啶的合成长期以来一直受到农药企业及科研人员的广泛关注,对于它的合成工艺进行研究与完善,具有非常重要的意义。
1 合成方法简介目前,2-氨基-4,6-二甲氧基嘧啶合成方法的文献报道主要有五种:(1)以2,4,6-三氯嘧啶为主要原料,控制温度在-78 ℃下进行,虽然只有两步反应,但反应条件苛刻,原料价格昂贵,收率低;(2)以4,6-二甲氧基-2-甲磺酰嘧啶为主要原料,与氨水在常温下反应72h 得到目标产物,此法虽然条件温和、操作简单、收率较高(85.4%),但反应时间太长,原料昂贵,不易得到;(3)以硝酸胍、盐酸胍等胍盐复合物与丙二酸二乙酯为原料制备目标产物。
此法原料虽然相对廉价易得,但要运用大大过量的三氯氧磷作氯化试剂和溶剂,过量的三氯氧磷不仅会加剧副产物4,6-二氯-2-嘧啶氨基磷酰二氯的生成,且遇水容易爆炸,给生产带来安全隐患。
另外更加不利的是中和、水解产生大量的强酸性、含盐、含磷废水,极难处理,对环境造成很大的破坏;(4)以2-氨基-4,6-二羟基嘧啶和重氮甲烷为原料,此反应路线短,收率高(83%),但重氮甲烷在常温下为强烈刺激性的有毒气体,它在撞击、加热或在化学反应时,能发生强烈的爆炸,遇水分解,不易储存,操作难度较大;(5)以丙二腈为主要原料,经1,3-二甲氧基丙二亚胺二盐酸盐、单盐酸盐、3-氨基-3-甲氧基-N-氰基-2-丙脒,最后加热闭环得到目标产物。

4,6-二甲氧基-2-甲磺酰基嘧啶生产工艺方案1. 背景介绍4,6-二甲氧基-2-甲磺酰基嘧啶是一种重要的有机中间体,广泛应用于化学合成和制药工业。
本文档将介绍一种有效的生产工艺方案,以合成4,6-二甲氧基-2-甲磺酰基嘧啶。
2. 反应方程4,6-二甲氧基-2-甲磺酰基嘧啶的合成反应方程如下:3. 生产工艺步骤步骤1: 原料准备- 进行原料的采购和检验,确保原料质量符合要求。
步骤2: 反应体系搭建- 在反应釜中加入4,6-二甲氧基嘧啶和甲磺酰胺。
- 加入适量的溶剂(例如二甲基亚砜)作为反应介质。
- 加入催化剂(例如过氧化氢)以促进反应的进行。
- 调整反应温度和时间,使反应达到最佳条件。
步骤3: 反应进行- 开始加热反应体系,控制反应温度在适当的范围内。
- 在反应过程中进行搅拌,以保证反应充分进行。
步骤4: 反应结束- 反应时间结束后,停止加热并冷却反应体系。
- 进行反应产物的分离和纯化,如结晶、洗涤、干燥等。
4. 质量控制- 在生产过程中,进行多次取样并进行质量检验,确保产品符合要求的纯度和含量。
- 对生产中的关键参数进行监控和调整,以保证产品质量的稳定。
5. 安全环保措施- 在进行反应操作时,采取必要的安全措施,如佩戴防护眼镜、穿戴防护服等。
- 对废物液体和残余物进行正确的处置和处理,以保护环境和人员安全。
6. 总结本文档介绍了一种合成4,6-二甲氧基-2-甲磺酰基嘧啶的生产工艺方案。
通过正确的操作步骤和质量控制措施,可以获得符合要求的产品。
在生产过程中,也要始终注意安全环保问题,确保人员和环境的安全。

2-氨基-4,6-二甲氧基嘧啶的合成研究
2-氨基-4,6-二甲氧基嘧啶是一种重要的药物中间体,具有广泛的应用领域,如抗癌药物合成、植物生长调节剂合成等。
其合成方法有多种途径,以下是其中一种常用的合成方法:
合成方案如下:
1. 制备2-氨基-4,6-二甲氧基苯乙酮:将2-溴乙酮与2-胺基-4,6-二甲氧基苯硼酸以苯并催化剂存在下反应,生成2-氨基-4,6-二甲氧基苯乙酮。
2. 嘧啶环的引入:将2-氨基-4,6-二甲氧基苯乙酮与氰化氢、氢氰酸钠在碱性条件下反应,发生Knoevenagel缩合反应,将氰基引入到2-氨基-4,6-二甲氧基苯乙酮上,产生2-氨基-4,6-二甲氧基嘧啶。
3. 甲氧基的引入:将2-氨基-4,6-二甲氧基嘧啶与甲基碘在碱性条件下反应,生成2-氨基-4,6-二甲氧基嘧啶的甲基化产物。
这样,通过以上反应步骤,就可以得到2-氨基-4,6-二甲氧基嘧啶。
整个合成过程需要注意反应条件的控制,以及产物的纯化和分离。
同时,在合成过程中还可以对反应温度、时间、溶剂等因素进行调控,以提高产物的收率和质量。
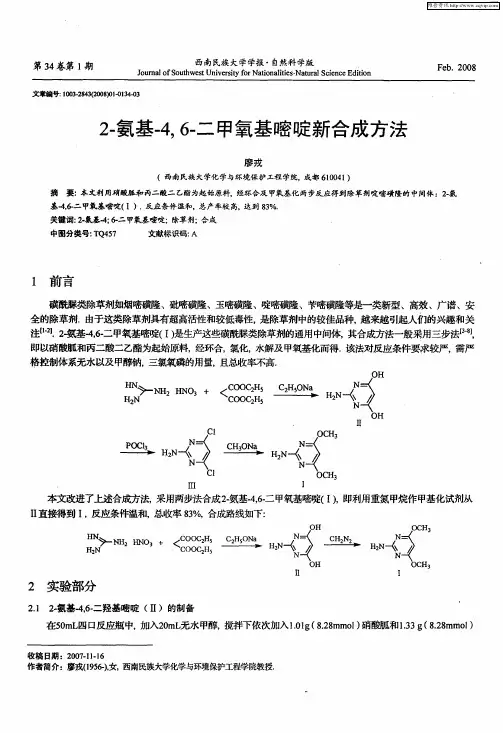
4,6-二甲氧基-2-甲磺酰基嘧啶合成工艺合成4,6-二甲氧基-2-甲磺酰基嘧啶的工艺如下:
步骤1: 甲基化反应
将2-甲磺酰基嘧啶与甲醇在碱性条件下反应。
在温度为60°C 的条件下搅拌反应1小时。
反应结束后,用冷水淘洗沉淀物并将其干燥,得到2-甲磺酰基-4,6-二甲氧基嘧啶。
步骤2: 亲核取代反应
将2-甲磺酰基-4,6-二甲氧基嘧啶与亲核试剂(例如醇、胺等)在碱性条件下反应。
在温度为90°C的条件下搅拌反应2小时。
反应结束后,用冷水淘洗沉淀物并将其干燥,得到4,6-二甲氧基-2-甲磺酰基嘧啶。
步骤3: 结晶纯化
将4,6-二甲氧基-2-甲磺酰基嘧啶用适当的溶剂在中温条件下结晶纯化。
将溶液过滤,然后冷却结晶。
得到纯度较高的4,6-二甲氧基-2-甲磺酰基嘧啶。
步骤4: 确认结构
通过核磁共振(NMR)、质谱(MS)等分析技术,对所合成的4,6-二甲氧基-2-甲磺酰基嘧啶进行结构确认。
以上即为合成4,6-二甲氧基-2-甲磺酰基嘧啶的工艺流程。
请注意,以上合成工艺仅供参考,具体实验条件和操作步骤需根据实际情况进行调整和优化,以确保反应的顺利进行和产物的高纯度。
4,6-二羟基嘧啶的合成及工艺优化4,6-二羟基嘧啶(4,6-Dihydroxypyrimidine)是一种重要的有机化合物,具有广泛的应用价值。
它是一种嘧啶核苷酸的前体物质,可以用于制备DNA和RNA分子,还可以用于合成多种生物活性化合物。
4,6-二羟基嘧啶的合成及工艺优化对于化学生产工艺的改进和这些有机化合物的应用具有重要意义。
一、4,6-二羟基嘧啶的合成方法4,6-二羟基嘧啶的合成方法主要有两种:一种是通过对氨基甲酸酯和醛缩合后环化得到4,6-二羟基嘧啶;另一种是通过氨基甲酸酯与脱氮剂作用得到噻唑啉-4-氧化物,然后再经过水解得到4,6-二羟基嘧啶。
不同的合成方法在工艺上有其特点,选择合适的合成方法可以有效降低生产成本,提高产物纯度。
二、合成方法的工艺优化1. 通过对氨基甲酸酯和醛缩合后环化得到4,6-二羟基嘧啶的工艺优化这种方法的工艺优化主要包括两个方面:一是对反应条件进行优化,二是对环化反应的控制。
首先是对反应条件进行优化,这包括温度、催化剂、溶剂和反应时间等因素。
在温度方面,可以通过实验确定合适的反应温度,通常在室温至50摄氏度之间。
催化剂的选择也是关键,常用的催化剂有氫氟酸、硫酸、磷酸等,不同的催化剂对产物的纯度和产率有显著影响。
溶剂的选择则要考虑到反应物的溶解度和反应的速度,通常用二甲基甲酰胺、乙醚、乙醇等。
其次是对环化反应的控制,这包括反应物的投加速度和对水的处理。
反应物的投加速度要适当控制,以保证反应的均匀性和产物的得率。
对水的处理也是非常重要的,很多环化反应都对水敏感,因此要采取相应的方法去除或保护水分。
其次是水解反应的条件优化,这主要包括水解剂的选择和水解条件的控制。
常用的水解剂有醋酸、氢氧化钠、硫酸等,不同水解剂对水解得率和产物的纯度有影响。
对水解条件的控制也很重要,包括温度、pH值、反应时间等。
通过对4,6-二羟基嘧啶的合成方法进行工艺优化,可以提高产物的得率和纯度,降低生产成本,使得合成方法在工业上更具应用潜力。
嘧啶类化合物的合成2-氯-4,6-二氨基-5-氰基嘧啶的合成摘要2-氯-4,6-二氨基-5-氰基嘧啶是很好的医药中间体,目前在有机合成特别是药物合成中已得到广泛的应用。
本文通过两步反应合成目标产物。
首先以双氰胺钠和丙二腈为原料,反应得到中间体1-氨基-1氰氨基-2,2-二氰基乙烯钠盐。
考察了投料量、溶剂、洗涤剂三者的质量比对反应产率的影响。
结果表明以双氰胺钠和丙二腈(摩尔比为1.1:1)在160℃下,总投料量(双氰胺钠和丙二腈):溶剂(N,N-二甲基乙酰胺):洗涤剂(仲丁醇)为1:2:4(质量比),反应时间1小时,洗涤时间1.5小时等条件下得到的产率最高,可达88.2%(纯度98.4%)。
将1-氨基-1-氰氨基-2,2-二氰基乙烯钠溶于溶剂中,在0 ℃-5 ℃下通入过量环化试剂可以得到2-氯-4,6-二氨基-5-氰基嘧啶,粗产品经提纯后纯度可达95.8%。
合成中间体和目标产物利用MS、IR 和NMR进行了结构表征。
另外,洗涤剂可进行回收再利用,经处理后其洗涤效果与分析纯洗涤剂几乎无异。
关键字:双氰胺钠;丙二腈;质量比;洗涤剂;2-氯-4,6-二氨基-5-氰基嘧啶;1-氨基-1氰氨基-2,2-二氰基乙烯钠盐Synthesis of2-chloro-4,6-amino-5-cyano-pyrimidineAbstract2-chloro-4,6-diamino-5-cyano-pyrimidine is a good pharmaceutical intermediates, present in organic synthesis, especially synthetic drugs has been widely used. This two-step reaction through the target compound. First of all, and malononitrile with sodium dicyandiamide as raw materials reaction intermediates,1-amino-1-cyanide amino-2,2-dicyano-ethylene sodium. Investigated feeding amount, solvents,detergent mass ratio of the three effects on the reaction yield. The results show that the double cyanide of sodium and malononitrile ammonia (molar ratio of 1.1:1) at 160 ℃, the total feeding amount (two-ammonia and sodium cyanide malononitrile): solvent (N, N-dimethylacetamide) : detergent (butanol) = 1:2:4 (mass ratio), reaction time 1 hour, washing time was 1.5 hours in the yield obtained under conditions of maximum, up to 88.2% (purity 98.4%). The 1-amino-1-cyanoacrylic amino-2,2-dicyano-ethylene dissolved in solvent of sodium, in the 0 ℃-5 ℃access over the next cyclization reagent can be 2-chloro-4,6-diamino-5-cyano pyridine, the crude product was purified, the purity of 95.8%. Synthetic intermediates and target products are using MS, IR, HPLC and NMR were characterized. In addition, detergents can be recycled, treated analytically pure after the washing detergent with almost the same effect.Keywords: sodium dicyandiamide; malondialdehyde cyanide; mass ratio; scour;1-amino-1-cyanide-amino-2,2-dicyano-ethylenesodium;2-chloro-4,6-diamino-5-cyano-Pyrimidine目录摘要 .......................................................................................................................... .. (I)ABSTRACT........................................................................................................... ............... I I 1 绪论. (1)1.1选题背景 (1)1.1.1 嘧啶化合物在农药领域的应用 (1)1.1.2 嘧啶类化合物在医药中的应用 (7)1.2嘧啶类化合物的研究进展 (8)1.3嘧啶类化合物的展望 (12)1.4本课题研究内容与意义 (12)2 实验部分 (13)2.1原料与试剂 (13)2.2主要仪器与设备 (13)2.3实验装置 (14)2.4实验步骤 (15)2.4.1 1-氨基-1-氰氨基-2,2-二氰基乙烯钠盐(中间体)的合成(15)2.4.2 2-氯-4,6-二氨基-5-氰基嘧啶的合成 (15)3 结果与讨论 (16)3.1中间体制备的条件优化及洗涤剂的回收再利用 (16)3.1.1 优化溶剂用量 (16)3.1.2 优化洗涤剂用量 (17)3.1.3 抽滤废液中洗涤剂的回收及洗涤效果研究 (18)3.22-氯-4,6-二氨基-5-氰基嘧啶合成方法的探索及粗产品的提纯(20)3.3化合物的谱图表征 (21)3.3.1 1-氨基-1-氰氨基-2,2-二氰基乙烯钠盐的谱图表征 (21)3.3.2 提纯所得2-氯-4,6-二氨基-5-氰基嘧啶的谱图表征 (25)结论 (29)致谢 (30)参考文献 (31)1 绪论1.1选题背景我国是农业大国,农业是国民经济发展的基础,而农药是农业发展不可缺少的重要物资。
4,6-二羟基嘧啶的合成及工艺优化4,6-二羟基嘧啶(4,6-dihydroxypyrimidine)是一种重要的药物中间体,广泛应用于制备核素标记化合物、药物前驱体等领域。
本文综述了4,6-二羟基嘧啶的合成方法及其工艺优化研究情况。
1. 合成方法目前,常用的4,6-二羟基嘧啶合成方法主要有以下几种。
1.1 胺基酸催化的异氰酸酯加成反应该方法利用异氰酸酯与二羟基酸反应生成4,6-二羟基嘧啶,反应过程中以二甲基甲酰胺(DMF)为溶剂,L-脯氨酸为催化剂,反应时间为24 h,反应温度为110°C。
该方法反应效率高,合成产物的纯度和收率都较高。
1.2 脱羧反应该方法以三羧基腺嘌呤为起始原料,通过脱羧反应生成4,6-二羟基嘧啶。
该反应会产生甲烷等有毒气体,需要采取特殊的防护措施。
此外,该方法需使用高温高压,反应过程较为危险,且产率较低。
1.3 磷酸催化的脱氧核糖反应该方法以磷酸为催化剂,以4-羟基-2-甲基嘧啶作为起始原料,在水中进行反应。
该方法反应温和、产率高。
但是,在实际工业生产中,该方法未得到广泛应用。
2. 工艺优化为了提高4,6-二羟基嘧啶的合成效率和产率,研究者一直在不断地进行工艺优化。
以下为几种常见的工艺优化方法。
选择合适的溶剂可以优化反应的效率和产率。
传统方法中常用的溶剂是DMF,但DMF 有毒性,不利于环境保护。
近年来,研究者尝试使用环保性较好的溶剂,如乙醇、水等。
目前,最常用的溶剂为水、甲醇和DMF的混合溶剂。
催化剂的种类和用量对反应的效率和产率有着重要的影响。
近年来,研究者发现,使用亲核性较强的胺类化合物作为催化剂可以提高反应效率和产率。
合适的反应温度可以提高反应的速度和产率。
目前,通常采用的反应温度为110-120°C,但研究者发现,降低反应温度可以减少副反应的发生,提高目标产物的产率。
2.4 反应时间优化适当的反应时间也对反应产率有着决定性的影响。
研究者们通过分析不同反应时间下产物的生成情况,得出了最佳反应时间为10-20 h。