第二节 分子的立体构型
- 格式:doc
- 大小:37.50 KB
- 文档页数:2



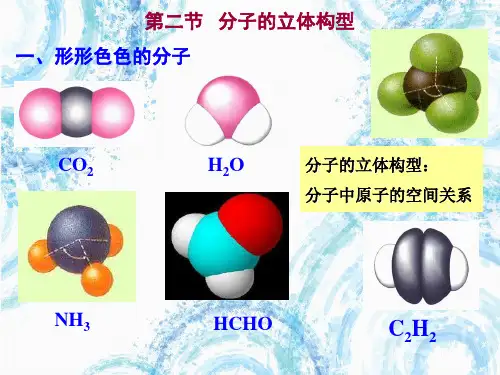






化学选修三第二章第二节分子的立体构型选修三第二章第2节分子的立体构型第2节分子的立体构型一、常见分子的空间构型1.双原子分子都是直线形,如:HCl、NO、O 2、N2等。
2.三原子分子有直线形,如CO2、CS2等;还有“V”形,如H2O、H2S、SO2等。
3.四原子分子有平面三角形,如BF3、BCl3、CH2O等;有三角锥形,如NH3、PH3等;也有正四面体,如P4。
4.五原子分子有正四面体,如CH4、CCl4等,也有不规则四面体,如CH3Cl、CH2Cl2、CHCl3。
另外乙烯分子和苯分子都是平面形分子。
二、价层电子对互斥理论(Valance Shell Electron Pair Repulsion Theory)简称VSEPR适用AD m 型分子1、理论模型分子中的价电子对(包括成键电子对和孤电子对),由于相互排斥作用,而趋向尽可能彼此远离以减小斥力,分子尽可能采取对称的空间构型。
2、用价层电子对互斥理论推断分子或离子的空间构型的一般步骤:(1)确定中心原子A价层电子对数目法1.经验总结中心原子的价层电子对数=1(中心离子价电子数+配2对原子提供电子总数)对于AB m型分子(A为中心原子,B为配位原子),计算方法如下: n =中心原子的价电子数+每个配位原子提供的价电子数×m2注意:①氧族元素的氧做中心时:价电子数为 6, 如 H 2O ,H 2S ;做配体时:提供电子数为 0,如在 CO 2中。
②如果讨论的是离子,则应加上或减去与离子电荷相应的电子数。
如PO -34中P 原子价层电子数5+(0×4)+3 = 8;NH +4中N 原子的价层电子数5+(1×4)-1 = 8。
③结果为单电子时视作有一个电子对。
例:IF 5 价层电子对数为21[7+(5×1)] = 6对 正八面体(初步判断)N H +4价层电子对数为21[5+(4×1)-1] = 4对 正四面体PO -34价层电子对数为21[5+(0×4)+3] = 4对 正四面体NO 2 价层电子对数为21[5+0] = 2.5−→−3对 平面三角形法2. 确定中心原子A 价层电子对数目-----普遍规则中心原子A 价层电子对数目=成键电子对数+孤对电子数 (VP = BP + LP )VP 是价层电子对,BP 是成键电子对(BOND ),LP 是孤对电子对(LONE PAIR )VP = BP + LP =与中心原子成键的原子数+中心原子的孤对电子对数LP=配位原子数+LP Lp =21(中心原子价电子数—配位原子未成对电子数之和)IF 5 Lp =21[7-(5×1)] = 1 构型由八面体−→−四方锥 NH +4Lp =21[(5-1)-(4×1)] = 0 正四面体PO -34Lp =21[(5+3)-(4×2)] = 0 正四面体SO -24Lp =21[(6+2)-(4×2)] = 0 正四面体NO 2 Lp =21[5-(2×2)] = 21−→− 1 构型由三角形−→−V 形 SO -23Lp =21[(6+2)-(3×2)] = 1 构型由四面体−→−三角锥法3:由Lewis 结构式或结构式直接写出,双键、三键都是1对电子P ClClCl ClCl P Cl Cl ClP ClClCl Cl+Cl P Cl ClClCl Cl -Cl Cl ClCl +Cl P Cl Cl Cl Cl Cl -VP: 5 4 4 6 4(2)确定价层电子对的空间构型价层电子对数目2 3 4 5 6价层电子对构型直线形三角形四面体三角双锥八面体(3)分子空间构型确定价层电子对互斥模型说明的是价层电子对的空间构型,而分子的空间构型指的是成键电子对空间构型,不包括孤对电子。
第二节 分子的立体构型第1课时 形形色色的分子 价层电子对互斥理论▍课标要求▍1.认识共价分子结构的多样性和复杂性。
2.能根据价层电子对互斥理论判断简单分子或离子的构型。
要点一 形形色色的分子1.分子的立体构型:指由两个以上的原子构成的分子中的原子的问题。
2.常见的分子结构分子 类型 化学式 立体构型结构式 键角 比例模型球棍 模型三原子分子CO 2 (CS 2) _____ ________ 180°H 2O (H 2S) _____________105°四原子分子CH 2O _________NH 3 (PH 3)_____________107°五原子分子CH 4 (CCl 4)_________思考1:五原子分子都是正四面体结构吗?要点二 价层电子对互斥理论(VSEPR) 1.价层电子对互斥理论分子中的价层电子对(包括 和 )由于 作用,而趋向尽可能彼此远离以减小斥力,分子尽可能采取对称的空间构型。
电子对之间的夹角越大,排斥力越小。
2.价层电子对的确定方法中心原子上的孤电子对数= 。
(1)a表示。
对于主族元素,a=;对于阳离子,a=价电子数离子电荷数;对于阴离子,a=价电子数离子电荷数。
(2)x表示。
(3)b表示与中心原子结合的原子最多能接受的电子数,氢为,其他原子为。
3.VSEPR模型和分子的立体构型(1)由价层电子对的相互排斥,得到含有孤电子对的VSEPR模型,然后略去VSEPR模型中的中心原子上的,便可得到分子的立体构型。
(2)H2O分子和NH3分子的分子构型分子H2O NH3价层电子对数σ键电子对数中心原子孤电子对数VSEPR模型分子立体构型立体构型名称43考点一常见分子的立体构型1.三原子分子的立体构型:直线形,如CO2、CS2等;V形,如H2O、SO2等。
2.四原子分子的立体构型:平面三角形,如甲醛分子等;三角锥形如氨气分子等。
四原子分子立体构型的多样性四原子分子不一定都是平面三角形或三角锥形。
第二节分子的立体构型第二节分子的立体构型第1课时分子空间结构与价层电子对互斥理论在宏观世界中,花朵、蝴蝶、冰晶等诸多物质展现出规则与和谐的美。
科学巨匠爱因斯坦曾感叹:“在宇宙的秩序与和谐面前,人类不能不在内心里发出由衷的赞叹,激起无限的好奇。
”实际上,宏观的秩序与和谐源于微观的规则与对称。
通常,不同的分子具有不同的空间构型。
例如,甲烷分子是正四面体形的、氨分子是三角锥形的、苯是正六边形的。
那么,这些分子为什么具有不同的空间构型呢?一、形形色色的分子1.三原子分子的立体构型有__直线____形和__V____形两种。
如__平面三角______三角锥______正四面体____1.价层电子对互斥理论(VSEPR)。
对AB n型的分子或离子,中心原子A的价层电子对(包括成键__σ键电子对____和未成键的__孤电子对____)之间由于存在排斥力,将使分子的几何构型总是采取电子对__相互排斥____最小的那种构型,以使彼此之间__斥力____最小,分子或离子的体系能量__最低____,__最稳定____。
2.价层电子对的空间构型(即VSEPR模型):电子对数目:2 3 4VSEPR模型:__直线形______平面三角形______正四面体形____三、VSEPR模型应用——预测分子立体构型:1.中心原子不含孤电子对的分子。
中心原子不含孤电子对的分子,VSEPR模型与分子的立体构型一致。
__直线形______直线形______平面三角形______平面三角形______正四面体形______正四面体形____中心原子若有孤电子对,孤电子对也要占据中心原子的空间,并与成键电子对互相排斥。
则VSEPR模型与分子的立体构型不一致。
推测分子的立体模型必须略去VSEPR模型中的孤电子对。
__正四面体形______三角锥形______V形______平面三角形______V 形____(1)价电子对之间的夹角越小,排斥力越小。
《第二节 分子的立体构型》
1.能说明CH 4分子的5个原子不在同一平面而为正四面体构型的是( )
A .两个键之间夹角为109°28′
B .
C —H 键为极性共价键
C .4个C —H 键的键能、键长相同
D .碳的价层电子都形成共价键
2.(2010年扬州高二检测)下列说法中正确的是( )
A .NO 2、SO 2、BF 3、NCl 3分子中没有一个分子中原子的最外层
电子都满足了8电子稳定结构
B .P 4和CH 4都是正四面体分子且键角都为109°28′
C .NH 4+
的电子式为[H ··N ··H ··H]+,离子呈平面正方形结构 D. NH 3分子中有一对未成键的孤电子对,它对成键电子的排斥作
用较强
3.(2010年泉州高二检测)用价层电子对互斥理论预测H 2S 和BF 3的立体构型,两个结构都正确的是( )
A .直线形;三角锥形
B .V 形;三角锥形
C .直线形;平面三角形
D .V 形;平面三角形
4.(2010年普宁高二检测)有关乙炔分子中的化学键描述不.
正确的是( ) A .两个碳原子均采用sp 杂化方式 B .两个碳原子均采用sp 2杂化方式
C .每个碳原子都有两个未杂化的2p 轨道形成π键
D .两个碳原子形成两个π键
5.下列有关苯分子中的化学键描述正确的是( )
A .每个碳原子的sp 2杂化轨道中的一个形成大π键
B .每个碳原子的未参与杂化的2p 轨道形成大π键
C .每个碳原子的三个sp 2杂化轨道与其他两个碳原子和一个氢原
子形成三个σ键
D .每个碳原子的未参加杂化的2p 轨道与其他原子形成σ键
6.下列对二氧化硫与二氧化碳的说法中正确的是( )
A .都是直线形结构
B .中心原子都采取sp 杂化
C .硫原子和碳原子上都没有孤电子对
D .SO 2为V 形结构,CO 2为直线形结构
7.下列分子中的中心原子的杂化轨道类型相同的是( )
A .CO 2与SO 2
B .CH 4与NH 3
C .BeCl 2与BF 3
D .C 2H 4与C 2H 2
8.膦(PH 3)又称磷化氢,在常温下是一种无色、有大蒜臭味的有毒气体,电石气的杂质中常含有磷化氢。
它的分子构型是三角锥形。
则下列关于PH 3的叙述正确的是( )
A .PH 3分子中有未成键的孤电子对
B .PH 3是空间对称结构
C .PH 3是一种强氧化剂
D .PH 3分子中的P —H 键间夹角是90°
9.已知:①红磷在氯气中燃烧可以生成两种化合物——PCl 3和PCl 5,氮与氢也可形成两种化合物——NH 3和NH 5。
②PCl 5分子中,磷原子的1个3s 轨道、3个3p 轨道和1个 3d 轨道发生杂化形成5个sp 3d 杂化轨道,PCl 5分子呈三角双锥形。
(1)NH3、PCl3和PCl5分子中,所有原子的最外层电子数都是8个的是____________(填分子式),该分子的形状是______________。
(2)有同学认为,NH5与PCl5类似,氮原子的1个2s轨道、3个2p轨道和1个2d轨道可能发生sp3d杂化。
请你对该同学的观点进行评价_______________________________________________________
___________________________________________________________。
(3)经测定,NH5中存在离子键,氮原子最外层电子数是8,所有氢原子的最外层电子数都是2,则NH5的电子式是______________。
10.20世纪50年代科学家提出价层电子对互斥理论(简称VSEPR模型),用于预测简单分子立体构型。
其要点可以概括为:
Ⅰ.用AX n E m表示只含一个中心原子的分子组成,A为中心原子,X为与中心原子相结合的原子,E为中心原子最外层未参与成键的电子对(称为孤电子对),(n+m) 称为价层电子对数。
分子中的价层电子对总是互相排斥,均匀的分布在中心原子周围的空间;
Ⅱ.分子的立体构型是指分子中的原子在空间的排布,不包括中心原子未成键的孤电子对;
Ⅲ.分子中价层电子对之间的斥力主要顺序为:ⅰ.孤电子对之间的斥力>孤电子对与共用电子对之间的斥力>共用电子对之间的斥力;ⅱ.双键与双键之间的斥力>双键与单键之间的斥力>单键与单键之间的斥力;ⅲ.X原子得电子能力越弱,A—X形成的共用电子对之间的斥力越强;ⅳ.其他。
请仔细阅读上述材料,回答下列问题:
2
___________________________________________________________;
(3)H2O分子的立体构型为:____________,请你预测水分子中∠H—O—H 的大小范围并解释原因:________________________
___________________________________________________________;
(4)SO2Cl2和SO2F2都属于AX4E0型分子,S—O之间以双键结合,S—Cl、S—F 之间以单键结合。
请你预测SO2Cl2和SO2F2分子的立体构型:________,SO2Cl2分子中∠Cl—S—Cl________(填“<”、“>”或“=”)SO2F2分子中∠F—S—F。