第三章-化学动力学基础
- 格式:ppt
- 大小:1.30 MB
- 文档页数:85

材料综合复试大纲(复试分为三部分内容,考生可以选择其中任一部分作答。
)第一部分无机化学参考书目:《无机化学》,大连理工大学无机化学教研室编,高等教育出版社。
第三章化学动力学基础掌握活化分子和活化能的概念,并能用其说明浓度、温度、催化剂对化学反应速率的影响;掌握化学反应速率、反应速率方程、反应级数等概念;熟悉Arrhenius 方程。
第五章酸碱平衡掌握酸碱质子理论基本要点;掌握同离子效应和缓冲溶液的概念、一元强弱酸、Lewis酸碱的相关内容;掌握配位化合物的基本概念。
第六章沉淀溶解平衡掌握相关理论并解释沉淀析出的实验现象。
第七章氧化还原反应电化学基础掌握电极电势的基本概念及应用;熟悉氧化还原反应的基本概念。
第八章原子结构掌握核外电子排布的基本原理;掌握周期表中元素的分区、结构特征;熟悉原子半径、电离能、电子亲和能和电负性的变化规律。
第十章固体结构熟悉晶体的类型、特征和组成晶体的微粒间的作用力;能用相关知识点解释结构对物性的影响。
元素部分(s、p、d区元素),掌握性质递变规律。
第二部分物理学参考书目:《物理学》上、下册,东南大学等七所工科院校编,马文尉改编,高等教育出版社。
第五章静电场理解电场强度,掌握场强叠加原理,了解电荷连续分布的带电体的场强,理解电场线、电通量,掌握高斯定理,理解环路定理,了解电势,电势差及电势叠加原理。
第六章静电场中的导体与电介质了解静电场中加入导体和电解质后电场发生的变化,了解电容器的概念。
第七章恒定磁场理解磁感应强度,掌握毕奥-萨伐尔定律,理解磁感线、磁通量,掌握磁场中的高斯定理和安培环路定理;理解洛沦兹力,了解霍尔效应。
第八章电磁感应电磁场理解电动势的概念,掌握法拉第电磁感应定律,理解动生电动势、感生电动势的本质。
第十一章光学理解光的相干条件及获得相干光的基本原理和一般方法;了解光程概念以及光程差与相位差的关系,了解反射时产生半波损失的条件;了解杨氏双缝干涉的基本装置和实验规律;了解干涉条纹的分布特点及其应用;了解薄膜干涉原理在实际中的应用。



第三章 化学反应动力学的计算化学反应的速度各不相同,有的反应速度极快,只要几个毫微秒就达到平衡(接近扩散速度,如无机酸碱中和),有的反应速度极慢,几乎看不到变化(如自然界的某些变化)。
大部分有机化学反应可用常规方法测量,对某些快速反应则可用停留法、驰豫法等测量。
不论反应速度的快慢,动力学方程都是类似的。
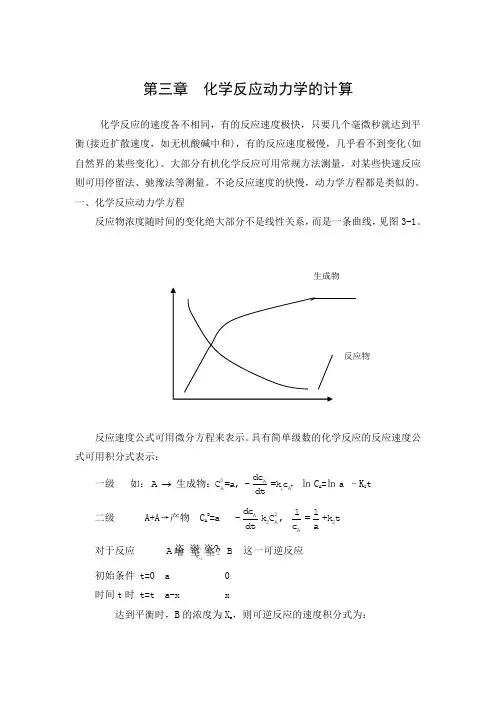
一、化学反应动力学方程反应物浓度随时间的变化绝大部分不是线性关系,而是一条曲线,见图3-1。
反应速度公式可用微分方程来表示。
具有简单级数的化学反应的反应速度公式可用积分式表示:一级 如:0AA1Adc A C =a, -=k c dt 生成物:,㏑C A =㏑a –K 1t 二级 A+A →产物 C A 0=a 2A 2A 2A d c 11-k C , =+k t d t c a对于反应 1-1k k A B 这一可逆反应初始条件 t=0 a 0 时间t 时 t=t a-x x达到平衡时,B 的浓度为X e ,则可逆反应的速度积分式为: 级数:1-1 1-10k A A e e 1A -1B k 0e 0C =a dc x xA B=-k C +k C : =kt dt a x -xC =0ln 1-21-10Ak0A e e e B 1A -1B C k e e 0CC =a dc x ax +x(a-x )A B+C C =0=-k C +k C C : =kt dt 2a-x a(x -x)C =0ln 二、常微分方程的解化学反应动力学方程是用微分方程表示的,对于简单的反应,可直接求得微分方程的解。
微分方程:()(1)(,,,......)......(1)n n y f x y y y -'=在区间a<x<b 的解,是指()y x ϕ=,这样一个函数,在所述区间内存在导数()(),(),......()n x x x ϕϕϕ'''。
且对于区间a<x<b 内的每一个x ,等式(1)都成立。

第三章 化学动力学基础Chapter 3 The Basis of Chemical Dynamics化学热力学成功预测了化学反应自发进行的方向,如: 2K(s) + 2H 2O(l)2K +(aq) + 2OH -(aq) + H 2(g) Δ r G m, 298K = -404.82 kJ·mol -1 222g g g 1H ()O ()H O()2+= Δ r G m, 298K = -228.59 kJ·mol -1 这两个反应的ΔG 298<0,所以此两个反应在298K 时向正反应方向进行有利,但它们的化学反应速率却相差十万八千里:钾在水中的反应十分迅速剧烈,以至于燃烧;而把H 2和O 2的混合物于常温、常压下放置若干年,也观测不出反应的进行。
前一类化学反应属于热力学控制的反应;后一类化学反应属于动力学控制的反应。
研究化学反应速率有着十分重要的实际意义。
若炸药爆炸的速率不快,水泥硬化的速率很慢,那么它们就不会有现在这样大的用途;相反,如果橡胶迅速老化变脆,钢铁很快被腐蚀,那么它们就没有了应用价值。
研究反应速率对生产和人类生活都是十分重要的。
在中学,我们已学过影响化学反应速率的因素: 1.The concentrations of the reactants :Steel wool burns with difficulty in air, which contains 20 percents O 2 , but burst into a brilliant white flame in pure oxygen. 2.The temperature at which the reaction occur :The rates of chemical reactions increase as temperature is increased. It’s for this reason that we refrigerate perishable food such as milk. 3.The presence of a catalyst :The rates of many reactions can be increased by adding a substance known as a catalyst. The physiology of most living species depends crucially on enzymes, protein molecules that act as catalysts, which increase the rates of selected biochemical reactions. 4.The surface area of solid or liquid reactants or catalysts :Reactions that involve solids often proceed faster as the surface area of the solid is increased. For example, a medicine in the form of a tablet will dissolve in the stomach and enter the bloodstream more slowly than the same medicine in the form of a fine powder.§3-1 化学反应速率 The Rates of Chemical Reactions一、化学反应速率表示法1.Definition :通常以单位时间内反应物浓度的减少或生成物浓度的增加来表示。




第三章化学动力学基础一判断题1.溶液中,反应物A 在t1时的浓度为c1,t2时的浓度为c2,则可以由(c1-c2 ) / (t1 - t2 ) 计算反应速率,当△t→ 0 时,则为平均速率。
......................................................................()2.反应速率系数k的量纲为1 。
..........................()3.反应2A + 2B → C,其速率方程式v = kc (A)[c (B)]2,则反应级数为3。
................()4.任何情况下,化学反应的反应速率在数值上等于反应速率系数。
..........()5.化学反应3A(aq) + B(aq) → 2C(aq) ,当其速率方程式中各物质浓度均为 1.0 mol·L-1时,其反应速率系数在数值上等于其反应速率。
......................................................................()6.反应速率系数k越大,反应速率必定越大。
......()7.对零级反应来说,反应速率与反应物浓度无关。
...........................................()8.所有反应的速率都随时间而改变。
........................()9.反应a A(aq) + b B(aq) → g G(aq) 的反应速率方程式为v = k [c(A)]a[ c(B)]b,则此反应一定是一步完成的简单反应。
........................()10.可根据反应速率系数的单位来确定反应级数。
若k的单位是mol1-n·L n-1·s-1,则反应级数为n。
...............................()11.反应物浓度增大,反应速率必定增大。
