一次性使用腹腔镜用穿刺器产品技术要求bh
- 格式:docx
- 大小:492.57 KB
- 文档页数:5
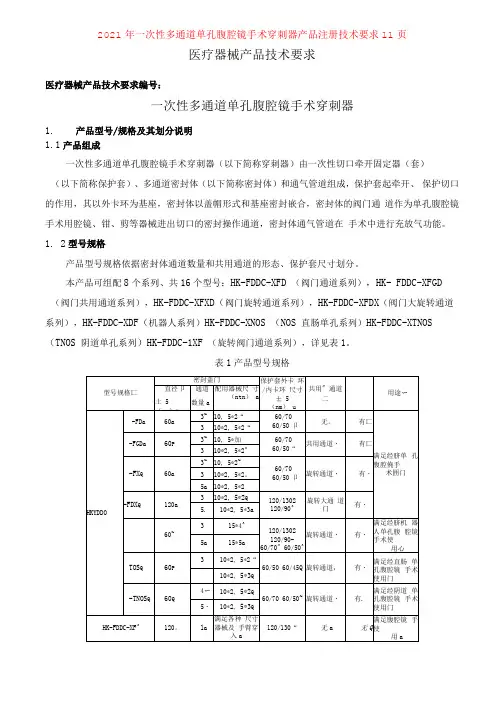
医疗器械产品技术要求医疗器械产品技术要求编号:一次性多通道单孔腹腔镜手术穿刺器1.产品型号/规格及其划分说明1.1产品组成一次性多通道单孔腹腔镜手术穿刺器(以下简称穿刺器)由一次性切口牵开固定器(套)(以下简称保护套)、多通道密封体(以下简称密封体)和通气管道组成,保护套起牵开、保护切口的作用,其以外卡环为基座,密封体以盖帽形式和基座密封嵌合,密封体的阀门通道作为单孔腹腔镜手术用腔镜、钳、剪等器械进出切口的密封操作通道,密封体通气管道在手术中进行充放气功能。
1. 2型号规格产品型号规格依据密封体通道数量和共用通道的形态、保护套尺寸划分。
本产品可组配8个系列、共16个型号:HK-FDDC-XFD (阀门通道系列),HK- FDDC-XFGD (阀门共用通道系列),HK-FDDC-XFXD(阀门旋转通道系列),HK-FDDC-XFDX(阀门大旋转通道系列),HK-FDDC-XDF(机器人系列)HK-FDDC-XNOS (NOS 直肠单孔系列)HK-FDDC-XTNOS (TNOS 阴道单孔系列)HK-FDDC-1XF (旋转阀门通道系列),详见表1。
表1产品型号规格注:配用器械尺寸:10号(大)阀门可进入直径12mm、10mm、5mm的器械,5号(小)阀门可进入直径5mm、3mm的器械。
另外,产品可根据临床要求,定制通道。
1.3产品结构1.3. 1 HK-FDDC-XFD型穿刺器(以三阀门为例)穿刺器中保护套由弹性外卡环、内卡环及可变高度的柔弹性管道构成,与三阀门通道密封体组配。
3俯视示意图1保护套1T内卡环1-2外卡环1-3管道2密封体2-1通道2-2阀门2-3外壳3通气管道图11.3.2HK-FDDC-XFGD型穿刺器(以四阀门为例)穿刺器中保护套由弹性外卡环、内卡环及管道(变高式或定高式)组成,与四阀门共用通道密封体组配。
俯视示意图1保护套1-1外卡环1-2管道1-3内卡环2密封体2-1阀门2-2通道2-3通气管道2-4 定位环2-5共用通道图21.3.3HK-FDDC-XFX型穿刺器(以四阀门为例)穿刺器中保护套由弹性外卡环、内卡环及管道(变高式管道)组成,与旋转通道密封体组配而成。


一次性使用腹部穿刺器穿刺力研究摘要:相对于开放性手术,腹腔镜手术由于其所具有的损伤性小、术后恢复快等优势被越来越多的应用到各种手术场景中。
在临床中,腹部穿刺器穿刺腹壁组织进入人体,发挥着为各类外科手术器械提供通道的桥梁作用。
现行行业标准《YY/T 1710-2020一次性使用腹部穿刺器》对一次性使用腹部穿刺器的穿刺性能作出了要求,但对于穿刺材料的选择尚不完善,给模拟检验及临床评价带来困难。
本文采行业标准YY/T 1710-2020一次性使用腹部穿刺器》穿刺性能试验方法所规定的猪腹部组织作为穿刺材料,针对不同肌肉层厚度猪腹部组织进行了穿刺力试验,结果表明随着肌肉层厚度的增大,穿刺力呈近似正比例增大趋势,不同肌肉层厚度的穿刺模拟物对实验结果有着较大影响。
实验结果为后后续标准的修订和完善以及企业产品技术要求参数的确定提供了依据。
关键词:一次性使用腹部穿刺器穿刺力穿刺材料一、引言腹腔镜手术是一种通过不同规格的穿刺器在手术部位创建操作通道,使用腔镜器械完成对病人病灶的诊断和治疗的手术方式。
相对于开腹手术,腹腔镜手术具有创伤小、出血少、术后恢复快等优势,在外科微创手术、妇科微创手术、胸外科等临床治疗中得到了广泛的应用。
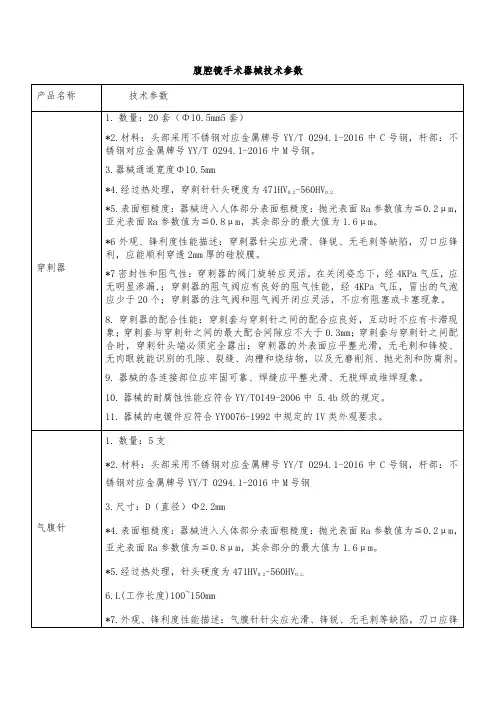
腹部穿刺器是腹腔镜中手术中的常用医疗器械,用于穿刺人体腹壁组织并维持气腹,从而为各种手术器械提供进出人体的通道。
腹部穿刺器由穿刺杆和穿刺套管两部分组成,穿刺杆头端分为带刀头与不带刀头,穿刺套管主体外壁上带有螺纹或横纹,起到辅助穿刺和固定作用。
图1 穿刺器穿刺腹部组织但是,在穿刺过程中,穿刺器穿刺力的大小对手术有着重要影响。
若穿刺力过小,则力度不易把控,使用过程中容易用力过猛而误伤患者腹腔脏器;反之若穿刺力过大,则不易穿透腹壁,穿刺器可用性较低。
因此,穿刺力大小的评价对于临床手术有着重要意义,而如何选择合适的穿刺材料使实验结果更好的贴近临床穿刺力又尤为重要。
现行行业标准《YY/T 1710-2020一次性使用腹部穿刺器》中规定采用带皮猪腹部组织作为实验材料,相对于《GB 15811-2016 一次性使用无菌注射针》及《YY 0043-2005 医用缝合针》标准中采用的硅胶、铝箔等模拟穿刺物,猪腹部组织作为一种生物性材料能更好的模拟穿刺器穿刺脂肪层和肌肉组织的过程,给评价穿刺器的临床穿刺力大小带来一定便利。


一次性使用腹腔镜用穿刺器适用范围:为内窥镜配套用手术器械,通过在腹壁穿刺并固定,供形成气腹注气通道和腹腔镜或其他手术器械的工作通道用。
1.1 名称及规格一次性使用腹腔镜用穿刺器由穿刺套管、穿刺针、接头组成。
1.2 材料一次性使用腹腔镜用穿刺器的穿刺针、穿刺导管和接头均采用聚碳酸酯(PC)材料制造,密封用胶垫等采用橡胶材料制成,气囊采用聚乙烯(PE)材料制成,注射器(不带针)采用聚丙烯(PP)、聚碳酸酯(PC)材料制成。
1.3 包装样式1.4 产品示意图图1穿刺套管图2接头图3穿刺针图4注射器(不带针)性能指标2.1 基本尺寸2.1.1 穿刺器2.1.2 注射器(不带针)2.1.3 固定架2.2 外观穿刺针表面应平整光滑、无毛刺和锋棱,无肉眼能识别的空隙、裂缝、沟槽和烧结物,以及无磨削剂、抛光剂和防腐剂。
穿刺套管表面应平整光滑、无毛刺和锋棱,无肉眼能识别的空隙、裂缝、沟槽和烧结物,以及无磨削剂、抛光剂和防腐剂。
接头表面应平整光滑、无毛刺和锋棱,无肉眼能识别的空隙、裂缝、沟槽和烧结物,以及无磨削剂、抛光剂和防腐剂。
注射器(不带针)不得有毛边、毛刺、塑流、缺损的缺陷;外套有足够的透明度,能清晰地看到基准线;内表面不得有明显可见的润滑剂汇集。
固定架应平整光滑、无毛刺和锋棱、无肉眼能识别的空隙、裂缝、沟槽和烧结物,以及无磨削剂、抛光剂和防腐剂。
2.3 灵活性2.3.1 一次性使用腹腔镜用穿刺器的注气阀开闭应灵活,不应有阻塞或卡塞现象。
2.3.2 注射器应有良好的滑动性能,其推、拉作用力应符合GB 15810-2001中5.10.1中要求。
2.4 配合性能2.4.1 穿刺套管与穿刺针之间的配合应良好,使用时不应有卡滞现象。
2.4.2 穿刺套管与穿刺针的最大配合间隙不大于0.3mm。
2.4.3 穿刺套管与穿刺针配合时,穿刺针头端必须完全露出。
2.4.4 固定架能很好地固定住穿刺套管、穿刺针、注射器。
2.4.5 注射器能与气囊注气阀很好的配合,无泄漏情况。
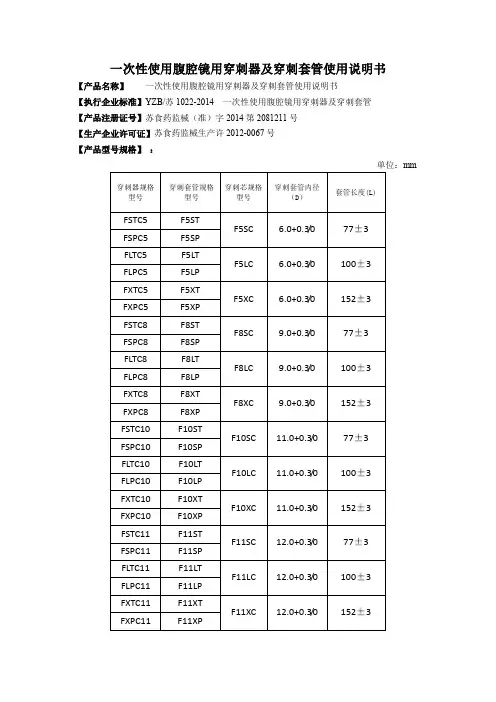
一次性使用腹腔镜用穿刺器及穿刺套管使用说明书【产品名称】一次性使用腹腔镜用穿刺器及穿刺套管使用说明书【执行企业标准】YZB/苏1022-2014 一次性使用腹腔镜用穿刺器及穿刺套管【产品注册证号】苏食药监械(准)字2014第2081211号【生产企业许可证】苏食药监械生产许2012-0067号【产品型号规格】:单位:mm穿刺器规格型号穿刺套管规格型号穿刺芯规格型号穿刺套管内径(D)套管长度(L)FSTC5 F5STF5SC 6.0+0.3/0 77±3 FSPC5 F5SPFLTC5 F5LTF5LC 6.0+0.3/0 100±3 FLPC5 F5LPFXTC5 F5XTF5XC 6.0+0.3/0 152±3 FXPC5 F5XPFSTC8 F8STF8SC 9.0+0.3/0 77±3 FSPC8 F8SPFLTC8 F8LTF8LC 9.0+0.3/0 100±3 FLPC8 F8LPFXTC8 F8XTF8XC 9.0+0.3/0 152±3 FXPC8 F8XPFSTC10 F10STF10SC 11.0+0.3/0 77±3 FSPC10 F10SPFLTC10 F10LTF10LC 11.0+0.3/0 100±3 FLPC10 F10LPFXTC10 F10XTF10XC 11.0+0.3/0 152±3 FXPC10 F10XPFSTC11 F11STF11SC 12.0+0.3/0 77±3 FSPC11 F11SPFLTC11 F11LTF11LC 12.0+0.3/0 100±3 FLPC11 F11LPFXTC11 F11XTF11XC 12.0+0.3/0 152±3 FXPC11 F11XPFSTC12 F12STF12SC 13.0+0.3/0 77±5 FSPC12 F12SPFLTC12 F12LTF12LC 13.0+0.3/0 100±3 FLPC12 F12LPFXTC12 F12XTF12XC 13.0+0.3/0 152±3 FXPC12 F12XPFSTC15 F15STF15SC 15.8+0.3/0 77±3 FSPC15 F15SPFLTC15 F15LTF15LC 15.8+0.3/0 100±3 FLPC15 F15LPFXTC15 F15XTF15XC 15.8+0.3/0 152±3 FXPC15 F15XPBSTC5 B5STB5SC 6.0+0.3/0 77±3 BSPC5 B5SPBLTC5 B5LTB5LC 6.0+0.3/0 100±3 BLPC5 B5LPBXTC5 B5XTB5XC 6.0+0.3/0 152±3 BXPC5 B5XPBSTC8 B8STB8SC 9.0+0.3/0 77±3 BSPC8 B8SPBLTC8 B8LTB8LC 9.0+0.3/0 100±3 BLPC8 B8LPBXTC8 B8XTB8XC 9.0+0.3/0 152±3 BXPC8 B8XPBSTC10 B10STB10SC 11.0+0.3/0 77±3 BSPC10 B10SPBLTC10 B10LTB10LC 11.0+0.3/0 100±3 BLPC10 B10LPBXTC10 B10XTB10XC 11.0+0.3/0 152±3 BXPC10 B10XPBSTC11 B11STB11SC 12.0+0.3/0 77±3 BSPC11 B11SPBLTC11 B11LT B11LC 12.0+0.3/0 100±3BLPC11 B11LPBXTC11 B11XTB11XC 12.0+0.3/0 152±3BXPC11 B11XPBSTC12 B12STB12SC 13.0+0.3/0 77±3BSPC12 B12SPBLTC12 B12LTB12LC 13.0+0.3/0 100±3BLPC12 B12LPBXTC12 B12XTB12XC 13.0+0.3/0 152±3BXPC12 B12XPBSTC15 B15STB15SC 15.8+0.3/0 77±3BSPC15 B15SPBLTC15 B15LTB15LC 15.8+0.3/0 100±3BLPC15 B15LPBXTC15 B15XTB15XC 15.8+0.3/0 152±3BXPC15 B15XP【主要技术指标】材料:穿刺芯、穿刺套管、穿刺芯固定座:ABS-1、MN、095-30-16-15穿刺芯管:12Cr18Ni9不锈钢性能:穿刺器的基本参数包括穿刺器的注气阀、密封帽应有良好的密封性,经4kPa 气压,应无泄漏及穿刺芯管表面粗糙度Ra应不大于0.4μm等。

YY ICS 11.040.30 C 31 中华人民共和国医药行业标准 YY 0672.1—2008 内镜器械 第1部分:腹腔镜用穿刺器 Endoscopic instruments—Part 1:Trocars for laparoscope use 2008-10-17发布 2010-06-01实施 国家食品药品监督管理局 发布.▲‘--JL刖 吾YY 0672{内镜器械》,由下列部分组成:——第1部分:腹腔镜用穿刺器;——第2部分:腹腔镜用钳;——第3部分:腹腔镜用剪。
本部分为YY 0672的第1部分。
本部分参考DIN 58298—19:2002{医疗器械的材料、精加工和测试第19篇:套管针》。
本部分由全国外科器械标准化技术委员会提出并归口。
本部分主要起草单位:上海金宝隆光纤电子技术研究所有限公司。
本部分主要起草人:方志能、陆静娣、郑会乐。
内镜器械 第1部分:腹腔镜用穿刺器1 范围 YY 0672的本部分规定了内镜器械——腹腔镜用穿刺器产品的分类与命名、要求、试验方法、检验规则、标志、使用说明书、包装、运输、贮存等要求。
本部分适用于腹腔镜用穿刺器(以下简称穿刺器),该产品与内窥镜配套使用,在内窥镜手术中对人体组织进行穿刺并建立腹腔通道用。
2规范性引用文件 下列文件中的条款通过YY 0672的本部分的引用而成为本部分的条款。
凡是注日期的引用文件,其随后所有的修改单(不包括勘误的内容)或修订版均不适用于本部分,然而,鼓励根据本部分达成协议的各方研究是否可使用这些文件的最新版本。
凡是不注日期的引用文件,其最新版本适用于本部分。
GB/T 230.1—2004金属洛氏硬度试验 第1部分:试验方法(A、B、C、D、E、F、G、H、K、N、T标尺)(ISO 6508.1:1999,MOD) GB/T 1220~2007不锈钢棒 GB/T 2828.1—2003计数抽样检验程序 第1部分:按接收质量限(AQL)检索的逐批检验抽样计划(ISO 2859.1:1999,IDT) GB/T 2829—2002周期检验计数抽样程序及表(适用于对过程稳定性的检验) GB/T 4340.1—1999金属维氏硬度试验第1部分:试验方法 GB/T 16886.5—2003医疗器械生物学评价第5部分:体外细胞毒性试验(ISO 10993~5:1999,IDT) GB/T 16886.10一2005 医疗器械生物学评价 第10部分:刺激与迟发型超敏反应试验(ISO 10993—10:2002,IDT) YY/T 0149—2006不锈钢医用器械耐腐蚀性能试验方法(ISO 13402:1995,MOD) YY/T 0171—2008手术器械包装、标志和使用说明书 YY/T 1052—2004手术器械标志3分类与命名3.1 穿刺器的型式和基本尺寸 穿刺器的型式和基本尺寸应符合图1和表1的规定。

医疗器械产品技术要求编号:一次性多通道单孔腹腔镜穿刺器1. 产品型号/规格及其划分说明1.1 型号规格型号:KL999,规格:32A、42A、43A、32B、42B、43B;型号:KL888,规格:32A、42A、43A、32B、42B、43B。
1.2 组成成分本产品由一次性切口保护套、多通道密封体和通气管道组成。
1.3 适用范围适用于腹腔镜手术时内窥镜和器械进出体内的通道。
2.性能指标2.1基本尺寸一次性多通道单孔腹腔镜穿刺器的基本尺寸应符合表 2、表 3 的规定。
2.2外观一次性多通道单孔腹腔镜穿刺器应结构完好,无裂纹、无污物、无杂质、无明显缺陷。
2.3物理性能2.3.1一次性多通道单孔腹腔镜穿刺器的充气组件开闭应灵活,不应有阻塞或卡塞现象。
2.3.2一次性多通道单孔腹腔镜穿刺器的主体连接座与主体底座的配合性应良好,并可透过扣件锁定(UNS-D 适用)。
多通道单孔腹腔镜穿刺器密封体和切口保护套可装可卸。
2.3.3多通道单孔腹腔镜穿刺器密封体和切口保护套装配后可具备一定密封性。
2.3.4切口保护套管道可承受 50N 拉力。
2.3.5切口保护套内外卡环皆具有弹性变形和弹性恢复功能。
2.3.6变高切口保护套外卡环可径向用手翻卷调节管道高度。
2.3.7套管可插入、抽出相应规格尺寸的手术器械,插入、推拉、抽出后仍可具备一定密封性。
2.4无菌环氧乙烷灭菌后应无菌。
2.5环氧乙烷残留量环氧乙烷残留量应不大于 10μg/g。
2.6酸碱度检验液与同批空白对照液作对照,pH 值之差应≤1.5。
2.7重金属溶出液重金属含量不应超过 1μg/mL。

国家药品监督管理局通告2019年第30号——关于发布国家医疗器械监督抽检结果的通告(第4号)文章属性•【制定机关】国家药品监督管理局•【公布日期】2019.05.31•【文号】国家药品监督管理局通告2019年第30号•【施行日期】2019.05.31•【效力等级】部门规范性文件•【时效性】现行有效•【主题分类】药政管理正文国家药品监督管理局通告2019年第30号关于发布国家医疗器械监督抽检结果的通告(第4号)为加强医疗器械质量监督管理,保障医疗器械产品使用安全有效,国家药品监督管理局组织对丙氨酸氨基转移酶测定试剂盒、腹部穿刺器、数控气压止血仪(带)等15个品种共877批(台)的产品进行了质量监督抽检,其中59批(台)产品不符合标准规定。
具体情况通告如下:一、被抽检项目不符合标准规定的医疗器械产品,涉及44家企业12个品种50批(台)。
具体为:(一)丙氨酸氨基转移酶测定试剂盒2家企业2批次产品。
保定长城临床试剂有限公司生产的1批次丙氨酸氨基转移酶测定试剂盒(速率法),准确度、线性不符合标准规定;洛阳恒恩生物科技有限公司生产的1批次丙氨酸氨基转移酶测定试剂盒(连续监测法),重复性不符合标准规定。
(二)腹部穿刺器12家企业15批次产品。
江苏凯尔特医疗科技有限公司生产的1批次一次性使用穿刺器,配合性能、密封性和阻气性不符合标准规定;常州健瑞宝医疗器械有限公司、江苏特普优微创医疗科技有限公司、常州海尔斯医疗器械科技有限公司生产的各1批次一次性使用腹腔镜用穿刺器,杭州桐庐医达器械设备有限公司生产的1批次腹部穿刺器、常州市微凯医疗科技有限公司和江苏明朗医疗器械科技有限公司生产的各1批次一次性使用腹腔镜穿刺器,常州健瑞宝医疗器械有限公司生产的1批次一次性使用腹壁穿刺器、泰州莱赛医疗器械有限公司生产的1批次一次性套管穿刺器,配合性能不符合标准规定;无锡市神康医疗器械设备有限公司、无锡市瑞源普斯医疗器械有限公司生产的各2批次一次性使用穿刺器,外观、配合性能、密封性和阻气性不符合标准规定;欣瑞德(江苏)医疗科技有限公司生产的1批次一次性使用穿刺器、常州杰瑞尔医疗器械有限公司生产的1批次一次性使用腹腔镜穿刺器,密封性和阻气性不符合标准规定。

一次性使用腹部穿刺器1 范围本标准规定了一次性使用腹部穿刺器的结构、材料、要求、试验方法、型式检验、标签、说明书和包装。
本标准适用于腹腔镜手术时穿刺人体腹壁组织建立人工气腹、操作手术器械通道的一次性使用腹部穿刺器(以下简称穿刺器)。
2 规范性引用文件下列文件对于本文件的应用是必不可少的。
凡是注日期的引用文件,仅所注日期的版本适用于本文件。
凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
GB/T 1220 不锈钢棒GB/T 1962.2注射器、注射针及其他医疗器械 6%(鲁尔)圆锥接头第2 部分:锁定接头GB/T 3280-2015 不锈钢冷轧钢板和钢带GB/T 12672 丙烯腈-丁二烯-苯乙烯(ABS)树脂GB/T 14233.1-2008 医用输液、输血、注射器具检验方法第1部分:化学分析方法GB/T 16886(所有部分)医疗器械生物学评价GB/T 6682-2008 分析实验室用水规格和试验方法GB/T 4340.1 金属材料维氏硬度试验第1部分:试验方法YY/T 0149-2006 不锈钢医用器械耐腐蚀性能试验方法YY/T 0466.1 医疗器械用于医疗器械标签、标记和提供信息的符号第1部分:通用要求YY/T 0806 医用输液、输血、注射及其他医疗器械用聚碳酸酯专用料中华人民共和国药典(2015年版)3 结构和材料3.1结构和标识3.1.1穿刺器主要由穿刺套和穿刺杆组成。
穿刺套的主要部件有套管、注气阀、鞘帽(含密封件)和阻气阀,套管表面可有螺纹;穿刺杆头端可带切割皮肤/不切割皮肤穿刺刀。
穿刺器结构型式、规格和基本尺寸见图1和表1。
2 说明:1——(穿刺套)套管;2——(穿刺套)注气阀;3——(穿刺套)套管座;4——(穿刺套)阻气阀5——(穿刺套)鞘帽(含密封件);6——穿刺杆;7——穿刺杆头端(可带穿刺刀);注:图示的穿刺器结构,非唯一型式。
图1穿刺器结构示意图表1 穿刺器的规格和基本尺寸单位为毫米规格穿刺套管内径φ穿刺套管工作长度L标称值极限偏差标称值极限偏差代号<5 +0.1550≤L≤200 ±2≥5 +0.33.1.2穿刺器的标识至少应包含下列要素,标识如下:□×□-□穿刺套管内径标称值穿刺套管工作长度标称值穿刺器规格代号标记示例:规格代号为12、穿刺套管内径12.5mm、穿刺套管工作长度为100 mm的穿刺器,标识为:12×100-12.5。
一次性使用腹腔镜用穿刺器适用范围:用于供腹腔镜检查和手术过程中,对人体腹壁组织穿刺,建立腹腔手术的工作通道。
1.1规格型号一次性使用腹腔镜用穿刺器的规格型号按穿刺套管大小和穿刺锥的结构形式分为A型、B型、C型、D型四种类型,如表1所示;按包装方式分为单支装和套装。
表1 一次性使用腹腔镜用穿刺器的规格型号单位:mm1.2规格型号划分说明1.3产品组成1.3.1产品的结构组成一次性使用腹腔镜用穿刺器由穿刺锥、穿刺套管、注气阀、阻气阀、密封帽、密封圈等组成。
选配件为转换器。
产品的结构示意图如图1所示。
图1 一次性使用腹腔镜用穿刺器结构示意图1.穿刺锥2.穿刺套管3.注气阀4.阻气阀5.密封帽6.密封圈7.转换器1.3.2产品的主要零件材料组成本产品一次性使用腹腔镜用穿刺器的主要零件材料组成如下表2所示:表2 一次性使用腹腔镜用穿刺器的主要零件材料表2.1 尺寸产品的尺寸应符合表1中的规定。
2.2 外观产品表面应平整光滑、无毛刺、无肉眼就能识别的孔隙、裂缝、沟槽和烧结物。
2.3 灵活性穿刺器的注气阀和阻气阀开闭应灵活,不应有阻塞或卡塞现象。
2.4 配合性能2.4.1 穿刺套管与穿刺锥之间的配合应良好,互动时不应有卡滞现象。
2.4.2 穿刺套管与穿刺锥的最大配合间隙应不大于0.3mm。
2.4.3 穿刺套管与穿刺锥配合时,穿刺锥头端必须完全露出。
2.5 密封性和阻气性2.5.1 穿刺器的注气阀、密封帽应有良好的密封性,经4kPa气压,应无泄漏。
2.5.2 穿刺器的阻气阀应有良好阻气性能,经4kPa气压,冒出的气泡应小于20个。
2.5.3 转换器应有良好的密封性,经4kPa气压,应无泄漏。
2.6 环氧乙烷残留量产品采用环氧乙烷灭菌,出厂前其环氧乙烷残留量应不大于10µg/g。
2.7 无菌产品应无菌。
2.8 酸碱度产品检验液与空白液的PH值之差应不超过1.5。
2.9 重金属总含量产品检验液的重金属总含量不得超过10μg/ml。
一次性使用腹腔镜用穿刺器
适用范围:用于供腹腔镜检查和手术过程中,对人体腹壁组织穿刺,建立腹腔手术的工作通道。
1.1规格型号
一次性使用腹腔镜用穿刺器的规格型号按穿刺套管大小和穿刺锥的结构形式分为A型、B型、C型、D型四种类型,如表1所示;按包装方式分为单支装和套装。
表1 一次性使用腹腔镜用穿刺器的规格型号单位:mm
1.2规格型号划分说明
1.3产品组成
1.3.1产品的结构组成
一次性使用腹腔镜用穿刺器由穿刺锥、穿刺套管、注气阀、阻气阀、密封帽、密封圈等组成。
选配件为转换器。
产品的结构示意图如图1所示。
图1 一次性使用腹腔镜用穿刺器结构示意图
1.穿刺锥
2.穿刺套管
3.注气阀
4.阻气阀
5.密封帽
6.密封圈
7.转换器
1.3.2产品的主要零件材料组成
本产品一次性使用腹腔镜用穿刺器的主要零件材料组成如下表2所示:表2 一次性使用腹腔镜用穿刺器的主要零件材料表
2.1 尺寸
产品的尺寸应符合表1中的规定。
2.2 外观
产品表面应平整光滑、无毛刺、无肉眼就能识别的孔隙、裂缝、沟槽和烧结物。
2.3 灵活性
穿刺器的注气阀和阻气阀开闭应灵活,不应有阻塞或卡塞现象。
2.4 配合性能
2.4.1 穿刺套管与穿刺锥之间的配合应良好,互动时不应有卡滞现象。
2.4.2 穿刺套管与穿刺锥的最大配合间隙应不大于0.3mm。
2.4.3 穿刺套管与穿刺锥配合时,穿刺锥头端必须完全露出。
2.5 密封性和阻气性
2.5.1 穿刺器的注气阀、密封帽应有良好的密封性,经4kPa气压,应无泄漏。
2.5.2 穿刺器的阻气阀应有良好阻气性能,经4kPa气压,冒出的气泡应小于20个。
2.5.3 转换器应有良好的密封性,经4kPa气压,应无泄漏。
2.6 环氧乙烷残留量
产品采用环氧乙烷灭菌,出厂前其环氧乙烷残留量应不大于10µg/g。
2.7 无菌
产品应无菌。
2.8 酸碱度
产品检验液与空白液的PH值之差应不超过1.5。
2.9 重金属总含量
产品检验液的重金属总含量不得超过10μg/ml。
2.10 蒸发残渣
每50ml产品检验液的蒸发残渣应不大于5mg。
2.11 还原物质(易氧化物)
产品检验液与空白液消耗高锰酸钾溶液[c(KMnO4)=0.002mol/L]的体积之差应不超过3.0ml。
2.12 紫外吸光度
产品检验液在220nm~340nm波长范围吸收值不超过0.4。