物理常数测定-有机分析
- 格式:ppt
- 大小:1.44 MB
- 文档页数:64


可编辑修改精选全文完整版(一)化验员入职考试-(及答案第一篇:(一)化验员入职考试-(及答案化验员考试试题(入职考试)姓名:所学专业:分数:一、选择题(每题4分,共计80分)1、34×10有效数字是(A)位。
A、2B、3C、4D、52、()pH=5.26中的有效数字是(B)位。
A、0B、2C、3D、43、比较两组测定结果的精密度(B)。
甲组:0.19%,0.19%,0.20%,0.21%,0.21%乙组:0.18%,0.20%,0.20%,0.21%,0.22%A、甲、乙两组相同B、甲组比乙组高C、乙组比甲组高D、无法判别4、分析某药物的纯度时,称取样品0.3580g,下列分析结果记录正确的为(C)A、36%B、36.4%C、36.41%D、36.412%5、实验测得右灰石中CaO含量为27.50%,若真实值为27.30%,则(27.50%-27.30%)/27.30%=0.73%为(B)A、绝对误差B、相对误差C、绝对偏差D、标准偏差6、酸碱滴定法进行滴定,消耗溶液体积结果记录应保留(A)A、小数点后2位B、小数点后4位C、二位有效数字D、四位有效数字7、用称量绝对误差为0.1mg的天平称出的50mg(以克为单位表示的质量),正确表示结果为(C)A、0.5000B、0.500C、0.0500D、0.05008、下列数据中具有三位有效数字的有(A)A、0.350B、1.412×103C、0.1020D、PKa=4.74 9、80、下列气体中,既有毒性又具可燃性的是(C)AO2BN2CCODCO210、在不加样品的情况下,用测定样品同样的方法、步骤,对空白样品进行定量分析,称之为(B)A、对照试验B、空白试验C、平行试验D、预试验11、对同一样品分析,采取一种相同的分析方法,每次测得的结果依次为31.27%、31.26%、31.28%,其-1-315、干燥器中的变色硅胶有效时的颜色是(A)A、蓝色B、红色C、黄色D、绿色16、直接法配制标准溶液必须使用(A)A、基准试剂B、化学纯试剂C、分析纯试剂D、优级纯试剂17、下列氧化物有剧毒的是(B)A、Al2OB、As2OC、SiOD、ZnO18、下列仪器中可在沸水浴中加热的有(D)A、容量瓶B、量筒C、比色管D、三角烧瓶19、下面不宜加热的仪器是(D)。

第七章有机化合物的波谱分析(一)概述研究或鉴圧一个有机化合物的结构,需对该化合物进行结构表征。
其基本程序如下: 分离提纯一物理常数测左一元素分析一确立分子式一确泄其可能的构适式(结构表 征(参见 P11-12)(1)结构表征的方法传统方法:(化学法)① 元素左性.泄量分析及相对分子质量测泄 —— 分子式:② 官能团试验及衍生物制备——分子中所含官能团及部分结构片断: ③ 将部分结构片断拼凑 —— 完整结构; ④ 查阅文献,对照标准样,验证分析结果。
特点:需要较多试样(半微量分析,用样虽为10-100mg ),大虽:的时间(吗啡碱,1805- 1952年).熟练的实验技巧,高超的智慧和坚韧不拔的精神。
缺点:①分子有时重排,导致错误结论;② P 及一C=C 一的构型确定困难。
波谱法:① 质谱(最好用元素分析仪验证)——分子式:② 各种谱图(UV 、IR 、NMR. MS ) —— 官能团及部分结构片断; ③ 拼凑——完整结构; ④ 标准谱图——确认。
特点:样品用量少(v30mg ),不损坏样品(质谱除外),分析速度快,对'C 及一C=C 一的 构型确左比较方便。
光谱法已成为有机结构分析的常规方法。
但是化学方法仍不可少,它与光谱法相辅相成, 相互补充,互为佐证。
(2)波谱过程分子运动:平动、振动、转动、核外电子运动等9量子化的(能量变化秘续)A 每个分子中只能存在一定数量的转? 动.振动、电子跃迁能级波谱过程可表示为:有机分子+电磁波选择性吸收 仪器记录用电磁波照射有机分子时, 分子便会吸收那些与分子内 的能级差相当的电磁波,引 起分子振动、转动或电子运 动能级跃迁,即分子可选择 性地吸收电磁波使分子内能 提高用仪器记录分子对不 同波长的电磁波的吸收情 况,就可得到光谱。
不饱和度亦称为分子中的环加双键数、缺氢指数、双键等价值等。
其定义为: 当一个化合物衍变为相应的绘后,与其同碳的饱和开链桂比较,每缺少2个氢为 1个不饱和度。

物理常数测定法、滴定分析法(一)一、最佳选择题1. 供试品在毛细管内开始局部液化出现明显液滴时的温度为A.全熔B.终熔C.初熔D.熔点E.熔融答案:C[解答] 本题考查的是熔点的定义。
熔点是指物质按照规定的方法测定,由固体熔化成液体的温度、熔融同时分解的温度或在熔化时自初熔至全熔的一段温度。
“初熔”系指供试品在毛细管内开始局部液化出现明显液滴时的温度:“全熔”系指供试品全部液化时的温度。
“熔融同时分解”是指样品在一定温度下熔融同时分解产生气泡、变色或浑浊等现象。
建议考生掌握熔点的定义。
故答案为C。
2. 旋光法测定的药物应具有A.不对称碳原子B.共轭体系C.立体结构D.氢键E.苯环结构答案:A[解答] 本题考查的是旋光法的应用。
平面偏振光通过某些光学活性物质的液体或溶液时,其振动平面向左或向右旋转的现象称为旋光现象,旋光法利用的是旋光现象,所以药物应有不对称碳原子。
建议考生熟悉旋光法的适应对象。
故答案为A。
3. 除另有规定外,比旋度测定的温度为D.30℃E.35℃答案:B[解答] 本题考查的是比旋度测定方法。
平面偏振光透过长1dm且每1ml含旋光物质1g的溶液,在一定的波长和温度下测得的旋光度称为比旋度。
《中国药典》规定温度t为20℃、用钠光D线(589.3nm)作光源用旋光计测定。
建议考生熟悉比旋度的测定条件。
故答案为B。
4. 用酸度计测定溶液的pH,测定前应用pH值与供试液较接近的一种标准缓冲液,调节仪器旋钮,使仪器pH示值与标准缓冲液的pH一致,此操作步骤为A.调节零点B.校正温度C.调节斜率D.平衡E.定位答案:E[解答] 本题考查的是pH值测定方法。
pH值测定多用“两次测量法”,即先用标准缓冲溶液对仪器进行校正符合要求后,再进行溶液pH值的测定。
仪器校正时应选择两种pH值相差3个单位的标准缓冲溶液,使供试品溶液的pH值处于二者之间;用与供试液pH值接近的第一种标准缓冲液定位后,再用第二种标准缓冲液进行测定以核对仪器示值,误差应小于±0.02pH单位。

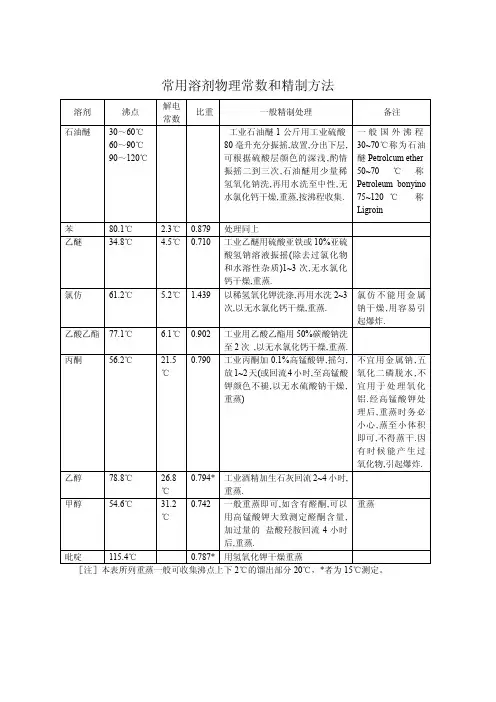
有机化学实验基本技能问题及简答1、如何查阅有机化合物的物理常数?答:在进行或设计一个有机合成实验之前,必须首先弄清楚反应物料和生成物的物理常数,这样在反应、分离纯化时,才能设计出合理的工艺路线,操作时才能做到心中有数。
通常查找物理常数有四个途径:(1)在教材书中,每一章的物理性质都列出了一些常见化合物的物理常数。
另外,在多数实验教材书的附表中,也列有一些常见溶剂和物料物理常数。
(2)在图书馆中,查阅相关的手册。
主要查阅有机化合物手册、有机合成手册、化学手册、物理化学手册等。
(3)在网上查找,有些网站和化学品电子手册专门提供物理常数。
(4)在实验室的试剂瓶上,一般都列有主要物理性质的常数。
2、简述使用小台秤的注意事项?答:小台秤是有机合成实验中,常用于称量物料质量的仪器。
在称量前,应先观察两臂是否平衡,指针是否在标尺中央。
如果不在中央,可调节两端的平衡螺丝,使指针指向标尺中央,两臂即达到平衡。
称量时,将物料放在左盘上,右盘上加砝码。
为了保持台秤清洁,所称物料不能直接放在托盘上,应放在清洁、干燥的称量瓶、表面皿、硫酸纸或烧杯中进行称量。
加砝码时,应用镊子(不能直接用手)先大后小的加。
称量后,应将砝码放回盒中,将游码复原至刻度0。
3、有机化学反应加热有哪些方法?答:有机反应最常用的是通过石棉网上加热,不能直接用火加热。
否则仪器容易受热不均匀而破裂。
如果要控制加热的温度,增大受热面积,使反应物质受热均匀,避免局部过热而分解,石棉网加热仍很不均匀,故在减压蒸馏、或回流低沸点易燃物等操作中不能适用,最好用适当的热浴加热。
(1)水浴:适用于加热温度不超过100℃的反应。
如果加热温度在90℃以下,可浸在水中加热。
如果加热温度在90-100℃时,可用沸水浴或蒸汽浴加热。
(2)油浴:加热温度在100℃-250℃时,可用油浴。
油浴的优点是可通过控温仪使温度控制在一定范围内,容器内的反应物料受热均匀。
容器内的反应温度一般要比油浴温度低20℃左右。

《有机分析》习题2.物理常数的测定1、用毛细管法测熔点时应注意哪些事项?固体试样的熔点敏锐是否能确证它是单纯化合物?两种化合物的熔点不下降是否能证明它们为同一化合物?为什么?2 、测定熔沸点时为什么要进行温度计外露段的校正?在什么情况下,可以不进行此项校正?3 、液体试样的沸程很窄是否能确证它是纯化合物?为什么?4 、测定沸点和沸程时为何要进行气压的校正?如何校正?5 、液体密度的测定方法有几种?简述各种测定方法的原理。
6 、简述阿贝折光仪测定液体折光率的原理?折光仪用标准液或标准玻璃校正的目的是什么?7 、作为液体纯度的标志,为什么折光率比沸点更为可靠?8 、旋光性物质溶液的旋光度大小与哪些因素有关?9 、举例说明旋光性物质溶液的比旋光度与溶液的浓度、PH 值、温度和所用溶剂有关?10 、圆盘旋光仪中半荫片能提高测量的准确度,为什么?11 、如何判断被测物是左旋还是右旋?12 、测定硫脲熔点得如下数据:初熔全熔主温度计读数172.0 ℃174.0 ℃辅助温度计读数38 ℃40 ℃温度计刚露出塞外刻度值149 ℃求校正后的熔点 .13 .已知四氯化碳试剂( 1 )今用韦氏天平测某试样密度,得以下数据:骑码 1 2 3 4水中位置10 0 0 6试样中位置 5 9 8 0( 2 )测定沸程得如下数据;初步判断试样的级别?14、已知分析纯:邻二甲苯ρ=0.8590 ~0.8820;对二甲苯ρ=0.8590~0.8630;氯苯ρ=1.1050~1.1090,用韦氏天平测定两试样,得如下数据:(1)初步鉴定样1是邻二甲苯还是对二甲苯?(2)初步鉴定样2是否为分析纯氯苯?15、根据以下条件鉴定未知物是否为果糖?称取 2.50g 试样溶于50.0mL水中;用1dm旋光管于20℃时,测得旋光度为-4.65 °。
16 、已知葡萄糖的纯度为95.0% ,如果此试样可以使偏振光振动面偏转+11.5 °,则应称取多少克葡萄糖。



有机化学专业博士研究生课程教学大纲课程名称:有机分析课程编号:0703031F05学分:3总学时数:60开课学期:2考核方式:开卷课程说明:通过本课程的学习掌握有机化合物系统鉴定,理解有机化合物物理常数的测定、元素定性、定量分析、官能团的检验等知识,学习和掌握波谱分析方法的基本理论、比较系统的获得紫外光谱、红外光谱、质谱、核磁共振光谱的基本理论、基本知识及利用现代光谱技术进行有机化合物结构的鉴定。
培养学生应用各类分析方法解决有机化合物进行物质成分和结构分析的能力。
掌握有机混合物的分离方法及分离方法的选择和拟定,能运用恰当的方法对混合物进行分离。
教学内容、要求及学时分配:第一章绪论 (6 学时)1.1有机分析的发展特点1.2有机分析的一般步骤1.3物理常数的测定1.4有机化合物的初步审察1.5有机化合物的灼烧试验1.6元素定性分析本章要求:了解有机分析的发展,掌握有机分析的一般步骤;掌握有机化合物的熔点、沸点、密度、折射率、比旋光度等物理常数的测定;能够进行有机化合物分析的初步试验。
第二章紫外光谱 (6 学时)2.1紫外光谱的基本原理2.2紫外光谱仪和实验中的一些问题2.3各类化合物的紫外光谱2.4紫外波谱的经验规律2.5紫外光谱的应用本章要求:掌握紫外光谱产生原理测定方法和影响因素;掌握含共轭体系和芳香族化合物的紫外光谱吸收规律;掌握共轭体系极大吸收波长的计算;掌握紫外光谱在有机化合物结构测定中的应用及定性、定量分析中的应用。
第三章红外光谱和拉曼光谱 (8 学时)3.1红外光谱的发展、特点及红外光谱图3.2基本原理3.3红外分光光度计3.4试样的调制3.5有机化合物基团的特征吸收3.6影响基团吸收频率的因素3.7红外光谱图的解析3.8拉曼光谱本章要求:了解红外光谱发展概况,掌握红外光谱的特点,懂得红外光谱谱图的表达方式及物理含义;了解指纹区与官能团区的划分;掌握化合物吸收带位置、个数、强弱及特征;掌握红外光谱解析的一般步骤,会结合元素分析和已知分子式条件下推测分子结构,确定谱带归属;懂得应用标准谱图验证结构解析的结果;了解瑞利散射与拉曼散射的产生;判断振动是否拉曼活性和红外活性,了解拉曼光谱的特点及在结构分析中的应用。
有机化学实验(B)教学大纲大纲说明本大纲是在1998年制定的有机化学实验(生物学科类专业)教学大纲的基础上根据上级教学部门的有关精神重新修订的。
其主要修订点如下:1.本课程统一为生命科学学院(包括协和医科大)和医学部临床医学专业二年级全体本科生的必修课程。
2.学时由原来的85学时改为75学时,仍为2.5 学分。
3.根据多年的教学实践和科学的发展,对教学内容进行了适当取舍,在保证基本操作训练的前提下,增加了两个有机合成实验。
鉴于学生来自生命科学和医学学科,我们增选了能增加实验的知识性和趣味性的药物合成。
4.对实验基本内容有了较详尽的介绍。
目的和要求有机化学是一门实践性很强的学科,有机化学实验是有机化学学科的一个重要组成部分,其主要目的是(1)使学生通过实验的第一手材料,加深对课堂所学的有机基本理论知识的理解。
(2)训练学生掌握有机化学实验的基本操作和技能,提高分析问题和解决问题的能力。
(3)培养学生实事求是,严谨的科学态度,良好的实验室工作作风和习惯。
训练学生掌握基本操作技术和技能是有机化学实验课的基本任务之一,是必须在实验课中切实加强的环节。
对于重要的基本操作单独安排训练,并在合成实验中加以运用和巩固,使学生达到正确和熟练的程度。
合成实验是对学生的综合训练,除了巩固学生的基本操作技术和技能,要求培养学生正确选择有机反应,认真分析反应过程的现象和影响因素,熟练产物的分离提纯鉴定。
通过这个教学环节,较全面培养学生的动手能力和学会分析问题和解决问题,为今后学习专业课和开展科研奠定良好的基础。
学生进行实验前,应对相关的有机化合物的性能有所了解,因而本课要求学生学会使用有关的手册、文献资料及信息网络查阅有机化合物的物理化学常数。
要求学生实验前认真预习,写出预习笔记;实验课中仔细观察和正确记录,整理分析数据;课后按规范书写实验报告。
安全、卫生、节约药品的教育和实施贯穿始终。
教师对学生的预习、仪器装置、基本操作、产品质量和数量、安全卫生、科学态度、合作精神、实验报告等方面进行考察,作为学生评分的依据。
紫外滴定法测定主客体包结常数
紫外滴定是一种常见的有机分析方法,可以用来测定各种有机物质中的包结常数。
本文旨在介绍紫外滴定法中使用的主客体包结常数的基本原理和试验实践方法。
一、包结常数的基本原理
包结常数(或称为结合常数)是一种物理参数,用于表示在主客体系统中,主客体(溶剂或溶质)之间的结合力。
它是一种描述溶质及其环境因素对彼此结合的能力的量化度量指标。
紫外滴定法中,实验者可以测定和计算两个溶质之间的包结常数,从而了解两者之间的结合力。
测量可以采用紫外滴定仪,并通过计算紫外滴定仪的测量数据而得出。
二、紫外滴定测定主客体包结常数的试验实践方法
1、实验准备
紫外滴定法测定主客体包结常数所需要准备的物品包括:紫外滴定仪、紫外光谱仪、质谱分析仪、溶质样品、溶剂样品等。
2、实验步骤
(1)实验开始前,用紫外光谱仪对溶质样品和溶剂样品进行聚焦扫描,测量它们在紫外区域的吸收率和消解指数;
(2)然后,将溶质样品和溶剂样品放入紫外滴定仪中,在规定的条件下进行测量,并根据测试结果计算出主客体之间的紫外滴定法包结常数;
(3)最后,使用质谱分析仪进行核素技术的实验,可以确定主
客体之间的结合关系,检验紫外滴定法测得的主客体包结常数是否精确。
三、结论
紫外滴定法是一种既简单又有效的有机分析方法,可以用于测定包含主客体系统的各种有机物质的包结常数。
本文介绍了紫外滴定法测定主客体包结常数的基本原理以及实验步骤,希望能够对此有所帮助。