苏州市立医院本部关于荧光定量PCR等询价采购公告(2020)
- 格式:doc
- 大小:1.83 KB
- 文档页数:2





实用妇科内分泌杂志Journal Of Practical Gynecologic Endocrinology1102017 年8月C 第4卷/第24期Aug.C 2017 V ol.4 No.24实时荧光定量PCR(RT-PCR)检测NG、UU和CT及MG结果分析李美珠,杨洁飞,李启欣(佛山市第一人民医院,广东佛山 528000)【摘要】目的 RNA恒温扩增实时荧光定量PCR(RT-PCR)检测淋病奈瑟菌(NG)、解脲脲原体(UU)、沙眼衣原体(CT)及生殖支原体(MG)结果。
方法选择我院2016年6月至2017年7月拟诊为泌尿生殖道感染患者的宫颈或者尿道分泌物标本426例,选择培养法对UU、MG及NG病原体进行检测,选择胶体金免疫层析法来对CT抗原进行检测,同时选择RT-PCR来对NG、UU、 MG和CT的核酸进行检测。
结果在病原体检出阳性率方面,RT-PCR检测显著高于金标法或者培养法检测,差异有统计学意义(P<0.05)。
结论在对NG、UU、 MG和CT感染进行检查诊断,采用RT-PCR检测NG、UU、MG和CT具有非常重要的作用,能对常规方法进行有效补充,值得临床推广和应用。
【关键词】荧光定量PCR;淋病奈瑟菌;解脲脲原体;沙眼衣原体;生殖支原体【中图分类号】R695 【文献标识码】B 【文章编号】ISSN.2095-8803.2017.24.110.02非淋菌性尿道炎和淋病是临床中发生率较高的性传播疾病,会引起女性盆腔炎、宫体炎、不孕、宫颈炎、输卵管炎和男性前列腺炎、附睾炎、尿道炎等,除此之外还可能引起女性早产、流产和宫颈癌等,会严重危害患者的生命健康和安全[1]。
泌尿生殖道感染的病原体主要为淋病奈瑟菌(NG)、解脲脲原体(UU)、沙眼衣原体(CT),生殖支原体(MG),而病原体常常表现为共同感染状态。
在临床表现方面,非淋菌性尿道炎和慢性淋病比较类似,临床中常常不能有效明确诊断。
在实际的临床诊断中,传统实验室检测方法存在一定的不足之处,在现代医学技术快速发展和进步的过程中,RT-PCR在临床中的应用也越来越广泛,该方法具有自动化、定量、快速、特异、敏感等特点[2]。


禽源性病毒荧光定量PCR(Q-PCR)检查法本法适用于禽源性生物制品的检测,包括流感全病毒灭活疫苗、流感病毒裂解疫苗种子批毒种的外源性禽病毒检测。
本法用提取的供试品RNA,反转录成cDNA后,或用提取的供试品DNA,针对3种外源性禽病毒设计特异性引物探针,进行荧光定量PCR 检测特异性扩增信号,从而测定供试品中外源性禽源病毒核酸序列,以检查供试品的外源性禽病毒污染。
要求检测的 3 种禽源性病毒:(1)禽腺病毒I 型(DNA 病毒)(2)禽腺病毒III 型(DNA 病毒)(3)外源性禽白血病病毒(逆转录病毒)试剂(1)RNA/DNA 提取试剂:RNA/DNA 的提取可使用酚-氯仿法、磁珠法、离心柱法等。
提取试剂中应含裂解液、洗涤液、洗脱液等,按试剂说明书要求配制。
(2)反转录试剂:含逆转录酶、RNA 酶抑制剂、dNTP 混合液、随机引物、逆转录反应缓冲液等,按试剂说明书要求配制。
(3)引物序列、探针序列见表1。
表 1 引物序列及探针序列(4)扩增缓冲液每20µl 反应体系中,含有上下游引物各5µmol,探针2.5µmol及适量荧光定量PCR混合液(Mix)。
(5)质粒标准品稀释液为DNA 稀释缓冲液或无RNA 酶水稀释。
(6)对照溶液以失活后无感染性的禽源性病毒为阳性对照。
以无RNA 酶水作为阴性对照。
提取核酸和逆转录步骤同(1),置-70℃保存备用。
(7)质粒标准品溶液及灵敏度供试品的制备选择病毒目的核酸序列,人工合成DNA,目的序列转入pMD19-T 质粒中,作为质粒标准品。
测定质粒标准品的DNA 核酸浓度后,对其进行10 倍稀释,从109Copies/µl 稀释至100Copies/µl。
取107Copies/µl~103Copies/µl 质粒标准品溶液作标准曲线各点。
101Copies/µl 稀释度作为灵敏度对照。
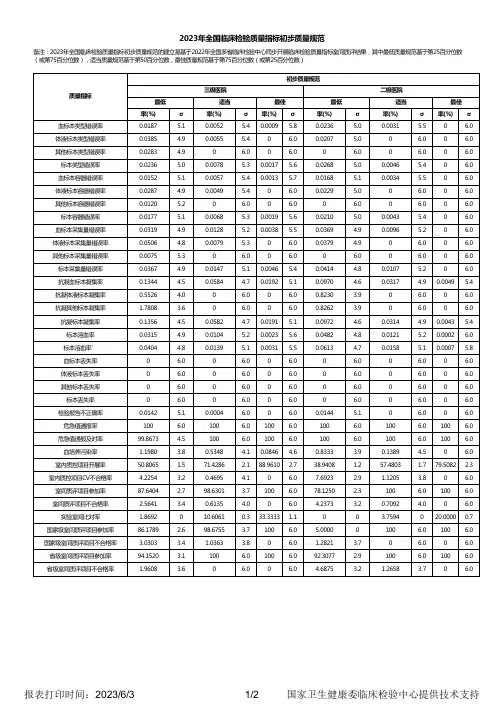
2023年全国临床检验质量指标初步质量规范备注:2023年全国临床检验质量指标初步质量规范的建立是基于2022年全国多省临床检验中心同步开展临床检验质量指标室间质评结果,其中最低质量规范基于第25百分位数(或第75百分位数),适当质量规范基于第50百分位数,最佳质量规范基于第75百分位数(或第25百分位数)质量指标初步质量规范三级医院二级医院最低适当最佳最低适当最佳率(%)σ率(%)σ率(%)σ率(%)σ率(%)σ率(%)σ血标本类型错误率0.0187 5.10.0052 5.40.0009 5.80.0236 5.00.0031 5.50 6.0体液标本类型错误率0.0385 4.90.0055 5.40 6.00.0207 5.00 6.00 6.0其他标本类型错误率0.0283 4.90 6.00 6.00 6.00 6.00 6.0标本类型错误率0.0236 5.00.0078 5.30.0017 5.60.0268 5.00.0046 5.40 6.0血标本容器错误率0.0152 5.10.0057 5.40.0013 5.70.0168 5.10.0034 5.50 6.0体液标本容器错误率0.0287 4.90.0049 5.40 6.00.0229 5.00 6.00 6.0其他标本容器错误率0.0120 5.20 6.00 6.00 6.00 6.00 6.0标本容器错误率0.0177 5.10.0068 5.30.0019 5.60.0210 5.00.0043 5.40 6.0血标本采集量错误率0.0319 4.90.0128 5.20.0038 5.50.0369 4.90.0096 5.20 6.0体液标本采集量错误率0.0506 4.80.0079 5.30 6.00.0379 4.90 6.00 6.0其他标本采集量错误率0.0075 5.30 6.00 6.00 6.00 6.00 6.0标本采集量错误率0.0367 4.90.0147 5.10.0046 5.40.0414 4.80.0107 5.20 6.0抗凝血标本凝集率0.1344 4.50.0584 4.70.0192 5.10.0970 4.60.0317 4.90.0049 5.4抗凝体液标本凝集率0.5526 4.00 6.00 6.00.8230 3.90 6.00 6.0抗凝其他标本凝集率 1.7808 3.60 6.00 6.00.8262 3.90 6.00 6.0抗凝标本凝集率0.1356 4.50.0582 4.70.0191 5.10.0972 4.60.0314 4.90.0043 5.4标本溶血率0.0315 4.90.0104 5.20.0023 5.60.0482 4.80.0121 5.20.0002 6.0标本溶血率’0.0404 4.80.0139 5.10.0031 5.50.0613 4.70.0158 5.10.0007 5.8血标本丢失率0 6.00 6.00 6.00 6.00 6.00 6.0体液标本丢失率0 6.00 6.00 6.00 6.00 6.00 6.0其他标本丢失率0 6.00 6.00 6.00 6.00 6.00 6.0标本丢失率0 6.00 6.00 6.00 6.00 6.00 6.0检验报告不正确率0.0142 5.10.0004 6.00 6.00.0144 5.10 6.00 6.0危急值通报率100 6.0100 6.0100 6.0100 6.0100 6.0100 6.0危急值通报及时率99.8673 4.5100 6.0100 6.0100 6.0100 6.0100 6.0血培养污染率 1.1980 3.80.5348 4.10.0846 4.60.8333 3.90.1389 4.50 6.0室内质控项目开展率50.8065 1.571.4286 2.188.9610 2.738.9408 1.257.4803 1.779.5082 2.3室内质控项目CV不合格率 4.2254 3.20.4695 4.10 6.07.6923 2.9 1.1205 3.80 6.0室间质评项目参加率87.6404 2.798.6301 3.7100 6.078.1250 2.3100 6.0100 6.0室间质评项目不合格率 2.5641 3.40.6135 4.00 6.0 4.2373 3.20.7092 4.00 6.0实验室间比对率 1.8692010.60610.333.3333 1.100 3.7594020.00000.7国家级室间质评项目参加率86.1789 2.698.6755 3.7100 6.0 5.00000100 6.0100 6.0国家级室间质评项目不合格率 3.0303 3.4 1.0363 3.80 6.0 1.2821 3.70 6.00 6.0省级室间质评项目参加率94.1520 3.1100 6.0100 6.092.3077 2.9100 6.0100 6.0省级室间质评项目不合格率 1.9608 3.60 6.00 6.0 4.6875 3.2 1.2658 3.70 6.0质量指标初步质量规范(周转时间(分钟))三级医院二级医院最低适当最佳最低适当最佳急诊检验前周转时间中位数生化312315301810自动化免疫342515302010三大常规302011261510凝血302215301510常规(住院)检验前周转时间中位数生化906041604830自动化免疫926041605030三大常规815733603830凝血805735604030急诊实验室内周转时间中位数生化604734604730自动化免疫896045706035三大常规261813302015凝血463529403028常规(住院)实验室内周转时间中位数生化1241007312011560自动化免疫1891319818012081三大常规593627603030凝血906045816039。

实时荧光定量PCR目前实时荧光定量PCR已得到广泛应用,如:扩增特异性分析、基因定量分析、基因分型、SNP分析等......荧光定量PCR最常用的方法是DNA结合染料SYBR Green I 的非特异性方法和Taqman水解探针的特异性方法SYBR Green I 的非特异性方法(试剂盒:LightCycler 480 SYBR Green I Master)SYBR Green I是一种结合于所有dsDNA双螺旋小沟区域的具有绿色激发波长的染料。
在游离状态下,SYBR Green I发出微弱的荧光,但一旦与双链DNA结合后,荧光大大增强。
因此,SYBR Green I的荧光信号强度与双链DNA的数量相关,可以根据荧光信号检测出PCR 体系存在的双链DNA数量。
一、实验前准备:实验试剂及耗材:试剂:特异性PCR引物,新鲜提取备用的总RNA试剂盒:Transcriptor First Strand cDNA Synthesis Kit、LightCycler 480 SYBR Green I Master1号管包含:热启动Taq DNA Polymerase、反应缓冲液、dNTP mix、SYBR Green I染料、MgCI2仪器及耗材:罗氏LightCycler 480全自动实时定量PCR仪以及配套使用的48或96孔板;Thermo Scientific Arktik PCR仪、F1单道移液器、冰盒、QSP盒装吸头等正式实验开始前,冰上解冻各个试剂【注意:SYBR Green I Master 需要避光放置】二、反转录实验操作时注意:所有RNA相关的操作均需要佩戴手套,防止RNase污染。
严格按照试剂盒使用说明进行相关操作。
按照体系配方在冰上的Rnasefree的灭菌PCR管中配置Templateprimer mix,总体系13ul。
本实验是联合使用anchored oligo dT引物和随机六聚体引物进行的反转录。

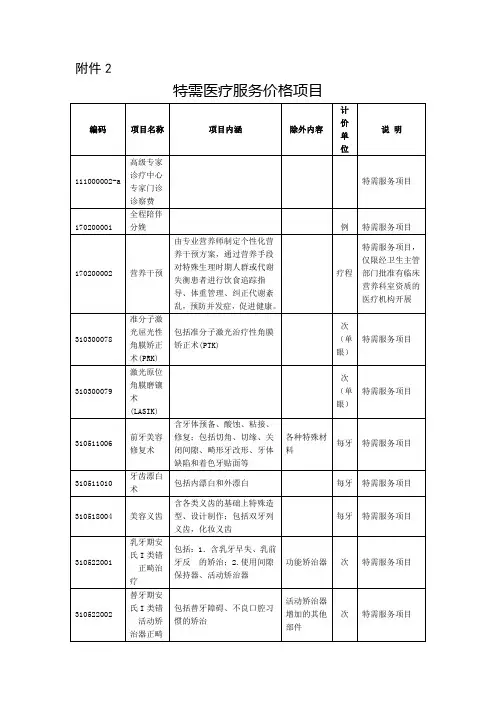
附件2
特需医疗服务价格项目
乳牙期安氏I类错正畸治疗包括:1.含乳牙早失、乳前牙反的矫治;2.使用间隙保持器、活动矫治器
替牙期安氏I类错活动矫治器正畸
替牙期安氏I类错固定矫治器正畸治疗
恒牙期安氏I类错固定矫治器正畸治疗
乳牙期安氏II类错正畸治疗包括:1.乳牙早失、上頦前突、乳前牙反的矫治;2.使用间隙保持器、活动矫治器治疗
替牙期安氏II类错口腔不良习惯正畸治疗
替牙期牙性安氏II 类错活动矫治器正畸治疗
替牙期牙性安氏II 类错固定矫治器正畸治疗
替牙期骨性安氏II 类错正畸治疗
恒牙早期安氏II 类错功能矫治器治疗包括:1.严重牙性II类错和骨性II类错;2.使用Frankel功能矫治器II型或Activator功能矫治器;其他功能矫治器
恒牙期牙性安氏II 类错固定矫治器治疗1.含上下颌所需带环、弓丝、托槽;2.包括牙性安氏II 类错拥挤不拔牙病例和简单拥挤拔牙病例
恒牙期骨
性安氏II 类错固定矫治器拔牙治疗包括骨性安氏II类错拔牙病例
乳牙期安氏III类错正畸治疗包括:1.乳前牙反;2.使用活动矫治器或下颌连冠式斜面导板治疗
替牙期安
氏III类错正畸治疗1.包括前牙反;2.使用活动矫治器
替牙期安氏III类错功能矫治器治疗包括:1.严重牙性III类错和骨性III类错;2.使用rankel功能矫治器III 型;其他功能矫治器
恒牙期安
氏III类错固定矫治器治疗包括:牙性安氏III类错拥挤不拔牙病例和简单拥挤拔牙病例
恒牙期骨性安氏
III类错
固定矫治器拔牙治疗包括骨性安氏III类错拔牙病例。
苏州市立医院本部关于病理科空气处理系统改造公开招标中标公告苏州市卫康招投标咨询服务有限公司受苏州市立医院(本部)的委托,就其拟采购的“病理科空气处理系统改造”项目进行公开招标采购,按规定程序进行了开标、评标、定标,现就本次采购的中标结果公布:一、项目名称及项目编号:项目名称:病理科空气处理系统改造项目编号:SZWK2020-G-007号二、采购项目的简要说明:苏州市市立医院(本部)病理科空气处理系统及设备采购及相关服务,包括:(1)苏州市立医院本部病理科空气处理系统及设备工程,地上4层,为多层建筑;本次工程为第2、第3层局部病理科改造工程,2、 3层建筑高度为3.6m,梁下高度为3米,2楼施工范围内的装修面积约为459,3楼施工范围内装修面积为148。
本工程主要包括以下房间:2F 技术室、取材室、仓库、图文室、诊断室一、诊断室二、诊断室三、细胞室、标本存放室、冰冻室、免疫组化室、专家诊断室、男卫生间、女卫生间、内部走道。
3F 技术办、会议室、暂库、会诊室、内部走廊。
(2)本次招标的范围包括病理科实验室、清洁走廊、配套功能用房等附属设施的洁净装饰、普通装饰、新风空调、普通空调、卫生冷水、给排水、电气(强电、弱电)、自动控制系统、屋顶净化空调机房搭建等的全套交钥匙工程。
三、采购公告媒体及时间:公告媒体:苏州市政府采购网、江苏政府采购网公告时间:2020年3月17日-2020年3月24日四、评标信息:开标时间:2020年4月9日9:30时开标地点:苏州市姑苏区平泷路251号城市生活广场西楼五楼,苏州市公共资源交易中心(政府采购)评标委员会名单:许元根、鲍俭、孙颐、闵奇萍、朱伟(采购人代表)五、中标信息:1、中标项目的简要说明(非正式文本,仅供参考。
若下载后打开异常,可用记事本打开)。
江苏省特殊医用材料价格管理目录-江苏省物价局江苏江苏省特殊医用材料价格管理目录特殊医用材料目录编码项目名称特殊医用材料名称一综合医疗服务类110400001 院前急救费 110400001-1 化验110400001-2 特殊检查 110400001-3 治疗110400001-4 药物 110400001-5 血液 110500001体检费 110500001-1 影像 110500001-2 化验 110500001-3 特殊检查1201 护理费 1201-1 药物 120100011 吸痰护理120100011-1 一次性吸痰管 1202 抢救费 1202-1药物 120300001 氧气吸入 120300001-1 一次性鼻导管 120300001-2 鼻塞 120300001-3 面罩1204 注射 1204-1 一次性输液器 1204-2 过滤器1204-3 采血器 1204-4 注射器等特殊性消耗材料1204-5 药物 1204-6 血液 1204-7 血制品120400010 静脉穿刺置管术 120400010-1 PIU导管120400011 120400011-1 中心静脉套件120400011-2 测压套件 1206 换药 1206 特殊药物 1206 引流管 120700001 雾化吸入120700001-1 药物 120800001 鼻饲管置管120800001-1 药物 120800001-2 一次性胃管121000001 洗胃 121000001-1 药物 121000001-2一次性胃管 121200001 坐浴 121200001-1 药物121300001 冷热湿敷 121300001-1 药物121400001 引流管冲洗 121400001-1 换药121400001-2 特殊药物 121500001 灌肠121500001-1 氧气 121600001 导尿 121600001-1导尿包 121600001-2 尿管 121600001-3 尿袋13 社区卫生服务及预防保健项目 13-1 药物13-2 化验 13-3 检查二医技诊疗类210102015 含数据采集存贮图象显示 210102015-1 胶片210103 含临床操作及造影剂过敏试验 210103-1 造影剂210103-2 胶片 210103-3 一次性插管 2102 磁共振扫描MRI 2102-1 造影剂2102-2 麻醉 2102-3药物 2103 X线计算机体层CT扫描 2103-1 造影剂2103-2 麻醉 2103-3 药物 2201 A超2201-1 图象记录 2202 B超 2202-1 图象记录2202-2 造影剂 220201006 输卵管超声造影220201006-1 一次性导管 2203 彩色多普勒超声检查2203-1 图象记录 2203-2 造影剂 2204 多普勒检查2204-1 图象记录 2204-2 造影剂 2206 心脏超声检查 2206-1 图象记录2206-2 造影剂 220600009负荷超声心动图 220600009-1 药物 220700007 心肌灌注超声检测220700007-1 造影剂 23 核医学23-1 药物 23-2 X光片 23-3 彩色胶片23-4 数据存贮介质 2306 核素内照射治疗 2306-1核素治疗药物 2306-2 一次性导管 2404 后装治疗2404-1 核素治疗药物 270100003 尸体化学防腐处理270100003-1 防腐药物三临床诊疗类 310300086 光动力疗法PDT 310300086-1 光敏剂 3105 口腔颌面3105-1 一次性无痛麻醉手柄 3105-2 一次器械盒3105-3 口腔特殊用药 310501007 口腔模型制备310501007-1 硅橡胶 310501007-2 琼脂材料310501007-3 进口石膏材料 310501008 记存模型制备310501008-1 硅橡胶 310501008-2 琼脂材料310501008-3 进口石膏材料 310501009 面部模型制备310501009-1 硅橡胶 310501009-2 琼脂材料310501009-3 进口石膏材料 310501009-4 进口蜡模材料310503005 菌斑微生物检测 310503005-1Periocheck试剂盒 310505001 310505001-1 录象带310505001-2 计算机软盘 310505001-3 照相及胶片310505002 云纹仪检查 310505002-1 化妆品310505002-2 照相底片及冲印 310505003 模型外科设计310505003-1 石膏模型制备 310505004 带环制备310505004-1 石膏模型制备 310505004-2 分牙及牙体预备 310505004-3 粘接带环 310505005 唇弓制备310505005-1 方弓丝 310505005-2 予成牵引弓310505005-3 唇弓 310505005-4 其他特殊材料310507002 错畸形治疗设计 310507002-1 模型制备310507003 固定矫治器复诊处置 310507003-1 更换弓丝310507003-2 弓丝附件 310507004 活动矫治器复诊处置310507004-1 各种弹簧 310507004-2 其他附件310507005 功能矫治器复诊处置 310507005-1 其他材料 310507005-2 其他材料附件 310507006 特殊矫治器复诊处置 310507006-1 其他材料 310507006-2 其他材料附件 310510002 氟防龋治疗 310510002-1 氟保护漆310510003 牙脱敏治疗 310510003-1 高分子脱敏剂310510007 口腔局部止血 310510007-1 特殊填塞310510007-2 止血材料 310510010 牙外伤结扎固定术310510010-1 特殊结扎固定材料 310511001 简单充填术310511001-1 特殊材料 310511002 复杂充填术310511002-1 特殊材料 310511003 牙体桩钉固位修复术310511003-1 各种特殊材料 310511003-2 桩310511003-3 钉 310511004 牙体缺损粘接修复术310511004-1 特殊材料 310511006 前牙美容修复术310511006-1 各种特殊材料 310511007 树脂嵌体修复术310511007-1 各种特殊材料 310511011 盖髓术310511011-1 特殊盖髓剂 310511017 根管充填术310511017-1 特殊充填材料 310511022 髓腔穿孔修补术310511022-1 特殊材料 310511023 根管壁穿孔外科修补术310511023-1 根管充填 310511025 根管内固定术310511025-1 钛桩 310511026 劈裂牙治疗310511026-1 根管治疗 310511027 后牙纵折固定术310511027-1 根管治疗 310511027-2 带环结扎丝310512001 根尖诱导成形术 310512001-1 特殊充填材料310512002 窝沟封闭 310512002-1 特殊窝沟封闭剂310512003 乳牙预成冠修复 310512003-1 树脂冠310512003-2 金属冠 310512004 儿童前牙树脂冠修复310512004-1 树脂冠 310512004-2 金属冠 310512005制戴固定式缺隙保持器 310512005-1 印模310512005-2 模型制备 310512005-3 下颌舌弓310512005-4 导萌式保持器 310512005-5 丝圈式保持器310512006 制戴活动式缺隙保持器 310512006-1 印模310512006-2 模型制备 310512007 制戴活动矫正器310512007-1 印模 310512007-2 模型制备310512007-3 特殊矫正装置 310512008 前牙根折根牵引310512008-1 矫正牵引装置材料 310512008-2 复诊更换牵引装置 310512008-3 印模 310512008-4 模型制备310512009 钙化桥打通术 310512009-1 特殊根管充填材料 310512009-2 银尖310512009-3 钛尖310512010 全牙列垫固定术 310512010-1 透明压模垫310512010-2 硬石膏 310512010-3 超硬石膏印模310512010-4 模型料 310512010-5 印模310512010-6 模型制备 310513003 牙周固定310513003-1 树脂 310513003-2 高强纤维310513005 牙面光洁术 310513005-1 特殊材料310513006 牙龈保护剂塞治 310513006-1 特殊保护剂310515003 干槽症换药 310515003-1 止血膏310515003-2 灭滴灵粉 310517 固定修复 310517-1冠 310517-2 嵌体 310517-3 桩核310517-4 根帽 310517-5 贴面 310517-6 桩冠 310517-7 固定桥 310517-8 特殊粘接材料310517009 粘结 310517009-1 特殊粘接剂 310518 可摘义齿修复 310518-1 活动桥 310518-2 个别托盘310518-3 义齿 310518-4 咬合板 310518-5 局部义齿 310518-6 总义齿 310518-7 特制暂基托310518-8 附着体 310518-9 模型制备 310518-10印模 310518-11 模型材料 31。
苏州市立医院本部关于荧光定量PCR等询价采购公告(2020)
2、交付使用时间:合同签订后7天内交货并安装调试完成。
3、免费质保期:提供至少3年的质保。
4、交货地点:苏州市立医院(本部)指定地点。
5、验收标准:产品安装后,采购单位按国际或国家标准及厂方标准进行质量验收。
二、供应商资格条件:
1、具有独立承担民事责任的能力;
2、具有良好的商业信誉和健全的财务会计制度;
3、具有履行合同所必需的人员和专业技术能力;
4、有依法缴纳税收和社会保障资金的良好记录;
5、参加政府采购活动前三年内,在经营活动中没有重大违法记录;
6、法律、行政法规规定的其他条件;
7、具有所投产品合法的经营许可资格;
8、非生产厂家投标的,须具有产品的合法代理商资格证明。
三、采购文件获取信息:
1、获取时间:自本次采购公告发布之日起至递交询价响应文件截止时间前。
2、获取方式:供应商自行至苏州政府采购网上下载询价采购文件。
四、递交询价响应文件时间、地点:
1、递交时间:2020年5月11日8:3010:30(北京时间)
2、递交截止时间:2020年5月11日10:30(北京时间)
3、递交地点:苏州市干将西路120号3号楼四楼苏州市卫康招投标咨询服务有限公司前台
4、本项目将于2020年5月11日下午13:30在苏州市姑苏区平泷路251号城市生活广
场西楼五楼,苏州市公共资源交易中心进行评审。
五、联系及监督
1、采购单位:苏州市立医院(本部)
电话(略)
地址:苏州市道前街26号
2、采购代理机构:
苏州市卫康招投标咨询服务有限公司联系人:吕兆莉、张田。
电话(略)电话(略)。
地址:苏州市干将西路120号3号楼四楼邮编:215005
3、政府采购监督电话(略)
六、信息发布媒体:
1、该信息刊登在江苏政府采购网、苏州市政府采购网,成交公告亦是刊登在此媒体,敬请各供应商注意。
七、公告期:自公告发布之日起三个工作日。
苏州市卫康招投标咨询服务有限公司
2020年5月6日
(非正式文本,仅供参考。
若下载后打开异常,可用记事本打开)。