钠离子电池综述
- 格式:doc
- 大小:408.50 KB
- 文档页数:11

钠离子电池的基本概念
钠离子电池是一种重要的能量存储设备,与传统锂离子电池相比具有更高的储
能密度和更低的成本。
它利用钠离子在正负极之间的迁移来储存和释放电能。
在钠离子电池中,正极通常由钠离子化合物(如钠离子盐)构成,负极则由碳
材料、金属钠或钠合金构成。
电解质可以是液态的或是固态的,用以允许钠离子在正负极之间进行迁移。
充放电过程中,钠离子在正负极之间通过电解质进行离子交换,从而实现能量的存储和释放。
钠离子电池具有多种优点。
首先,钠是地球上丰富而廉价的资源,相较于锂离
子电池中稀有的锂资源,钠资源更易获取。
其次,钠离子电池具有更高的能量密度,可以存储更多的电能。
这使得钠离子电池成为储能系统的理想选择,可以广泛应用于家庭能源存储、电动车辆和可再生能源项目等领域。
然而,钠离子电池也存在一些挑战和限制。
首先,由于钠离子相对较大,它们
在电解质中的迁移速率较慢,可能导致电池性能的下降。
其次,钠离子电池的寿命和循环稳定性还需要进一步改进和优化。
总而言之,钠离子电池是一种具有巨大潜力的储能技术。
随着科学技术的进步
和不断的研发工作,钠离子电池有望成为可持续能源存储领域的重要一环,并为推动清洁能源的普及和应用做出贡献。

钠离子电池技术路线概述说明1. 引言1.1 概述随着能源需求的不断增长和对环境污染问题的日益关注,可再生能源和电动交通等领域的快速发展带来了对高效储能技术的迫切需求。
在众多储能技术中,离子电池作为一种重要的能量储存方式,受到广泛关注。
钠离子电池作为一种新兴的储能技术,在近年来取得了显著进展。
本文对钠离子电池的技术路线进行概述和说明,并与目前主流的锂离子电池进行对比。
通过介绍钠离子电池的基本原理、发展历程以及应用领域,分析其相对于锂离子电池的优势和劣势,并探讨钠离子电池在特定应用场景中代替锂离子电池的可行性。
此外,还将深入介绍两种不同钠离子电池技术路线(xxx 和yyy),包括其理论原理、发展现状以及在不同领域中的实际应用案例。
最后,我们将总结并展望钠离子电池未来的技术路线选择和发展趋势,并探讨钠离子电池对能源领域的影响与挑战。
同时,给出钠离子电池技术的前景和应用推广的建议,以期为未来钠离子电池的研究和应用提供参考。
1.2 文章结构本文主要分为六个部分:引言、技术路线概述、锂离子电池与钠离子电池的对比、钠离子电池技术路线一(xxx)介绍、钠离子电池技术路线二(yyy)介绍以及结论。
在引言部分,将首先概述文章的目的,并简要介绍本文所涵盖内容。
之后,将依次详细介绍各个部分的主题和内容。
1.3 目的本文旨在全面阐述钠离子电池的技术路线,包括基本原理、发展历程、应用领域等方面。
通过与锂离子电池进行对比,探讨其优势和劣势,并进行可替代性分析。
同时,重点介绍两种不同技术路线(xxx 和yyy),包括其理论原理、发展现状以及实际应用案例。
最后,通过总结和展望,分析钠离子电池的发展趋势,并提出对其未来前景和应用推广方面的建议。
通过本文的阐述,旨在为读者提供有关钠离子电池技术的全面了解,并促进该领域的研究和发展。
2. 技术路线概述2.1 钠离子电池介绍钠离子电池是一种新型的储能技术,它通过将钠离子在正负极之间的迁移来实现电荷和放电过程。

硫化钴钠离子电池综述
硫化钴钠离子电池是一种新型的电池技术,它具有很高的能量
密度和循环寿命,因此备受关注。
首先,让我们来看一下硫化钴钠
离子电池的工作原理。
硫化钴钠电池的正极材料是硫化钴,负极材
料是钠金属或者钠合金。
在充放电过程中,钠离子在正负极之间传输,从而完成电荷和放电的过程。
硫化钴钠电池的优势之一是其高
能量密度,这意味着它可以存储更多的能量,因此在电动汽车和储
能系统中具有广阔的应用前景。
此外,硫化钴钠电池的循环寿命也
相对较长,可以进行数千次的充放电循环而不损失太多容量,这使
得其在储能系统中具有更长久的使用寿命。
除了这些优点,硫化钴钠电池也存在一些挑战和局限性。
首先,钠金属作为负极材料存在着安全隐患,因为钠在充放电过程中容易
发生枝晶生长,导致电池内部短路和安全问题。
其次,硫化钴钠电
池的循环寿命虽然较长,但仍然需要进一步提高,特别是在高温环
境下的稳定性和循环寿命方面仍有待改进。
此外,硫化钴钠电池的成本也是一个需要考虑的因素。
虽然硫
化钴钠电池的材料相对较为常见,但是其制造工艺和生产成本仍然
需要进一步降低,以提高其在市场上的竞争力。
总的来说,硫化钴钠离子电池作为一种新型的电池技术,具有很高的能量密度和循环寿命,但是在安全性、循环寿命和成本等方面仍存在一些挑战和局限性。
随着科学技术的不断进步和创新,相信这些问题都可以得到有效解决,硫化钴钠电池有望在电动汽车和储能系统等领域发挥重要作用。

钠离子电池钠离子电池是一种新型的高能量密度电池,其正极材料为钠离子储存材料。
钠离子电池相较于传统锂离子电池具有更高的储能密度和更低的成本,因此在能源存储和电动汽车领域具有巨大的应用潜力。
钠离子电池的工作原理与锂离子电池类似,通过正极和负极之间的钠离子在电解质中的迁移实现电荷的存储和释放。
正极材料一般采用氧化钠、钠磷酸盐等化合物,负极材料则采用稳定的炭材料。
电解质则选择具有良好离子导电性能的材料,如盐溶液或是离子液体。
钠离子电池的优点之一是其丰富的资源,钠作为地壳中第六丰富元素,具有广泛的储藏量。
相比之下,锂资源较为有限,且分布不均。
因此,利用钠离子电池可以有效避免锂资源的短缺问题,降低生产成本。
钠离子电池还具有更高的能量密度。
由于钠离子的半径较大,使得电池的存储能力更高。
传统锂离子电池的储能密度一般在150-250Wh/kg之间,而钠离子电池的储能密度可以达到300Wh/kg,甚至更高。
这使得钠离子电池在电动汽车等领域具有更长的续航里程和更高的能量输出功率。
然而,钠离子电池也存在一些挑战。
首先,钠离子的电化学反应机制相较于锂离子较为复杂,包括钠离子的溶解、析出和嵌入等多个反应过程。
这要求设计合适的电极和电解质材料以实现高效的电荷迁移和循环稳定性。
其次,由于钠离子的半径较大,会导致电池的体积增大和充放电速率降低。
此外,钠离子电池还存在着较高的安全风险,在电池充放电过程中可能会出现不稳定的化学反应。
目前,钠离子电池的研究和开发工作正紧张进行中。
各国科研机构和企业加大了对钠离子电池技术的投入,以期从理论到实验进一步突破技术瓶颈。
中国也加强了对钠离子电池的研究,积极探索其在能源存储和电动汽车领域的应用。
预计在不久的将来,钠离子电池将能够商业化并推动电动汽车和能源存储领域的发展。
总之,钠离子电池作为一种新型高能量密度电池,具有丰富的资源、更高的储能密度和更低的成本。
虽然面临着一些挑战,但其在能源存储和电动汽车等领域具有广阔的应用前景。
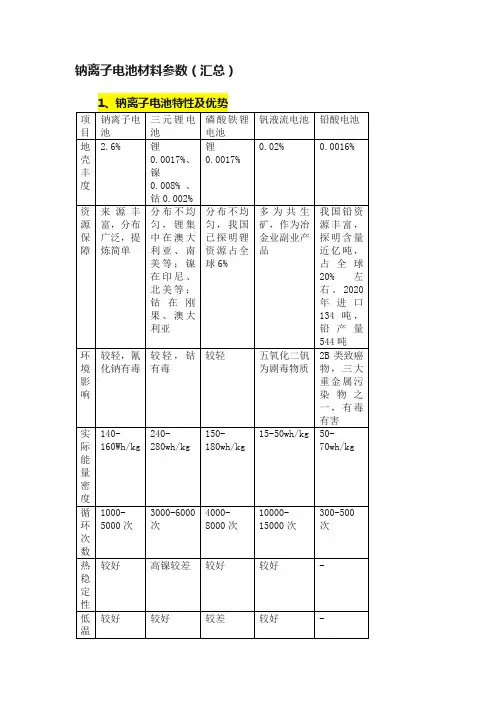
钠离子电池材料参数(汇总)
锂盐替换成钠盐,溶剂基本可复用锂离子中成熟体系,但需要根据钠离子特性做配方调整。
钠离子电池负极一般不使用石墨,在碳基体系中多采用无定形碳。
早期观点认为Na+直径是Li+的1.3倍。
无法在石墨层间自由移动,本质还是热力学问题,钠离子与石墨层间相互作用力弱。
硬碳比容量高,成本和规模化存在劣势。
硬碳前驱体为热固性材料,高温下难以石墨化,结构排布更无序,有丰富微孔、材料间隙更大、比容量更高,膨胀系数小。
但孔洞导致比表大,首次效率低。
软碳储能钠容量低,但前驱体产碳率高,有成本优势。
软碳前驱体为热塑性材料,高温下易石墨化,结构更有序,层间距更短,储钠容量较低。
层状氧化物(成熟方案):结构类似三元正极材料,比容量相对较高,综合性能好。
通过过渡金属选择和比例,可兼顾动力和储能等需求。
普鲁士蓝白(攻克方案):过渡金属可仅使用成本较低的Fe和Mn,理论能量密度高,合成温度低,属于初期路线。
但量产时结晶水控制难,稳定性差。
聚阴离子(储备方案):类似磷酸铁锂的橄榄石结构,稳定性高,具备较优的循环寿命,适合储能。
但导电性差、能量密度低,其中掺钒路线成本高、掺铁路线能量密度表现差。

钠离子电池正极材料综述理想的正极材料应具有高容量、合适的工作电压、高功率密度、足够的电子/离子电导率以及高化学/环境稳定性等优点。
为了保证SIB的稳定性和安全性,商用正极材料还应具有环境影响小、制备容易、原料丰富、热稳定性高等优点。
目前,研究人员已经开发出各种类型的正极材料,包括聚阴离子化合物、普鲁士蓝类似物、有机化合物和过渡金属氧化物。
聚阴离子化合物由于其稳定的框架结构,聚阴离子化合物被认为是先进SIB极具发展前景的正极材料。
聚阴离子化合物通过阴离子基团共价连接并且通常提供三维Na离子扩散通道。
与层状氧化物相比,3D框架结构可以有效缓解结构重排,抑制Na+插入/脱出过程中氧(O)的溶解,从而具有良好的可循环性和热稳定性。
然而,由于其独特的结构,这些正极材料具有低导电性。
因此,为了改善本质上较低的电子导电性,人们提出了导电碳(C)涂层、纳米结构设计和元素掺杂等方法。
一般认为,高导电性的C层涂层是提高磷酸钒钠NVP电化学性能最有效的材料。
这些材料的使用增强了循环稳定性和倍率性能,因为引入的C涂层不仅增加了电子导电性,而且还充当缓冲层,防止活性材料受到破坏。
综上所述,具有高结构稳定性的聚阴离子化合物被认为是潜在的商用正极材料,但需要进一步优化组分设计和合成方法,以降低生产成本和增加体积能量密度。
层状氧化物过渡金属氧化物由于其高比容量,易于合成和良好的电化学性能而被认为是SIB极有前途的正极材料。
根据Na离子的配位环境(三角棱柱位或八面体位)和重复堆叠单元中,Na层状氧化物主要分为P2(ABBA氧化物离子堆叠)和O3 (ABCABC 氧化物离子堆叠)两种类型。
在较窄的电压窗内, P2相正极材料通常表现出优异的循环稳定性,但在较宽的电压范围内,其容量衰减速度很快。
P2型正极在较宽的电位窗内的不稳定性主要源于在4.2 V时,严重相变(P2到O2结构)和TM离子在低电压下的溶解。
更重要的是,由于P2型正极材料的Na含量较低,它们普遍表现出较低的首电荷容量和异常的ICE,极大地阻碍了Na满电池的大规模应用。

钠离子电池文献摘要:1.钠离子电池概述2.钠离子电池的优点3.钠离子电池的缺点4.钠离子电池的研究现状5.钠离子电池的应用前景正文:钠离子电池是一种新型的可充电电池技术,与锂离子电池类似,但在正极、负极或电解质中使用钠(Na)元素替代锂(Li)。
近年来,随着对可再生能源和电动汽车需求的不断增长,钠离子电池因其具有较高的能量密度、较低的成本和较好的环境友好性而备受关注。
钠离子电池具有以下优点:1.高能量密度:钠离子电池的能量密度较高,可以满足大部分电子产品和电动汽车对续航能力的要求。
2.成本较低:相较于锂离子电池,钠离子电池的原材料成本较低,有利于降低电池的制造成本。
3.环境友好:钠元素在地壳中含量较高,分布广泛,且生产过程中产生的环境污染相对较小。
然而,钠离子电池也存在一些缺点:1.体积较大:由于钠离子的体积较大,相同能量密度下,钠离子电池的体积和重量通常会大于锂离子电池。
2.循环寿命较短:钠离子电池的循环寿命相较于锂离子电池较短,会影响电池的使用寿命。
3.稳定性有待提高:钠离子电池在高温、过充、过放等条件下的稳定性相对较差,需要采用更先进的技术和材料来解决这些问题。
目前,钠离子电池的研究主要集中在提高能量密度、延长循环寿命和改善安全性等方面。
研究者通过改变正负极材料、优化电解质和改进结构设计等方法,不断推动钠离子电池技术的发展。
在应用前景方面,钠离子电池有望在以下领域发挥重要作用:1.电动汽车:钠离子电池可以作为锂离子电池的补充,满足电动汽车市场的快速增长需求。
2.储能系统:钠离子电池具有较高的能量密度和较低的成本,可应用于太阳能、风能等可再生能源的储能系统。
3.便携式电子产品:钠离子电池可为手机、笔记本电脑等便携式电子产品提供较长的续航时间。
总之,钠离子电池作为一种具有潜力的新型电池技术,在能量密度、成本和环境友好性等方面具有优势,但仍需在循环寿命、稳定性等方面进行进一步研究。

钠离子电池原理钠离子电池原理摘要:钠离子电池由正极材料,负极材料,电解液和隔膜组成,是目前最为流行的电池之一也是有效地存储太阳能的一种最具前景的电池技术。
文针对钠离子电池技术做出综述,对其各个部分如正/负极材料,电解液和电池结构分别作出详细的介绍。
关键词:钠离子电池;结构;正/负极材料;电解液;电池性能1 、介绍钠离子电池是一种功率型电池,由正极材料,负极材料,电解液和隔膜组成。
它是一种可以对太阳能进行有效储备的电池技术,由于其具有高能量密度,较低的成本,高质量的可再生能源等优点,似乎前景广阔。
本文将介绍其原理,构造,正/负极材料,电解液及其性能。
2 、原理钠离子电池原理是通过正极和负极的电池反应形成新的离子,使电荷从正极流入负极,电荷回路形成,从而使电池发生电流变化,从而产生功率。
当太阳能充电时,电极发生变化,此时正极其中含有的钠离子会经由电极到负极,同时负极也会是此过程,从而产生电流回路。
通过此过程,电流就可以更有效地从太阳能到电池的转换。
3、结构钠离子电池的结构包括正极,负极和晶格结构,相应的电解液和隔膜。
正极(钠基二氧化钠)由凝胶离子交换膜、离子交换树脂和无定型夹心材料组成;负极(碳粉/木炭)通过改变体系确定,也可用合金建立复合;隔膜可以是隔膜电解质,也可以是隔膜抗阻材料;电解可以是金属氟离子液体,也可以是绝缘液体(如碳酰液)。
4、正/负极材料正极材料:正极材料是钠基二氧化钠,负极材料是金属合金或者活性炭粉/木炭,其中金属就是钠和钾,钠离子是电荷中会由正极进入负极并通过隔膜形成圆环,由此形成电池能量,一些金属合金可以改变体系结构,有助于改善电流充放电性能。
负极材料:负极材料可以是金属合金或活性炭粉/木炭,其中金属通常是镁(Mg),钾(K)等金属元素,电流的传递过程与正极类似,此过程中钠离子会与负极金属结合形成氢钠溶液,并由隔膜的氢离子所组成的带电团发生变化从而产生电池能量。
5、电解液钠离子电池的电解液不同于传统电解液,它可以是金属氟离子液体,也可以是绝缘液体,如碳酰液,其质量阻力随着温度的变化而变化,此过程中加入特定的金属可以改变它的密度,可以改变钠离子带电移动速度,可使池室内反应减缓,从而改善充放电性能。

sodium-ion batteries 钠离子电池钠离子电池(Sodium-ion batteries,或称为Na-ion电池)是一种新兴的可再充电电池技术,它采用钠离子作为储存和释放电能的载体。
相对于传统的锂离子电池而言,钠离子电池具有很多潜在的优势,如资源丰富、低成本、高功率密度和长寿命等。
本文将重点探讨钠离子电池的工作原理、优势和应用前景等方面。
钠离子电池的工作原理与锂离子电池类似,都是通过离子迁移在正负极之间储存和释放电能。
钠离子电池的正极通常采用的是钠化合物,如钠二氧化物(Na2O2)、氧化钠(NaCoO2)或磷酸钠(Na3V2(PO4)3)等。
而负极则使用碳材料或NaNi3等材料来吸附和释放钠离子。
另外,钠离子电池中的电解质通常是有机盐溶液或固态氧化物膜。
通过这种离子迁移的机制,电池可以在充放电过程中实现钠离子的输运和电荷平衡,从而实现能量的转化。
相较于锂离子电池,钠离子电池具有许多优势。
首先,钠资源更为丰富,世界上已知的钠储量是锂储量的100倍以上。
这意味着钠离子电池的生产成本更低,有望在电动汽车等大规模应用中具有竞争力。
其次,钠离子电池可以实现高功率密度,可快速充电和放电,适合于一些需要大功率输出的应用,比如电动工具和储能电站等。
此外,钠离子电池的寿命相对较长,循环稳定性更好,有望满足一些对电池寿命要求较高的应用,如电网调度和储能系统等。
然而,钠离子电池也存在一些挑战和限制。
首先,钠离子电池的能量密度相对较低,即单位质量或单位体积的电能储存量较小。
这一问题涉及到材料性能的改进和电池设计的优化。
其次,钠离子电池的循环稳定性和安全性问题还需要进一步解决。
目前,钠离子电池的循环寿命和安全性相对不如锂离子电池。
通过改进电解质和电极材料以及优化电池结构,可以提高钠离子电池的性能和安全性。
尽管钠离子电池还存在一些挑战和限制,但它在一些领域的应用前景仍然十分广阔。
首先,钠离子电池可以作为电动汽车的一种替代能源技术,以应对锂资源的紧张和成本的上升。

钠离子电池技术的研究与应用摘要钠离子电池作为一种新型的储能技术,具有较高的能量密度和较低的成本,因此受到了广泛关注。
本文综述了钠离子电池技术的研究进展和应用前景,包括钠离子电池的工作原理、正负极材料的选择、电解液的优化、电池性能的提升等方面。
同时,我们还讨论了钠离子电池在可再生能源储能、电动车辆、大规模能源存储等领域的应用前景,并提出了当前研究中存在的挑战和未来发展方向。
1. 引言随着全球经济的快速发展和环境问题的日益严重,储能技术在可再生能源利用和电动交通领域的重要性日益凸显。
钠离子电池作为一种新兴的储能技术,具有能量密度高、资源丰富和成本低等优势,在近年来得到了广泛的研究和关注。
2. 钠离子电池的工作原理钠离子电池与传统的锂离子电池类似,都是基于电化学反应来进行能量的存储和释放。
钠离子电池的工作原理主要包括充电和放电两个过程。
在充电过程中,钠离子从正极(如钠离子化合物)脱嵌,经由电解液传输至负极(如碳材料),同时伴随着电子的流动,形成钠金属和碳材料之间的锂离子化合物。
而在放电过程中,则是反过来的过程,钠离子从负极脱嵌,通过电解液传输至正极,同时释放出电子,完成能量的释放。
3. 钠离子电池的正负极材料正负极材料是钠离子电池中的关键组成部分,直接影响着电池的能量密度和循环寿命。
常用的正极材料包括氧化物、磷酸盐和硫化物等,而负极材料主要有碳材料和金属钠。
选择适合的正负极材料可以提高钠离子电池的能量密度和循环寿命。
4. 电解液的优化电解液是钠离子电池中的重要组成部分,主要起着传导离子和电子的作用。
优化电解液的组成可以提高钠离子电池的离子传输速率和电池性能。
目前,常用的电解液包括有机电解液和固态电解液两种类型。
有机电解液具有传导性好、电池成本低等优势,而固态电解液具有安全性好、循环寿命长等优势。
5. 钠离子电池性能的提升钠离子电池的性能主要包括能量密度、功率密度、循环寿命和安全性等方面。
为了提高钠离子电池的性能,研究人员采取了多种策略,包括优化正负极材料、改变电解液组成、改善电池结构等。

钠离子电池调研报告全文共四篇示例,供读者参考第一篇示例:钠离子电池是一种新型的离子锂电池替代品,其研究与应用正在逐渐受到关注。
钠离子电池在电动汽车、储能系统和其他领域具有广阔的应用前景。
本文将对钠离子电池的原理、优势、挑战和未来发展进行调研和分析。
一、钠离子电池原理钠离子电池是一种基于钠离子的电池,具有负极和正极两个基本部分。
负极通常由碳材料、金属钠或复合材料制成,正极则通常由金属氧化物或磷酸盐等材料制成。
当电池充放电时,钠离子在负极和正极之间往复迁移,从而实现电能的转化和储存。
二、钠离子电池优势1. 成本低廉:钠是丰富的、廉价的元素,相比于锂,钠的资源更为丰富,因此钠离子电池具有较低的制造成本。
2. 安全性高:与锂电池相比,钠离子电池的燃烧和爆炸风险更低,具有更高的安全性。
3. 周期性长:钠离子电池具有更长的循环寿命和更高的充电次数,能够更加持久稳定地提供电能。
三、钠离子电池挑战1. 能量密度低:目前钠离子电池的能量密度较低,仍需进一步提高才能满足高能量密度应用的需求。
2. 循环寿命短:目前钠离子电池的循环寿命、充放电速率等性能仍有待改进和优化。
3. 工业化规模化难度大:由于钠离子电池的工艺和生产规模尚不成熟,其在工业化应用中仍存在挑战。
四、钠离子电池未来发展1. 新型材料研究:未来的钠离子电池研究将重点关注新型高容量、高能量密度的正负极材料,并探索材料设计与合成的新方法。
2. 工艺优化与创新:未来的钠离子电池工艺将不断优化和创新,以提高电池性能、循环寿命和安全性。
3. 应用拓展与市场化:未来钠离子电池将在电动汽车、储能系统和其他领域得到更广泛的应用和市场化。
第二篇示例:钠离子电池(Sodium-ion battery,简称Na-ion电池)是一种新型的储能技术,近年来备受关注。
与锂离子电池相比,钠离子电池具有成本更低、储量更丰富和资源更广泛等优势。
随着新能源汽车、可再生能源等领域的快速发展,钠离子电池正逐渐成为备受瞩目的替代品。
钠离子电池的性能和寿命分析及优化设计随着能源需求的不断增长和环保意识的提高,寻找替代传统化石能源的高能量、环保、安全的新型能源已经成为全球关注的焦点。
其中,电池被认为是一种潜力很大的替代能源。
近年来,钠离子电池因其可能替代锂离子电池、钛酸锂电池的优势而受到广泛关注。
本文将就钠离子电池的性能和寿命进行分析,并提出优化设计建议。
一、钠离子电池的基本原理钠离子电池是以过渡金属氧化物作为正极材料,石墨或其他碳质材料作为负极材料,并使用非水电解质电池的一种类型。
钠离子电池的充放电反应如下:正极反应:Na_xMO_2+ xLi^+ + xe^- → Na_xMO_2Li_x负极反应:xC + yNa^+ + ye^- → Na_xC_y其中,M表示过渡金属元素,x和y表示材料的钠离子插入量,即单位重量材料中插入的钠离子数。
在这个过程中,正极和负极通过电解液中的离子交换电子,从而实现了电荷的储存和释放。
钠离子电池的优点在于其材料成本低、能量密度高、能够适应高温工作环境等特点。
但同时也存在着很多制约因素,例如靶材缺乏、精度不足、电解液稳定性等问题,这些问题使得钠离子电池的性能和使用寿命无法达到理想状态。
二、钠离子电池的性能问题及原因1.能量密度低钠离子电池的比能量(即单位质量电池所能提供的能量)略低于锂离子电池。
这是由于钠离子电池中正极材料的化学反应相对复杂,同时电池中储存的钠离子也会发生聚集和自发反应,导致电池能量密度下降。
2.寿命不长钠离子电池的使用寿命通常不到锂离子电池的一半。
其原因在于充电过程中,电池内部的电解液会逐渐分解,而且会释放出氧气。
这种现象称为过量电化,它会造成电压不稳定、电池容量下降,最终会影响电池的寿命。
3.电解液不稳定电解液在钠离子电池中承担着一个重要的作用,即充当两极之间的电子传递媒介。
但是,电解液的稳定性却经常受到压力和温度的影响。
电容器内的质子和阳离子在逐渐减小时,电解液的酸度会下降,从而危及电池的使用寿命。
钠离子电池近年来,随着电子设备、电动工具、小功率电动汽车等迅猛发展,研究高能效、资源丰富及环境友好的储能材料是人类社会实现可持续性发展的必要条件。
为满足规模庞大的市场需求,仅依靠能量密度、充放电倍率等性能衡量电池材料是远远不够的。
电池的制造成本与能耗是否对环境造成污染以及资源的回收利用率也将成为评价电池材料的重要指标。
电池发展有以下显著特点:绿色环保电池发展迅猛;一次电池向二次电池转化,这有利于节约地球有限的资源,符合可持续发展的战略;电池进一步向小、轻、薄方向发展。
钠是地球上储量较丰富的元素之一,与锂的化学性能类似,因此也可能适用于锂离子电池体系。
钠离子电池相比锂离子电池有诸多优势,如成本低,安全性好,随着研究的深入,钠离子电池将越来越具有成本效益,并有望在未来取代锂离子电池而被广泛应用。
1钠离子电池电化学原理同为元素周期表第I主族的钠离子和锂离子的性质有许多相似之处,钠离子完全有可能和锂离子电池一样构造一种广泛使用的二次电池。
并且钠离子电池与锂离子电池相比,原材料成本比锂离子电池低,半电池电位(E0Na+/Na二E°Li+/Li +0.3)比锂离子电池高,适合采用分解电压更低的电解液,因而安全性能更佳。
钠离子电池不以钠作为负极,而是由硬碳或嵌入化合物组成。
钠离子电池实际上是一种浓差屯池,正负极由两种不同的钠离子嵌入化合物组成。
充电时,Nh从正极脱嵌经过电解质嵌入负极,负极处于富钠态,正极处于贫钠态,同时电子的补偿电荷经外电路供给到极才保证止负极电荷平衡F放电时则相反,Nh从负极脱嵌,经过电解质嵌入正极,正极处丁-处丁富钠态口(1)钠离子电池优点:依据目前的研究进展,钠离子电池与锂离子电池相比有3个突出优势:①原料资源丰富,成本低廉,分布广泛;②钠离子电池的半电池电势较锂离子电势高0.3〜0.4 V,即能利用分解电势更低的电解质溶剂及电解质盐,电解质的选择范围更宽;③钠离子电池有相对稳定的电化学性能,使用更加安全。
钠离子电池的研究与开发钠离子电池作为一种新兴的储能技术,在能源存储领域备受关注。
随着对可再生能源的需求不断增加,传统的锂离子电池面临着容量限制、成本高昂等问题,而钠离子电池因其钠资源丰富、成本低廉等优势,被认为是一种具有广阔应用前景的替代技术。
钠离子电池的研究与开发已经取得了一系列重要进展,但是仍然面临着诸多挑战。
本文将对钠离子电池的研究现状、关键技术及未来发展方向进行综述。
钠离子电池的研究起源于对锂离子电池的改进和替代。
传统的锂离子电池具有能量密度高、循环寿命长等优点,但是由于锂资源有限、成本较高,限制了其在大规模能源储存应用中的广泛应用。
相比之下,钠资源相对丰富,价格低廉,因此钠离子电池被看作是一种潜在的替代技术。
钠离子电池的正极材料一般采用氧化钠、磷酸铁锂等,负极材料则可选用石墨等材料。
其中,氧化钠作为正极材料具有较高的电压和能量密度,但是其化学稳定性较差,循环寿命短。
磷酸铁锂具有较好的循环性能和稳定性,但是能量密度较低。
石墨作为钠离子电池的负极材料稳定性较好,但是容量较低。
因此,钠离子电池正负极材料的设计优化是当前研究的重点之一。
除了材料选择外,电解液的选择也对钠离子电池的性能影响巨大。
目前常用的电解液主要包括有机电解液和固态电解液。
有机电解液具有传导性好、界面稳定等优点,但是存在着挥发性差、热稳定性差等问题。
固态电解液具有高的安全性、耐高温性等优点,但是目前还存在着导电率低、固溶度低等问题。
因此,寻找一种具有高导电率、高固溶度、优越的界面稳定性的电解液对于钠离子电池的发展至关重要。
另外,钠离子电池的循环寿命、安全性等性能也是当前研究的热点和难点。
循环寿命受到正负极材料的结构稳定性、充放电过程中电解液对材料的影响等因素影响。
目前的研究主要集中在设计新型材料、优化电解液配方、改进电池结构等方面,以提高钠离子电池的循环寿命。
此外,提高钠离子电池的安全性也是当前研究亟待解决的问题。
钠离子电池在充放电过程中会产生较大的体积变化,可能引起电极材料破裂、内部短路等问题,进而导致电池短路、爆炸等安全隐患。
钠离子电池英文综述文章Sodium-Ion Batteries: A Comprehensive ReviewSodium-ion batteries have emerged as a promising alternative to the widely used lithium-ion batteries, offering a more abundant and cost-effective solution for energy storage applications. As the global demand for energy continues to rise, the need for reliable and sustainable energy storage technologies has become increasingly critical. In this comprehensive review, we will explore the fundamental principles, materials, and advancements in sodium-ion battery technology, highlighting its potential to contribute to a more sustainable energy future.The basic working principle of sodium-ion batteries is similar to that of lithium-ion batteries, where the reversible intercalation and deintercalation of sodium ions between the anode and cathode materials drive the charge and discharge processes. However, the larger ionic radius of sodium compared to lithium presents unique challenges in the design and development of sodium-ion battery components.One of the key advantages of sodium-ion batteries is the abundanceand low cost of sodium resources, which are more widely available compared to lithium. This makes sodium-ion batteries a more attractive option for large-scale energy storage applications, such as grid-scale energy storage and electric vehicle charging infrastructure. Additionally, the safety profile of sodium-ion batteries is generally considered to be better than that of lithium-ion batteries, as the use of metallic sodium anodes can be avoided, reducing the risk of thermal runaway and fire hazards.In terms of anode materials, researchers have explored a variety of options to address the challenges posed by the larger sodium ion size. Carbon-based materials, such as hard carbon and graphite, have been extensively studied as anode materials due to their ability to accommodate sodium ions and their relatively low cost. However, the capacity and cycling performance of these materials are often limited. Alternative anode materials, including transition metal oxides, alloys, and conversion-type materials, have also been investigated to improve the energy density and rate capability of sodium-ion batteries.On the cathode side, the development of suitable materials has been a significant focus of research in the field of sodium-ion batteries. Layered transition metal oxides, such as NaNi0.5Mn0.5O2 andNaFe0.5Mn0.5O2, have shown promising performance as cathode materials, with high specific capacities and good cycling stability.Polyanionic compounds, like Na3V2(PO4)3, have also been explored due to their structural stability and high operating voltages.In addition to the development of anode and cathode materials, the electrolyte system plays a crucial role in the performance and safety of sodium-ion batteries. Researchers have investigated various electrolyte compositions, including organic liquid electrolytes, solid-state electrolytes, and hybrid electrolytes, to optimize ionic conductivity, electrochemical stability, and safety.The advancement of sodium-ion battery technology has also been driven by the development of novel cell designs and architectures. Three-dimensional structured electrodes, hierarchical porous materials, and composite materials have been explored to enhance the energy and power densities of sodium-ion batteries, as well as to improve their rate capability and cycling stability.Moreover, the integration of sodium-ion batteries into energy storage systems, such as grid-scale energy storage and electric vehicles, has been a growing area of research and development. The scalability, safety, and cost-effectiveness of sodium-ion batteries make them a promising candidate for these applications, where the need for reliable and sustainable energy storage solutions is paramount.In conclusion, sodium-ion batteries have emerged as a viable alternative to lithium-ion batteries, offering a more abundant and cost-effective solution for energy storage applications. The continuous advancements in anode and cathode materials, electrolyte systems, and cell designs have contributed to the improvement of sodium-ion battery performance, paving the way for their widespread adoption in various energy storage sectors. As research and development in this field continue to progress, the future of sodium-ion batteries looks promising, with the potential to play a significant role in the transition towards a more sustainable energy future.。
钠离子电池研究进展一、本文概述随着全球能源需求的持续增长,以及对环境保护和可持续发展的日益关注,高效、环保、可再生的能源存储技术已成为当前研究的热点。
其中,钠离子电池作为一种新型的二次电池,凭借其原料丰富、成本低廉、环境友好等优势,近年来受到了广泛的关注。
本文旨在综述钠离子电池的研究进展,包括其基本原理、材料体系、制造工艺以及应用前景等方面的内容,以期为钠离子电池的进一步研究和应用提供参考和借鉴。
通过深入了解钠离子电池的研究现状和发展趋势,我们有望为未来的能源存储技术找到更加环保、经济、高效的解决方案。
二、钠离子电池的基本原理与结构钠离子电池(Sodium-ion Batteries,SIBs)是一种新型的可充电电池技术,其基本原理与已广泛应用的锂离子电池(LIBs)相似,主要区别在于阳离子从锂变为钠。
钠离子电池的核心组成部分包括正极、负极、电解质以及隔膜。
正极材料:正极是钠离子电池的重要组成部分,其性能直接影响电池的能量密度和循环寿命。
目前,研究者们已经开发出多种适用于钠离子电池的正极材料,如层状氧化物(如NaCoO₂、NaMnO₂等)、聚阴离子型化合物(如NaFePO₄、Na₃V₂(PO₄)₃等)以及普鲁士蓝类似物等。
这些材料具有高的钠离子存储容量和良好的结构稳定性,使得钠离子电池具有较高的能量密度和循环稳定性。
负极材料:负极材料在钠离子电池中同样扮演着关键角色。
目前,碳基材料(如硬碳、石墨等)是最常用的钠离子电池负极材料,它们具有较高的比容量和良好的循环性能。
研究者们还在探索其他新型负极材料,如金属氧化物、硫化物和合金等,以进一步提高钠离子电池的性能。
电解质:电解质是钠离子电池中连接正负极的关键部分,负责离子的传输。
常用的电解质包括有机液体电解质、无机固体电解质和聚合物电解质等。
这些电解质需要具有良好的离子导电性、化学稳定性和机械强度,以确保电池的安全性和性能。
隔膜:隔膜位于正负极之间,用于防止电池内部短路。
钠离子电池近年来,随着电子设备、电动工具、小功率电动汽车等迅猛发展,研究高能效、资源丰富及环境友好的储能材料是人类社会实现可持续性发展的必要条件。
为满足规模庞大的市场需求,仅依靠能量密度、充放电倍率等性能衡量电池材料是远远不够的。
电池的制造成本与能耗是否对环境造成污染以及资源的回收利用率也将成为评价电池材料的重要指标。
电池发展有以下显著特点:绿色环保电池发展迅猛;一次电池向二次电池转化,这有利于节约地球有限的资源,符合可持续发展的战略;电池进一步向小、轻、薄方向发展。
钠是地球上储量较丰富的元素之一,与锂的化学性能类似,因此也可能适用于锂离子电池体系。
钠离子电池相比锂离子电池有诸多优势,如成本低,安全性好,随着研究的深入,钠离子电池将越来越具有成本效益,并有望在未来取代锂离子电池而被广泛应用。
1钠离子电池电化学原理同为元素周期表第I主族的钠离子和锂离子的性质有许多相似之处,钠离子完全有可能和锂离子电池一样构造一种广泛使用的二次电池。
并且钠离子电池与锂离子电池相比,原材料成本比锂离子电池低,半电池电位(E0Na+/Na=E0Li+/Li+0.3)比锂离子电池高,适合采用分解电压更低的电解液,因而安全性能更佳。
钠离子电池不以钠作为负极,而是由硬碳或嵌入化合物组成。
(1)钠离子电池优点:依据目前的研究进展,钠离子电池与锂离子电池相比有3个突出优势:①原料资源丰富,成本低廉,分布广泛;②钠离子电池的半电池电势较锂离子电势高0.3~0.4 V,即能利用分解电势更低的电解质溶剂及电解质盐,电解质的选择范围更宽;③钠离子电池有相对稳定的电化学性能,使用更加安全。
(2)钠离子电池缺陷:钠离子电池也存在着缺陷,如钠元素的相对原子质量比锂高很多,导致理论比容量小,不足锂的1/2;钠离子半径比锂离子半径大(Na+半径:95pm,Li+半径:60pm),使得钠离子在电池材料中嵌入与脱出更难。
下图为钠离子电池的电极材料:2钠离子电池正极材料用于钠离子电池正极的材料主要有贫钠的Na x CoO2、Na x MnO2层状晶体化合物及它们的掺杂化合物。
这些化合物的存在形态取决于其组成(x值)和制备方法。
其它一些见诸报道的嵌入式正极材料有:NaxTiS2,NaxNbS2Cl2,NaxWO3-y,NaxV0.5Cr0.5S,NaxMoS3(非定形),NaxTaS2,各式中0<x<2,0<y<1。
2.1五氧化二钒(V2O5)五氧化二钒(V2O5)是阿贡国家实验室和芝加哥大学的研究小组开发的一种可用于充电钠离子电池的正极材料。
这种双层五氧化二钒(V2O5)材料可用于室温下,具有250mAh/g的比容量,接近理论比容量,倍率放电能力和循环寿命优良,电池的比能量和比功率高达760Wh/kg和1200W/kg。
用双层V2O5材料作钠离子电池正极的充放电反应机理如图所示,电化学反应改变了五氧化二钒层的静电吸引力,可为钠离子(Na+) 提供强大的迁移动力; 钠离子嵌入到V2O5的过程如图所示。
由图上可以看出,钠离子的嵌入可导致钒的整体结构有序化,同时层间长程有序。
钠脱出后,这种长程有序也消失,而层内结构仍保存着。
这个研究小组的方法是,要使钠离子嵌入,就要使用纳米材料,这种材料具有双层层状结构,可调层间距,能适应很大的体积变化。
非原位和原位同步特性研究表明,钠离子的嵌入可导致钒的整体结构有序化,同时层间长程有序。
钠脱出后,这种长程有序也消失,而层内结构仍保存着。
因此,通过优化平衡静电力,诱导纳米材料的排列,会取得尽可能高的电极容量。
这种开放式框架结构具有好的“弹性”和卓越的长期稳定性,可使双层五氧化二钒成为一种合适的可用于高能量密度钠充电电池的正极材料。
2.2 单晶Na0.44MnO2纳米线高功率钠离子蓄电池近年来吸引了越来越多人的兴趣,因此,急需开发一种纳米结构的电极材料,因为纳米材料具有很高的比表面积,缩短了钠离子的扩散距离,所以使电池具有高的功率密度。
用水热法合成的单晶Na0.44MnO2纳米线,可用于钠离子电池。
将0.1g的Mn3O4粉末分散在NaOH溶液中(40ml/5mol/l),然后将溶液放在Teflon-lined高压锅(45ml)中,在205℃加热96h。
之后,冷却反应物,过滤沉淀物,用水反复冲洗,然后在室温下真空干燥。
SEM和TEM实验证明水热法合成Na0.44MnO2具有单晶纳米线形貌。
实验证明,该材料的可逆比容量为120mAh/g。
另外,单晶Na0.44MnO2纳米线具有高的充放电倍率循环性能和循环稳定性,因此是一种非常有前途的钠离子电池正极材料。
2.3 可逆NaFePO4电极通过置换橄榄石LiFePO4中Li的置换可获得橄榄石型NaFePO4正极。
实验证明橄榄石型NaFePO4电极是一种非常有潜力的钠离子电池电极材料。
这种材料中,理论比容量最大的为橄榄石结构NaFePO4,为154 mA·h/g。
但和LiFePO4的不同点是,NaFePO4最稳定存在的相是磷铁钠矿结构,该结构Na+占据4c 的Wyckoff 点阵位置,Fe2+占据4a点阵位置。
这点刚好与LiFePO4相反,Li+ 占据4a位置,Fe2+占据4c 位置。
导致这种结构差异的可能原因是Na 离子半径比Li 大。
NaFePO4材料在60 ℃,C/24倍率下,充放电的首次比容量达到147 mA·h/g。
但这种材料到目前为止没有得到良好的循环性能,有待更多的深入研究。
2.4 Na x CoO2及其参杂化合物在NaxCoO2化合物中,Na+主要位于层状(CoO2)n八面体之间:数量少时,钠离子间呈三棱柱状排列;数量多时,它们则配位成八面体。
尽管NaxCoO2化合物电性能较优,但钴盐价格昂贵,使得电池成本大幅上升,故出现了其它各种替代材料。
2.5 NaxMnO2及其参杂化合物3 钠离子电池的负极材料3.1碳材料用石墨作负极,由于钠离子在石墨层间迁移需要高跃迁能,脱/嵌困难。
钠金属会形成枝晶,如锂金属一样。
钠金属的安全性也受到质疑,因为其熔点只有97.7℃,而锂金属为180.5℃。
硬碳被认为可以作为负极材料,钠合金是否能作为负极材料也正被广泛的研究。
在实验室中应用较多的钠离子电极负极材料有各类碳材料,如石墨,乙炔黑,中间相碳微球(MCMB),它们的电化学性能与各自的结构和含氢量密切相关,一般的规律是:晶粒小,比表面积大,与电解质接触面也大,从而用来形成保护层所消耗的电解质也多;而含氢量越多,容量滞后也越大。
中间相碳微球(MCMB)的制备及其电化学性能已有详细的研究,与不经处理和经高温(3 000℃)处理的MCMB相比,750℃热处理后的MCMB电化学性能最优,这是因为它未完全失氢和适中的石墨化程度。
报道称其比容量达750mAh/g,为石墨理论比容量372mAh/g(NaC6)的两倍多;石墨化缺陷则避免了无谓的有机溶剂分解,又是低温制备,可见,这是一种较为理想的负极材料。
3.2合金另一类重要的负极材料是钠合金,其制备是将单质钠与其它金属按一定比例在惰性气氛中于合适温度下熔融,再经退火结晶即可。
目前研究较多的是钠的二元与三元合金,可与钠制成负极用合金的元素有:Pb,Sn,Bi,Ga,Ce,Si等,选择这些金属的原因是:可增加负极材料与电解质的相容性,防止在过充电时生成枝晶,增加了安全性,故能延长电池的使用寿命;且它们氢过电位较高,能减少电池的自放电反应,从而提高电池的贮存性能。
合金负极的缺点是降低了比能量,如Na15Pb4/P2NaxCoO2系统为350Wh/kg,是Na/P2 NaxCoO2系统的3/4左右,但其高体积比能量仍然很有吸引力(Na15Pb4/P2 NaxCoO21500Wh/L,与Na/P2 NaxCoO21600 Wh/L接近)。
另外,出于环保考虑,应尽量避免使用重金属(如Pb)作为钠的合金化元素。
有学者对利用高分子掺杂以改变合金晶型以及提高其比容量作了相应的研究。
3.3金属氧化物材料4 电解质按其存在状态讲,钠离子二次电池的电解质有液态和固态两类之分。
与锂离子二次电池相似,用于钠离子电池的液态电解质也是由钠盐溶于有机溶剂中,钠盐一般可以为:NaPF6,Na-ClO4,NaAlCl4,NaFeCl4,NaSO3CF3,NaBF4,NaBCl4,NaNO3, NaPOF4,NaSCN,NaCN,NaAsF6,NaCF3CO2,NaSbF6,NaC6H5CO2,Na(CH3 )C6H4SO3,NaHSO4,NaB(C6H5)4等等;对有机溶剂则有以下要求:介电常数大,熔点低(常温时为液态),钠离子导电能力强。
为满足前叙几点要求,电解质溶剂一般为无水二元组分,其成分可以是碳酸乙烯酯(EC),碳酸丙烯酯(PC),碳酸二乙酯(DEC),1,2-二甲氧基乙烷(DME),四氢呋喃(THF),2-甲基四氢呋喃(2-MTHF)等。
在最终配制成的电解质中,Na+摩尔浓度以1mol/L左右为宜。
液态电解质配置要求高(无水)、易泄漏、不安全(如造成单质金属负极生成枝晶,导致电池内部短路而发生爆炸)。
特别是以单质钠为电池负极材料时,它与液态电解质间的反应造成该类电池发展困难。
使用合金负极是一种方案,但合金中钠离子扩散困难,而且在多次循环之后,其体积有显著变化。
另外一种解决方案是改进电解质,即在选择适当溶剂的同时,加入添加剂。
但人们也在寻找新型电解质材料,近年来发展较快的聚合物电解质就是一个典型的例子。
一般来讲,所谓聚合物电解质就是将盐类物质以掺杂的形式混入聚合物制成导电(主要是离子导电)的高分子。
常见的用作固体聚合物电解质(Solid Polymer Electrolyte,SPE)的高聚物有聚氧化乙烯、聚苯胺、聚吡咯、乙烯丙烯酸共聚物、聚四氟物等,按高聚物的构型不同,它们可分别形成线形高分子电解质、梳状高分子电解质、交联网络高分子电解质等不同种类的聚合物电解质。
碱金属盐则有NaI、NaBH4、NaBF4以及聚磷酸钠等,它们一般都有带负电荷的大体积阴离子。
将来开发新盐时可考虑:①有宽的电化学窗,②与聚合物基体形成低共熔复合材料,③阴离子结构对称或柔顺,有增塑作用。
这类高分子复合材料的导电性可能是导电通道、隧道效应和场致发射三种机理作用的竞争结果。
而已发现的PEO-NaBH4体系中,由于阴离子配对的阻碍作用,降低了离子导电性。
为满足充电电池的导电需要,应要求SPE的离子导电性在10-3S/cm以上。
然而在盐类掺杂后所获得的固态聚合物电解质的离子导电性能尚不能达到这一水平。
因此,今后这方面的研究工作应侧重于开发出对正、负极材料具有稳定性的同时又具有较高的离子导电性的固体聚合物电解质。
Nasicon也是近十几年发展起来的一种钠离子导体,它是由钠、锆、硅、磷、氧5种元素构成的复合电解质。