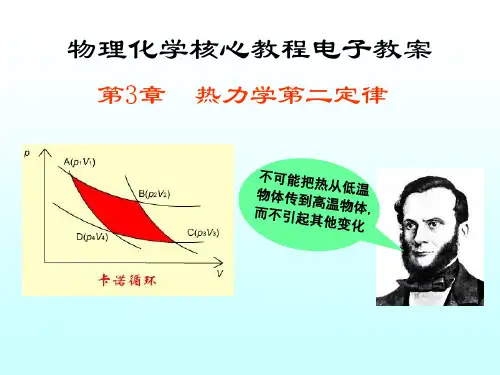
物理化学电子教案-第三章-热力学第二定律
- 格式:ppt
- 大小:3.53 MB
- 文档页数:133









物理化学The Second Law of Thermodynamics 版权所有:武汉科技大学化学工程与技术学院Copyright © 2015 WUST. All rights reserved.•掌握热机效率的表达、卡诺循环及其重要结论;•掌握热力学第二定律以及由第二定律导出卡诺定理的方法,卡诺定理的推论;•掌握克劳修斯等式和状态函数-熵,克劳修斯不等式和熵增原理,熵判据;•掌握系统熵变(简单pVT变化、相变过程、化学变化)及环境熵变的计算;•掌握热力学第三定律的普朗克表述及熵的物理意义,理解规定摩尔熵、标准摩尔熵、标准摩尔反应熵及能斯特热定理。
•掌握亥姆霍兹自由能和吉布斯自由能定义、亥姆霍兹自由能判据、吉布斯自由能判据,理解亥姆霍兹自由能变和吉布斯自由能变的物理意义及计算,理解可逆与平衡、不可逆与自发的关系;•理解热力学基本方程和热力学关系式(麦克斯韦关系、对应系数关系,其它重要关系);•掌握热力学第二定律应用实例——克拉佩龙方程、克劳修斯-克拉佩龙方程。
本章主要内容§3.1 卡诺循环§3.2 热力学第二定律§3.3 熵增原理§3.4 单纯pVT变化熵变的计算§3.5 相变过程熵变的计算§3.6 热力学第三定律和化学变化过程熵变计算§3.7 亥姆霍兹函数和吉布斯函数§3.8 热力学基本方程§3.9 克拉佩龙方程§3.10 吉布斯-亥姆霍兹方程和麦克斯韦关系式§3.1 热力学第二定律•自发过程举例•自发过程逆向进行必须消耗功•自发过程的共同特征•热力学第二定律出现问题1.符号:宏观量与微观量2.单位:3.公式4.解题过程:d d δ δU H W Q U H W Q ∆∆d d W Q W Q U H∆∆不带单位计算;单位混用;简写Rδd amb W p V =- () =W pV W pV W pV H U W==-=∆∆∆-缺少必要说明、过程错结果正确amb d W p V=-,m 21amb 21()()V nC T T p V V -=--222p V nRT =由于绝热Q = 0,故∆U =W)1(22)1(11γγγγ--=p T p T W = ∆U = n C V , m (T 2-T 1)2211d d V V amb V V nRT W p V V V=-=-⎰⎰W = -p amb ∆V(1)(2)(3)(4)1. 自发过程举例自发变化某种变化有自动发生的趋势,一旦发生就无需借助外力,可以自动进行,这种变化称为自发变化。