丙烯腈介绍报告
- 格式:ppt
- 大小:297.00 KB
- 文档页数:39

22 丙烯腈生产丙烯腈是三大合成材料的重要单体,是精细化工产品的重要原料,它的合成在基本有机化工中占有相当重要的地位。
本节就丙烯腈生产,特别是对丙烯氨氧化法生产丙烯腈的工艺 进行讨论。
1 •概述 (1)丙烯腈的性质和用途丙烯腈是无色、易挥发的透明液体,剧毒、微臭、有桃仁气味。
沸点77. 3C ,凝固点3一 83. 5 C,密度806 kg •m , 25C 时在空气中的爆炸浓度范围为3.05 %〜17 % (体积分数)。
能溶于丙酮、苯、四氯化碳、乙醚、乙醇等有机溶剂,微溶于水,并能与水、苯和异丙醇形 成共沸物。
丙烯腈的分子式是 GHN,结构式为 CH=CHCN 能发生聚合、加成、氰基和氰乙基化等 反应。
聚合和加成反应都发生在丙烯腈的C=C 双键上,纯丙烯腈在光的作用下能自行聚合。
在浓碱存在的条件下能强烈聚合,它还能与苯乙烯、丁二烯、乙酸乙烯、氯乙烯、丙烯酰胺 等中的一种或儿种发生共聚反应。
典型的丙烯腈加成反应有电解加氢偶联反应制取已二腈 等;氰基反应包括水合反应、水解反应、醇解反应及烯烃的反应等,如丙烯腈和水在铜催化剂存在下,直接水合制取丙烯酰胺;氰乙基化反应有丙烯腈与醇制取烷氧基丙胺等。
丙烯腈的用途非常广泛,图2—25展示了丙烯腈的主要用途。
聚丙烯腈(腈纶)保暖性和弹性都很好,有耐磨和轻而柔的特点,可作毛线、衣物等; ABS 塑料耐冲击强度好.有较好的抗张强度、刚性、硬度和耐低温性能等,可用作管材、仪表外壳及设备零件等;丁腈橡胶 有良好的耐油性、耐磨损、耐溶剂等性能,主要用作胶管、垫圈等;丙烯腈水解生产丙烯酰 胺、电解加氢二聚生产己二腈、涂料和尼龙等;丙烯腈与醇反应制取的烷氧基丙胺可作分散 剂、表面活性剂等。
-忒 ------ ---- 彳网烯酰胺| 电解帕臥-聚图2-25 丙烯胎的用途(2) 生产丙烯腈的原料和方法丙烯腈于1893年在法国的 Mourea 实验室合成成功,早期的生产方法是用较昂贵的 G结构单元如环氧乙烷、乙炔和乙醛等为原料与氢氰酸反应而制得的。

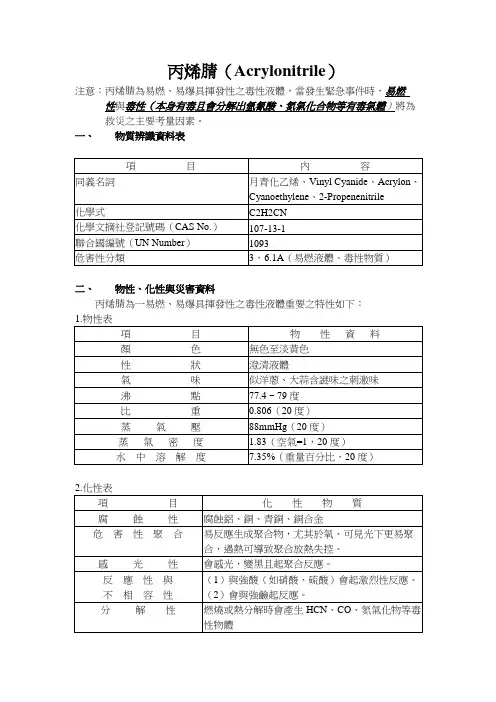
丙烯腈(Acrylonitrile)注意:丙烯腈為易燃、易爆具揮發性之毒性液體,當發生緊急事件時,易燃性與毒性(本身有毒且會分解出氫氰酸、氮氣化合物等有毒氣體)將為救災之主要考量因素。
一、物質辨識資料表二、物性、化性與災害資料丙烯腈為一易燃、易爆具揮發性之毒性液體重要之特性如下:三、防災設備丙烯月青之救災須針對人員防護、火災爆炸預防及洩漏控制等方面選用適當防災器材設備:附註:依據毒性化學物質管理法施行細則第18條及第20條之規定,丙烯月青之運作場所需裝設偵測及警報設備。
四、中毒症狀丙烯月青可經由呼吸道、皮膚或誤食而使人體中毒,早期中毒徵候為眼睛腫痛、頭暈、頭痛甚至嘔吐,引起神經系統、消化系統及皮膚粘膜等之危害,再高濃度時產生意識不明及呼吸停止造成死亡。
4.眼睛接觸之症狀眼睛接觸丙烯月青會引起流淚,而其蒸氣及液體可能造成嚴重的刺激及損害。
五、急救方式丙烯月青中毒之搶救者須按前述救災設備中之個人防護設備完整穿戴,方可進入災區救人。
而丙烯月青中毒之急救最重要是將患者迅速搬離現場至通風處,檢查患者之中毒症狀,判斷出中毒路徑給予適當之救護。
丙烯月青之解毒劑為亞硝酸戊酯(吸)、亞硝酸鈉(針劑)、硫代硫酸鈉。
3.皮膚接觸性傷害之急救七、救災方式及災後處理3.災後之處理(1)需對洩漏區進行通風換氣,且其清理工作需由受過遜之人員負責(2)以細沙吸收洩漏液後,小心得將污沙移入密閉桶中,產生之廢棄物一相關法規處理(3)大量洩漏時以合適幫浦回收處理(需防騎易燃性)(4)事後可以使用5%碳酸鈉(Sodium carbonate)與5%磷酸鈉(Sodium phosphate tribasic)水溶液和水當作人員或污燃處之除污,產生之廢水應導入廢水處理場。

一.丙烯腈的概况1.丙烯腈的概况中文名称:丙烯腈;氰乙烯;2-丙烯腈;乙烯基氰英文名称:Acrylonifrile;Cyanoethyene;2-Propenenitrile;Vinyl cyanide分子式:C3H3NC A S 号:107-13-1卫生标准:我国车间空气中丙烯腈的MAC为mg/m3。
丙烯腈,是一种无色易燃易挥发的液体,具有特殊的杏仁气味。
微溶于水,其低浓度水溶液很不稳定,易溶于一般溶剂。
水解时生成丙烯酸,还原时生成丙腈。
易聚合,也能与醋酸乙烯、氯乙烯等单体共聚。
丙烯腈是重要的有机合成原料,主要由于制造聚丙烯腈纤维(腈纶)、丁腈橡胶、ABS树脂、AS树脂、聚丙烯酰胺、丙烯酸酯类、已二腈、抗水剂和粘胶剂等。
也用于其他有机合成和医药工业中,并用作谷类熏蒸剂等。
此外,本品也是一种非质子型极性溶剂。
丙烯腈属于高毒类,进入人体后可引起急性中毒和慢性中毒。
加热时在光、碱和过氧化物作用下,本品发生聚合。
遇热发生猛烈的燃烧和爆炸,分解生成含有一氧化碳、氮氧化物、氰化氢的有毒烟雾。
本品系强烈还原剂,可与氧化剂剧烈反应。
与碱剧烈反应,引起火灾和爆炸。
2.丙烯腈理化特性丙烯腈无色、高毒、易挥发液体,有特殊杏仁味。
蒸气与空气混合物可燃限3.05~17% 。
与许多有机溶剂混溶; 水中溶解度7.35%(20℃)。
腐蚀铜和铜合金,穿透皮革,高浓度腐蚀铝。
接触光或过量热引起自发聚合,有碱存在剧烈聚合并放热。
遇热、明火或氧化剂易燃、爆炸。
加热或燃烧,可产生氰化氢和氮氧化物。
化学式:CH2=CH-CN分子量:53.1性状:无色或淡黄色液体,有特殊气味。
沸点:77℃熔点:-83.5℃相对密度:1.83(水=1)蒸气压:11.0KPa(20℃)闪点:-1.1℃自然温度:481℃爆炸极限:在空气中3.0%~17%(体积)油水分配系数:辛醇/水分配系数的对数值为-0.923.丙烯腈包装储运须知包装标志:易燃液体。
副标志:毒害品。

丙烯腈目录表一、丙烯腈概述 (2)二、世界丙烯腈生产概况 (2)三、市场分析及预测 (3)1、国际市场分析 (3)2、国内市场分析 (3)四、发展 (4)五、物理性质 (4)六、用途 (5)七、制备原理 (6)八、生产工艺流程 (7)1、操作条件 (7)2、工艺流程 (9)3、三废治理 (10)九、主要工艺技术指标和特点 (10)一、丙烯腈概述【名称】:丙烯腈【化学式】:CH2═CHCN【化学性质】:分子量 53.06丙烯腈是一种无色的有辛辣气味液体,属大众基本有机化工产品,是三大合成材料——合成纤维、合成橡胶、塑料的基本且重要的原料,在有机合成工业和人民经济生活中用途广泛。
丙烯腈是我国丙烯的第二大衍生物,2003年,我国丙烯腈的产量约为56.0万吨,消费丙烯约62.7万吨,约占全国丙烯总消费量的10.2%;2004年产量约为58.0万吨,消费丙烯约为65.0万吨,比2003年增长约3.7%。
二、世界丙烯腈生产概况全世界丙烯腈的生产主要集中在美国、西欧和日本等国家和地区。
目前,全世界丙烯腈总生产能力为6658 kt/a。
美、日、西欧丙烯腈生产能力合计为4063 kt/a,占世界总能力的61%。
美国是世界上丙烯腈最大的生产国与出口国,现有丙烯腈生产装置6 套,主要生产厂家为BP化学、Sterling、Monsanto、American Cyanamid、Solutia公司等。
BP公司丙烯腈生产能力占世界总丙烯腈生产能力的11.7%,占有份额最大。
目前美国生产能力为1892 kt/a,约占世界总生产能力的28.4%。
美国丙烯腈出口量几乎占本国产量的50%,主要出口到远东,预计如此高的出口比例可一直延续到2005年。
西欧丙烯腈的生产装置共有9 套,主要集中于德国Erdoelchenie、BASF、PCK公司,意大利EniChem公司,荷兰的DSM公司,西班牙Repsol公司。
西欧总生产能力约为1315 kt/a,占全球总生产能力的19.8%。

丙烯腈简介丙烯腈属大众基本有机化工产品,是三大合成材料——合成纤维、合成橡胶、塑料的基本且重要的原料,在有机合成工业和人民经济生活中用途广泛。
有机合成中引入氰乙基。
谷类烟熏剂。
合成表面活性剂和抗氧剂。
丙烯腈用来生产聚丙烯纤维(即合成纤维腈纶)、丙烯腈-丁二烯-苯乙烯塑料(ABS)、苯乙烯塑料和丙烯酰胺(丙烯腈水解产物)。
另外,丙烯腈醇解可制得丙烯酸酯等。
丙烯腈在引发剂(过氧甲酰)作用下可聚合成一线型高分子化合物——聚丙烯腈。
聚丙烯腈制成的腈纶质地柔软,类似羊毛,俗称“人造羊毛”,它强度高,比重轻,保温性好,耐日光、耐酸和耐大多数溶剂。
丙烯腈与丁二烯共聚生产的丁腈橡胶具有良好的耐油、耐寒、耐溶剂等性能,是现代工业最重要的橡胶,应用十分广泛。
可以丙烯、氨、空气为原料,采用直接氧化法生产丙烯腈。
目录第一部分:化学品名称第二部分:成分/组成信息第三部分:危险性概述第四部分:急救措施第五部分:消防措施第六部分:泄漏应急处理第七部分:操作处置与储存第八部分:接触控制/个体防护第九部分:理化特性第十部分:稳定性和反应活性第十一部分:毒理学资料第十二部分:生态学资料第十三部分:废弃处置第十四部分:运输信息第十五部分:管制信息第十六部分:质量指标第十七部分:事故案例第一部分:化学品名称化学品中文名称:丙烯腈(抑制了的)化学品英文名称:acrylonitrile中文名称2:乙烯基氰,氰乙烯英文名称2:cyanoethylene,Vinylcyanide,2-Propenenitrile技术说明书编码:255CAS No.:107-13-1分子式:C3H3N / CH2=CH-CN结构式:三维模型结构简式:H2CCHCN分子量:53.06第二部分:成分/组成信息有害物成分含量CAS No.丙烯腈(抑制了的) ≥99% 107-13-1第三部分:危险性概述危险性类别:极毒、易燃易爆、可疑致癌物。
物理危险性:蒸汽比空气重,可能沿地面流动,可能造成远处着火。

第一章 综述1.1 丙烯腈简述丙烯腈是非常重要的有机的化工产品,丙烯腈在丙烯系列的产品当中是比较重要的,在世界范围内,丙烯腈的产量在丙烯系列产品中仅仅少于聚丙烯,居于第二位。
丙烯腈也是重要的有机合成原料,由丙烯腈经催化水合克制得丙烯酰胺,由丙烯酰胺制得的聚丙烯酰胺是三次采油的重要助剂。
由丙烯腈经电解加氢偶联可制得已二腈,再加氢可制得已二胺,已二胺是生产尼龙的主要单体。
由丙烯腈还可以制得一系列精细化工产品,如谷氨酸钠、医药、农药熏蒸剂、高分子絮凝剂、化学灌浆剂、纤维改性剂、纸张增强剂、固化剂、密封胶、涂料和橡胶硫化促进剂等。
丙烯腈在常温常压在是一种没有颜色的液体,味道有些甜,微臭,它的沸点是77.3℃。
丙烯腈它是有毒的,在室内范围内允许的浓度是0.002mg/L 。
丙烯腈的分子当中含有氰基和C —C 双键,所以它的化学性质是活泼的,而且能够发生加成、聚合等反应,可以制出各种的合成橡胶、合成纤维、塑料、涂料等。
1.2 丙烯腈的合成方法在生产丙烯腈的历史上,曾采用过四种方法来生产。
(1)以环氧乙烷为原料的氰乙醇法:环氧乙烷和氢氰酸在水和三甲胺的存在下反应得到氰乙醇,然后以碳酸镁为催化剂,于200~280℃脱水制得丙烯腈,收率约为75%。
此方法生产的丙烯腈纯度较高,但是氢氰酸毒性大,生产成本也很高。
(2)乙炔法:乙炔和氢氰酸在氯化亚铜-氯化钾-氯化钠的稀酸盐的溶液的催化作用下,在80~90℃反应得到丙烯腈。
CN CH CH HCN CH CH -=→+≡2这种方法工艺过程简单,收率也不错,但是副反应比较多,产物精致困难,毒性也比较大,而且乙炔的原料价格要高于丙烯。
这种方法在1960年以前是全世界各国生产丙烯腈的主要方法。
(3)乙醛-氢氰酸氧化法:乙醛可以由依稀大量的廉价的制得,而且生产成本也比上面的两种方法低,但是就是由于后面紧接着出现了丙烯氨氧化法的工业化,所以说这种方法最终也没能得到发展下去。
(4)丙烯氨氧化法:这种方法最早是由美国的Sohio 公司研发成功的,并且于1960年建成了第一套工业化生产装置。

1 丙烯腈概述1.1 丙烯腈简介丙烯腈是一种重要的有机合成单体,在丙烯产品系列中居第二,仅次于聚丙烯,是三大合成材料(纤维、橡胶、塑料)的重要化工原料,主要用来生产聚丙烯腈纤维(腈纶)、丙烯腈- 丁二烯-苯乙烯(ABS)塑料、苯乙烯(AS)塑料、丙烯酰胺等。
丙烯腈在合成纤维、合成树脂等高分子材料中占有显著地位,应用前景广阔。
除此之外,丙烯腈聚合物与丙烯腈衍生物也广泛应用于建材及日用品中。
1.2 丙烯腈物化性质1.2.1 丙烯腈物理性质性状:无色或淡黄色液体,有特殊气味分子量:53.06沸点:77.3℃冰点:-83.5 ℃生成热:184.2 kJ/mol(25℃)燃烧热:1761.5 kJ/mol聚合热:72.4 kJ/mol蒸汽压:11.0KPa(20℃)闪点:0℃自燃点:481℃爆炸极限:在空气中3.0%~17%(体积)油水分配系数:辛醇/水分配系数的对数值为-0.92毒性:剧毒,毒作用似氢氰酸溶解性:溶于丙酮、苯、四氯化碳、乙醚、乙醇等有机溶剂,微溶于水1.2.2 丙烯腈化学性质丙烯腈由于分子结构带有C=C 双键及-CN 键,所以化学性质非常活泼,可以发生加成、聚合、腈基及氢乙基化等反应。
聚合反应和加成反应都发生在丙烯腈的C=C 双键上,纯丙烯腈在光的作用下能自行聚合,所以在丙烯腈成品及丙烯腈生产过程中,通常要加少量阻聚剂,如对苯酚甲基醚(阻聚剂MEHQ)、对苯二酚、氯化亚铜和胺类化合物等。
除发生自聚外,丙烯腈还能与苯乙烯、丁二烯、乙酸乙烯、丙烯酰胺等发生共聚反应,由此可制得合成纤维、塑料、涂料和胶粘剂等。
丙烯腈经电解加氢偶联反应可以制得已二腈。
氰基反应包括水合反应、水解反应、醇解反应等,丙烯腈和水在铜催化剂存在下,可以水合制取丙烯酰胺。
氰乙基化反应是丙烯腈与醇、硫醇、胺、氨、酰胺、醛、酮等反应;丙烯腈和醇反应可制取烷氧基丙胺,烷氧基丙胺是液体染料的分散剂、抗静电剂、纤维处理剂、表面活性剂、医药等的原料。

•CH2=CHCN,无色透明液体,蒸气有毒。
相对密度0.8060,熔点-83~-84℃,沸点77.3~77.4℃。
微溶于水,易溶于一般有机溶剂。
易燃烧,蒸气与空气形成爆炸混合物,爆炸极限 3.05%~17.0%(体积)。
水解时生成丙烯酸,还原时生成丙腈,易聚合,也能与醋酸乙烯、氯乙烯等单体共聚。
可由丙烯氨氧化,或由乙炔和氢氰酸直接化合而制得。
用于制造聚丙烯腈、丁腈橡胶和其它合成树脂等。
也用于电解制己二腈和水解成丙烯酸酰胺。
- 来源:化学物质辞典简称“AN”。
化学式CH2=CHCN。
分子量53.06。
一种共轭不饱和腈。
无色易燃液体。
有毒! 比重0.8060。
沸点77.3℃。
折光率1.3888 (25℃)。
略溶于水,易溶于一般有机溶剂。
分子中含氰基、碳-碳双键等,能参与各种反应:工业合成路线主要有下列几种:(1) 乙炔法:(2) 乙烯法:(3)丙烯氨氧化法: 参见“氨氧化反应”。
主要用以制合成纤维(丙烯腈纤维)、腈基橡胶 (丁腈橡胶,BAN)及ABS塑料 (丁二烯-丙烯腈-苯乙烯共聚物)等。
- 来源:化学词典化学式CH2=CHCN。
为无色、具杏仁气味、易燃、易挥发的液体。
比重0.8,沸点77.3℃,蒸气比重1.9,水中溶解度7.3%(20℃),易溶于有机溶剂。
是制备聚丙烯腈的单体,与依康酸、丁二烯、醋酸乙烯、苯乙烯、氯乙烯和偏氯乙烯等单体共聚。
用于制造合成纤维、合成橡胶、塑料和合成树脂等,故丙烯腈是有机合成工业中的重要单体。
本品属高毒类,毒作用似氰化氢。
主要经吸入或经皮肤进入人体,急性中毒症状与氰化氢中毒相似。
此外,尚可致接触性皮炎,表现为红斑、疱疹及脱屑,愈后可残留色素沉着;对眼也有强烈刺激作用。
预防重点是防止跑、冒、滴、漏;加强排风措施;使用手套、防毒口罩(活性炭滤料可吸附丙烯腈)等个人防护用品。
急救治疗同氰化氢,但用亚硝酸钠剂量宜较小。
车间空气中最高容许浓度为2mg/m3。
- 来源:卫生学大辞典分子式C3H3N,分子量53.05,结构简式CH2=CH—CN。

第一章综述1.1 丙烯腈简述丙烯腈是非常重要的有机的化工产品,丙烯腈在丙烯系列的产品当中是比较重要的,在世界范围内,丙烯腈的产量在丙烯系列产品中仅仅少于聚丙烯,居于第二位。
丙烯腈也是重要的有机合成原料,由丙烯腈经催化水合克制得丙烯酰胺,由丙烯酰胺制得的聚丙烯酰胺是三次采油的重要助剂。
由丙烯腈经电解加氢偶联可制得已二腈,再加氢可制得已二胺,已二胺是生产尼龙的主要单体。
由丙烯腈还可以制得一系列精细化工产品,如谷氨酸钠、医药、农药熏蒸剂、高分子絮凝剂、化学灌浆剂、纤维改性剂、纸张增强剂、固化剂、密封胶、涂料和橡胶硫化促进剂等。
丙烯腈在常温常压在是一种没有颜色的液体,味道有些甜,微臭,它的沸点是77.3℃。
丙烯腈它是有毒的,在室内范围内允许的浓度是0.002mg/L。
丙烯腈的分子当中含有氰基和C—C双键,所以它的化学性质是活泼的,而且能够发生加成、聚合等反应,可以制出各种的合成橡胶、合成纤维、塑料、涂料等。
1.2 丙烯腈的合成方法在生产丙烯腈的历史上,曾采用过四种方法来生产。
(1)以环氧乙烷为原料的氰乙醇法:环氧乙烷和氢氰酸在水和三甲胺的存在下反应得到氰乙醇,然后以碳酸镁为催化剂,于200~280℃脱水制得丙烯腈,收率约为75%。
此方法生产的丙烯腈纯度较高,但是氢氰酸毒性大,生产成本也很高。
(2)乙炔法:乙炔和氢氰酸在氯化亚铜-氯化钾-氯化钠的稀酸盐的溶液的催化作用下,在80~90℃反应得到丙烯腈。
=≡CH-+→CNCHCHHCNCH2这种方法工艺过程简单,收率也不错,但是副反应比较多,产物精致困难,毒性也比较大,而且乙炔的原料价格要高于丙烯。
这种方法在1960年以前是全世界各国生产丙烯腈的主要方法。
〔3〕乙醛-氢氰酸氧化法:乙醛可以由依稀大量的廉价的制得,而且生产成本也比上面的两种方法低,但是就是由于后面紧接着出现了丙烯氨氧化法的工业化,所以说这种方法最终也没能得到发展下去。
〔4〕丙烯氨氧化法:这种方法最早是由美国的Sohio 公司研发成功的,并且于1960年建成了第一套工业化生产装置。

2.15 丙烯腈丙烯腈,别名氰基乙烯,英文名Acrylonitrile(AN),是一种无色有辛辣气味的液体,易燃,有剧毒,分子式为C3H3N,分子量53.06,CAS号107-13-1,溶于水、乙醚、乙醇、丙酮、苯和四氯化碳,与水形成共沸物,易挥发,有腐蚀性。
丙烯腈属于高毒类化学品,进入人体后可引起急性中毒和慢性中毒。
丙烯腈是三大合成材料——合成纤维、合成橡胶、合成树脂的重要原料,主要用于生产腈纶、丙烯腈-丁二烯-苯乙烯(ABS)树脂/苯乙烯-丙烯腈(SAN)树脂、己二腈、丙烯酰胺、丁腈橡胶等。
丙烯腈主要生产工艺是丙烯氨氧化法,该法于1960年由美国Standard石油公司开发成功,又称Sohio法。
BP公司收购Sohio公司,拥有Sohio工艺,其他专利许可公司还包括日本旭化成公司、日东公司、Solutia公司和中国石油化工集团公司等。
目前全球95%以上的装置采用BP公司的丙烯氨氧化法技术。
正在开发的丙烯腈生产工艺,以丙烷为原料的丙烯腈合成工艺最值得关注。
催化剂的改进主导着丙烯腈新工艺的开发。
2.15.1世界供需分析及预测亚洲、北美和西欧是世界丙烯腈的主要生产地区。
2004年全球丙烯腈的生产能力为599万吨/年,2010年达到630万吨/年,2013年达到685万吨/年。
其中,2013年亚洲地区产能为388万吨/年,北美地区产能为156万吨/年,西欧地区产能为85.5万吨/年。
2008年之前世界丙烯腈的生产较为平稳,2008年的金融危机使得丙烯腈的生产有所下滑,产量下降,随后逐渐恢复。
2012年全球丙烯腈产量达到507.2吨,2013年为561.5万吨。
近年来,世界丙烯腈需求呈现向亚洲转移的趋势。
2013年,亚洲消费量达到361.4万吨,占全球消费量的64.7%,其次为北美和西欧,消费占比均约为13.4%。
表2.15-1 2013年世界各地区丙烯腈供需状况2.15.1.1 世界供应状况分析及预测目前丙烯腈生产的主要路线是一步氨氧化工艺,丙烯、氨和空气在流化床反应器中反应生成丙烯腈,并副产乙腈和氢氰酸。
丙烯腈市场分析报告1.引言1.1 概述丙烯腈是一种重要的化工原料,广泛用于合成合成纤维、树脂、橡胶和塑料等产品。
随着全球化和经济发展的趋势,丙烯腈市场也逐渐呈现出增长态势。
本报告将对丙烯腈市场进行全面分析,包括市场概况、需求分析、供给分析、市场发展趋势、竞争格局和前景展望等内容,为相关经营者和投资者提供参考和决策依据。
1.2 文章结构文章结构部分的内容可以包括本文的主要章节和内容安排,以及每个章节的重点内容和逻辑连接。
例如可以描述正文部分包括了丙烯腈市场概况、市场需求分析和市场供给分析,用以全面分析市场的现状和趋势。
结论部分包括了市场发展趋势、市场竞争格局和市场前景展望,用以总结分析并展望未来市场的发展方向。
文章布局合理,逻辑清晰,内容丰富,能够全面深入地分析丙烯腈市场的现状和未来发展趋势。
1.3 目的:本报告旨在通过对丙烯腈市场进行全面深入的分析,揭示其市场规模、发展趋势、竞争格局以及未来前景展望。
通过对市场需求和供给的分析,为相关行业的投资者、企业决策者提供决策参考,帮助他们更好地把握市场机会,规避风险。
同时,也旨在为相关研究者和行业从业者提供可靠的数据支持,促进丙烯腈市场的健康发展和可持续增长。
1.4 总结总的来说,通过对丙烯腈市场的概况、需求分析和供给分析,我们可以看到丙烯腈市场具有较高的发展潜力和市场需求。
市场发展趋势显示,丙烯腈市场将持续增长,并且市场竞争格局也将发生变化。
在未来,丙烯腈市场有望迎来更广阔的发展前景,对于投资者和相关产业也将带来更多机遇和挑战。
因此,我们对丙烯腈市场的未来展望是乐观的。
2.正文2.1 丙烯腈市场概况丙烯腈是一种重要的有机化工原料,也是合成纤维聚丙烯腈的主要原料之一。
丙烯腈市场在全球范围内具有广泛的需求和应用。
根据市场调研数据显示,丙烯腈市场在近年来呈现稳步增长的趋势。
首先,丙烯腈作为一种重要的合成纤维原料,在纺织、服装等行业中有着广泛的应用。
随着全球纺织产业的发展,对丙烯腈的需求不断增加。
丙烯腈丙烯腈⼀、简介丙烯腈是聚丙烯腈纤维的重要单体,属⼤宗基本有机化⼯产品,是三⼤合成材料——合成纤维、合成橡胶、塑料的基本且重要的原料,在有机合成⼯业和⼈民经济⽣活中⽤途⼴泛。
丙烯腈是合成纤维,合成橡胶和合成树脂的重要单体,也是杀⾍剂⾍满腈的中间体。
⼆、名称1、化学名称2-丙烯腈、⼄烯基氰2、商品名称三、系统编号CAS号107-13-1EINECS号:203-466-5四、物质颜⾊性状1、颜⾊⽆⾊2、性状3、相态液体4、臭味有⾟辣刺激性,有苦杏仁味5、挥发性五、化学结构1、化学组成2、化学式C3H3N3、分⼦量分⼦量:53.064、分⼦结构(结构式)CH2=CH-C≡N5、分⼦结构数据6、计算化学数据7、⽣态化学数据8、毒理学数据有毒六、物化性质1、物理性质1)、溶解性与⽔部分互溶,溶解性:微溶于⽔,易溶于多数有机溶剂。
2)、酸碱性3)、熔点熔点(℃):-83.64)、密度相对密度(⽔=1):0.81;相对蒸⽓密度(空⽓=1):1.83 5)、饱和蒸⽓压(kPa)其蒸⽓和空⽓形成爆炸性混合物。
饱和蒸⽓压(kPa):13.33(22.8℃) 6)、爆炸上下限极易燃,爆炸上限%(V/V):28.0爆炸下限%(V/V):2.8易燃,其蒸⽓与空⽓可形成爆炸性混合物。
遇明⽕、⾼热易引起燃烧,并放出有毒⽓体。
爆炸上限%(V/V):(17.0±5)%爆炸下限%(V/V):3.05%7)、凝固点8)、⽐热容(燃烧热)燃烧热(kJ/mol):1757.79)、沸点沸点(℃):77.310)、临界温度压⼒临界温度(℃):263临界压⼒(MPa):3.511)、⾟醇/⽔分配系数的对数值⾟醇/⽔分配系数的对数值:-0.9212)、闪点闪点(℃):-513)、引燃温度引燃温度(℃):4802、化学性质(化学反应)1)、腐蚀性2)、弱碱性3)、稳定性4)、沉淀性5)、络合性6)、还原性7)、氧化性与氧化剂、强酸、强碱、胺类、溴反应剧烈。
第一章综述1.1 丙烯腈简述丙烯腈是非常重要的有机的化工产品,丙烯腈在丙烯系列的产品当中是比较重要的,在世界范围内,丙烯腈的产量在丙烯系列产品中仅仅少于聚丙烯,居于第二位.丙烯腈也是重要的有机合成原料,由丙烯腈经催化水合克制得丙烯酰胺,由丙烯酰胺制得的聚丙烯酰胺是三次采油的重要助剂.由丙烯腈经电解加氢偶联可制得已二腈,再加氢可制得已二胺,已二胺是生产尼龙的主要单体.由丙烯腈还可以制得一系列精细化工产品,如谷氨酸钠、医药、农药熏蒸剂、高分子絮凝剂、化学灌浆剂、纤维改性剂、纸张增强剂、固化剂、密封胶、涂料和橡胶硫化促进剂等.丙烯腈在常温常压在是一种没有颜色的液体,味道有些甜,微臭,它的沸点是77.3℃.丙烯腈它是有毒的,在室内范围内允许的浓度是0.002mg/L.丙烯腈的分子当中含有氰基和C—C双键,所以它的化学性质是活泼的,而且能够发生加成、聚合等反应,可以制出各种的合成橡胶、合成纤维、塑料、涂料等.1.2 丙烯腈的合成方法在生产丙烯腈的历史上,曾采用过四种方法来生产.(1)以环氧乙烷为原料的氰乙醇法:环氧乙烷和氢氰酸在水和三甲胺的存在下反应得到氰乙醇,然后以碳酸镁为催化剂,于200~280℃脱水制得丙烯腈,收率约为75%.此方法生产的丙烯腈纯度较高,但是氢氰酸毒性大,生产成本也很高.(2)乙炔法:乙炔和氢氰酸在氯化亚铜-氯化钾-氯化钠的稀酸盐的溶液的催化作用下,在80~90℃反应得到丙烯腈.=≡CH-+→CNCHCHHCNCH2这种方法工艺过程简单,收率也不错,但是副反应比较多,产物精致困难,毒性也比较大,而且乙炔的原料价格要高于丙烯.这种方法在1960年以前是全世界各国生产丙烯腈的主要方法.〔3〕乙醛-氢氰酸氧化法:乙醛可以由依稀大量的廉价的制得,而且生产成本也比上面的两种方法低,但是就是由于后面紧接着出现了丙烯氨氧化法的工业化,所以说这种方法最终也没能得到发展下去.〔4〕丙烯氨氧化法:这种方法最早是由美国的Sohio 公司研发成功的,并且于1960年建成了第一套工业化生产装置.O H CHCN CH O NH H C 222363323+=→++1.3 方案的选择由于丙烯是可以通过石油烃热裂解大量的廉价制得,而且这个反应又是可以一步就合成的,同时这种方法的生产成本也很低,仅仅为上面三种方法的50%左右,这种方法还不需要用到氢氰酸,在生产过程中的安全性也比上面的三种方法要好的多.因此,丙烯氨氧化法现在是世界上生产丙烯腈的主要方法. 1.4 反应过程分析 〔1〕丙烯氨氧化的原理丙烯氨氧化反应是一个非均相催化氧化反应:CH3CH=CH2+NH3+3/2O2→CH2=CHCN +3H2O 与此同时,在催化剂表面还发生如下一系列副反应. ①生成乙腈<ACN>.CH3CH=CH2+3/2NH3+3/2O2→3/2CH3CN+3H2O ②生成氢氰酸<HCN>.CH3CH=CH2+3NH3+3O2→3HCN+6H2O ③生成丙烯醛.CH3CH=CH2+O2→CH2=CHCHO+H2O ④生成乙醛.CH3CH=CH2+3/4O2→3/2CH3CHO ⑤生成二氧化碳CH3CH=CH2+9/2O2→3CO2+3H2O ⑥生成一氧化碳.CH3CH=CH2+3O2→3CO+3H2O上面的这些副反应都是比较强的放热反应,特别是深度氧化反应.在反应的过程当中,必然会生成一些副产物,上列副反应中,生成乙腈和氢氰酸的反应是主要的.CO2、CO和H2O可以由丙烯直接氧化得到,也可以由丙烯腈、乙腈等再次氧化得到.除上述副反应外,还有生成微量丙酮、丙腈、丙烯酸和乙酸等副反应.那么这样就会降低我们想要的产物的收率,这样不仅仅浪费了原料,而且也会使生成的产物比较复杂,给我们接下来的分离和精制也会带来困难,那么这样也会影响产品的质量.如果我们想要提高我们的目的产物的收率,那么我们就必须减少过程中的副反应,除了要考虑设备和工艺流程合理之外,我们主要还要考虑选择比较合适的催化剂,使那些副反应能够得到抑制.<2>催化剂丙烯氨氧化所采用的催化剂主要有两类,即Mo系和Sb系催化剂.Mo系催化剂由Sohio公司开发的C-41、C-49.Sb系催化剂由英国酿酒公司首先开发,在此基础上,日本化学公司又相继开发成功第三代的NS-733A和第四代的NS-733B.我们国家目前主要采用的催化剂是Mo系的催化剂,钼系的代表性的催化剂除了有美国的Sohio公司的C-41、C-49外,还有我国的MB-82、MB-86.一般的时候,Mo-Bi是主要的催化剂,P-Ce是助催化剂,作用是能够提高催化剂活性并且能够延长催化剂的使用寿命.如果按质量计算的话,Mo-Bi占这个活性组分的绝大部分,虽然单一的MoO3具有一定的催化活性,但是它的选择性是比较差的,单一的BiO3对生成丙烯腈也没有催化活性,所以只有二者的组合才能表现出比较好的活性、稳定性和选择性.如果单独使用助催化剂P-Ce时,对这个反应不能够起到加速或者是极少加速的作用,但是如果它们和Mo-Bi配合使用时,那么就能够改进Mo-Bi催化剂的性能了.一般来说,我们对助催化剂的用量都会控制在5%以下的.当然载体的选择也是很重要的,由于这个反应它是一个强放热的反应,所以在工业生产的过程当中,我们会采用流化床反应器.流化床反应器对催化剂的强度要求是很高的,而且要求它的耐磨性也要好,所以我们就会采用粗孔微球型硅胶作为我们这个催化剂的载体.<3>工艺条件的选择①原料纯度:原料丙烯是经过催化裂化气或者是烃类裂解气分离得到的,那么这个过程中避免不了的会产生一些杂质,像是丙烷或者是其他的一些烷烃,但是这些烷烃对反应不会产生一些不利的影响;又或者是像乙烯也不会对反应产生影响,因为乙烯不含有活泼的α-H,所以乙烯在这类反反应中没有丙烯活泼,必然也就不会产生影响;但是如果杂质中含有丁烯或者是更高级的烯烃,那么就会产生不利的影响了,那是因为丁烯和其它更高级的烯烃比丙烯更容易发生氧化,那么这些杂质就会消耗反应中的氧气,也就会造成反应过程缺氧,会使催化剂活性降低;所以,必须严格控制原料的纯度,尽量控制丁烯以与其他一些更高级的烯烃的含量;硫化物的存在,也会降低催化剂的活性,所以必须提前去除.②丙烯:氨:氧气事实上物质的量之比为1:1-1.2:1.8-2.3.理论上丙烯:氨的物质的量的比值为1:1,但是实际上为1:1.2,如果氨的物质的量大于丙烯物质的量,那么副产物丙烯醛的产量就会增多;如果丙烯的物质的量大于氨的物质的量,那么在处理氨的过程中就会特别麻烦.理论上丙烯:氧的物质的量的比值为1:1.5,但是实际上为1:1.8-2.5.之所以要让氧气多一点,主要是为了保护催化剂的活性,不至于让催化剂因为缺氧而造成催化剂失活.如果降低氧气比会使选择性增加,那么丙烯的转化率就会随之降低,同样丙烯腈的收率也会下降的;如果增大氧气比,那么就会增加二氧化碳的生成量,减弱丙烯腈的选择性,也会扩大反应器的体积.③.反应温度的影响:在丙烯氨氧化的反应过程中温度是一个很重要的影响因素.当温度低于350℃是,就不怎么生成丙烯腈.所以我们要是想要或得较高的丙烯腈,那么我们就只能升高温度,同时还必须得控制好反应温度.因为反应温度的变化不仅对丙烯腈的产量有影响,也会对副产物的产量、反应物的转化率,催化剂的空时收率产生影响.如果增加反应温度就会发现,反应物丙烯的转化率、生成物丙烯腈的产率都会增加,但是同时也会发现,副产物的收率也会有所增加.随着温度的升高,丙烯腈的收率会出现一个最大值,大约是在460℃左右,同样,副产物乙腈的收率也会随着温度的升高出现一个最大值,大约是在417℃左右.在实验过程中,我们经常会采用大约在460℃左右下进行.④.反应压力的影响:通过丙烯氨氧化法来生产丙烯腈实际上是一个体积减小的一个过程,那么理论上来说,如果增大反应压力,那么就会增加反映转化率,从而提高丙烯腈转化率,同样如果增大压力,那么也会增大反应气体的密度,这样也就可以增加设备的反映能力.但是实验结果表明事实上不是这样的,如果增大压力就会发现,丙烯腈的收率不但没有上升反而是呈直线下降,那么就说明增大了压力,反而对副产物的生成产生了一个更有利的条件,那么也就增加的副产物的产率,所以我们一般情况下还是只能选择在常压下操作了,如果过程中适当的加了一点压,那么也只是为了克服反应后面的设备和管线的阻力.我们一般情况下都会把反应压力设置在0.1-0.3MPa.⑤.反应接触时间的影响:丙烯氨氧化反应一般是在催化剂表面进行的,它是一种气-固相催化反应.因此,我们必须把原料气与催化剂的接触时间控制在一个合理范围内,使原料气的转化率达到最大.在理论上来说,如果适当的增多接触时间,就会增大丙烯腈的产率和丙烯的转化率,副产物的产量不怎么会发生变化,如果这样的话对我们的生产是有利的.但是事实上并不是这样的,如果过多的增加接抽时间,那么就会造成丙烯腈过度氧化,这样就会使丙烯腈的产率下降,过多的消耗氧气,也会造成催化剂的活性降低,同样还会使设备的生产能力降低,所以我们一般情况下会把接触时间控制在5-10s.第二章工艺流程2.1 设计任务〔1〕设计题目:年产10000吨丙烯腈合成工段工艺设计〔2〕生产原料:①丙烯—液态丙烯原料其中含丙烯85%,丙烷15%〔均为mol〕②空气—取自大气③氨—液态氨,来自合成氨工业,含氨100%〔3〕生产方法:用丙烯氨氧化法合成丙烯腈〔4〕产品为丙烯腈水溶液,含丙烯腈1.8%〔wt〕2.2 生产工艺流程图第三章工艺设计计算3.1物料衡算与热量衡算3.1.1 小时生产能力按年工作日300天计算,丙烯腈损失率3.1%,设计裕量6%计算,丙烯腈小时产量为:10000×1000×1.06×1.031/<300×24>=1517.86kg/h3.1.2反应器的物料衡算和热量衡算<1>计算依据a.丙烯腈产量1517.86kg/h,即28.63kmol/hb.原料组成〔摩尔分数〕含C3H6 85%,C3H8 15%c.进反应器的原料配比〔摩尔比〕为:C3H6:NH3:O2:H2O=1:1.05:2.3:3d.反应后各产物的单程收率如表1所示表1反应后各产物的单程收率e.操作压力进口0.203MPa,出口0.162MPaf.反应器进口温度110℃,反应温度470℃,出口气体温度360℃.g.化学参数<2>物料衡算a.反应器进口原料气中各组分的流量C3H628.63/0.6=47.72kmol/h=2004.2kg/hC3H847.72/0.85×0.15=8.42kmol/h=370.5kg/hNH347.72×1.05=50.11kmol/h=851.87kg/hO247.72×2.3=109.76kmol/h=3512.32kg/hH2O47.72×3=143.16kmol/h=2576.88kg/hN2109.76/0.21×0.79=412.9kmol/h=11561.4kg/hb.反应器出口混合气中各组分的流量丙烯腈<AN>28.63kmol/h=1517.86kg/h乙腈<ACN>3/2×47.72×0.07=5.01kmol/h=205.4kg/h丙烯醛<ACL>47.72×0.007=0.33kmol/h=18.48kg/hCO23×47.72×0.12=17.18kmol/h=755.9kg/hHCN3×47.72×0.065=9.31kmol/h=251.2kg/hC3H88.42kmol/h=370.5kg/hN2412.9kmol/h=11561.4kg/hO2:109.76-〔3/2〕×28.63-9.31-0.33-5.01-9/〔3×2〕×17.18=26.40kmol/h=844.8kg/h C3H647.72-〔1/3〕×9.31-0.33-〔2/3〕×5.01-28.63-〔1/3〕×17.18=6.59kmol/h=276.7kg/h NH3:50.11-28.63-5.01-9.31=7.16kmol/h=121.7kg/hH2O:143.16+3×28.63+2×5.01+2×9.31+17.18+0.33=275.2kmol/h=4953.6kg/hc.反应器物料平衡表如表2表2反应器物料平衡表(3)热量衡算各物质0~t℃的平均定压比热容如表3所示表3各物质0~t℃的平均定压比热容如下:CP/[kJ/<kg·k>]a. 浓相段热衡算求浓相段换热装置的热负荷与产生蒸汽量 假设热力学途径:△H 1△H 3各物质25~t ℃平均比热容用0~t ℃的平均比热容代替,误差不大,因此:△H△H 2△H 1=<2004.2×1.841+370.5×2.05+851.87×2.301+3512.32×0.941+11561.4×1.046+2576.88×1.883>× <25-110>=-2.266×106kJ/h△H 2=-<28.3×512.5+5.01×362.3+9.31×315.1+0.33×353.1+17.18×641> = -3.055×107kJ/h△H 3=<276.7×2.929+370.5×3.347+121.7×2.939+844.8×1.046+11561.4×1.109+4953.6×2.092+1517.86×2.209+205.4×2.10+251.2×1.724+18.48×2.172+755.9×1.213>×<470-25>=1.396×107kJ/h △H =△H 1+△H 2+△H 3= -2.266×106-3.055×107+1.396×107= -1.886×107kJ/h若热损失取ΔH 的5%,则需由浓相段换热装置取出的热量〔即换热装置的热负荷〕为: Q=<1-0.05>×1.886×107=1.792×107kJ/h浓相段换热装置产生0.405Mpa 的饱和蒸汽〔饱和温度143℃〕 143℃饱和蒸汽焓I steam=2736kJ/kg 143℃饱和水焓I H2O =601.2kJ/kg∴ 产生的蒸汽量=2.601273610792.17-⨯=8394kg/hb.稀相段热衡算求稀相段换热装置的热负荷与产生蒸汽量 以0℃气体为衡算基准进入稀相段的气体带入热为:Q 1=<276.7×2.929+370.5×3.347+121.7×2.939+844.8×1.046+11561.4×1.109+4953.6×2.092+1517.86×2.209+205.4×2.10+251.2×1.724+18.48×2.172+755.9×1.213>×<470-0> =1.334×107kJ/h 离开稀相段的气体带出热为:Q 2=<276.7×2.678+370.5×3.013+121.7×2.636+844.8×1.004+11561.4×1.088+4953.6×2.088+1517.86×1.874+205.4×1.933+251.2×1.640+18.48×1.966+755.9×1.130>×<360-0> =1.083×107kJ/h 若热损失为4%,则稀相段换热装置的热负荷为:Q3=<1-0.04><Q1-Q2>=<1-0.04>×<1.334×107-1.083×107>=2.410×106kJ/h稀相段换热装置产生0.405Mpa的饱和蒸汽,产生的蒸汽量为:G=2.410×106/<2736-601.2>=1128.9kg/h3.1.3废热锅炉的热量衡算(1) 计算依据a.入口气和出口气的组成与反应器出口气体相同b.入口气体温度360℃,压力0.162MPac.出口气体温度180℃,压力0.152MPad.锅炉水侧产生0.405MPa的饱和蒸汽(2) 热衡算以0℃气体为衡算基准,各物质的平均比热容为表4所示.表4各物质0~180℃的平均比热容为:a. 入口气体带入热〔等于反应器稀相段的气体带出热〕Q1=1.083×107kJ/hb.出口气体带出热Q2=<276.7×2.071+370.5×2.342+121.7×2.406+844.8×0.926+11561.4×1.154+4953.6×1.925+1517.86×1.552+205.4×1.607+251.2×1.485+18.48×1.586+755.9×1.004>×<180-0>=5.269×106kJ/hc.热衡算求需要取出的热量Q按热损失10%计,需要取出的热量为Q=0.9<Q1-Q2>=0.9×<1.083×107-1.083×107>=5.005×106kJ/hd.产生蒸汽量产生0.405MPa的饱和蒸汽量为G=5.005×106/<2736-601.2>=2344kg/h3.1.4空气饱和塔物料衡算和热量衡算(1) 计算依据a.入塔空气压力0.263MPa,出塔空气压力0.243MPab.空压机入口空气温度30℃,相对湿度80%,空压机出口气体温度170℃c.饱和塔气、液比为152.4〔体积比〕,饱和度0.81d.塔顶喷淋液为乙腈解吸塔釜液,温度105℃,组成如表5所示:表5塔顶喷淋液各组成e.塔顶出口湿空气的成分和量按反应器入口气体的要求为O2109.76kmol/h即3512.32kg/hH2O412.9kmol/h即11561.4kg/hN2143.16kmol/h即2576.88kg/h(2) 物料衡算a.进塔空气量进塔干空气量=<109.76+412.9>=522.65kmol/h=15073kg/h查得30℃,相对湿度80%时空气湿含量为0.022kg水气/kg干空气,因此,进塔空气带入的水蒸汽量为:0.022×15073=331.6kg/hb.进塔热水量气液比为152.4,故进塔喷淋液量为<109.76+412.9>×22.4×<273+170>/273×0.1013/0.263×1/152.4=49.59m3/h塔顶喷淋液〔105℃〕的密度为958kg/m3,因此进塔水的质量流量为49.59×958=47507kg/hC.出塔湿空气量出塔气体中的O2、N2、H2O的量与反应器入口气体相同,因此:O2109.76kmol/h 即3512.32kg/hN2412.9kmol/h 即11561.4kg/hH2O143.16kmol/h 即2576.88kg/hd.出塔液量塔内水蒸发量=2576.88—331.6=2245.28kg/h∴塔液流量=47507—2245.28=45261.7kg/he.饱和塔物料衡算表<3>热衡算a.空气饱和塔出口气体温度从物料平衡表得知,空气饱和塔出口气体中,蒸汽的摩尔分数为0.215,根据分压定律,蒸汽的实际分压为:P H2O=Y H2O P=0.215×0.243=0.05655MPa因饱和度为0.81,所以饱和蒸汽分压应为:0.05655/0.81=0.0698Mpa=69800Pa查饱和蒸汽表,得到对应的饱和温度为90℃,因此,必须控制出塔气体温度在90℃,才能保证工艺要求的蒸汽量b.入塔热水温度入塔水来自精制段乙腈解吸塔塔釜,105℃c.由热衡算求出热水温度t热衡算基准:0℃气态空气,0℃液态水<a>170℃进塔空气带入热量Q1170℃蒸汽焓值为2773.3kJ/kg,干空气在0~170℃的平均比热容为1.004kJ/<kg·K>.Q1=<3512.32+11561.4>×1.004×<170-0>+331.6×2773.3=3.492×106kJ/h<b>出塔湿空气带出热量Q290℃蒸汽焓2660kJ/kg,空气比热容取1.004kJ/<kg·K>.Q2=<3512.32+11561.4>×1.004<90-0>+2576.88×2660=8.217×106kJ/h<c>105℃入塔喷淋液带入热量Q3Q3=47507×4.184×<105-0>=2.087×107kJ/h<d>求出塔热水温度t出塔热水带出的热量Q4=45261.7×4.184t=189375t热损失按5%计,则Q5=0.05<3.492×106+1.983×107>=1.170×106kJ/h热平衡方程Q1+Q3=Q2+Q4+Q5代入数据:3.492×106+2.087×107=8.217×106+189375t+1.170×106解得t=79℃因此,出塔热水温度为79℃.3.1.5氨中和塔物料衡算和热量衡算(1) 计算依据a. 入塔气体流量和组成与反应器出口气体相同.b.在中和塔内全部氨被硫酸吸收,生成硫酸铵.c.新鲜硫酸吸收剂的含量为93%〔wt〕.d.塔底出口液体〔即循环液〕的组成如表6:表6塔底出口液体的组成组分H2O AN ACN HCN H2SO4<NH4>SO4合计%<wt>68.530.030.020.0160.530.90100e.进塔气温度180℃,出塔气温度76℃,新鲜硫酸吸收剂温度30℃.f.塔顶压力0.122MPa,塔顶压力0.142MPa.(2) 物料衡算a.排除的废液量与其组成进塔气中含有72.95kg/h的氨,在塔内被硫酸吸收生成硫酸铵,氨和硫酸反应的方程式如下:2NH3+H2SO4<NH4>SO4<NH4>SO4的生成量,即需要连续排出的<NH4>SO4流量为:121.7×132/<2×17>=472.5kg/h塔底排出液中,<NH4>SO4的含量为30.9%〔wt〕,因此排放的废液量为:472.5/0.309=1529.1kg/h排放的废液中,各组分的量:H2O1529.1×0.6853=1047.9kg/hAN1529.1×0.0003=0.459kg/hACN1529.1×0.0002=0.3058kg/hHCN1529.1×0.00016=0.2447kg/hH2SO41529.1×0.005=7.647kg/h<NH4>2SO41529.1×0.309=472.7kg/hb.需补充的新鲜硫酸吸收剂〔93%H2SO4〕的量为:<1529.1×0.005+121.7×98/34>/0.93=385.5kg/hc.出塔气体中各组分的量C3H6 276.7kg/hC3H8 370.5kg/hO2 844.8kg/hN2 11561.4kg/hAN 1517.86-0.459=1517.401kg/hACN 205.4-0.3058=205.09kg/hACL 18.48kg/hHCN 251.2-0.2447=250.96kg/hCO2 755.9kg/hH2O 出塔气中的水=入塔气中的水+新鲜吸收剂带入水-废液排出的水=4593.6+385.5×0.07-1047.9=3932.685kg/ha.氨中和塔循环系统物料平衡表(3) 热衡算a.出塔气体温度塔顶气体中实际蒸汽分压为P H2O=Y H2O P=0.2980×0.122=0.0363MPa设饱和度为0.98,则与塔气体温度平衡的饱和蒸汽分压为:P○H2O=0.03636/0.98=0.03710MPa入塔喷淋液的硫酸铵含量为100×30.9/68.53=45g<NH4>2SO4/100g H2O,已知硫酸铵溶液上方的饱和蒸汽压如下表.根据入塔喷淋液的硫酸铵含量和P○H2O的值,内插得到出塔气的温度为76℃.b.入塔喷淋液的温度入塔喷淋液温度比气体出口温度低6℃,故为70℃.c.塔釜排出液温度表7硫酸铵溶液上方的饱和蒸汽压/MPad.热衡算求循环冷却器的热负荷和冷却量:Q1+Q3+Q4+Q5+Q6+Q8=Q7+Q2+Q9<a>入塔气体带出热Q1入塔气体带入热量与废热锅炉出口气体带出热量相同.Q1=5.269×106kJ/h<b>出塔气体带出热Q2,各组分在0~76℃的平均比热容的值如表8表8各组分在0~76℃的平均比热容的值如下:Q2=<276.7×1.715+370.5×1.966+844.8×0.9414+11561.4×1.046+3932.685×1.883+1517.86×1.347+205.1×1.393+250.96×1.406+18.48×1.343+755.9×0.921>×<76-0>=1.892×106kJ/h<c>蒸汽在塔内冷凝放热Q3蒸汽在塔内的冷凝量=进塔气体带入蒸汽-出口气带出蒸汽=4953.6-3932.685=1020.9kg/h蒸汽的冷凝热为2246.6kJ/kgQ3=1020.9×2246.6=2.294×106kJ/h<d>有机物冷凝放热Q4AN的冷凝量0.459kg/h,其冷凝热为615kJ/kgACN的冷凝量0.3058kg/h,其冷凝热为728kJ/kgHCN的冷凝量0.2447kg/h,其冷凝热为878.6kJ/kgQ4=0.459×615+0.3058×728+0.2447×878.6=719.9kJ/h<e>氨气和放热Q5每生成1mol硫酸铵放热273.8kJQ5=472.7×1000/132×273.8=9.801×105kJ/h<f>硫酸稀释放热Q6硫酸的稀释热为749kJ/kg H2SO4∴Q6=358.515×749=2.685×105kJ/h<g>塔釜排放的废液带出热量Q7根据塔釜排放的废液中H2O与<NH4>2SO4的摩尔比,查氮肥设计手册得此组分的硫酸铵水溶液比热容为3.347kJ/〔kg·K〕∴Q7=1529.1×3.347×〔81-0〕=4.145×105kJ/h<h>新鲜吸收剂带入热Q830℃、93%H2SO4的比热容为1.603kJ/〔kg·K〕∴Q8=385.5×1.603×〔30-0〕=18539kJ/h<i>求循环冷却器热负荷Q9因操作温度不高,忽略热损失.把数据代入平衡方程:5.269×106+2.294×106+719.9+9.801×105+2.685×105+18539=1.892×106+4.145×105+Q9解得Q9=6.524×106kJ/h<j>循环冷却器的冷却水用量W设循环冷却器循环水上水温度32℃,排水温度36℃.W=6.524×106/[4.184<36-32>]=3.898×105kg/h=389.8t/he.求循环液量m0℃循环液的比热容为3.368kJ/〔kg·K〕,循环液与新鲜吸收液混合后的喷淋液比热容为3.364kJ/〔kg·K〕.设循环液流量为m kg/h,循环冷却器出口循环液温度t℃.对新鲜吸收剂与循环液汇合处列热平衡方程得:m×3.368t+18539=<m+395.5>×3.364×70<1>对循环冷却器列热平衡方程得:m×3.347×81-m×3.368t=Q9=6.524×106〔2〕解析〔1〕和〔2〕得m=183051kg/ht=70.04℃3.1.6换热器物料衡算和热量衡算AN溶液去精制AN溶液来自水吸收塔气体来自氨中和塔气液混合物去水吸收塔76°C40°C(1)计算依据进口气体76℃,组成和流量与氨中和塔出口气体相同;出口气体温度40℃,操作压力115.5kPa.<2>物料衡算出口气体温度40℃,40℃饱和蒸汽压力为: P o H 2O=55.32mmHg=7.375kPa 设出口气体中含有x kmol/h 的蒸汽,根据分压定律有:375.75.115)5.21818.733(=⨯+-xx解得 x=35.10kmol/h=631.8kg/h∴ 蒸汽的冷凝量为 3932.685-631.8=3300.885kg/h(3)热量衡算a.换热器入口气体带入热Q1=1.892×106kJ/hb.蒸汽冷凝放热Q2 Q2=3300.85×2401.1=7.925×106kJ/hc.冷凝液带出热Q3 Q3=3300.85×4.184<40﹣0>=5.524×105kJ/hd.出口气体带出热Q4出口气体各组分在0~40℃的平均比热容如下:出口气体各组分在0~40℃的平均比热容Q4=<6.59×61.92+8.42×72.38+26.40×29.46+412.9×29.29+35.10×36.75+28.63×63.35+5.01×52.09+9.31×62.76+0.33×65.61+17.18×38.66><40-0>=7.410×105e.热衡算求换热器的热负荷热平衡方程:Q1+Q2=Q3+Q4+Q5带入数据得:1.892×106+7.925×106=5.524×105+7.410×105+Q5解得Q5=8.534×106kJ/h3.1.7水吸收塔物料衡算和热量衡算<1>计算依据a.入塔气流量和组成与换热器出口气相同b.入塔气温度40℃,压力112kPa.出塔气温度10℃,压力101kPac.入塔吸收液温度5℃d.出塔AN溶液中含AN1.8%〔wt〕〔2〕物料衡算a.进塔物流流量和组成与换热器出口相同b.出塔气量和组成设入塔气中的AN、HCN、ACL、CAN等组分全部被水吸收,C3H6,C3H8,O2,N2,CO2,等组分不溶于水,因此,出塔干气体有:C3H6 6.59Kmol/h<276.7KJ/h>,C3H88.42Kmol/h<370.5KJ/h>,O226.40Kmol/h<844.8KJ/h>,N2412.9Kmol/h<11561.4KJ/h>,CO217.18Kmol/h<755.9KJ/h>.出塔气中含有蒸汽的量按分压定律求得,计算如下:10℃水的饱和蒸汽压p○H2O=1228Pa,总压为101325Pa,出塔气中干气总量=6.59+8.42+26.40+412.9+17.18=471.49Kmol/h则出塔气中含有水蒸气的量:1228/<101325-1228>×471.49=5.784kmol/h=104.12kg/h出塔气总量为:276.7+370.5+844.8+11561.4+755.9+104.12=13193.42kg/hc.塔顶加入的吸收水量〔a〕出塔AN溶液总量1517.86/0.018=84325.6kg/h〔b〕塔顶加入的吸收水量作水吸收塔的总质量衡算得:入塔吸收液量=塔底AN溶液量+出塔气体总量-入塔气量-凝水量=84325.6+13913.42-16555.2-3300.885=78383kg/hd.塔底AN溶液的组成和量AN溶液中的水=塔顶加入的水+进塔气液混合物中带入的水-出塔气中带出的水=78383+631.8+3300.885-104.12=82211.56kg/he.水吸收塔物料平衡如下:f.检验前面关于AN、HCN、ACN、ACL全部溶于水的假设的正确性因为系统压力<1MPa,气相可视为理想气体,AN、HCN、ACN、ACL的量相对于水很小,故溶液为稀溶液,系统服从亨利定律和分压定律.压力和含量的关系为:P*1=E1X1或P1=E1X1塔底排出液的温度为15℃,该温度下AN、HCN、ACN、ACL的亨利系数E值为:ACN E=4atm=405.3kPaHCN E=18atm=1824kPaACL E=3333mmHg=444.4kPaAN E=8atm=810kPa(a)AN塔底P AN=0.0514×112=5.75681kPax*AN=P AN/E AN=5.7568/810=0.00711以上计算可以看出,X AN=0.006209<X*AN,可见溶液未达饱和.<b>丙烯醛ACLP ACL=0.00059×112=0.06608kPaX*ACL=P ACL/E ACL=0.066608/444.4=0.0001487以上计算可以看出,X ACL=0.0000716<X*ACL,可见溶液未达饱和.<c>乙腈ACNP ACN=0.0089×112=1.00576kPaX*ACN=P ACN/E ACN=1.00576/405.3=0.002481以上计算可以看出,X ACN=0.001084<X*ACN,可见溶液未达饱和.<d>HCNP HCN=0.0167×112=1.8704kPaX*HCN=P HCN/E HCN=1.8704/1824=0.0010254以上计算可以看出,X HCN=0.00201>X*HCN,在吸收塔的下部,对HCN的吸收推动力为负值,但若吸收塔足够高,仍可使塔顶出口气中HCN含量达到要求.(3)热量衡算a.入塔气带入热Q1气体各组分在0~40℃的平均摩尔热容为Q1=〔6.59×61.92+8.42×72.38+26.4×29.46+412.9×29.29++35.10×36.75+28.63×63.65+5.00×52.10+0.33×65.01+9.29×37.62+17.18×38.66〕〔40-0〕=7.315×105KJ/hb.入塔凝水带入热Q2Q2=3300.885×4.184〔40-0〕=5.524×105KJ/hc.出塔气带出热Q3Q3=<6.59×61.29+8.42×72.38+26.4×29.46+412.9×29.29+5.784×36.75+7.18×38.66><10-0>=1.438×105KJ/hd.吸收水带入热Q4Q4=78383×4.184<5-0>=1.640×106KJ/he.出塔AN溶液带出热Q5AN溶液中各组分的液体摩尔热容如下:Q5=<4567.3×75.3+28.63×121.1+5×107.3+9.29×71.55+0.33×123.8>t=348626.8tf.水冷凝放热Q6水冷凝量=631.8-104.12=527.68kg/h水的冷凝热为2256kJ/kg∴Q6=527.68×2256=1.19×106KJ/ha.AN、HCN、ACN、ACL等气体的溶解放热Q7AN、HCN、ACN、ACL的冷凝热数据如下:Q7=1517.8×610.9+205.09×765.7+18.48×493.7+250.96×937.2=1.329×106kJ/hb.热衡算求出塔液温度tQ1+Q2+Q4+Q6+Q7=Q3+Q57.315×105+5.524×105+1.640×106+1.19×106+1.329×106=1.438×105+348626.8t3.1.8空气水饱和塔釜液槽<1>计算依据空气饱和塔液体进、出口流量和出口液体的温度由空气饱和塔物料和热衡算确定;去水吸收塔的液体流量由水吸收塔物料衡算确定;排污量按乙腈解吸塔来的塔釜液量的15%考虑;乙腈解吸塔塔釜液量和去萃取解吸塔的液体量由精制系统的物料衡算确定.<2>物料衡算进料:a.乙腈解析塔釜液入槽量=113300-47507=65793kg/hb.空气饱和塔塔低液入槽量=45255-17000=28255kg/hc.入槽软水量x kg/h出料:a.去水吸收塔液体量78496kg/hb.去萃取解析塔液体量30000kg/h做液体釜的总质量平衡得65793+28255+x=78496+30000c.解得x=14448kg/h(3)热量衡算a.入槽乙腈解析塔釜液带入热Q1:Q1=65793×4.184×〔105-0〕=2.89×107kJ/hb.入槽软水带入热:Q2Q2=14448×4.184×〔30-0〕=1.184×106kJ/hc.空气饱和塔底液带入热Q3Q3=28255×4.184×〔79-0〕=9.339×106kJ/hd.去吸收塔液体带出热Q4Q4=78496×4.184〔t-0〕=328427t kJ/he.去萃取解析塔带出热Q5Q5=30000×4.184×〔t-0〕=125520t kJ/hf.热衡算求槽出口液体温度t热损失按5%算,热平衡方程为:0.95×〔Q1+Q2+Q3〕=Q4+Q50.95×〔2.89×107+1.814×106+9.339×106〕=〔328427+125520〕t解得t=88.23℃3.1.9丙烯蒸发器热量衡算(1)计算依据蒸发压力0.405Mpa;加热剂用0℃的冷盐水,出口温度-2℃;丙烯蒸发量2004.2kg/h(2)有关资料a.0.405Mpa下丙烯的沸点为-13℃,汽化热410KJ/kgb.0.405Mpa下丙烷的沸点为-5℃,汽化热376.6KJ/kg(3)热衡算秋丙烯蒸发器的热负荷和冷冻盐水用量a.丙烯蒸发吸收的热Q1=2004.2×410=8.217×105kJ/hb.丙烷蒸发吸收的热量Q2=370.5×376.6=1.40×105kJ/hc.丙烯蒸发器的热负荷冷损失按10%考虑Q=1.1×〔8.27×105+1.40×105〕=1.057×105kJ/hd.冷冻盐水用量W平均温度〔-1℃〕下,冷冻盐水比热容为3.47kJ/<kg·K>W=1.057×105/<3.47×〔0-〔-2〕〕>=152305kg/h3.1.10丙烯过热器热量衡算〔1〕计算依据丙烯进口温度-13℃,出口温度65℃,用0.405Mpa蒸汽为加热剂.〔2〕热衡算求丙烯过热器热负荷和加热蒸汽量丙烯气的比热容为1.464KJ/<kg.K>,丙烷气比热容1.715KJ/<kg.K>,热损失按10%考虑,需要加热蒸汽提供的热量为:Q=1.1×〔2004.2×1.464+370.5×1.715〕×[65 -〔-13〕]=2.78×105kJ/h加热蒸汽量为:W=2.78×105/2138=130.2kg/h上式中2138KJ/kg是0.405Mpa蒸汽的冷凝热.3.1.11氨蒸发器热量衡算〔1〕计算依据a.蒸发压力0.405Mpa.b.加热剂用0.405Mpa饱和蒸汽,冷凝热为2138KJ/h〔2〕有关资料0.405Mpa下氨的蒸发温度为-7℃,汽化热为1276KJ/kg〔3〕热衡算求氨蒸发器的热负荷和加热蒸汽用量冷损失按10%考虑,氨蒸发器的热负荷Q:Q=851.87×1276×1.1=1.1957×106kJ/h加热蒸汽量为:W=1.1957×106/2138=559.25kg/h3.1.12气氨过热器〔1〕计算依据a.气氨进口温度-7℃,出口温度65℃b.用0.405Mpa蒸汽为加热剂.c.气氨流量851.87kg/h(2)热衡算求其气氨过热器的热负荷和加热蒸汽用量氨气的比热容为2.218KJ/<kg.K>,冷损失按10%算.气氨过热器的热负荷为:Q=851.87×2.218×[65-〔-7〕]×1.1=1.496×105kJ/h加热蒸汽用量为:W=1.496×105/2138=70kg/h3.1.13混合器(1)计算依据气氨进口温度65℃,流量851.87kg/h丙烯气进口温度65℃,流量2004.2kg/h,丙烷气进口温度65℃,流量370.5kg/h 出口混合气温度110℃.湿空气来自空气加热器.(2)热衡算求进口湿空气的温度t,以0℃为热衡算基准.C3H6、C3H8、NH3在0~65℃的平均比热容的值如下:a.气态丙烯、丙烷带入热Q1Q1=〔2004.2×1.569+370.5×1.82〕×〔65-0〕=2.482×105kJ/hb.气态氨带入热Q2Q2=851.87×2.197×〔65-0〕=1.217×105kJ/hc.湿空气带入热Q3N2、O2和蒸汽在0~137℃的平均比热容分别为1.046kJ/<kg·k>、1.841kJ/<kg·k>和1.925kJ/<kg·k>.Q3=〔11561.4×1.046+3512.32×1.841+2576.88×1.925〕×〔t-0〕=23520t kJ/hd.混合器出口气体带出热Q4=〔2004.2×1.569+370.5×1.82+851.87×2.197+11561.4×1.046+3512.32×1.841+2576.88×1.925〕×〔110-0〕=3.213×106kJ/he.热衡算求进口湿空气的温度t热损失按10%考虑.0.9×〔Q1+Q2+Q3〕=Q4代入数据:0.9×〔2.482×105+1.217×105+23520t〕=3.213×106解得t=136℃3.1.14空气加热器的热量衡算〔1〕计算依据a.入口空气温度90℃,出口空气温度136℃.b.空气的流量和组成如下:C.热衡算求空气加热器的热负荷和加热蒸汽量N2,O2和蒸汽90~136℃的平均比热容分别为:1.046KJ/<kg.K>1.84KJ/<kg.K>,1.925KJ/<kg.K>.热损失按10%考虑,空气加热器的热负荷为:Q=〔11561.4×1.046+3512.32×1.841+2576.88×1.925〕×〔136-90〕×1.1=1.190×106kJ/h用0.608Mpa蒸汽为加热剂,其饱和温度为164.2℃,冷凝热为2066KJ/kg,加热。
第1篇一、前言丙烯腈作为一种重要的有机合成原料,广泛应用于ABS、腈纶、丙烯酰胺等领域。
随着我国经济的快速发展和工业技术的进步,丙烯腈产业在我国得到了迅速发展。
本文对丙烯腈技术进行总结,以期为我国丙烯腈产业的发展提供参考。
二、丙烯腈生产工艺1. 丙烯氨氧化法丙烯氨氧化法是目前国内外丙烯腈生产的主要工艺。
该工艺以丙烯为原料,通过氨氧化反应生成丙烯腈。
主要反应式如下:C3H6 + 2NH3 + 3O2 → C3H3N + 3H2O2. 丙烯腈催化加氢法丙烯腈催化加氢法是另一种丙烯腈生产工艺。
该工艺以丙烯腈为原料,通过催化剂加氢反应生成丙烯腈。
主要反应式如下:C3H3N + H2 → C3H6N三、丙烯腈生产技术特点1. 丙烯氨氧化法(1)原料来源丰富:丙烯腈生产原料丙烯的来源广泛,包括石油、天然气、煤等。
(2)工艺流程简单:丙烯氨氧化法工艺流程相对简单,易于操作。
(3)产品品质高:丙烯腈产品品质较高,符合国内外市场需求。
2. 丙烯腈催化加氢法(1)原料利用率高:丙烯腈催化加氢法对原料丙烯腈的利用率较高。
(2)工艺流程复杂:丙烯腈催化加氢法工艺流程相对复杂,对操作人员的技术要求较高。
(3)产品品质较高:丙烯腈产品品质较高,但可能存在一定的副产物。
四、丙烯腈生产技术发展趋势1. 绿色环保:随着环保意识的不断提高,绿色环保型丙烯腈生产工艺将得到进一步发展。
2. 高效节能:高效节能型丙烯腈生产工艺将得到广泛应用,以降低生产成本。
3. 智能化:智能化丙烯腈生产技术将得到推广,提高生产效率和产品质量。
4. 多元化:丙烯腈产业链将向多元化方向发展,拓展应用领域。
五、结论丙烯腈作为一种重要的有机合成原料,在我国工业发展中具有重要作用。
通过对丙烯腈生产技术的总结,有助于我国丙烯腈产业的持续发展。
在今后的发展过程中,我国应加大对丙烯腈生产技术的研发投入,提高产业竞争力,为我国丙烯腈产业的可持续发展提供有力保障。
第2篇一、引言丙烯腈作为一种重要的有机化工原料,广泛应用于ABS、腈纶、丙烯酰胺等产品的生产中。