重大药害事件
- 格式:ppt
- 大小:3.74 MB
- 文档页数:51

世界历史上的药害事件药物不良反应与药源性疾病是不合理用药的两种最常见表现。
药物在给予人们健康与生存希望的同时,由于不合理使用,导致的药物不良反应与药源性疾病如影随形,极端体现为药害事件的发生。
经百年来世界上致死、致残的药害事件屡屡发生,我国近年来药害事件的频发也令人担忧。
以下列举了历史上的部分药害事件。
(一)甘汞作为幼儿的轻泻药和驱虫药引发肢端疼痛病。
国外用汞和汞化合物作为药物已有1000多年的历史,在阿拉伯国家应用含汞的软膏治疗慢性皮肤病、麻风等。
哥伦布远航归来后,欧洲流行梅毒,汞剂成为治疗梅毒的唯一有效药物。
在英联邦,婴儿用的牙粉、尿布漂洗粉中含有汞和汞化合物,并曾经广泛用甘汞(氯化亚汞)作为幼儿的轻泻药和驱虫药。
1890年以后,首先在英国,然后在其它国家不断发现一些儿童发生肢端疼痛病,同时还有口腔发炎、牙龈肿胀、流涎、脱发、牙齿脱落等临床症状和体征。
经过长期的流行病学调查,证明许多病人是由于使用含汞药物所致。
仅在英格兰和威尔士地区,在1939~1948年间死于含汞药物中毒的儿童就有585人,其中多数是3岁以下的儿童。
(二)氨基比林致白细胞减少症氨基比林是1893年合成的一种解热镇痛药,1897年开始在欧洲上市,约1909年进入美国市场。
1922年以后,德国、英国、丹麦、瑞士、比利时和美国等国家逐渐发现,许多服用过此药的病人出现口腔炎,发热咽喉痛等症状。
临床检验结果为白细胞减少症、粒细胞减少症,调查证明二者有因果关系。
最终证实,氨基比林可导致粒细胞缺乏。
从1931年到1934年,仅美国一个国家死于氨基比林引起白细胞减少症的就有1981人,欧洲死亡200余人。
1938年,美国决定把氨基比林从合法药品目录中取消,1940年以后,该国这种病人迅速减少。
在丹麦,从30年代起就完全禁用该药,在1951~1957年间调查时,没有再发生由氨基比林引起的粒细胞减少症、白细胞减少症。
(三)磺胺酏剂致肾功能衰竭磺胺类药于20世纪30年代问世。

我国近年来十大药害事件
1、2011年8月梅花K黄柏胶囊事件:在黄柏胶囊生产过程中非法添加过期的盐酸四环素,致128人中毒,出现腹痛、呕吐、乏力等。
有1人成为植物人.
2、1993—2004年龙胆泻肝丸(兰木通)事件:因兰木通中含马兜铃酸致“马兜铃酸致肾病”,致病人数约十万人,其中肾衰死亡者无法准确统计。
3、2002年—2006年奥美定事件:化学名为聚丙烯酸胺水凝胶,用隆胸等美容术,出现炎症、感染、硬结、变形等约2万人受害。
4、2006年4月茵陈注射液事件:其中含有工业用二甘醇引起肾衰竭致13人死亡。
5、从70年代—2006年鱼腥草注射液事件:注射液内含有48种化学成分,静脉注射后致过敏性休克死亡等。
因使用时间长、散落数量多,发生不良反应数字和死亡人数难以准确统计,已叫停使用。
6、2006年7月辛弗事件:即克林霉素磷酸酯葡萄糖注射液,出现胸闷、心悸、寒战过敏性休克,肝肾功能损害,因灭菌温度及灭菌时间不足发生93例,死亡11人。
药厂老总以死谢罪,自终身亡。
7、2007年7月甲氨蝶呤事件:生产过程中被长春新碱污染,导致130位病人使用后下肢疼痛、麻木,无法直立或正常走。
8、2008年5月博雅人免疫球蛋白事件:因质量问题静注后致病人死亡。
9、2009年10月刺五加注射液事件:因该制剂的某一批次被雨林水泡污染后,临床使用中出现恶心、胸闷、呕吐、昏迷血压下降等不良反应,其中4人循环衰竭死亡。
10、2009年1月假糖脂宁事件:假糖脂宁胶囊中加入了大量格列本脲等化学成分,发生严重低血糖致心、肺、脑功能不可逆的损伤直至病人死亡。

近年药害事件1. “齐二药”事件齐齐哈尔第二制药公司用工业原料二甘醇替代药用辅料丙二醇生产“亮菌甲素注射液”国家局调查结果表明:“齐二药”生产和质量管理混乱,检验环节失控,检验人员将二甘醇判为丙二醇投料生产,造成假药案件的发生结局:5种假药现身市场,11名病人被夺去生命,《药品生产许可证》被吊销,企业被关闭,职工失业2.“欣弗”事件克林霉素磷酸酯葡萄糖注射液,由安徽华源生物药业有限公司生产未按批准的工艺参数灭菌,降低灭菌温度,缩短灭菌时间,增加灭菌柜装载量,影响了灭菌效果。
经中国药品生物制品检定所对相关样品进行检验,结果表明,无菌检查和热原检查不符合规定。
由于使用它造成的上百例严重不良反应,其中8人不幸死亡 8月3日卫生部叫停“欣弗”,安徽华源药厂全面停产,近两千多名员工停工回家停产后,其母公司上海华源股份有限公司开盘后跌停,公司损失了1.967亿元市值3. 广东佰易“静注人免疫球蛋白”事件非法购进血浆原料、不能提供有效完整的生产记录和检验记录、套用正常生产批号上市销售,涉案药品市场流通量大于批生产记录产量,即实际销售量大于生产量。
故意造假,套用正常产品的批号生产并上市销售,妄图逃避监管,把非法产品合法化,把违法行为隐秘化佰易药业生产的药品“静注人免疫球蛋白”,导致部分患者检验出丙肝抗体呈阳性结局:收回“药品GMP”证书,停止生产和销售产品4. “刺五加注射液”事件黑龙江省完达山制药厂完达山药业公司生产的刺五加注射液部分药品在流通环节被雨水浸泡,使药品受到细菌污染,后被更换包装标签并销售。
中国药品生物制品检定所、云南省食品药品检验所在被雨水浸泡药品的部分样品中检出多种细菌。
此外,完达山药业公司包装标签管理存在严重缺陷。
完达山药业公司管理人员质量意识淡薄,包装标签管理不严,提供包装标签说明书给销售人员在厂外重新贴签包装。
导致云南省红河州3人死亡2人重伤,1人轻伤的严重后果。
结局:责令全面停产,收回药品GMP证书,对该企业违法违规行为依法处罚,直至吊销《药品生产许可证》。


十大药害事件最近十年来,各大药害(医疗器械不良)事件屡见于报端。
笔者以一名药学工作者的视角,从其中遴选出危害性大、影响面广的十起事件,尽量以简练的文字构画出每起事件的脉络,系统、客观地展现整个事件的面目,以供关心药政事业的同仁们共同思考。
一、“梅花K”事件(一)事件简介:2001年8月24日,湖南省株洲市药监局接到群众举报:该市多人服用“梅花K”黄柏胶囊中毒住院。
株洲市局感到事态严重,迅速派人赶到市一医进行调查,发现患者服用的问题“梅花K”,均标示“广西半宙制药集团第三制药厂”(后更名为“广西金健制药厂”,以下简称“广西半宙”)生产。
据患者反映,该产品在当地媒体大作宣传,声称能通淋排毒、解毒疗疮,治疗多种女性炎症(夸大宣传)。
许多女性经不住广告诱惑,纷纷到市内药店购买,但服用几天后出现了胃痛、呕吐、浑身乏力等不良症状。
经株洲市药检所抽样检验,检出非法添加的四环素成分,初步认定该“梅花K”系假药。
几日后湖南省在全省范围内封杀“梅花K”黄柏胶囊。
8月31日,国家药监局下发紧急通知,要求在全国范围内立即暂停销售、使用“梅花K”黄柏胶囊。
通知强调,对凡标为“广西半宙”生产的“梅花K”黄柏胶囊一律暂控,批批抽验,除按标准检验外,加做四环素成分的检验。
发现问题药品,立即追查来源和流向。
“梅花K”事件也引起了国务院的高度重视,国务院副总理吴邦国就此事作了重要批示。
经过药监、公安等部门的调查,事件的内幕水落石出。
2000年9月,陕西省咸阳市杰事杰医药科技有限公司负责人程书群和“广西半宙”副厂长方党礼洽谈生产、销售药品黄柏胶囊,为加大药效,双方商定在黄柏胶囊中掺加已经变质过期的盐酸四环素。
2001年1月和4月,由“广西半宙”生产了掺有盐酸四环素的“梅花K”牌黄柏胶囊两箱共18.8万余板,经程书群在这批胶囊说明书上扩大药品功效和适应症、组织外包装后,向湖南等省市销售,致使发生群体性的中毒事件。
湖南省药检所检测表明:由于厂家添加了过期的四环素,其含有的降解产物远远超过国家允许的安全范围,特别是差向脱水四环素,服用后引起肾小管性酸中毒,临床上表现为多发性肾小管功能障碍综合症。


药物不良反应的重大“药害”事件药物是人们用于治疗、预防和诊断疾病或调节机体生理机能的化学物质。
欧美国家较早走了合成药物的道路,使大批量的药物生产成为可能。
以阿司匹林为例,全世界每年生产超过4.5万吨,仅德国拜耳公司1996年的销售量就高达110亿片。
正是在这样的情况下,一旦发生药物不良反应的“药害”事件,其涉及面会很广,危害就很大。
100年以来,全球曾发生重大的“药害”事件有40余起,使人们对药物的不良反应危害的严重性加深了认识。
其中比较突出的事件如下:沙利度胺与海豹畸胎沙利度胺(反应停)1957年首先在德国上市,因其能治疗孕妇的妊娠呕吐,迅速被推广到欧洲、亚洲、澳洲、北美(不包括美国)、拉丁美洲等几十个国家。
1961年10月,三位德国医生在西德妇科学家会议上报告了一些海豹肢畸形患儿的病例,引起了大家的重视。
以后其他地方报告接踵而来,许多新生婴儿的上肢、下肢特别短,甚至没有臂部和腿部,手和脚直接连在身体上。
经过长时间的流行病调查,证明这种“海豹肢畸形”是与患者的母亲在怀孕期间服用沙利度胺有关。
调查发现,该药在几个国家里共引起畸形1万余人,仅在西德就有6000到8000例。
值得注意的是,尽管反应停事件的危害如此之大,但是在美国、瑞士和当时的东德,由于对进口药品审批严格把关,基本上没有受到这个事件的冲击。
己烯雌酚与少女阴道癌1966—1969年间,美国波士顿市妇科医院的大夫们在较短的时间里先后发现有8名十多岁的少女患阴道癌,比同年龄组一个世纪以来报道的总数还多。
经过深入的调查,证明这些病例的发生与患者母亲妊娠期间服用己烯雌酚保胎有因果关系。
服药妇女所生的女儿患此癌的危险性比不服药的高出132倍。
其他医院也陆续有报道,至1972年,各地共收到91例8~25岁的阴道癌患者的报告,其中49例患者的母亲在妊娠期间服用过己烯雌酚。
非那西丁、磺胺酏剂与肾脏损害非那西丁曾是一种广泛使用的解热镇痛药。
1953年后,欧洲许多国家,特别是瑞士、西德、捷克等国家突然发现肾脏病人大量增加。

1.含汞药物与肢端疼痛病从19世纪末开始,欧洲大陆和英、美、澳等国家,曾经广泛应用一些含汞药物作为儿童驱虫药、止泻药等使用,用后不断发现一些儿童发生了肢端疼痛病、口腔发炎、牙龈肿胀、流涎、脱发、牙齿脱落等症状。
经查证,是含汞的药物所致。
仅英格兰和威尔士地区,死于这种含汞药物中毒的儿童,就达585人。
2.磺胺制剂与肾功能衰竭磺胺药是1932年德国克提拉和米奇合成的。
同年杜马克等进行动物实验,发现其具有抗细菌感染作用,成为医用磺胺药的开创者,荣获诺贝尔医学奖。
1937年秋天,美国田纳西州一个药厂,用工业溶剂二甘醇代替乙醇和糖,生产出一种磺胺制剂,供应美国南方的几个州,用于治疗感染性疾病。
不久后,该地区忽然发现肾脏衰竭的病人大量增加,经调查证实,由于服用该种磺胺制剂而发生肾衰竭者358人,死亡107人。
磺胺药的主要副作用是肾毒作用,容易在泌尿道析出结晶,引起血尿、尿闭等。
3.氨基比林与白细胞减少症氨基比林又叫匹拉米洞,属解热镇痛药。
1884年,克诺尔以安替匹林、盐酸、亚硝酸钠合成。
1897年首先在欧洲上市。
1922年以后,德、英、丹麦、瑞士、比利时和美国逐渐发现许多服用该药的病人发生了白细胞减少症,仅3年,美国死于该症者就有1 981人。
经证实,氨基比林是罪魁祸首。
许多药物,初上市时尚难发现其危害性,但经过一段时间,毒性便显示出来。
由此可见,“久经考验”的老药,比新药有更大的优越性。
4.黄热病疫苗与病毒性肝炎1942年,美国普遍接种黄热病疫苗,因为当时黄热病曾一度在美国军队中流行,使军队士气大减。
然而,在接受疫苗的300万军人中,有2.8万人发生了传染性肝炎,死亡62人。
调查结果发现,在注射的疫苗中,有9批疫苗的血清中混进了传染性肝炎已痊愈的志愿者的血清。
在我国,被传染乙型肝炎的人数十分惊人,应当引起足够的重视。
5.二碘二乙基锡与中毒性脑炎综合征1954年,在巴黎附近的一个药房里,配制生产出一种含二碘二乙基锡的抗感染药物。

国外发生的重大药害事件百余年来,世界上屡屡发生致死、致残的药害事件。
回顾这些历史,可时时提醒我们密切关注药品的安全问题,最大限度地减少药品给人类健康带来的危害,使这些悲剧不再重演。
1. 含汞药物与肢端疼痛病国外用汞和汞化合物作为药物已有1000多年的历史,在阿拉伯国家应用含汞的软膏治疗慢性皮肤病、麻风等。
哥伦布远航归来后,欧洲流行梅毒,汞剂成为治疗梅毒的唯一有效药物。
在英联邦,婴儿用的牙粉、尿布漂洗粉中含有汞和汞化合物,并曾经广泛用甘汞(氯化亚汞)作为幼儿的轻泻药和驱虫药。
1890年以后,首先在英国,然后在其它国家不断发现一些儿童发生肢端疼痛病,同时还有口腔发炎、牙龈肿胀、流涎、脱发、牙齿脱落等临床症状和体征。
经过长期的流行病学调查,证明许多病人是由于使用含汞药物所致。
仅在英格兰和威尔士地区,在1939~1948年间死于含汞药物中毒的儿童就有585人,其中多数是3岁以下的儿童。
2. 磺胺酏剂与肾功能衰竭磺胺类药于20世纪30年代问世。
1937年秋天,美国田纳西州Massengill公司用工业溶剂二甘醇代替乙醇和糖来生产一种磺胺酏剂,供应该国南方的几个州,用于治疗感染性疾病。
到这一年9~10月间,这些地方忽然发现肾功能衰竭的病人大量增加。
经调查,由于服用这种磺胺酏剂而发生肾功能衰竭的有358人,死亡107人。
尸检表明肾脏严重损害,死于尿毒症,究其原因,主要是二甘醇在体内经氧化代谢成草酸致肾损害所致。
3. 氨基比林与白细胞减少症氨基比林是1893年合成的一种解热镇痛药,1897年开始在欧洲上市,约1909年进入美国市场。
1922年以后,德国、英国、丹麦、瑞士、比利时和美国等国家逐渐发现,许多服用过此药的病人出现口腔炎,发热咽喉痛等症状。
临床检验结果为白细胞减少症、粒细胞减少症,调查证明二者有因果关系。
最终证实,氨基比林可导致粒细胞缺乏。
从1931年到1934年,仅美国一个国家死于氨基比林引起白细胞减少症的就有1981人,欧洲死亡200余人。
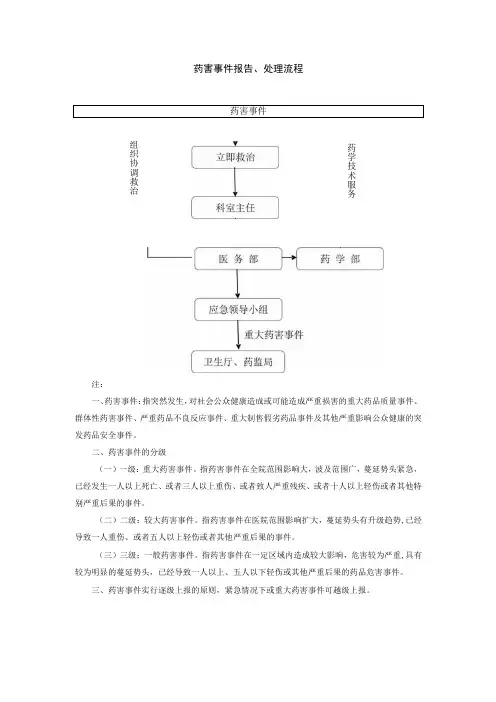
药害事件报告、处理流程 药害事件
注:
一、药害事件:指突然发生,对社会公众健康造成或可能造成严重损害的重大药品质量事件、群体性药害事件、严重药品不良反应事件、重大制售假劣药品事件及其他严重影响公众健康的突发药品安全事件。
二、药害事件的分级
(一)一级:重大药害事件。
指药害事件在全院范围影响大,波及范围广,蔓延势头紧急,已经发生一人以上死亡、或者三人以上重伤、或者致人严重残疾、或者十人以上轻伤或者其他特别严重后果的事件。
(二)二级:较大药害事件。
指药害事件在医院范围影响扩大,蔓延势头有升级趋势,已经导致一人重伤、或者五人以上轻伤或者其他严重后果的事件。
(三)三级:一般药害事件。
指药害事件在一定区域内造成较大影响,危害较为严重,具有较为明显的蔓延势头,已经导致一人以上、五人以下轻伤或其他严重后果的药品危害事件。
三、药害事件实行逐级上报的原则,紧急情况下或重大药害事件可越级上报。
组
织
协
调救
治 药学技术服
务。
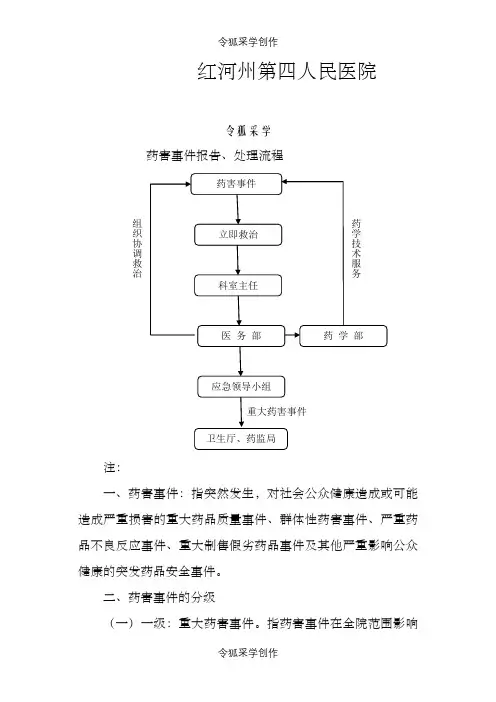
红河州第四人民医院
令狐采学
药害事件报告、处理流程
注:
一、药害事件:指突然发生,对社会公众健康造成或可能造成严重损害的重大药品质量事件、群体性药害事件、严重药品不良反应事件、重大制售假劣药品事件及其他严重影响公众健康的突发药品安全事件。
二、药害事件的分级
(一)一级:重大药害事件。
指药害事件在全院范围影响
大,波及范围广,蔓延势头紧急,已经发生一人以上死亡、或者三人以上重伤、或者致人严重残疾、或者十人以上轻伤或者其他特别严重后果的事件。
(二)二级:较大药害事件。
指药害事件在医院范围影响扩大,蔓延势头有升级趋势,已经导致一人重伤、或者五人以上轻伤或者其他严重后果的事件。
(三)三级:一般药害事件。
指药害事件在一定区域内造成较大影响,危害较为严重,具有较为明显的蔓延势头,已经导致一人以上、五人以下轻伤或其他严重后果的药品危害事件。
三、药害事件实行逐级上报的原则,紧急情况下或重大药害事件可越级上报。
红河州第四人民医院药事管理委员会
8月1日。
2023年药害事件总结概述2023年,在全球范围内发生了多起涉及药品安全的重大事件,引起了公众的广泛关注和担忧。
本文将就此次药害事件进行总结,并分析其中的原因及教训。
事件一:药品A致死事件2023年1月,在某个国家发生了一起由药品A引发的死亡事件。
据报道,药品A是一种常用的治疗心脏病的药物,然而该药品含有一种过量的成分,导致服用者心脏骤停并最终死亡。
该事件引发了社会上对药品安全的担忧和不信任。
调查结果显示,该药品生产商在生产过程中存在不当操作和质量控制不严的问题,导致了药品A的不合格批次上市。
这一事件揭示了药品监管体系存在的漏洞,也让公众对药品安全的关注提升到新的高度。
事件二:副作用波及全国的药品B2023年6月,国家药品监管部门通报了一种常用药品B的副作用问题。
据报道,药品B被广泛使用于感冒症状的缓解,然而近期发现该药品的副作用引发了大量患者的不适症状,包括恶心、呕吐和头晕等。
进一步的调查发现,药品B的生产商在制造过程中使用了一种新的添加剂,但没有充分测试和评估该添加剂的安全性。
导致这一副作用问题的出现。
药品监管部门迅速下发紧急通知,要求对该药品的销售进行召回并展开全面调查。
这一事件引发了公众对药品研发和测试的关注,同时也暴露了药品生产商在推出新药品前不充分测试和评估的风险。
事件三:假药A卷土重来2023年10月,国家警方在一次打击制假售假行动中发现了一起假冒药品A的案件。
据报道,一家非法制药厂商制造了一批假冒的药品A,并销售给广大市民,导致多名患者出现严重的不良反应。
调查发现,非法制药厂商通过使用与药品A相似的包装和商标来欺骗消费者,同时在药品中掺杂了大量不明成分。
这一事件再次揭示了药品监管的薄弱环节,让人们对药品安全产生了更深的担忧。
分析和教训2023年的药害事件凸显了药品安全监管体系中的漏洞和问题,同时也为未来的改进提供了重要的教训。
首先,药品生产商应加强质量控制。
在生产过程中,严格遵守相关规定和标准,并进行全面检测,确保药品的质量和安全性。
国外发生的重大药害事件百余年来,世界上屡屡发生致死、致残的药害事件。
回顾这些历史,可时时提醒我们密切关注药品的安全问题,最大限度地减少药品给人类健康带来的危害,使这些悲剧不再重演。
1. 含汞药物与肢端疼痛病国外用汞和汞化合物作为药物已有1000多年的历史,在阿拉伯国家应用含汞的软膏治疗慢性皮肤病、麻风等。
哥伦布远航归来后,欧洲流行梅毒,汞剂成为治疗梅毒的唯一有效药物。
在英联邦,婴儿用的牙粉、尿布漂洗粉中含有汞和汞化合物,并曾经广泛用甘汞(氯化亚汞)作为幼儿的轻泻药和驱虫药。
1890年以后,首先在英国,然后在其它国家不断发现一些儿童发生肢端疼痛病,同时还有口腔发炎、牙龈肿胀、流涎、脱发、牙齿脱落等临床症状和体征。
经过长期的流行病学调查,证明许多病人是由于使用含汞药物所致。
仅在英格兰和威尔士地区,在1939~1948年间死于含汞药物中毒的儿童就有585人,其中多数是3岁以下的儿童。
2. 磺胺酏剂与肾功能衰竭磺胺类药于20世纪30年代问世。
1937年秋天,美国田纳西州Massengill公司用工业溶剂二甘醇代替乙醇和糖来生产一种磺胺酏剂,供应该国南方的几个州,用于治疗感染性疾病。
到这一年9~10月间,这些地方忽然发现肾功能衰竭的病人大量增加。
经调查,由于服用这种磺胺酏剂而发生肾功能衰竭的有358人,死亡107人。
尸检表明肾脏严重损害,死于尿毒症,究其原因,主要是二甘醇在体内经氧化代谢成草酸致肾损害所致。
3. 氨基比林与白细胞减少症氨基比林是1893年合成的一种解热镇痛药,1897年开始在欧洲上市,约1909年进入美国市场。
1922年以后,德国、英国、丹麦、瑞士、比利时和美国等国家逐渐发现,许多服用过此药的病人出现口腔炎,发热咽喉痛等症状。
临床检验结果为白细胞减少症、粒细胞减少症,调查证明二者有因果关系。
最终证实,氨基比林可导致粒细胞缺乏。
从1931年到1934年,仅美国一个国家死于氨基比林引起白细胞减少症的就有1981人,欧洲死亡200余人。
史上最大药害事件:“反应停”事件1961年,一种曾用于妊娠反应的药物“反应停”。
导致了成千上万的畸胎,波及世界各地,受害人数超过15000人。
该事件被公认为史上最大的药害事件。
受药物影响的孕妇生出的婴儿没有手臂和腿,手直接连在躯干上,形似海豹,被称为“海豹肢”,这样的畸形婴儿死亡率达50%以上。
在怀孕一二个月之间,服用了反应停的母亲便生出这样的畸形儿。
这种婴儿手脚比正常人短,甚至根本没有手脚。
截至1963年在世界各地,如西德、美国、荷兰和日本等国,由于服用该药物而诞生了12 000多名这种形状如海豹一样的可怜的婴儿。
这个在市场上流通了6年的药品没有经过严格的临床试验,并且最初生产该药品的药厂隐瞒了收到的有关该药品毒性的一百多例报告。
致使日本等一些国家,迟至1963年才停止使用反应停,导致了近千例畸形婴儿的出生。
话说,“反应停”在实验室被称为MER-32,德国格郁能化学公司购买了反应停的专利。
公司对于反应停的宣传卖点是镇静效果,相比当时药效强副作用大的剂巴比妥酸盐及其类似产品来说,反应停药效一样且无副作用。
在当时大部分国家的药品监管制度宽松,几乎没有一个国家的药监部门提出,药品只有进行严格临床实验才能上市,企业只要组织一些不太严谨的研究资料就可以上市。
1957年,反应停仅以几份实验室报告和证词为基础的反应停即得到了德国、英国等国家的上市批准,并迅速延伸到20多个国家的市场。
自此,其“阴暗”的一面逐渐暴露出来。
在美国,销售这一药品的梅瑞公司,着重宣传该药物对于怀孕早期恶心的疗效。
可怕的是,该公司从未在这方面做过研究,在不知道药物是否会透过胎盘影响胎儿,且没有临床实验依据的前提下,大规模向1267名医生发放了250万片反应停试用。
当时的法律,在患者同意的基础上,医生可以以“实验”的名义给病人使用未经批准的新药,且不限制剂量,对于制药公司来说,赠送药物其实是一个更好的宣传推销途径。
当时的FDA的一些有良知的官员反曾对反应停的上市,他们发现反应停的临床研究不但数据不全,而且结果神乎其神,甚至有伪科学的胡言乱语。
国外发生的重大药害事件百余年来,世界上屡屡发生致死、致残的药害事件。
回顾这些历史,可时时提醒我们密切关注药品的安全问题,最大限度地减少药品给人类健康带来的危害,使这些悲剧不再重演。
1. 含汞药物与肢端疼痛病国外用汞和汞化合物作为药物已有1000多年的历史,在阿拉伯国家应用含汞的软膏治疗慢性皮肤病、麻风等。
哥伦布远航归来后,欧洲流行梅毒,汞剂成为治疗梅毒的唯一有效药物。
在英联邦,婴儿用的牙粉、尿布漂洗粉中含有汞和汞化合物,并曾经广泛用甘汞(氯化亚汞)作为幼儿的轻泻药和驱虫药。
1890年以后,首先在英国,然后在其它国家不断发现一些儿童发生肢端疼痛病,同时还有口腔发炎、牙龈肿胀、流涎、脱发、牙齿脱落等临床症状和体征。
经过长期的流行病学调查,证明许多病人是由于使用含汞药物所致。
仅在英格兰和威尔士地区,在1939~1948年间死于含汞药物中毒的儿童就有585人,其中多数是3岁以下的儿童。
2. 磺胺酏剂与肾功能衰竭磺胺类药于20世纪30年代问世。
1937年秋天,美国田纳西州Massengill公司用工业溶剂二甘醇代替乙醇和糖来生产一种磺胺酏剂,供应该国南方的几个州,用于治疗感染性疾病。
到这一年9~10月间,这些地方忽然发现肾功能衰竭的病人大量增加。
经调查,由于服用这种磺胺酏剂而发生肾功能衰竭的有358人,死亡107人。
尸检表明肾脏严重损害,死于尿毒症,究其原因,主要是二甘醇在体内经氧化代谢成草酸致肾损害所致。
3. 氨基比林与白细胞减少症氨基比林是1893年合成的一种解热镇痛药,1897年开始在欧洲上市,约1909年进入美国市场。
1922年以后,德国、英国、丹麦、瑞士、比利时和美国等国家逐渐发现,许多服用过此药的病人出现口腔炎,发热咽喉痛等症状。
临床检验结果为白细胞减少症、粒细胞减少症,调查证明二者有因果关系。
最终证实,氨基比林可导致粒细胞缺乏。
从1931年到1934年,仅美国一个国家死于氨基比林引起白细胞减少症的就有1981人,欧洲死亡200余人。