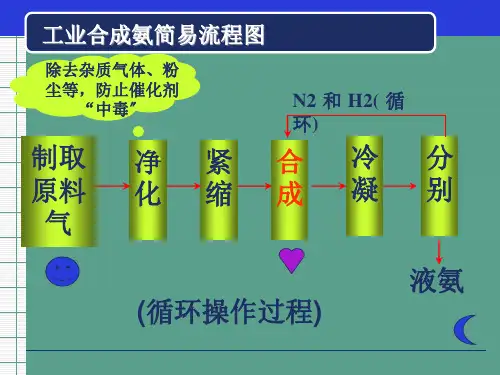
例已知2SO2(g)+O2(g)
其实验数据见表
2SO3 (g) △H<0
(1) 应选用的温度是_4_5_0_℃__。
(2)应采用的压强是_常__压___,理由是因__为__常__压__下_S__O2 _的__转_化__率__已__经__很_高__,__若__采__用_较__大__压__强__,_S__O_2_的_转__化__率__ 提高__很__少__,_但__需__要__的__动_力__更__大__,__对_设__备__的__要__求_更__高__。_。
_低__ 温、高___压有利于化学平衡正向移动, N2、H2浓度比为_1_:__3_有利于原料充分反应, 从而提高氨的产率。
讨论:能否用过量氮气提高氢气转
NH3% 化率?工业合成氨是否采用此方法?
实验表明:适当提高氮气比例为1:2.8,有利于合成氨 0.6 0.5 0.4
0.3
0.2
0.1
1:1 1:2 1:3 1:4 1:5 1:6
N2:H2
二、合成氨反应的速率
交流·研讨 (P66)
1、升高温度、增大压强 增大反应物浓度、使用催化剂
2、增大N2 、H2浓度,将氨及时 从混合气中分离出去
3、使用催化剂可以使合成氨 的速率提高上万亿倍
三、合成氨的适宜条件
1、请填写下表
外界条件
压强 温度 催化剂 反应物的浓度 生成氨的浓度
使NH3生产多 平衡分析
了以下反应途径,假设反应都能进行,你
C 认为最合理的是(
)
A. C3H8 高高温温脱氢C+H2
B. C3H8
C3H6+H2
C. C3H8+H2O 催化剂 CO+H2