离子交换膜电化学中的应用
- 格式:doc
- 大小:197.06 KB
- 文档页数:2

隔膜在电化学中的功能1.常见的隔膜隔膜又叫离子交换膜,由高分子特殊材料制成。
离子交换膜分三类:(1)阳离子交换膜,简称阳膜,只允许阳离子通过,即允许H+和其他阳离子通过,不允许阴离子通过。
(2)阴离子交换膜,简称阴膜,只允许阴离子通过,不允许阳离子通过。
(3)质子交换膜,只允许H+通过,不允许其他阳离子和阴离子通过。
2.隔膜的作用(1)能将两极区隔离,阻止两极区产生的物质接触,防止发生化学反应。
(2)能选择性的通过离子,起到平衡电荷、形成闭合回路的作用。
3.离子交换膜选择的依据离子的定向移动。
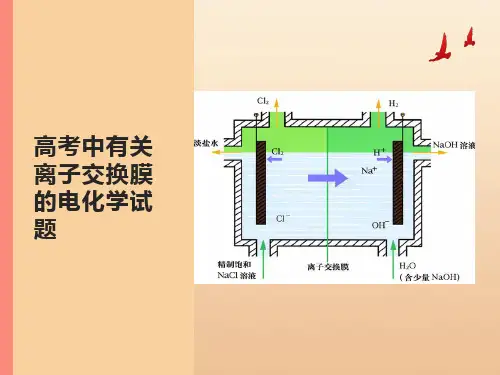
4.离子交换膜的应用1.用下面的装置制取NaOH、H2和Cl2,此装置有何缺陷?答案缺陷1:Cl2和H2混合而引起爆炸;缺陷2:Cl2与NaOH反应生成NaClO,影响NaOH的产量。
2.用下图装置电解饱和食盐水,其中阳离子交换膜的作用有哪些?答案(1)平衡电荷,形成闭合回路;(2)防止Cl2和H2混合而引起爆炸;(3)避免Cl2与NaOH反应生成NaClO,影响NaOH的产量;(4)避免Cl-进入阴极区导致制得的NaOH不纯。
每小题有一个或两个选项符合题意。
1.已知:电流效率等于电路中通过的电子数与消耗负极材料失去的电子总数之比。
现有两个电池Ⅰ、Ⅱ,装置如图所示。
下列说法正确的是()A.Ⅰ和Ⅱ的电池反应不相同B.能量转化形式不同C.Ⅰ的电流效率低于Ⅱ的电流效率D.5 min后,Ⅰ、Ⅱ中都只含1种溶质答案 C解析Ⅰ、Ⅱ装置中电极材料相同,电解质溶液部分相同,电池反应、负极反应和正极反应式相同,A项错误;Ⅰ和Ⅱ装置的能量转化形式都是化学能转化成电能,B项错误;Ⅰ装置中铜与氯化铁直接接触,会在铜极表面发生反应,导致部分能量损失(或部分电子没有通过电路),电流效率降低,而Ⅱ装置采用阴离子交换膜,铜与氯化铜接触,不会发生副反应,放电过程中交换膜左侧负极的电极反应式为Cu-2e-===Cu2+,阳离子增多,右侧正极的电极反应式为2Fe3++2e-===2Fe2+,负电荷过剩,Cl-从交换膜右侧向左侧迁移,电流效率高于Ⅰ装置,C正确;放电一段时间后,Ⅰ装置中生成氯化铜和氯化亚铁,Ⅱ装置中交换膜左侧生成氯化铜,右侧生成了氯化亚铁,可能含氯化铁,D项错误。




离子交换膜在电化学中的应用公开课导言:离子交换膜是一种特殊的薄膜,其具有离子选择性通透性,可以在电解过程中起到重要作用。
本文将探讨离子交换膜在电化学中的应用,并介绍其原理和优势。
一、离子交换膜的原理离子交换膜是由聚合物材料制成的,其内部有大量的离子交换基团。
这些基团可以选择性地吸附和释放电解质中的离子,实现离子的传输。
离子交换膜通常分为阳离子交换膜和阴离子交换膜两种类型,可以根据需要选择使用。
二、离子交换膜在电解过程中的应用1. 燃料电池燃料电池是一种将化学能转化为电能的装置,其中离子交换膜起到关键作用。
在燃料电池中,离子交换膜将氢离子(H+)从阳极传输到阴极,同时阻止了氢气与氧气的直接反应,保证了电池的正常工作。
2. 电解水在电解水过程中,离子交换膜可以将水分解为氢气和氧气。
离子交换膜的选择性传输特性使得只有阳离子或阴离子能够通过,从而实现了氢气和氧气的分离。
这对于制取纯净的氢气具有重要意义。
3. 盐水淡化离子交换膜还可以应用于盐水淡化过程中。
通过将盐水通过离子交换膜,离子交换膜可以选择性地阻止盐离子的传输,从而将盐水中的盐分去除,得到淡水。
这是一种高效的海水淡化方法。
4. 电解质传感器离子交换膜还可以应用于电解质传感器中。
电解质传感器通过测量电解质的浓度来检测化学反应或生物过程的变化。
离子交换膜可以实现离子的选择性传输,从而提高传感器的灵敏度和准确性。
三、离子交换膜的优势1. 高选择性:离子交换膜可以选择性地传输特定类型的离子,从而实现分离和纯化的目的。
这种高选择性使得离子交换膜在许多电化学应用中非常有用。
2. 低电阻:离子交换膜具有较低的电阻,可以有效地传输离子。
这有助于提高电化学反应的效率,并减少能量的损耗。
3. 高稳定性:离子交换膜具有较好的化学和物理稳定性,可以在广泛的温度和pH范围内工作。
这使得离子交换膜适用于各种极端条件下的应用。
4. 易于制备:离子交换膜的制备相对简单,成本较低。

电解池中离子交换膜
离子交换膜是一种能选择性穿透离子的薄膜,常用于电解池中。
电解池是一种电化学设备,其中发生化学反应,通过电解分解物质或将物质转化为其他物质。
电解池中的离子交换膜扮演着将正负离子分离的角色。
它使用某些材料的特殊结构,将溶液中的正负离子分开,只允许特定类型的离子通过。
这种膜可让溶液中的阳离子通过,但不允许阴离子通过(或相反)。
这样,电解池的正负极之间形成了离子的流动路径。
离子交换膜有许多应用,最常见的是在电解过程中用于分离正、负离子以及电解产物。
例如,水分解时,正极吸收阴离子(氧气产生),负极吸收阳离子(氢气产生)。
离子交换膜防止氢氧气混合。
此外,离子交换膜还用于许多其他领域,如电池、燃料电池、电解水制氢、离子交换色层分析法等。
电解池中的离子交换膜在加速化学反应、提高能量转化效率、减少产物污染等方面发挥着重要作用。


电化学中离子交换膜的应用电化学中离子交换膜是一种用于控制电流流量的复合薄膜,因其特殊的结构和性质,在电化学反应中可以起到有效的抑制和分离的作用,并可实现液膜的有序传输。
离子交换膜的应用最广泛的是在氢能电池、燃料电池、蓄电池和电解池当中。
首先,离子交换膜可以抑制氧还原反应,减少消耗,使电池在反应过程中能量损失小,提高其能量密度。
其次,离子交换膜能够有效地防止外界电荷到燃料电池内,使之维持净电池状态,同时可以改善电流分布,延长电池的使用寿命和液体充电/放电效率。
最后,离子交换膜在电解池的应用还可以降低水的蒸发,避免形成气泡。


高考化学:离子交换膜在电化学中的应用
离子交换膜在原电池和电解池中均有较广泛的应用,且常出常新。
1.离子交换膜的功能使离子选择性定向迁移,其目的是平衡整个电解质的离子电荷守恒。
2.交换膜在电化学中的作用
(1)防止副反应的发生,避免影响所制取产品的质量;防止引发不安全因素(如在电解饱和食盐水中,利用阳离子交换膜,防止阳极产生的Cl2进入阴极室与氢氧化钠反应,导致所制产品不纯,防止与阴极产生的H2混合发生爆炸)。
(2)用于物质的分离、提纯等。
(3)用于制备纯净的物质。
3.离子交换膜的类型根据透过的微粒,离子交换膜可以分为多种,在高考试题中主要出现过阳离子交换膜、阴离子交换膜和质子交换膜三种。
阳离子交换膜只允许阳离子通过,阻止阴离子和气体通过,阴离子交换膜只允许阴离子通过,质子交换膜只允许质子(H+)通过,另外还有特殊离子交换膜,只允许相应的离子通过。
4.离子交换膜类型的判断根据电解质溶液呈电中性的原则,判断膜的类型:
(1)首先写出阴、阳两极上的电极反应,依据电极反应式确定该电极附近哪种离子剩余。
(2)根据溶液呈电中性,判断出离子移动的方向,从而确定离子交换膜的类型。
(3)在利用电解原理制备物质时,选择离子交换膜的类型,既要考虑阴、阳极电极反应式,同时也要考虑产品室和原料室在装置图中的位置。
如:利用电解NaB(OH)4溶液制备H3BO3,装置图如下:
阳极室放出O2,消耗OH-余出H+,则H+应向产品室移动,阴极室放出H2,消耗H+余出OH-,则原料室中的Na+应向阴极室移动,B(OH)4-应向产品室移动,所以a膜、c 膜为阳离子交换膜、b膜为阴离子交换膜,选择离子交换膜时产品室和原料室的位置也起到关键性的作用。
专题5.9 电化学离子交换膜的分析与应用【必备知识】1、离子交换膜的含义和作用(1)含义:离子交换膜又叫隔膜,由高分子特殊材料制成(2)作用①能将两极区隔离,阻止两极区产生的物质接触,防止发生化学反应,如:在电解饱和食盐水中,利用阳离子交换膜,防止阳极产生的Cl2进入阴极室与氢氧化钠反应,导致所制产品不纯;防止与阴极产生的H2混合发生爆炸②能选择性的通过离子,起到平衡电荷、形成闭合回路的作用③用于物质的分离、提纯等④用于物质的制备,电解后溶液阴极区或阳极区得到所制备的物质2、离子交换膜的类型(1)阳离子交换膜——只允许阳离子和水分子通过,阻止阴离子和气体通过以锌铜原电池为例,中间用阳离子交换膜隔开①负极反应式:Zn-2e-===Zn2+②正极反应式:Cu2++2e-===Cu③Zn2+通过阳离子交换膜进入正极区④阳离子透过阳离子交换膜原电池正极(或电解池的阴极)(2)阴离子交换膜——只允许阴离子和水分子通过,阻止阳离子和气体通过以Pt为电极电解淀粉-KI溶液,中间用阴离子交换膜隔开①阴极反应式:2H2O+2e-===H2↑+2OH-②阳极反应式:2I--2e-===I2③阴极产生的OH-移向阳极与阳极产物反应:3I2+6OH-===IO-3+5I-+3H2O④阴离子透过阴离子交换膜电解池阳极(或原电池的负极)(3)质子交换膜——只允许H+和水分子通过在微生物作用下电解有机废水(含CH3COOH),可获得清洁能源H2①阴极反应式:2H++2e-===H2↑②阳极反应式:CH3COOH-8e-+2H2O===2CO2↑+8H+③阳极产生的H+通过质子交换膜移向阴极④H+透过质子交换膜原电池正极(或电解池的阴极)3、离子交换膜类型的判断——根据电解质溶液呈电中性的原则,判断膜的类型方法与 技巧(1)首先写出阴、阳两极上的电极反应,依据电极反应式确定该电极附近哪种离子剩余 (2)根据溶液呈电中性,判断出离子移动的方向,从而确定离子交换膜的类型实例分析:电解饱和食盐水分析 方法电解饱和食盐水时,阴极反应式为2H 2O +2e -===H 2↑+2OH -,则阴极区域破坏水的电离平衡,OH -有剩余,阳极区域的Na +穿过离子交换膜进入阴极室,与OH -结合生成NaOH ,故电解食盐水中的离子交换膜是阳离子交换膜【精准训练1】1、Kolbe 法制取乙烯的装置如图所示,电极a 上的产物为乙烯和碳酸根离子。
ptfe离子交换膜
聚四氟乙烯(PTFE)离子交换膜是一种用于电化学分离和反应
的薄膜材料。
它具有许多独特的特性和应用,下面我将从多个角度
来介绍。
首先,PTFE离子交换膜具有优异的化学稳定性和耐腐蚀性。
这
使得它在各种酸、碱和溶剂中都能保持稳定,适用于各种恶劣的化
学环境下的应用。
这种稳定性使得PTFE离子交换膜在电化学领域中
得到广泛应用,例如在电解池中用于离子选择性透过和分离。
其次,PTFE离子交换膜具有良好的热稳定性和机械强度。
它能
够在高温下保持稳定性,并且具有较高的机械强度和耐磨损性,这
使得它在高温高压下的应用中表现出色。
因此,它常被用于燃料电
池和电解反应器等高温高压环境中。
此外,PTFE离子交换膜还具有良好的离子传导性能。
它能够选
择性地传递特定离子,如阳离子或阴离子,而阻止其他离子的通过。
这种离子选择性传导性能使得PTFE离子交换膜在电解、电渗析和电
化学传感器等领域有着广泛的应用。
总的来说,PTFE离子交换膜由于其优异的化学稳定性、热稳定性、机械强度和离子传导性能,在电化学分离和反应领域有着广泛的应用前景。
它在能源、环保、化工等领域都有着重要的作用,是一种功能性材料,对于推动科技进步和社会发展具有重要意义。
DAY7高考化学之电化学离子交换膜的分析与应用电化学离子交换膜是一种能够选择性地通过离子的膜材料,其在电化学反应和离子传输方面具有重要的分析和应用价值。
本文将从电化学离子交换膜的原理、分析方法和应用方面进行阐述。
首先,电化学离子交换膜的原理是基于离子在电场作用下的迁移特性。
它是由具有离子交换基团的聚合物材料构成的,其中离子交换基团能够选择性地吸附和释放离子。
当在电场存在下,离子交换膜会根据离子的电荷和大小而选择性地通过一些离子,从而实现离子的分离和纯化。
其次,电化学离子交换膜在分析中具有广泛的应用。
其中一种重要的应用是电化学分析,例如电化学法测定溶液中离子浓度和电荷的方法。
通过放置电化学离子交换膜在电化学池中,可以选择性地通过特定离子,然后测量通过离子交换膜的离子电流,进而计算出溶液中的离子浓度。
此外,电化学离子交换膜还可以用于电化学合成、电解制备和阳极保护等过程的离子传输。
此外,电化学离子交换膜还广泛应用于电池、燃料电池、电解池等器件中。
在电池中,电化学离子交换膜作为隔膜起到分隔阳极和阴极的作用,防止电子直接传递而产生短路。
在燃料电池中,离子交换膜则起到将氢离子从阴极传输到阳极,同时阻止氧气与氢离子直接反应的作用。
在电解池中,电化学离子交换膜可以选择性地传输特定离子,实现离子的纯化和分离。
总之,电化学离子交换膜在电化学分析和电化学器件中具有重要的分析和应用价值。
通过选择性地通过离子,它可以实现离子浓度的测定、离子传输的控制和离子分离纯化的目的。
未来,电化学离子交换膜的研究和应用将会越来越受到关注,并在更多领域中得到广泛应用。
1.如图所示阴阳膜组合电解装置用于循环脱硫,用NaOH溶液在反应池
中吸收尾气中的二氧化硫,将得到的Na2SO3溶液进行电解又制得
NaOH。
其中a、b离子交换膜将电解槽分为三个区域,电极材料为石
墨,产品C为H2SO4溶液。
下列说法正确的是()
A. b为只允许阳离子通过的离子交换膜
B. 阴极区中B最初充入稀NaOH溶液,产品E为氧气
C. 反应池采用气、液逆流方式,目的是使反应更充分
D. 阳极的电极反应式为
2.如图是利用一种微生物将废水中的有机物(如淀粉)和废气NO的化学能直接转化为电
能,下列说法中一定正确的是()
A.质子透过阳离子交换膜由右向左移动
B. 电子流动方向为
C. M电极反应式:
D. 当M电极微生物将废水中 g淀粉转化掉时,N电极产生 L 标况下
3.三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,ab、cd均为离子
交换膜,在直流电场的作用下,两膜中间的Na+和SO42-可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室。
下列叙述正确的是()
A. 通电后中间隔室的离子向正极迁移,正极区溶液pH增大
B. 该法在处理含废水时可以得到NaOH和产品
C. 负极反应为,负极区溶液pH降低
D. 当电路中通过1mol电子的电量时,会有的生成
4.某电源装置如图所示,电池总反应为2Ag+Cl2=2AgCl.下列说法正确的是()
A. 正极反应为
B. 放电时,交换膜右侧溶液中有大量白色沉淀生成
C. 若用NaCl溶液代替盐酸,则电池总反应随之改变
D. 当电路中转移时,交换膜左侧溶液中约减少离子
5.科学家用氮化镓(GaN)材料与铜作电极组装如图所示的人工光合系统,成功地实现了
以CO2和H2O合成CH4.下列说法不正确的是
A. 该过程是将太阳能转化为化学能和电能
B. GaN表面发生氧化反应,有产生
C. 电解液中从质子交换膜右侧向左侧迁移
D. Cu 表面电极反应式:
6.以铬酸钾(K2CrO4)为原料用电化学法制备K2Cr2O7的装置如图,下列说法正确的是
A. a极的电极反应式为
B. 电解过程中氢氧化钾溶液的浓度保持不变
C. b极上发生氧化反应生成
D. 电解过程中从右侧通过离子交换膜迁移到左侧。