第三章 第二节 第三课时 铁的重要化合物
- 格式:ppt
- 大小:1.69 MB
- 文档页数:45


第三章第二节第三课时铁的重要化合物课时跟踪训练一、选择题1. (2019云南玉溪峨山一中月考)下列说法中正确的是()A. 铁在干燥的空气中剧烈燃烧有黑色固体生成B. 铁跟盐酸反应生成氯化铁和氢气C. 铁丝浸入硫酸铜溶液中片刻,其表面出现红色的铁锈D. 烤蓝是在铁制品表面通过化学反应生成致密的氧化膜以防止铁生锈解析:选 D 铁丝在空气中只能烧至发红,不会剧烈燃烧,在纯氧中剧烈燃烧火星四射生成黑色的四氧化三铁固体, A 错误;铁跟盐酸反应生成氯化亚铁和氢气, B 错误;铁丝浸入硫酸铜溶液中片刻,铁与硫酸铜反应生成硫酸亚铁和铜,取出,表面出现红色的铜,而不是红色的铁锈, C 错误;烤蓝是在铁制品表面通过化学反应生成致密的氧化膜,可以防止生锈, D 正确。
故选D。
2. (2019山东荣成六中高一月考)化学与生活密切相关,下列说法错误的是()A. 用粘土焙烧制得的红陶,陶器显红色的原因可能是含有F@O3B. 制指南针的磁石主要成分是四氧化三铁C. 碳酸钠可以制成抗酸药,服用时喝些醋能提高药效D. K-Na合金可作核反应堆的导热剂;Mg-AI合金可用于制造飞机部件解析:选C Fe2O3为红色粉末,可用作陶器的着色剂,故A项正确;四氧化三铁有磁性,可制成磁石,故 B 项正确;醋酸会与碳酸钠反应,消耗碳酸钠,降低药效,故 C 项错误;钠钾合金熔点低,可作原子反应堆的导热剂,Mg-AI 合金的密度小硬度大,可用于制造飞机部件,故 D 项正确。
故选C。
3. (2019贵州剑河期末)在空气中氢氧化亚铁白色沉淀可转化为红褐色沉淀。
关于该反应的下列叙述中不正确的是()A. 生成物为氢氧化铁B.该反应是化合反应C.该反应是氧化还原反应D.氢氧化亚铁作氧化剂解析:选 D 由上述分析知道,氢氧化亚铁白色沉淀转化为红褐色沉淀,生成物是氢氧化铁,故 A 正确;上述反应符合化合反应的特征,该反应是化合反应,故B 正确;该反应中有化合价变化,是氧化还原反应,故C正确;在4Fe(OH)2 + 2H2O + O2===4Fe(OH)3中,氢氧化亚铁作还原剂,O2作氧化剂,故D错误。

第三章金属及其化合物第二节几种重要的金属化合物(第3课时)一、说教材本节教材是人教版化学必修1第三章第二节“几种重要的金属化合物”中的一部分。
前面学生已经学习了从实验学化学和化学物质及其变化的知识,本章开始学习具体的元素化合物知识,这是为前面两章实验和理论知识补充感性认识的材料,又为以后学习必修2 的物质结构、元素周期律打下基础。
铁是中学阶段需要重点学习的唯一的变价金属元素,铁主要呈现+2、+3价。
铁元素是人体生命活动比不缺少的微量元素之一。
二、说目标知识与技能目标:(1)铁的氧化物及其物理、化学性质特点(FeO、Fe2O3、Fe3O4)。
(2)铁的氢氧化物的制备、物理性质、化学性质。
(3)Fe3+的检验方法,及Fe2+和Fe3+的相互转化。
过程与方法目标:(1)通过运用分类、比较、归纳的方法学习铁的重要化合物的性质,使学生学会分类、比较、归纳的学习方法。
(2)以Fe(OH)2可被氧化成Fe(OH)3预测Fe2+能被氧化成Fe3+,使学生学会运用已知物质的性质推断未知物质的性质,再通过实验探究验证假设的科学研究方法。
情感态度和价值观:(1)通过活动,让学生体验合作探究的过程,使学生体验科学研究的严谨态度。
(2)通过二价铁和三价铁的相互转化,使学生领悟到在一定条件下物质是可以相互转化的辩证思想。
(3)通过对生活中相关素材的研究,培养学生用化学视角关注生活的习惯,体会化学对人类生活的重要影响。
三、说重难点教学重点:氢氧化亚铁的性质、Fe3+的检验及Fe2+和Fe3+的相互转化;教学难点: Fe2+和Fe3+的相互转化和氧化还原反应原理的应用。
二、学情分析:在知识上,学生已经具备了氧化还原反应、离子反应的理论基础知识,并学习了Na和Al的化合物性质,对铁盐、亚铁盐等铁的化合物有一定的认识。
在能力上,学生已经初步具备了观察能力、实验能力、思维能力。
在情感上乐于探究物质变化的奥妙。
但由于学生刚刚开始学习元素化合物,对氧化还原知识尚不能熟练应用,对常见的氧化剂、还原剂并不熟悉,加上实验能力有限,导致他们的探究能力有限,所以要对学生做好引导。




铁的重要化合物一、教材内容分析《铁的重要化合物》是人教版高中化学必修一第三章第二节内容。
在“第一章从实验学化学”和“第二章化学性质及其变化”的基础上,进入元素化学的学习,从构成常见的物质的元素知识开始,引导学生从化学的角度了解丰富多彩的世界。
元素化合物知识是中学化学的基础知识,也是工作和生活中经常接触和了解的基本知识,这些知识既可以为前面学习的实验和理论知识补充感性认识材料,又能为介绍接下来介绍物质的结构、元素周期律、化学反应与能量等理论知识打下重要的基础,也可以帮助学生逐步掌握学习化学的一些基本方法,还能使学生认识到化学在促进社会发展、改善人类的生活条件等方面起到重要的作用。
本节课教材内容突出了课程标准中要求的铁的化合物的主要性质,注意与已学知识的联系与衔接,引导学生主动运用已有知识分析和解决新的问题,并逐步形成较为系统的知识网络。
(1)对钠、铝、铁、铜四种重要金属的化合物的性质从“物质分类”角度按氧化物、氢氧化物和相应盐的顺序编写,有利于从一类化合物的性质中找出共性,形成规律性的知识,也有利于对同类其他化合物的认识和推断;(2)与离子反应及氧化还原反应知识的衔接。
二、教材内容处理本节教材按照“金属氧化物——氢氧化物——盐”的顺序来编排,其中铁的金属氧化物和铁盐相关知识点是通过设计验证性实验和探究性实验的形式来展示,故在教学过程中可以用实验演示或者学生动手实验的模式来进行教学,形象、直观地将知识点传授给学生。
教材中有很多实验的图片,教学可以充分利用这些图片进行相关讲解和演示;同时教材的每个实验都有进行相关归纳的表格,利用表格的填写和对实验的归纳可以培养学生观察实验、归纳知识的能力。
在这节课中,铁的氢氧化物、Fe2+和Fe3+之间的相互转化是重点,而且Fe2+和Fe3+之间的相互转化又是难点,掌握这节课就要掌握好这些重点难点。
三、学生情况分析高中学生是处于心理发展成熟期,思维发展处于从形象到抽象的过渡期,而这节课是高一学生学习完化学实验和化学性质及变化后接触到金属元素化合物其中一个内容,要求学生对这些物质的性质和应用有所了解、掌握,为接下来的学习奠定基础。



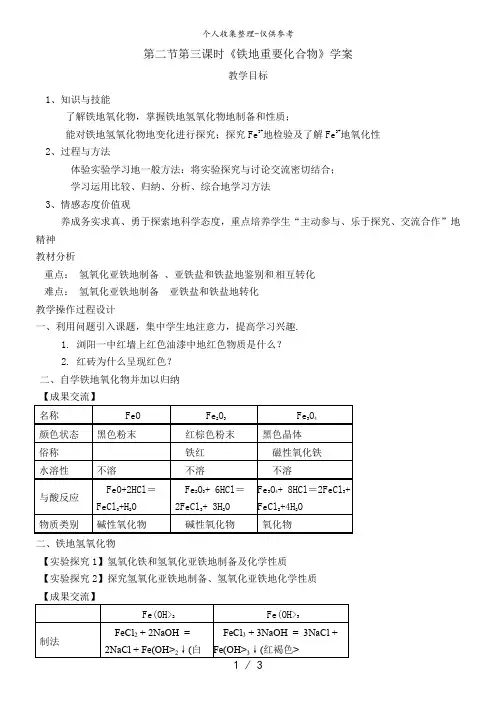
第二节第三课时《铁地重要化合物》学案
教学目标
1、知识与技能
了解铁地氧化物,掌握铁地氢氧化物地制备和性质;
能对铁地氢氧化物地变化进行探究;探究Fe3+地检验及了解Fe3+地氧化性
2、过程与方法
体验实验学习地一般方法:将实验探究与讨论交流密切结合;
学习运用比较、归纳、分析、综合地学习方法
3、情感态度价值观
养成务实求真、勇于探索地科学态度,重点培养学生“主动参与、乐于探究、交流合作”地精神
教材分析
重点:氢氧化亚铁地制备、亚铁盐和铁盐地鉴别和相互转化
难点:氢氧化亚铁地制备亚铁盐和铁盐地转化
教学操作过程设计
一、利用问题引入课题,集中学生地注意力,提高学习兴趣.
1. 浏阳一中红墙上红色油漆中地红色物质是什么?
2. 红砖为什么呈现红色?
二、自学铁地氧化物并加以归纳
【成果交流】
二、铁地氢氧化物
【实验探究1】氢氧化铁和氢氧化亚铁地制备及化学性质
【实验探究2】探究氢氧化亚铁地制备、氢氧化亚铁地化学性质
【成果交流】
三、铁盐和亚铁盐
【提问】有哪些方法可以鉴别Fe 3+和 Fe 2+?
【讨论】根据前面地实验,归纳总结:二价铁盐、三价铁盐地鉴别方法
【实验探究3】硫氰化钾溶液加入铁盐和亚铁盐溶液中地现象
【实验探究4】
溶液中加入【小结】
【问题2【问题3】铝盐和铁盐地净水作用地实验探究? 【作业】离子方程式地地巩固和课后习题
申明:
所有资料为本人收集整理,仅限个人学习使用,勿做商业用途.。