溶解平衡图像
- 格式:doc
- 大小:332.00 KB
- 文档页数:5

某温度时, Ag2SO4在水中的沉淀溶解平衡曲线如图所示。
该温度下,下列说法正确的是A.含有大量 SO42-的溶液中肯定不存在 Ag+B.0.02mol/L 的 AgNO3溶液与 0.2mol/L 的 Na2SO4溶液等体积混合不会生成沉淀C.Ag2SO4的溶度积常数( Ksp)为 1×10- 3 D.a 点表示 Ag2SO4的不饱和溶液,蒸发可以使溶液由 a 点变到 b 点某温度时, Ag2SO4在水中的沉淀溶解平衡曲线如图所示。
该温度下,下列说法正确的是A.含有大量 SO42-的溶液中肯定不存在 Ag+【Ag+是一定存在的,只是量的多少而已,排除A】B.0.02mol/L的AgNO3溶液与0.2mol/L的Na2SO4溶液等体积混合不会生成沉淀【假设不沉淀,则 c(Ag+)×c( Ag+)×c( SO4^(2-) )=0.01 ×0.01 ×0.1 =0.00001 】根据图像可判定 Ksp=【图像不清晰,可依据图像求出】【如果横纵坐标的数量级均为10- 2 次方,则 Ksp= 0.00002 】【然后依据 Ksp 与上面求出的浓度积比较,不出现沉淀】C.Ag2SO4的溶度积常数( Ksp)为 1×10- 3【Ksp=c(Ag+)× c( Ag+)× c( SO4^(2-) )= 0.00002 ,排除 C】D.a 点表示 Ag2SO4的不饱和溶液,蒸发可以使溶液由 a 点变到 b 点【蒸发的过程中,Ag+和硫酸根离子浓度均将增大,因而不会水平变化,排除D】【考点】沉淀溶解平衡 , 沉淀溶解平衡常数的概念 , 浓度的定义 , 图像信息的提取【分析】 A 选项考查学生对沉淀的理解是否准确 ;B 选项可以直接利用图像得出结论 ;D 选项要求学生理解浓度的概念和影响因素 , 并隐含考查了用图像表达实验结果的能力 , 可以拓展问学生如果出 a 点蒸发溶液成分变化趋势在图中如何反映出来 . 本题得分率很不理想 ,可见学生对于沉淀溶解平衡的方程式以及溶度积常数的表达式很不熟悉, 这个要求是必须要达到的 , 是化学平衡常数的直接迁移应用.C[ 相应知识点归纳 ]⑴.在温度不变时,无论改变哪种离子的浓度,另一种离子的浓度只能在曲线上变化,不会出现在曲线外的点⑵.溶液在蒸发时,离子浓度的变化分两种情况:ⅰ、原溶液不饱和时,离子浓度要增大都增大;ⅱ、原溶液饱和时,离子浓度都不变。

高考化学一轮总复习教师用书:
沉淀溶解平衡图像及分析
必备知识·梳理夯实
知识梳理
1.两类沉淀溶解平衡图像
(1)沉淀溶解平衡——浓度图像
①典型示例(以某温度下AgBr在水中的沉淀溶解平衡曲线为例)
②图中点的变化及分析
a →c曲线上变化,增大c(Br-)
d→c加入AgNO3(忽略溶液体积变化)
c→a曲线上变化,增大c(Ag+)
曲线上方的点表示有沉淀生成,曲线下方的点表示不饱和溶液,曲线上的点处于平衡状态
(2)沉淀溶解平衡——对数图像
图像分析
pM=-lg c(M) (M:Mg2+、Ca2+、Mn2+),p c(CO2-3)=-lg c(CO2-3)
横坐标数值越大,c(CO2-3)越小
纵坐标数值越大,c(M)越小
线上方的点为相应物质的不饱和溶液线下方的点表示有相应物质的沉淀生成
线上的点为相应物质的饱和溶液
根据线上任意一点的坐标,可计算相应物质的K sp
沉淀滴定曲线是沉淀滴定过程中构成难溶电解质的离子浓度与沉淀剂加入量之间的关
系曲线。
T℃,分别向10.00 mL 0.1 mol·L-1的KCl和K2CrO4溶液中滴加0.1 mol·L-1AgNO3溶液,滴定过程中-lg c(M)(M为Cl-或CrO2-4)与AgNO3溶液体积(V)的变化关系如图所示。
(1)曲线L1代表与-lg c(Cl-) 与V(AgNO3溶液)的变化关系。
(2)T℃时,溶度积K sp(Ag2CrO4)= 4.0×10-12。
(3)相同实验条件下,若改为0.05 mol·L-1的KCl和K2CrO4溶液,则曲线L2中N点向点Q上方移动。

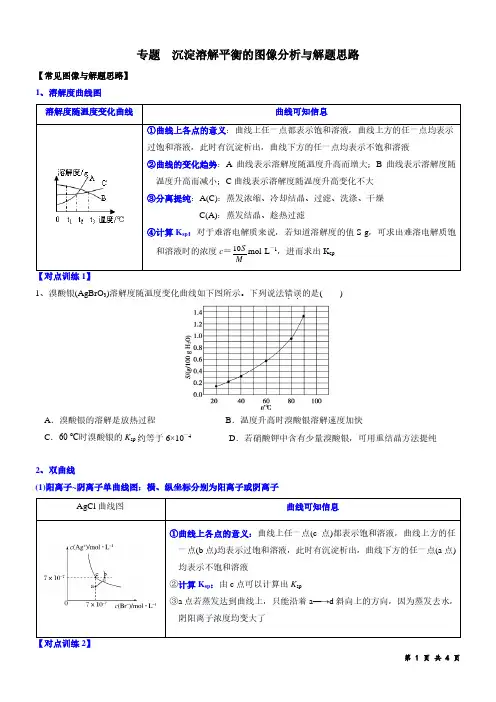
第 1 页 共 4 页 专题 沉淀溶解平衡的图像分析与解题思路【常见图像与解题思路】1、溶解度曲线图1、溴酸银(AgBrO 3)溶解度随温度变化曲线如下图所示。
下列说法错误..的是( )A .溴酸银的溶解是放热过程B .温度升高时溴酸银溶解速度加快C .60 ℃时溴酸银的K sp 约等于6×10-4 D .若硝酸钾中含有少量溴酸银,可用重结晶方法提纯2、双曲线 (1)阳离子~阴离子单曲线图:横、纵坐标分别为阳离子或阴离子AgCl 曲线图曲线可知信息①曲线上各点的意义:曲线上任一点(c 点)都表示饱和溶液,曲线上方的任一点(b 点)均表示过饱和溶液,此时有沉淀析出,曲线下方的任一点(a 点)均表示不饱和溶液②计算K sp :由c 点可以计算出K sp③a 点若蒸发达到曲线上,只能沿着a ―→d 斜向上的方向,因为蒸发去水,阴阳离子浓度均变大了【对点训练2】第 2 页 共 4 页1、在T ℃时,铬酸银(Ag 2CrO 4)在水溶液中的沉淀溶解平衡曲线如图所示。
下列说法中不正确的是( )A .T ℃时,在Y 点和Z 点,Ag 2CrO 4的K sp 相等B .向饱和Ag 2CrO 4溶液中加入固体K 2CrO 4不能使溶液由Y 点变为X 点C .T ℃时,Ag 2CrO 4的K sp 为1×10-8D .图中a =2×10-4(2)阴阳离子浓度~温度双曲线图:横、纵坐标分别为阳离子或阴离子,两条曲线为不同温度 BaSO 4 曲线可知信息 ①曲线上各点的意义:每条曲线上任一点都表示饱和溶液,曲线上方的任一点均表示过饱和溶液,此时有沉淀析出,曲线下方的任一点均表示不饱和溶液T 1曲线:a 、b 点都表示饱和溶液,c 点表示过饱和溶液T 2曲线:a 、b 点都表示不饱和溶液,c 点表示不饱和溶液②计算K sp :由a 或b 点可以计算出T 1温度下的K sp③比较T 1和T 2大小:因沉淀溶解平衡大部分为吸热,可知:T 1<T 2【对点训练3】1、已知溴酸银的溶解是吸热过程,在不同温度条件下,溴酸银的溶解平衡曲线如图所示,下列说法正确的是( )A .T 1>T 2 B .加入AgNO 3固体,可从a 点变到c 点C .a 点和b 点的K sp 相等D .c 点时,在T 1、T 2两个温度条件下均有固体析出3、对数曲线①当坐标表示浓度的对数时,要注意离子浓度的换算,如lg c (X)=a ,则c (X)=10a②当坐标表示浓度的负对数(-lgX =pX)时,pX 越大,c (X)越小,c (X)=10-pX (1)正对数[lg c (M +)~lg c (R -)]曲线:横、纵坐标分别为阳离子或阴离子的正对数第 3 页 共 4 页 CuS 、ZnS 曲线可知信息①曲线上各点的意义:每条曲线上任一点都表示饱和溶液,曲线上方的任一点均表示过饱和溶液,此时有沉淀析出,曲线下方的任一点均表示不饱和溶液ZnS 曲线:a 点表示饱和溶液,c 点表示不饱和溶液CuS 曲线:b 点都表示不饱和溶液,c 点表示过饱和溶液②计算K sp :由曲线上面给定数据可以计算CuS 、ZnS 的K sp③比较K sp 大小:K sp (ZnS)>K sp (CuS)【对点训练4】1、硫酸锶(SrSO 4)可用于烟火和陶瓷工业,该物质是矿物天青石的主要成分,可由Na 2SO 4溶液加入锶盐溶液沉淀而得。




第4课时难溶电解质沉淀溶解平衡图像分析[核心素养发展目标] 1.理解难溶电解质沉淀溶解平衡并会应用解决相关问题。
2.学会沉淀溶解平衡图像的分析方法。
一、曲线型图像1.沉淀溶解平衡K sp曲线(1)典型示例(2)点的变化①a→c:曲线上变化,增大c(SO2-4);②b→c:加入1×10-5 mol·L-1 Na2SO4溶液(加水不行);③d→c:加入BaCl2固体(忽略溶液的体积变化);④c→a:曲线上变化,增大c(Ba2+);⑤曲线上方的点表示有沉淀生成;曲线下方的点表示不饱和溶液。
2.c(M n+)—pH图像Fe(OH)3和Cu(OH)2的c—pH关系如图(温度一定):图中曲线为相应金属阳离子氢氧化物的沉淀溶解平衡曲线,可利用图像判断有关氢氧化物的K sp的大小以及离子分离方法的选择。
1.(2022·青岛高二检测)一定温度下,AgCl(s)Ag+(aq)+Cl-(aq)体系中,c(Ag+)和c(Cl-)的关系如图所示。
下列说法不正确的是()A .在AgCl 溶于水形成的饱和溶液中:c (Ag +)=c (Cl -)B .b 点的溶液中加入少量AgNO 3固体,会析出白色沉淀C .d 点溶液中加入少量AgCl 固体,c (Ag +)和c (Cl -)均增大D .a 、b 、c 三点对应的AgCl 的K sp 和溶解度皆不相等答案 D解析 在AgCl 溶于水形成的饱和溶液中存在沉淀溶解平衡:AgCl(s)Ag +(aq)+Cl -(aq),AgCl 溶解生成的c (Cl -)=c (Ag +),故A 正确;b 点溶液为饱和溶液,加入少量的AgNO 3固体,使c (Ag +)增大,沉淀溶解平衡逆向移动,会析出白色沉淀,故B 正确;d 点溶液为不饱和溶液,加入少量AgCl 固体会继续溶解,则c (Cl -)和c (Ag +)都增大,故C 正确;a 、b 、c 三点都在沉淀溶解平衡曲线上,且温度不变,则K sp 不变,AgCl 的溶解度也只与温度有关,则a 、b 、c 三点对应的AgCl 的K sp 和溶解度均相等,故D 错误。

第2课时 沉淀溶解平衡的应用【课程标准要求】1.能用平衡移动原理分析理解沉淀的溶解与生成、沉淀转化的实质。
2.学会用沉淀溶解平衡的移动解决生产、生活中的实际问题。
一、沉淀的溶解与生成1.溶度积规则利用浓度商(Q )与平衡常数(K sp )的相对大小判断沉淀的溶解和生成:(1)Q >K sp ,溶液中的离子生成沉淀,直至平衡; (2)Q =K sp ,沉淀溶解与离子生成沉淀处于平衡状态;(3)Q <K sp ,若体系中有足量固体,则固体溶解,直至平衡。
2.应用(1)常使用BaSO 4作为内服造影剂,这种透视技术俗称钡餐透视,但BaCO 3不可用作钡餐,如果误服可溶性钡盐,中毒者应尽快使用5%的Na 2SO 4洗胃。
(2)石笋、钟乳石和石柱的形成,涉及的化学反应有:CaCO 3+CO 2+H 2O===Ca(HCO 3)2、Ca(HCO 3)2=====△CaCO 3↓+H 2O +CO 2↑。
(3)珊瑚虫可以从周围的海水中获取Ca 2+和HCO -3,经反应Ca 2++2HCO -3CaCO 3+CO 2+H 2O 形成珊瑚。
【微自测】1.下列描述中,正确的画“√”,错误的画“×”。
(1)为了减少BaSO 4的损失,洗涤BaSO 4沉淀时可用稀硫酸代替水(√)(2)CaCO 3溶解时常用盐酸而不用稀硫酸,是因为稀硫酸不与CaCO 3反应(×)(3)温度不变,向AgCl 悬浊液中加入少量NaCl 粉末,平衡向左移动,K sp 减小(×)二、沉淀的转化1.ZnS 沉淀转化为CuS 沉淀(1)当向ZnS 沉淀上滴加CuSO 4溶液时,ZnS 沉淀逐渐转化为CuS ,这种转化的总反应为ZnS(s)+Cu 2+(aq)===CuS(s)+Zn 2+(aq)。
(2)沉淀转化实质是沉淀溶解平衡的移动,一种沉淀可以转化为更难溶的沉淀;两种难溶物的溶解能力差别越大,这种转化的趋势就越大。

微专题11常见的溶解平衡图像类型总结类型1c(M n+)、c(A n-)型图像:如图为BaSO4沉淀溶解平衡曲线(温度一定):(1)曲线上的任意一点均为达到溶解平衡的平衡点,可利用曲线上点的坐标来计算K sp(BaSO4);(2)曲线上方的点溶液过饱和,c(Ba2+)·c(SO2-4)>K sp(BaSO4),有沉淀生成;(3)曲线下方的点为不饱和溶液,c(Ba2+)·c(SO2-4)<K sp(BaSO4),无沉淀生成,加入BaSO4可继续溶解。
类型2S—pH或c(M n+)—pH图像:Fe(OH)3和Cu(OH)2的c—pH关系如图(温度一定):图中曲线为相应金属离子氢氧化物的沉淀溶解平衡曲线,可利用图像判断有关氢氧化物的K sp 的大小以及离子分离方法的选择。
类型3离子浓度负对数(pX)—溶液体积(V)图0.1 mol·L-1 AgNO3溶液滴定20.00 mL含有Cl-、Br-、I-且浓度均为0.1 mol·L-1的混合溶液,绘得滴定曲线如图:(1)图中曲线的起始部分,滴入c(Ag+)不足,c(X-)变化较小,在恰好反应时出现突跃,突跃后的三条曲线为相应AgX的沉淀溶解平衡曲线。
(2)若已知a、b、c所代表的卤素离子的曲线,则可比较相应AgX的K sp大小或利用K sp的大小分析a、b、c分别代表哪种卤素离子的曲线。
类型4离子浓度对数或负对数曲线难溶电解质溶液中离子浓度都很小,为研究方便,常取离子浓度的对数或负对数。
如果横、纵坐标是离子浓度的对数或负对数,则二者的关系应是一条直线。
例如在一定温度下,三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如下图所示(已知:pM=-lg c(M),p(CO2-3)=-lg c(CO2-3)图中曲线为相应碳酸盐的沉淀溶解平衡曲线,因此可对比不同碳酸盐K sp的大小,对比线外点对不同碳酸盐来说是过饱和溶液还是不饱和溶液,以及判断相应金属离子与碳酸根离子浓度的大小。

微专题13常见的溶解平衡图像类型总结类型1c(M n+)、c(A n-)型图像如图为BaSO4沉淀溶解平衡曲线(温度一定):(1)曲线上的任意一点均为达到溶解平衡的平衡点,可利用曲线上点的坐标来计算K sp(BaSO4)。
(2)曲线上方的点溶液过饱和,c(Ba2+)·c(SO2-4)>K sp(BaSO4),有沉淀生成。
(3)曲线下方的点为不饱和溶液,c(Ba2+)·c(SO2-4)<K sp(BaSO4),无沉淀生成,加入BaSO4可继续溶解。
类型2S—pH或c(M n+)—pH图像Fe(OH)3和Cu(OH)2的c—pH关系如图(温度一定):图中曲线为相应金属离子氢氧化物的沉淀溶解平衡曲线,可利用图像判断有关氢氧化物的K sp 的大小以及离子分离方法的选择。
类型3离子浓度负对数(pX)—溶液体积(V)图0.1 mol·L-1 AgNO3溶液滴定20.00 mL含有Cl-、Br-、I-且浓度均为0.1 mol·L-1的混合溶液,绘得滴定曲线如图:(1)图中曲线的起始部分,滴入c(Ag+)不足,c(X-)变化较小,在恰好反应时出现突跃,突跃后的三条曲线为相应AgX的沉淀溶解平衡曲线。
(2)若已知a、b、c所代表的卤素离子的曲线,则可比较相应AgX的K sp大小或利用K sp的大小分析a、b、c分别代表哪种卤素离子的曲线。
类型4离子浓度对数或负对数曲线难溶电解质溶液中离子浓度都很小,为研究方便,常取离子浓度的对数或负对数。
如果横、纵坐标是离子浓度的对数或负对数,则二者的关系应是一条直线。
例如在一定温度下,三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如下图所示。
已知:pM=-lg c(M),p(CO2-3)=-lg c(CO2-3)图中曲线为相应碳酸盐的沉淀溶解平衡曲线,因此可对比不同碳酸盐K sp的大小,对比线外点对不同碳酸盐来说是过饱和溶液还是不饱和溶液,以及判断相应金属离子与碳酸根离子浓度的大小。
微专题7难溶电解质沉淀溶解平衡图像分析1.曲线型图像第一步:明确图像中纵、横坐标的含义纵、横坐标通常是难溶物溶解后电离出的离子浓度。
第二步:理解图像中线上点、线外点的含义(1)以氯化银为例,在该沉淀溶解平衡图像上,曲线上任意一点都达到了沉淀溶解平衡状态,此时Q=K sp。
在温度不变时,无论改变哪种离子的浓度,另一种离子的浓度只能在曲线上变化,不会出现在曲线以外。
(2)曲线上方区域的点均为过饱和溶液,此时Q>K sp。
(3)曲线下方区域的点均为不饱和溶液,此时Q<K sp。
2.对数型图像(1)图像类型pH图像将溶液中c(H+)取负对数,即pH=-lg c(H+),反映到图像中是c(H+)越大,则pH越小pOH图像将溶液中c(OH-)取负对数,即pOH=-lg c(OH-),反映到图像中是c(OH-)越大,则pOH越小pC图像将溶液中某一微粒浓度[如c(A)]或某些微粒浓度的比值取负对数,即pC=-lg c(A),反映到图像中是c(A-)越大,则pC越小(2)解题要领解题时要理解pH、pOH、pC的含义,以及图像横坐标、纵坐标代表的含义,通过曲线的变化趋势,找到图像与已学化学知识间的联系。
1.在t℃时,AgBr在水中的沉淀溶解平衡曲线如图所示。
又知t℃时AgCl的K sp=4×10-10,下列说法不正确的是()A.在t℃时,AgBr的K sp为4.9×10-13B.在AgBr饱和溶液中加入NaBr固体,可使溶液由c点到b点C.图中a点对应的是AgBr的不饱和溶液D.在t℃时,AgCl(s)+Br-(aq)AgBr(s)+Cl-(aq)的平衡常数K≈8162.如图所示,有T1、T2两种温度下两条BaSO4在水中的沉淀溶解平衡曲线,下列说法不正确的是() A.加入Na2SO4可使溶液由a点变到b点B.在T1曲线上方区域(不含曲线)任意一点时,均有BaSO4沉淀生成C.蒸发溶剂可能使溶液由d点变为曲线上a、b之间的某一点(不含a、b)D.升温可使溶液由b点变为d点3.一定温度下,三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如下图所示。
沉淀溶解平衡曲线沉淀溶解平衡图像题的解题策略1.沉淀溶解平衡曲线类似于溶解度曲线,曲线上任一点都表示饱和溶液,曲线上方的任一点均表示过饱和溶液,此时有沉淀析出,曲线下方的任一点均表示不饱和溶液。
2.从图像中找到数据,根据K sp 公式计算得出K sp 的值。
3.比较溶液的Q c 与K sp 的大小,判断溶液中有无沉淀析出。
4.涉及Q c 的计算时,所代入的离子浓度一定是混合溶液中的离子浓度,因此计算离子浓度时,所代入的溶液体积也必须是混合溶液的体积。
1.在t ℃时,AgBr 在水中的沉淀溶解平衡曲线如图所示。
又知t ℃时AgCl 的K sp =4×10-10,下列说法不正确的是( )A .在t ℃时,AgBr 的K sp 为4.9×10-13B .在AgBr 饱和溶液中加入NaBr 固体,可使溶液由c 点变到b 点C .图中a 点对应的是AgBr 的不饱和溶液D .在t ℃时,AgCl(s)+Br -(aq)AgBr(s)+Cl -(aq)的平衡常数K ≈816答案 B解析 根据图中c 点的c(Ag +)和c(Br -)可得该温度下AgBr 的K sp 为4.9×10-13,A 正确;在AgBr 饱和溶液中加入NaBr 固体后,c(Br -)增大,溶解平衡逆向移动,c(Ag +)减小,故B 错;在a 点时Q c <K sp ,故为AgBr 的不饱和溶液,C 正确;选项D 中K =c(Cl -)/c(Br -)=K sp (AgCl)/K sp (AgBr),代入数据得K ≈816,D 正确。
2.已知25℃时,CaSO 4在水中的沉淀溶解平衡曲线如图所示,向100mL 该条件下的CaSO 4饱和溶液中加入400mL0.01mol·L -1Na 2SO 4溶液,下列叙述正确的是( ) A .溶液中析出CaSO 4固体沉淀,最终溶液中c(SO 2-4)比原来的大 B .溶液中无沉淀析出,溶液中c(Ca 2+)、c(SO 2-4)都变小 C .溶液中析出CaSO 4固体沉淀,溶液中c(Ca 2+)、c(SO 2-4)都变小 D .溶液中无沉淀析出,但最终溶液中c(SO 2-4)比原来的大 答案 D解析 由图像可知K sp (CaSO 4)=9.0×10-6,当加入400mL0.01mol·L-1Na 2SO 4溶液时,此时c(Ca2+)=3.0×10-3mol·L -1×0.1L 0.5L =6×10-4mol·L -1,c(SO 2-4)=3.0×10-3mol·L -1×0.1L +0.01mol·L -1×0.4L 0.5L=8.6×10-3mol·L -1,Q c =5.16×10-6<K sp (CaSO 4),所以溶液中无沉淀析出,但最终溶液中c(SO 2-4)比原来大。
3.(2013·江苏,14)一定温度下,三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如图所示。
已知:pM=-lgc(M),p(CO2-3)=-lgc(CO2-3)。
下列说法正确的是( )A.MgCO3、CaCO3、MnCO3的K sp依次增大B.a点可表示MnCO3的饱和溶液,且c(Mn2+)=c(CO2-3)C.b点可表示CaCO3的饱和溶液,且c(Ca2+)<c(CO2-3)D.c点可表示MgCO3的不饱和溶液,且c(Mg2+)<c(CO2-3)答案BD解析结合沉淀溶解平衡曲线及溶度积常数进行分析。
碳酸盐MCO3的溶度积可表示为K sp(MCO3)=c(M2+)·c(CO2-3),由图像可知,MgCO3、CaCO3、MnCO3的pM为一定值时,其p(CO2-3)逐渐增大,由溶度积表达式可知三种物质的K sp逐渐减小,A错;a点在MnCO3的沉淀溶解平衡曲线上,为其饱和溶液,结合MnCO3图中曲线可知,c(CO2-3)=c(Mn2+),B对;b点在CaCO3的沉淀溶解平衡曲线上,为其饱和溶液,结合CaCO3图中曲线可知,c(CO2-3)<c(Ca2+),C错;c点在MgCO3的沉淀溶解平衡曲线的上方,为其不饱和溶液,溶液中c(CO2-3)>c(Mg2+),D正确。
4.一定温度时,Cu2+、Mn2+、Fe2+、Zn2+等四种金属离子(M2+)形成硫化物沉淀所需S2-最低浓度的对数值lgc(S2-)与lgc(M2+)的关系如图所示。
下列有关判断不正确的是A. 该温度下,Ksp(MnS)大于1.0×10-35B. 向含Mn2+、Zn2+的稀溶液中滴加Na2S溶液,Mn2+最有可能先沉淀C. 向c(Fe2+)=0.1mol·L-1的溶液中加入CuS粉末,有FeS沉淀析出D. 该温度下,溶解度:CuS>MnS>FeS>ZnS【答案】D粉末后c (Fe2+)×c(S2-)大于10-20,所以有FeS沉淀析出,C正确;D、依据此图可知,CuS的Ksp最小,其次是MnS、FeS和ZnS,所以该温度下,溶解度:CuS<MnS<FeS<ZnS,D错误,答案选D。
5.(2014·新课标全国卷Ⅰ,11)溴酸银(AgBrO3)溶解度随温度变化曲线如下图所示。
下列说法错误的是( )A.溴酸银的溶解是放热过程B.温度升高时溴酸银溶解速度加快C.60℃时溴酸银的K sp约等于6×10-4D.若硝酸钾中含有少量溴酸银,可用重结晶方法提纯答案 A解析A项,由题图可知,随着温度升高,溴酸银的溶解度逐渐增大,因此AgBrO3的溶解是吸热过程;B项,由图像曲线可知,温度升高斜率增大,因此AgBrO3的溶解速度加快;C项,由溶解度曲线可知,60℃时,AgBrO3的溶解度约为0.6g,则其物质的量浓度约为0.025mol·L-1,AgBrO3的K sp=c(Ag+)·c(B rO-3)=0.025×0.025≈6×10-4;D项,若KNO3中含有少量AgBrO3,可通过蒸发浓缩得到KNO3的饱和溶液,再冷却结晶获得KNO3晶体,而AgBrO3留在母液中。
6.25℃时,PbCl2固体在不同浓度盐酸中的溶解度曲线如图。
在制备PbCl2的实验中,洗涤PbCl2固体最好选用( ) A.蒸馏水B.1.00mol·L-1盐酸C.5.00mol·L-1盐酸D.10.00mol·L-1盐酸答案 B解析观察题图知,PbCl2固体在浓度为1.00m ol·L-1的盐酸中溶解度最小。
7.已知:pAg=-lgc(Ag+),K sp(AgCl)=1×10-12。
如图是向10mLAgNO3溶液中逐渐加入0.1mol·L-1的NaCl溶液时,溶液的pAg随着加入NaCl溶液的体积变化的图像(实线)。
根据图像所得下列结论正确的是[提示:K sp(AgCl)>K sp(AgI)]( )A.原AgNO3溶液的物质的量浓度为0.1mol·L-1B.图中x点的坐标为(100,6)C.图中x点表示溶液中Ag+被恰好完全沉淀D.把0.1mol·L-1的NaCl换成0.1mol·L-1NaI则图像在终点后变为虚线部分答案 B解析A项,加入NaCl之前,pAg=0,所以c(AgNO3)=1mol·L-1,错误;B项,由于c(Ag+)=10-6mol·L-1,所以Ag+沉淀完全,n(NaCl)=n(AgNO3)=0.01L×1mol·L-1=0.01mol,所以V(NaCl)=100mL,B正确,C错误;若把NaCl换成NaI,由于K sp(AgI)更小,所以c(Ag+)更小,pAg更大,D错误。
8.【衡阳市2017年十校高考调研冲刺预测卷(五)】如图是Ca(OH)2在温度分别为T1、T2时的沉淀溶解平衡曲线[图中浓度单位为mol·L-1,温度为T1时Ca(OH)2的Ksp = 4×10-6, ≈1.6]。
下列说法正确的是A . 温度: T l <T 2B . 温度为T 1时,P 点分散系中分散质粒子直径均小于1nmC . Q 点的溶液中c (OH -)约为0.0125molD . 加水稀释时溶液碱性减弱,Z 点溶液可转化为Q 点溶液 【答案】C【解析】A 、氢氧化钙溶解度是随着温度的升高而降低,根据图像,因此T 1>T 2,故A 错误;B 、P 点属于过饱和溶液,即悬浊液,因此分散质粒子直径大于100nm ,故B 错误;C 、根据K sp =c (Ca 2+)×c 2(OH -),4×10-6=4a ×(2a )2,解得a =6.25×10-3,因此c (OH -)=2×6.25×10-3mol ·L -1=0.0125mol ·L -1,故C 正确;D 、加水稀释,c (Ca 2+)和c (OH -)都减小,故D 错误。
9.【2017新课标3卷】在湿法炼锌的电解循环溶液中,较高浓度的Cl -会腐蚀阳极板而增大电解能耗。
可向溶液中同时加入Cu 和CuSO 4,生成CuCl 沉淀从而除去Cl -。
根据溶液中平衡时相关离子浓度的关系图,下列说法错误的是( )A .SP (CuCl)K 的数量级为710-B .除Cl -反应为Cu+Cu 2++2Cl -=2CuClC .加入Cu 越多,Cu +浓度越高,除Cl -效果越好D .2Cu +=Cu 2++Cu 平衡常数很大,反应趋于完全 【答案】C【解析】K sp (CuCl)=c(Cu +)·c(Cl -),在横坐标-1(Cl )lg mol L c --⋅为1时,纵坐标-1(Cu )lg mol L c +⋅大于-6,小于-5,所以K sp (CuCl)的数量级是10-7,A 正确;除去Cl -反应应该是Cu+Cu 2++2Cl -=2CuCl ,B 正确;溶液中存在平衡:Cu ++Cl-CuCl 、2Cu +Cu 2++Cu ,加入纯固态物质Cu 对平衡无影响,故C 错误;D .在没有Cl -存在的情况下,反应2Cu+Cu 2++Cu 的平衡常数约为2 6.77.927.32(Cu )1010(Cu )(10)c c +-+-==,平衡常数 很大,反应趋于完全,D 正确。
10.金属氢氧化物在酸中溶解度不同,因此可以利用这一性质,控制溶液的pH ,达到分离金属离子的目的。