第八章配位化合物与配位滴定
- 格式:ppt
- 大小:1.63 MB
- 文档页数:139



第八章配位化合物与配位滴定第八章配位化合物与配位滴定第一节配位化合物一、配位化合物的定义配位化合物(简称配合物,也称络合物)是指独立存在的稳定化合物进一步结合而成的复杂化合物。
例:[Cu(NH3)4]SO4是由一个Cu2+和四个NH3分子组成的独立基团。
特点:1.在结构中都包含有中心离子和一定数目的中性分子或阴离子相结合而成的结构单元,此结构单元表现出新的特征。
2.在配位化合物中中心离子或阴离子或中性分子通过形成配位共价键而结成独立的结构单元。
配位化合物的定义:由中心离子(或原子)和一定数目的中性分子或阴离子通过形成配位共价键相结合而成的复杂结构单元称配位单元,凡是由配位单元组成的化合物称配位化合物。
若配位单元带电荷称配离子,如[Ag(CN)2]-,配离子与带相反电荷的离子组成中性配合物。
若配位单元不带电荷,则配位单元本身就是配合物,如Fe(CO)5另外,必须指出有一类叫复盐的化合物,如KCl·MgCl2·6H2O、KAl(SO4)2·12H2O无复杂离子和复杂的配位单元,不是配合物。
二、配合物的组成配合物在组成上一般包括内界和外界两部分。
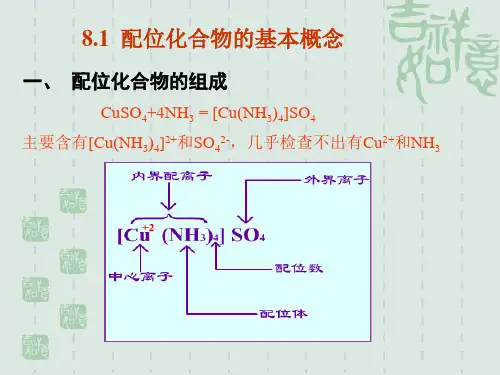
中心体(离子或原子)内界配合物配体(单齿或多齿配体)外界现以[Cu(NH3)4]SO4为例说明配合物的组成。
内界外界[ Cu (NH3) 4 ]2+ SO42-中配配配外心位位位界离原体数离子子子组成:配合物的组成由外界离子、配体、中心离子(或原子)构成。
1.中心离子(或原子)也叫形成体,它位于配合物的中心,一般是金属离子,以过渡态金属离子最常见,也有中性原子或高氧化态的非金属元素。
如:Fe(CO)5中的Fe为形成体,是原子。
[PF6]-中的P是形成体,非金属元素。
作为中心离子的条件是:必须具有空的价电子轨道,可以接受配体所给予的孤对电子。
周期表中绝大多数元素可作为中心离子,常见的一些过渡元素如铁、铜、银、金、锌、汞、铂等元素的离子或原子,它们具有(n-1)d、ns、np、nd等的空的价电子轨道,都是强的形成体。

第八章配位化合物与配位滴定法【知识导航】本章知识在《中国药典》(2010年版)中主要应用于含金属离子药物的含量测定,以配位反应为基础的滴定分析法。
目前多用氨羧配位剂为滴定液,其中以乙二胺四醋酸(EDTA)应用最广。
《中国药典》中使用直接滴定法对葡萄糖酸钙、葡萄糖酸钙口服液、葡萄糖酸钙含片、葡萄糖酸钙注射剂、葡萄糖酸钙颗粒、葡萄糖酸锌、葡萄糖酸锌口服液、葡萄糖酸锌片、葡萄糖酸锌颗粒进行含量测定;使用间接滴定法对氢氧化铝、氢氧化铝片、氢氧化铝凝胶进行含量测定。
在历年执业药师考试中也有相关考题出现。
学好本章内容有利于掌握配位滴定法的原理、配位滴定法在药物分析中的应用以及备战执业药师考试。
【重难点】1.配位化合物(coordination compound)简称配合物,以具有接受电子对的空轨道的原子和离子为中心(中心离子),与一定数量的可以给出电子对的离子或分子(配体)按一定的组成和空间构型形成的化合物。
配位键的形成:中心离子(原子)提供空轨道,配位体上的配位原子提供孤对电子。
例如:[Cu(NH3)4]SO4、K3[Fe(NCS)6]等。
这些化合物与简单的化合物区别在于分子中含有配位单元,而简单化合物中没有这些配位单元。
以[Cu(NH3)4]SO4为例:[Cu (NH3)4 ] SO4↓ ↓↓内界配体外界配位体中提供孤电子对的,与中心离子以配位键结合的原子称为配位原子。
一般常见的配位原子是电负性较大的非金属原子。
常见配位原子有C、N、O、P及卤素原子。
由于不同的配位体含有的配位原子不一定相同,根据一个配位体所提供的配位原子的数......目.,可将配位体分为单齿配位体(unidentate ligand)和多齿配位体(multidentate ligand)。
只含有一个配位原子配位体称单齿配位体如H2O、NH3、卤素等。
有两个或两个以上的配位原子配位体称多齿配位体,如乙二胺NH2一CH2一CH2一NH2(简写为en),草酸根C2O42-(简写为ox)、乙二胺四醋酸根(简称EDTA)等。





第八章 配位化合物与配位滴定习题1:配位化合物部分1 无水CrCl 3和氨作用能形成两种配合物A 和B ,组成分别为CrCl 3·6NH 3和CrCl 3·5NH 3。
加入AgNO 3,A 溶液中几乎全部氯沉淀为AgCl ,而B 溶液中只有2/3的氯沉淀出来。
加入NaOH 并加热,两种溶液均无氨味。
试写出这两种配合物的化学式并命名。
解:因加入AgNO 3,A 溶液中几乎全部氯沉淀为AgCl ,可知A 中的三个Cl -全部为外界离子,B 溶液中只有2/3的氯沉淀出来,说明B 中有两个Cl -为外界,一个Cl -属内界。
加入NaOH ,两种溶液无氨味,可知氨为内界。
因此A 、B 的化学式和命名应为,A :[Cr(NH 3)6]Cl 3 三氯化六氨合铬(Ⅲ) B :[Cr(NH 3)5Cl]Cl 2 二氯化一氯五氨合铬(Ⅲ)2 指出下列配合物的中心离子、配体、配位数、配离子电荷数和配合物名称。
解:3 试用价键理论说明下列配离子的类型、空间构型和磁性。
解:(1)CoF 63-和Co(CN)63-CoF 63-为外轨型,空间构型为正八面体,顺磁性,磁矩=B μ90.4)24(4=+。
Co(CN)63-为内轨型,空间构型为正八面体,抗磁性,磁矩为零。
(2)Ni(NH 3)42+和Ni(CN)42-Ni(NH 3)42+为外轨型,正四面体型,顺磁性,磁矩=B μ83.2)22(2=+。
Ni(CN)42-为内轨型,平面正方型,抗磁性,磁矩为零。
4 将0.1mol·L -1ZnCl 2溶液与1.0 mol·L -1NH 3溶液等体积混合,求此溶液中Zn(NH 3)42+和Zn 2+的浓度。
解:等体积混合后,ZnCl 2和NH 3各自的浓度减半,生成的Zn(NH 3)42+的浓度为0.05 mol·L -1,剩余的NH 3的浓度为0.3 mol·L -1,设Zn 2+的浓度为x mol·L -1。