ISO6888食品和动物饲料的微生物学金黄色葡萄球菌检验
- 格式:doc
- 大小:44.50 KB
- 文档页数:10


ISO 6888-1:1999食品和动物饲料的微生物学血清凝固酶阳性葡萄球菌(金黄色葡萄球菌和其他球菌)序ISO是国际标准的全球性组织。
准备国际标准这项工作通常由ISO技术联盟来完成。
每一个团体成员负责各自的学科。
与ISO有合作的国际性机构、政府与非政府机构,也有参与这项工作。
ISO与国际电子组织(IEC)在电子标准化方面有着密切的合作关系。
国际性标准的起草原则在《ISO/IEC 细则》第三部分中有给出。
起草的国际性标准被技术委员会采用是通过全体成员投票决定的。
发布一个国际性标准需要至少75%成员投赞成票。
国际性标准ISO 6888-1 由ISO/IEC 34技术委员会(农产品,小组委员会SC9,微生物)起草的。
ISO 6888-1的第一个版本,以及ISO 6888-2,取代ISO 6888:1983,做了计数上的修改。
ISO 6888由以下部分组成,一般标题为食品与动物饲料微生物学——一般方法计数血浆凝固酶阳性葡萄球菌(金黄色葡萄球菌和其它种类):——第一部分:方法使用BP琼脂培养基;——第二部分:方法使用兔血浆纤维蛋白琼脂培养基。
0. 绪论0.1 由于食品与饲料的种类繁多,这个标准不一定适合某一类产品。
在这种情况下,可使用不同的方法,但必须有绝对的技术上的理由。
否则,要尽可能地完全遵循本标准。
当这个标准下一次回顾时,将会对这个标准的使用做数据统计,特殊产品偏离本标准使用也会做相关统计。
同一类产品的检测方法也有可能不统一,国际性标准和/或国家标准也不一定完全与本标准相符合。
希望相关标准做回顾时,会遵循本标准做出相关的修改,以使只有已被证明的技术上的理由才能与本标准偏离。
0.2 ISO 6888描述了两种平行的方法(第一部分和第二部分)来检测血浆凝固酶阳性葡萄球菌,其中以证明该菌产生肠毒素。
其中较大可能是金黄色葡萄球菌,也有可能是中间链球菌或猪葡萄球菌。
0.3 ISO 6888本部分的目的在于,葡萄球菌的证实基于血浆凝固酶的阳性反应,但也有研究证明一些受损的金黄色葡萄球菌会出现血浆凝固酶弱阳性。



金黄色葡萄球菌国家标准检验方法一、国家标准检验办法参见GB 4789.10-2010《食品平安国家标准食品微生物学检验金黄色葡萄球菌检验》其次法和第三法。
1、Baird-Parker平板计数(其次法)本办法适用于金黄色葡萄球菌含量较高的食品中金黄色葡萄球菌的计数。
1.1、检验流程 1.2、试验步骤 (1)样品的稀释①固体和半固体样品:称取25g样品置盛有225mL 缓冲液或生理盐水的无菌均质杯内,8000-10000r/min均质1-2min,或置盛有225mL稀释液的无菌均质袋中,用拍击式均质器拍打1~2min,制成1:10的样品匀液。
②液体样品:以无菌吸管吸取25mL样品,置盛有225mL磷酸盐缓冲液或生理盐水的无菌锥形瓶(瓶内预置适当数量的无菌玻璃珠)中,充分混匀,制成1:10的样品匀液。
③用1mL无菌吸管或微量移液器吸取1:10样品匀液1mL,沿管壁缓慢注于盛有9mL 稀释液的无菌试管中(注重吸管或吸头尖端不要触及稀释液面),振摇试管或换用1支1mL无菌吸管反复吹打使其混合匀称,制成1:100的样品匀液。
④按③操作程序,制备10倍系列稀释样品匀液。
每递增稀释一次,换用1次1mL无菌吸管或吸头。
(2)样品的接种按照对样品污染情况的估量,挑选2-3个相宜稀释度的样品匀液(液体样品可包括原液),在举行10倍递增稀释时,每个稀释度分离吸取1mL样品匀液以0.3mL, 0.3mL, 0.4mL接种量分离加入三块Baird-Parker平板,然后用无菌L棒涂布囫囵平板,注重不要触及平板边缘。
用法前,如Baird-Parker平板表面有水珠,可放在25-50℃的培养箱里干燥,直到平板表面的水珠消逝。
(3)培养在通常状况下,涂布后,将平板静置l0min,如样液不易汲取,可将平板放在培养箱((36±1)℃培养1h;等样品匀液汲取后翻转平皿,倒置于培养箱,(36±1)℃培养,45一48h。

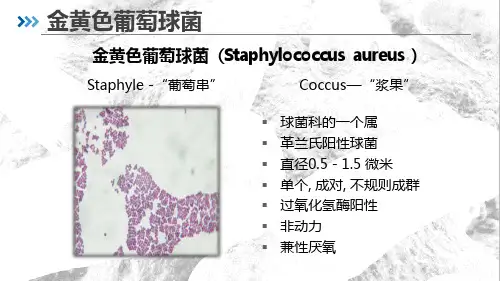
食品中金黄色葡萄球菌检验方法金黄色葡萄球菌 (Staphylococcus aureus ) 是人类的一种重要病原菌,隶属于葡萄球菌属(Staphylococcus),有“嗜肉菌"的别称,是革兰氏阳性菌的代表,可引起许多严重感染。
而对于金黄色葡萄球菌在速冻食品中的存在量,卫生部于2011年11月24日公布食品安全国家标准《速冻面米制品》,允许金葡菌限量存在。
实验设备耗材吸管(1ml、10ml)、恒温培养箱(36±1℃)、冰箱、均质器、振荡器、平皿、稀释瓶、天平、显微镜、接种棒等培养基和试剂普通肉汤培养基、胰蛋白胨大豆肉汤、Baird-Prker琼脂平板、缓冲蛋白胨水(BP)、凝固酶试验冻干血浆检验程序(非选择性增菌法)检样25g+225mlBP胨水10ml匀液+10ml双料胰胨肉汤操作步骤1.称取25g固体样品;吸取25mL液体样品,加入225mLBP胨水,固体样品研磨或置均质器中制成混悬液。
2.吸取10mL上述混悬液,接种于10mL双料胰蛋白胨大豆肉汤中,置36±1℃培养2h。
3.再加入20ml 含20%NaCl的单料胰蛋白胨大豆肉汤,置36±1℃培养24±2h。
4.划线转种2个表面干燥的Baird-Parker琼脂平板上,36±1℃培养46±2h。
5.挑取可疑菌落移种到肉汤培养基中,置36±1℃温箱培养24h。
6.取肉汤培养物0.3ml同0.5ml凝固酶试验冻干血浆于8mm*100mm试管内充分混合,置36±1℃培养,定时观察是否有凝块形成,至少观察6h,以内容物完全凝固,使试管倒置或倾斜时不流动为阳性。
试验中需同时做已知阳性和阴性对照。
对可疑结果,应进行革兰氏染色、镜检和其他辅助试验。
7.本菌为革兰氏阳性球菌,排列是葡萄球状,无芽胞,无荚膜,致病性葡萄球菌菌体较小,直径约为0.5~1μm。
在Baird-Parker平板上为圆形、光滑凸起、湿润、直径为2~3mm,颜色呈灰色到黑色,边缘为淡色,周围为一混浊带,在其外层有一透明圈。

金黄色葡萄球菌检验技术介绍及分析金黄色葡萄球菌是一种常见的细菌,它是引起人体多种感染的病原菌之一。
金黄色葡萄球菌检验技术是通过分离、培养和鉴定来检测和确定金黄色葡萄球菌的存在与类型。
以下是金黄色葡萄球菌检验技术的介绍及分析。
金黄色葡萄球菌的分离是检验的第一步。
样品通常是从患者的伤口、分泌物或体液中获取的,也可以从环境中收集。
分离可以通过将样品涂抹到适当的察尔染色的琼脂平板上,然后进行培养和鉴定来完成。
金黄色葡萄球菌会在琼脂平板上形成金黄色的菌落。
培养是金黄色葡萄球菌检验的关键步骤。
常用的培养基包括牛肉蛋白胨琼脂、亚洲互联网的Tag:脑心制剂琼脂、亚洲互联网的Tag:镜光菌属琼脂等。
金黄色葡萄球菌是革兰氏阳性球菌,它可以在各种营养富集培养基中生长,但最好使用富含血液、蛋白质和碳水化合物的培养基。
培养的时间通常为24小时,金黄色葡萄球菌菌落会呈现金黄色且凸起。
鉴定是确认金黄色葡萄球菌的类型的步骤。
鉴定方法包括形态学观察、生化试验和分子生物学方法。
形态学观察是通过显微镜观察菌落和细胞形态来判断。
金黄色葡萄球菌是圆形或椭圆形的,常呈簇状分布。
生化试验可以通过检测金黄色葡萄球菌对特定底物的代谢能力来进行鉴定。
一些常用的测试包括氧化酶试验、半乳糖发酵试验等。
分子生物学方法可以通过检测特定基因或DNA序列来鉴定金黄色葡萄球菌。
金黄色葡萄球菌检验技术的分析主要集中在以下几个方面。
金黄色葡萄球菌的检验可以帮助医生确定感染的病原菌,从而指导合理的治疗方案。
金黄色葡萄球菌是耐药菌中的重要成员,对多种抗生素具有耐药性,因此及早检测和鉴定金黄色葡萄球菌可以避免无效的药物治疗。
金黄色葡萄球菌还可以引起食物中毒和医院相关感染等,检验技术的应用可以有助于减少相关疾病的发生。



本文从网络收集而来,上传到平台为了帮到更多的人,如果您需要使用本文档,请点击下载,另外祝您生活愉快,工作顺利,万事如意!食品中金黄色葡萄球菌的检测方法1.范围本标准规定了食品中金黄色葡萄球菌的检测方法。
本标准第一法适用于金黄色葡萄球菌的定性检测;第二法适用于金黄色葡萄球菌含量较高的食品中金黄色葡萄球菌的计数。
第三法适用于金黄色葡萄球菌含量较低而杂菌含量较高的食品中金黄色葡萄球菌的计数。
2.设备和材料除微生物实验室常规灭菌及培养设备外,其他设备和材料如下:2.1恒温培养箱:36℃±1℃。
2.2冰箱:2℃~5℃。
2.3恒温水浴箱:37℃~65℃。
2.4天平:感量0.1g。
2.5均质器。
2.6振荡器。
2.7无菌吸管:1mL(具0.01mL刻度)、10mL(具0.1mL刻度)或微量移液器。
2.8无菌锥形瓶:容量100mL、500mL。
2.9无菌培养皿:直径90mm。
2.10注射器:0.5mL。
2.11 pH计或pH比色管或精密pH试纸。
2.12全自动微生物生化鉴定系统。
(BD Crystal或Phoenix)。
2.13比浊仪。
(BD Phoenix比浊仪,货号440910)。
2.14比浊仪定标盒。
(BD Phoenix定标盒,货号440911)。
3.培养基和试剂3.110 %氯化钠胰酪胨大豆肉汤。
3.27.5 %氯化钠肉汤。
3.3血琼脂平板。
(BD 货号脑心浸液琼脂241830胰蛋白大豆琼脂236950作为基础加兔血浆)3.4Baird-Parker 琼脂平板。
(BD 货号 276840)3.5脑心浸出液肉汤(BHI)。
(BD 货号 237400)3.6稀释液:磷酸盐缓冲液。
(BD 货号211544)3.7营养琼脂小斜面。
(BD 货号212000)3.8革兰氏染色液。
(BD 货号212539)3.9无菌生理盐水。
第一法金黄色葡萄球菌的定性检验4.检验程序金黄色葡萄球菌定性检验程序见图1:图1 金黄色葡萄球菌检验程序5.操作步骤5.1样品的处理称取25g样品至盛有225mL7.5%氯化钠肉汤或10%氯化钠胰酪胨大豆肉汤的无菌均质杯内,8000r/min~10000r/min均质1min~2min,或放入盛有225mL7.5%氯化钠肉汤或10%氯化钠胰酪胨大豆肉汤的无菌均质袋中,用拍击式均质器拍打1min~2min。
实验七食品中金黄色葡萄球菌的检验一、实验目的要求1、了解食品的质量与金黄色葡萄球菌检验的意义.2、掌握金黄色葡萄球菌的生物学特性.3、掌握金黄色葡萄球菌检验的生化试验的操作方法和结果的判断。
4、掌握食品中金黄色葡萄球菌检验的方法和技术。
二、原理葡萄球菌在自然界分布极广,空气、土壤、水、饲料、食品(剩饭、糕点、牛奶、肉品等)以及人和动物的体表粘膜等处均有存在,大部分是不致病,也有一些致病的球菌.金黄色葡萄球菌是葡萄球菌属一个种。
可引起皮肤组织炎症,还能产生肠毒素。
如果在食品中大量生长繁殖,产生毒素,人误食了含有毒素的食品,就会发生食物中毒,故食品中存在金黄色葡萄球菌对人的健康是一种潜在危险,检查食品中金黄色葡萄球菌及数量具有实际意义。
金黄色葡萄球菌能产生凝固酶,使血浆凝固,多数致病菌株能产生溶血毒素,使血琼脂平板菌落周围出现溶血环,在试管中出现溶血反应.这些是鉴定致病性金黄色葡萄球菌的重要指标。
三、试剂和仪器(一)最先准备的器材规格名称数量用途1、500ml广口瓶1个稀释样品2、500ml三角瓶1个制生理盐水3、250ml三角瓶3个制培养基等4、10×100mm试管6支血浆凝固酶试验5、1ml移液管2支6、10ml移液管 2 支7、直径为90 mm平皿12套制血平板B—P平板8、250ml量筒1支(二)应灭菌的其它器材剪刀1把不锈钢汤匙1把称量纸适量(三)应制备的培养基培养基总量所用容器1.无菌水50ml/瓶1瓶250ml三角瓶(全班共用)2.0。
85%生理盐水70ml/瓶1瓶250ml三角瓶(全班共用)3.0.85%生理盐225ml/瓶1瓶500ml三角瓶4.7。
5%NaCl肉汤50ml/瓶1瓶250ml三角瓶5.普通营养琼脂100ml/瓶1瓶250ml三角瓶6.B—P培养基95ml/瓶1瓶250ml三角瓶7.兔血液5ml四、实验内容(一)、增菌培养法样品处理→→选择性增菌→→选择性平板分离→→血浆凝固酶试验鉴别→→结果报告第一天样品处理和增菌培养(一)、样品处理固体或半固体食品:以无菌操作称取25g样品,放入装有225mL灭菌生理盐水的灭菌均质杯内,于8000r/min均质1~2min,制成1:10样品匀液。
ISO 6888-1:1999食品和动物饲料的微生物学血清凝固酶阳性葡萄球菌(金黄色葡萄球菌和其他球菌)序ISO是国际标准的全球性组织。
准备国际标准这项工作通常由ISO技术联盟来完成。
每一个团体成员负责各自的学科。
与ISO有合作的国际性机构、政府与非政府机构,也有参与这项工作。
ISO与国际电子组织(IEC)在电子标准化方面有着密切的合作关系。
国际性标准的起草原则在《ISO/IEC 细则》第三部分中有给出。
起草的国际性标准被技术委员会采用是通过全体成员投票决定的。
发布一个国际性标准需要至少75%成员投赞成票。
国际性标准ISO 6888-1 由ISO/IEC 34技术委员会(农产品,小组委员会SC9,微生物)起草的。
ISO 6888-1的第一个版本,以及ISO 6888-2,取代ISO 6888:1983,做了计数上的修改。
ISO 6888由以下部分组成,一般标题为食品与动物饲料微生物学——一般方法计数血浆凝固酶阳性葡萄球菌(金黄色葡萄球菌和其它种类):——第一部分:方法使用BP琼脂培养基;——第二部分:方法使用兔血浆纤维蛋白琼脂培养基。
0. 绪论0.1 由于食品与饲料的种类繁多,这个标准不一定适合某一类产品。
在这种情况下,可使用不同的方法,但必须有绝对的技术上的理由。
否则,要尽可能地完全遵循本标准。
当这个标准下一次回顾时,将会对这个标准的使用做数据统计,特殊产品偏离本标准使用也会做相关统计。
同一类产品的检测方法也有可能不统一,国际性标准和/或国家标准也不一定完全与本标准相符合。
希望相关标准做回顾时,会遵循本标准做出相关的修改,以使只有已被证明的技术上的理由才能与本标准偏离。
0.2 ISO 6888描述了两种平行的方法(第一部分和第二部分)来检测血浆凝固酶阳性葡萄球菌,其中以证明该菌产生肠毒素。
其中较大可能是金黄色葡萄球菌,也有可能是中间链球菌或猪葡萄球菌。
0.3 ISO 6888本部分的目的在于,葡萄球菌的证实基于血浆凝固酶的阳性反应,但也有研究证明一些受损的金黄色葡萄球菌会出现血浆凝固酶弱阳性。
这种细菌可能会和其它种类的细菌混淆,但它能通过后续的试验区分开来,在本标准中没有做说明,例如溶葡球菌酶敏感性,产生溶血素、耐热核酸酶,发酵甘露醇产酸(见参考文献2)。
1 范围本标准适用于检测人类食物或动物饲料产品的血浆凝固酶阳性葡萄球菌的检测,通过计数BP平板35℃或37℃培养后的菌落数。
2 参考标准以下标准文件是本标准的参考标准。
已过期的文献,后来改善或修订的,部分这种文献已经不适用。
然而,有大部分学者正在争取发布最新版的文献如以下列出。
对于无限期的文献,最新版本都是适用的。
ISO和IEC成员保存当前有效国际性标准的记录。
ISO 6887-1,食物与动物饲料原料微生物学——样品准备原则,微生物检测样品原液及十倍法稀释——第一部分:样品原液和十倍法稀释的指导准则。
ISO 7218,食物与动物饲料原料微生物学——微生物检验指导准则。
3 术语与定义本标准中使用的相关术语与定义如下。
3.1 血浆凝固酶样品葡萄球菌在选择性平板上的典型和/或不典型菌落,按照本标准操作呈现凝固酵素阳性反应。
3.2 血浆凝固酶阳性葡萄球菌计数按照本标准操作,得出血浆凝固酶阳性葡萄球菌每克或每毫升样品的含量。
4 原理4.1 接种固体选择性培养基表面,做两个平行,如果为液体样品,接种一定体积的样品,如果是其它类型的样品,接种一定体积的样品悬液。
在同样的条件下,接种样品或样品悬液的十倍稀释溶液,每个梯度两个平行。
4.2 在需氧条件下35℃或37℃培养,然后24h和48h检查。
4.3 计算每克或每毫升样品中血浆凝固酶阳性葡萄球菌的数量,稀释梯度的选择和平板上典型与不典型菌落的数量都有重要的意义,并通过凝固酵素试验确证。
5 稀释液与培养基 5.1 概要正确的实验室操作,参照ISO 7218。
5.2 稀释液参照ISO 6887-1 和特殊产品的相关标准。
5.3 BP 琼脂培养基注意:商业上可买到的培养基可以使用。
必须参照厂商的说明书操作。
5.3.1 基础培养基 5.3.1.1 成分5.3.1.2 准备将所有成分或培养基干粉溶解于水中并煮沸。
如需要,调整pH 值至7.2±0.2,在25℃下。
将培养基转移至适当容量的三角瓶中,每瓶100ml 。
121℃灭菌15min 。
5.3.2 配套试剂 5.3.2.1 亚碲酸盐钠 5.3.2.1.1 成分5.3.2.1.2 准备将亚碲酸盐钠充分溶解在水中,最小程度加热。
固体粉末应该是易溶的。
如果有白色的不溶物出现,丢弃该粉末。
过滤0.22µm孔膜灭菌。
在3℃±2℃保存期不超过1个月。
如有白色混浊,丢弃它。
5.3.2.2 蛋黄乳状液注意:如果有商业的成品,可以使用。
使用有完整外壳的新鲜鸡蛋。
用液体清洁剂将表面刷干净。
在流动水下冲洗干净。
然后在70%乙醇中浸泡30s消毒,自然晾干,或者喷射酒精后用火焰灭菌。
在无菌环境下,打开鸡蛋并将蛋黄从蛋白中分离出来。
将蛋黄放入灭菌三角瓶中,加入四倍体积无菌水。
充分混匀。
在47℃水浴锅中加热2h,然后在3℃±2℃下保存18h~24h,使之形成沉淀物。
无菌的收集澄清液体至无菌容器中待使用。
该乳状液在3℃±2℃下最大保存期为72h。
5.3.2.3磺胺二甲嘧啶溶液注意:该溶液仅使用于容易变化的样品中。
5.3.2.3.1 成分5.3.2.3.2 准备将磺胺二甲嘧啶溶解在氢氧化钠溶液中,用水稀释至100ml。
过滤0.22µm 孔膜灭菌。
在3℃±2℃保存期不超过1个月。
5.3.3 完全培养基5.3.3.1 成分5.3.3.2 准备融化基础培养基,水浴冷却至47℃。
然后,在无菌条件下,添加亚碲酸钠溶液和蛋黄乳状液,如有必要,添加将磺胺二甲嘧啶溶液。
每一种溶液都必须水浴预热至47℃。
然后充分混匀。
5.3.4 准备琼脂平板倾注适当量培养基至无菌平皿中,以获得4mm厚度平板,并凝固。
在使用之前,要烘干平板表面水分,可在25℃~50℃培养箱中烘干。
5.4 脑心浸液肉汤5.4.1 成分5.4.2 准备将各成分或脱水干粉培养基于水中,如需要可加热。
调整pH值至7.2±0.2,在25℃下。
将培养基转移至适当容积的玻璃管中,每管5ml~10ml。
121℃灭菌15min。
5.5 兔血浆使用商业成品并根据厂商说明再水化。
如果购买不到成品兔血浆,用三倍体积无菌水稀释灭菌的新鲜兔血。
添加EDTA,使其在溶液中的含量为0.1%,如果兔血中含有柠檬酸钾或柠檬酸钠。
再水化或自制的兔血浆须立即使用。
在使用之前,用血浆凝固酶阳性葡萄球菌做阳性质控。
6 设备及玻璃器皿一般的微生物实验室设备(参照ISO 7218),特别的,增加以下几项。
6.1 干热灭菌和湿热灭菌设备6.2 培养箱,可恒温35℃±1℃或37℃±1℃6.3 干燥箱或培养箱,可恒温25℃±1℃和50℃±1℃6.4 水浴锅,可恒温47℃±2℃6.5 试管,三角瓶带螺帽6.6 灭菌平皿,玻璃或塑料的6.7 接种针和接种环6.8 移液器,1ml,2ml和10ml,分割分别为0.1ml,0.1ml和0.5ml6.9 灭菌的涂布棒,玻璃或塑料的6.10 pH计7 取样ISO 6888中并不涉及取样。
如果没有相关的国际标准,建议需经过多方同意。
微生物实验室接收到的样品必须是真实代表样品的,并在运输和储藏期间没有损坏或改变微生物的性状。
8 样品前处理参照样品的相关国际标准进行前处理。
如果没有相关的国际标准,建议需经过多方同意。
9 程序9.1 测试部分,样品原始悬液和稀释参照ISO 6887-1,相关细节可参考各个样品的标准。
9.2 接种9.2.1如果样品为液体,各吸取0.1mL样液至两个BP平板上,涂布平板,如果样品为非固体,则吸取1:10稀释度样液0.1mL至BP平板上,依次类推,检测1:100或更多的稀释度。
9.2.2若是样品的金黄色葡萄球菌限度较低,可吸取1.0mL样液涂布平板,得到更低检出结果。
1mL样液可涂布到一个大的140mm直径平板,或三个小的90mm 平板上。
9.2.3小心涂布平板,注意不要涂到平板的边缘上。
涂布完毕,盖好平板,室温静置15min至干燥。
9.3 培养35℃或37℃培养,24h和48h观察结果。
9.4 挑选平板及计数9.4.1 平板计数培养24h后,在平板背面标识典型菌落。
继续培养24h,标识新长出的典型菌落。
(典型菌落为黑色或灰色,光亮凸起,培养24h 后,直径为1~1.5mm ,培养48h 后,直径为1.5~2.5mm 。
周围有部分不透明的浑浊圈。
非典型菌落和典型菌落的大小一致,黑色光亮有乳白色边缘,不带浑浊圈,或者是灰色菌落。
)挑取菌落总数小于300个,含有15~150个典型或非典型菌落的平板计数。
挑取5个菌落做证实试验(若平板中只有典型菌落,则挑取5个典型菌落;若只有非典型菌落,则挑取5个非典型菌落;若同时存在典型和非典型菌落,则挑取5个典型菌落和5个非典型菌落)。
如果最低稀释度平板上少于15个典型或非典型菌落,可按照9.4.3和10.2估计读数。
9.4.2若取1mL 涂布到三个平板上,计数三个平板的菌落总数。
9.4.3估计平板的金黄色葡萄球菌菌落总数,保留存在典型或非典型菌落的平板,把所有菌落跳出做鉴定试验。
9.5证实试验将挑选的菌落接种至脑-心浸萃液态培养基中,35℃或37℃培养24h 。
在0.3mL 的培养液中加入0.1mL 兔血浆,35℃或37℃培养。
培养4~6h 后,倾斜培养管检查是否凝固。
若为阴性反应,延长培养时间至24h 。
10 结果表达10.1计算每个平板上金黄色葡萄球菌的菌落数,记为a其中A c ——选取做证实试验的典型菌落数; A nc ——选取做证实试验的非典型菌落数; b c ——血浆凝固酶阳性的典型菌落数; b nc ——血浆凝固酶阳性的非典型菌落数; c c ——平板上典型菌落总数; c nc ——平板上非典型菌落总数。
c b nc A nc+× c nc10.2计算样品中金黄色葡萄球菌菌落数,记为N其中∑a——所有平板上阳性菌落的总数; V ——每个平板上接种体的体积,mL ; n1——第一个稀释度被选用的平板数; n2——第二个稀释度被选用的平板数; d ——第一个稀释梯度的稀释度(如10-1)。
11 精密度 11.1 概述方法的精密度可表现为重复性和再现性,在ISO 5725-2中有定义。
然而,ISO 5725-2中基于这个定义的计算,并不适用于所有微生物分析。
因此,本标准也参考ISO 16140,它已将微生物分析独立开来。